栀子金花丸HPLC指纹图谱及其与体外抗氧化活性的相关性分析
陈 帅,王慧竹,薛健飞,钟方丽#,李玲丽
(1.吉林化工学院化学与制药工程学院,吉林吉林 132022;2.沈阳药科大学药学院,沈阳 110016)
栀子金花丸HPLC指纹图谱及其与体外抗氧化活性的相关性分析
陈帅1,2*,王慧竹1,薛健飞1,钟方丽1#,李玲丽1
(1.吉林化工学院化学与制药工程学院,吉林吉林132022;2.沈阳药科大学药学院,沈阳110016)
目的:建立栀子金花丸指纹图谱,并分析与其体外抗氧化活性之间的相关性,为栀子金花丸的质量控制提供依据。方法:采用高效液相色谱法(HPLC)。色谱柱为Sinochrom ODS-BP C18(200 mm×4.6 mm,5 μm),流动相为0.2%磷酸溶液(含3 mmol/L庚烷磺酸钠溶液)-乙腈(梯度洗脱),检测波长为254 nm,流速为0.8 ml/min,柱温为38℃,进样量为10µl。采用国家药典委员会“中药色谱指纹图谱相似度评价系统软件”(2012.130723版)对12批栀子金花丸液相图谱进行相似度评价,以黄芩苷为参照峰,对各指纹共有峰进行归属。采用1,1-二苯基-2-三硝基苯肼自由基清除试验考察12批栀子金花丸的体外抗氧化活性,并对其指纹图谱与体外抗氧化活性之间的谱-效关系进行研究。结果:建立了栀子金花丸指纹图谱,12批次栀子金花丸指纹图谱与对照图谱相似度均在0.9以上(S1、S2、S3、S12除外);标记了30个共有峰,并全部归属到各成方药材中;体外抗氧化试验结果显示,不同批次栀子金花丸抗氧化能力存在差异;谱-效关系结果显示,13个共有峰与抗氧化活性呈正相关,17个共有峰呈负相关,在已知成分中发挥抗氧化活性的成分主要集中在金银花、黄芩和大黄3味药材中。结论:所建立的指纹图谱及其与抗氧化活性的谱-效关系可为该药的质量控制提供参考。
栀子金花丸;指纹图谱;高效液相色谱法;抗氧化
栀子金花丸始载于《宣明论方》,是由栀子、黄芩、黄连等8味药组成的中药制剂,具有凉血解毒、清热泻火等功效,常用于治疗口舌生疮、牙龈肿痛、咽喉肿痛等症[1]。目前栀子金花丸标准中除去对各味药材的定性鉴别外,在含量测定项下仅以栀子苷的含量作为栀子金花丸的定量测定指标,对其他成方药材的质量未作要求。栀子金花丸中主要含有栀子苷[2]、黄芩苷[3]、番泻苷A、番泻苷B[4]、芒果苷[5]、小檗碱、大黄素、大黄酚[6]等活性成分。目前关于栀子金花丸的质量控制研究主要集中在多指标定量和薄层色谱鉴别方面[7-8],但这些研究均无法体现栀子金花丸发挥药效的物质基础及化学成分的整体性,不能使其质量得到全面的控制。
指纹图谱技术因其在评价中药质量时具有整体性和模糊性的特点,被广泛用于中药材及其中药制剂的质量控制;而且,随着检测要求的不断提高,通过建立指纹图谱可以比较全面地掌握药品信息,将其纳入质量标准已成现行趋势[9]。中药药效的发挥有赖于多个成分的协同作用,指纹图谱虽能标示中药中的多种成分,但这些化学成分的标示与中药药效的发挥可能不完全一致,因此仅仅研究中药的化学指纹图谱远远不够。只有将中药的化学指纹图谱与中药的药效紧密结合起来,建立具有实际意义的谱-效关系,才能为中药质量控制提供更科学的依据[10]。为了更好地控制栀子金花丸的质量,保证其药效,笔者选择其抗氧化活性为药效指标,对3个企业生产的12批栀子金花丸的指纹图谱与抗氧化活性关系进行初步研究,为科学评价其质量提供依据。
1 材料
1.1仪器
1260型高效液相色谱仪(包括四元低压梯度泵、在线真空脱气机、DAD检测器、Chemstation色谱工作站)购自美国Agilent公司;AUY220型分析天平(日本岛津精密仪器分析公司)。
1.2药品、对照品与试剂
12批栀子金花丸(规格均为6 g/袋)具体来源见表1。栀子苷对照品、黄芩苷对照品、汉黄芩苷对照品、黄芩素对照品、汉黄芩素对照品、大黄素对照品(成都曼斯特生物科技有限公司,批号:MUST-15022411、MUST-13112909、MUST-14052312、MUST-14062204、MUST-13053012、MUST-20140107,纯度:均≥98%);1,1-二苯基-2-三硝基苯肼[DPPH,梯希爱(上海)化成工业发展有限公司,批号:2175918,纯度:>97%];乙腈(色谱纯,天津市永大化学试剂有限公司,批号:20130617);维生素C(VC)原料药(天津市北辰方正化学试剂厂,批号:20150402,纯度:99%);其余试剂均为分析纯。

表1 不同批次栀子金花丸样品编号及生产厂家Tab 1 The numbers of different batches of ZZJHW and their manufacturers
1.3药材
栀子(批号:20150421)、黄芩(批号:20141016)、大黄(批号:20150608)、黄连(批号:20150805)、黄柏(批号:20141101)、金银花(批号:20150616)、知母(批号:20141015)、天花粉(批号:20140903)均由吉林市吉林大药房提供,经吉林化工学院钟方丽教授鉴定均符合2015年版《中国药典》(一部)标准。
2 方法与结果
2.1色谱条件
色谱柱为Sinochrom ODS-BP C18(200 mm×4.6 mm,5 μm);流动相A为0.2%磷酸溶液(含3 mmol/L庚烷磺酸钠溶液),流动相B为乙腈(梯度洗脱程序:0~8 min,5%~12%B;8~20 min,12%~20%B;20~29 min,20%~23%B;29~35 min,23%~29%B;35~40 min,29%~32%B;40~46 min,32%~32%B;46~50 min,32%~49%B;50~58 min,49%~ 50%B;58~62 min,50%~60%B;62~65 min,60%~87%B;65~70 min,87%~90%B;70~75 min,90%B);流速为0.8 ml/min;检测波长为254 nm;柱温为38℃;进样量为10 μl。
2.2溶液的制备
2.2.1混合对照品溶液精密称取栀子苷对照品、黄芩苷对照品、汉黄芩苷对照品、黄芩素对照品、汉黄芩素对照品、大黄素对照品适量,加流动相溶解,制成栀子苷、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、大黄素质量浓度分别为328、270、74.8、214、95.8、41.4 μg/ml的混合对照品溶液。
2.2.2供试品溶液取栀子金花丸粉末约6.0 g,精密称定,置圆底烧瓶中,加入75%甲醇60 ml,回流提取2次,第1次1 h、第2次40 min;滤渣再用75%乙醇提取1次,时间为30 min;合并3次滤液,减压回收溶剂,置于100 ml量瓶中,流动相稀释并定容,摇匀,4℃条件避光保存。进样前用0.45 μm微孔滤膜过滤,取续滤液,即得。
2.2.3缺味阴性对照溶液按2015版《中国药典》(一部)[1]中规定的栀子金花丸处方比例,分别配制不含栀子、黄芩、大黄、黄连、黄柏、金银花、知母、天花粉以及不含黄连和黄柏2味药材的缺味阴性样品处方,并按栀子金花丸成方工艺制备,分别按“2.2.2”项下方法处理,即得各缺味阴性对照溶液。
2.2.4单味药材溶液按2015年版《中国药典》(一部)[1]中规定的栀子金花丸处方比例,以6.0 g为处方总量,计算各单味药材的质量,分别按“2.2.2”项下方法处理,即得各单味药材溶液。
2.3方法学考察
2.3.1专属性实验精密吸取混合对照品溶液和供试品溶液各10 μl,按“2.1”项下色谱条件进样,记录色谱图。通过比较保留时间和在线紫外光谱,确定供试品溶液的色谱图中6、15、19、22、25、28号峰分别为栀子苷、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、大黄素峰。其中因15号(黄芩苷)色谱峰比较稳定且信号强,故选其为参照峰。在此系统中15号峰理论板数不低于60 000,其余各峰与相邻峰的分离度均大于1.5,表明该条件下方法专属性良好。
2.3.2精密度试验取同一份供试品溶液(按“2.2.2”项下方法制备的S4供试品溶液),按“2.1”项下色谱条件连续进样6次,以黄芩苷峰为参照。结果,各共有峰相对保留时间RSD均小于0.5%,相对峰面积RSD均小于2.3%,表明仪器精密度良好。
2.3.3稳定性试验取S4供试品溶液,按“2.1”项下色谱条件分别在0、2、6、8、12、24 h进样,以黄芩苷峰为参照。结果各共有峰相对保留时间RSD均小于1.8%,相对峰面积RSD均小于2.1%,表明供试品溶液在24 h内稳定性良好。
2.3.4重复性试验取S4供试品溶液,按“2.1”项下色谱条件进行测定,以黄芩苷峰为参照。结果,各共有峰的相对保留时间RSD均小于1.2%,相对峰面积RSD均小于3.0%,表明该方法重复性良好。
2.4指纹图谱的研究
2.4.1指纹图谱的建立取12批栀子金花丸样品适量,按“2.2.2”项下方法制备供试品溶液,并按“2.1”项下色谱条件进样分析,记录75 min内的色谱图,以色谱峰出现率100%记录共有峰。结果显示,30个色谱峰为各样品所共有,共有峰的总面积占总峰面积的85%以上,以混合对照品(栀子苷、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、大黄素)进行峰定位,色谱图见图1。
2.4.2指纹图谱分析将经过积分处理的样品色谱图“AIA文件”导入国家药典委员会“中药色谱指纹图谱相似度评价系统”软件(2012.130723版),以样品S4的图谱为参照图谱,设定时间窗为0.3 min,采用中位数法,按Mark峰进行自动匹配,生成对照指纹图谱。指纹图谱详见图2,相似度评价结果见表2。
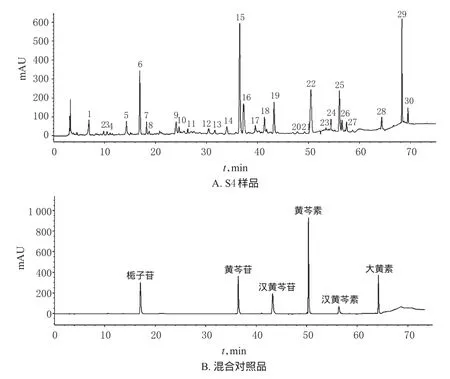
图1 栀子金花丸S4样品和混合对照品的HPLC图谱Fig 1 HPLC chromatograms of ZZJHW sample of S4 and mixed control
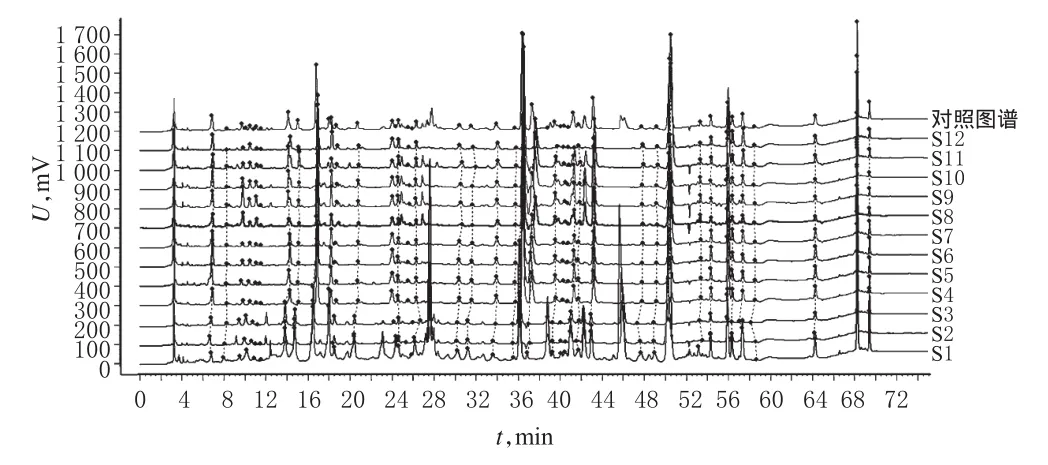
图212 批栀子金花丸的HPLC指纹图谱及对照图谱Fig 2 HPLC fingerprint chromatogram and reference fingerprint of 12batches of ZZJHW
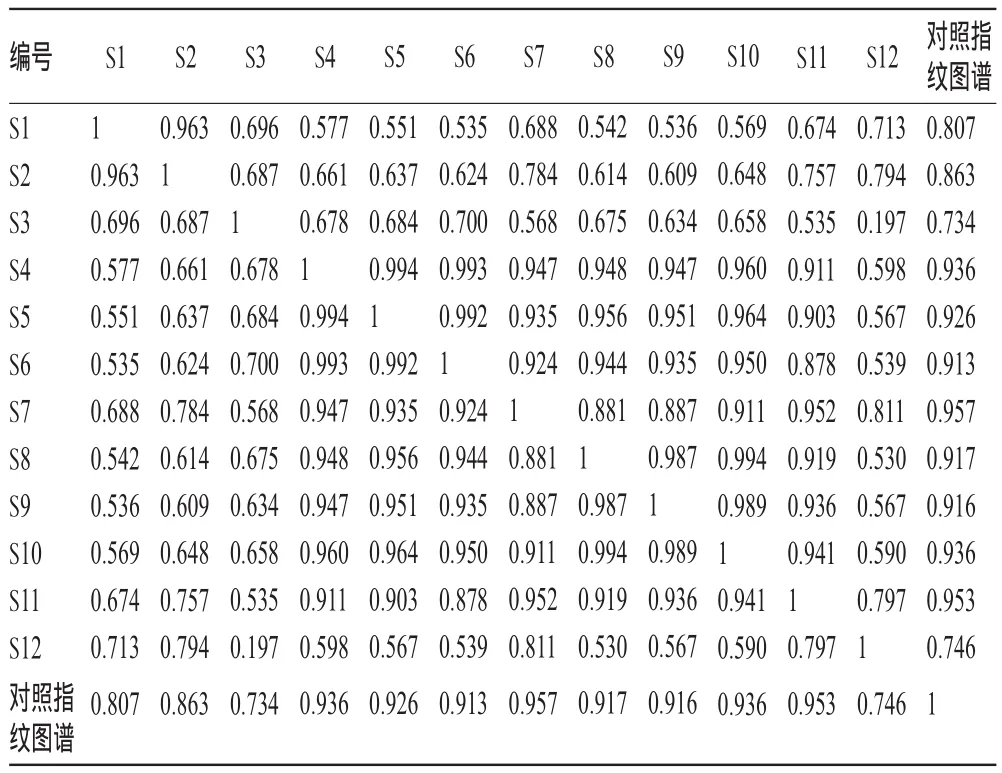
表2 12批栀子金花丸相似度结果Tab 2 The similarity results of 12batches of ZZJHW
由表2可见,12批样品中除S1、S2、S3、S12外,其余批次样品与对照指纹图谱间相似度均在0.9以上。这表明栀子金花丸成方制剂不同批次间相似度较好、质量比较稳定。
2.5色谱峰的归属
取“2.2.3”项下得到的各缺味阴性溶液及单味药材溶液10 μl,按“2.1”项下条件进样,记录色谱图,见图3。对比各吸收峰的保留时间及在线紫外光谱图,可以得到栀子金花丸图谱中的25个特征峰在8味药材中的归属,其中1号色谱峰为金银花提供,2、3、4、16号色谱峰为栀子提供,7、18号色谱峰为知母提供,9、11、14、15、17、18、19、20、21、22、24、25、26、27号色谱峰为黄芩提供,13号色谱峰为黄连提供,10、12、23、28、29、30号色谱峰为大黄提供,5号色谱峰为栀子和知母共同提供。因此在本试验确定的色谱条件下得到的栀子金花丸指纹图谱能够基本反映制剂中的主要化学成分。
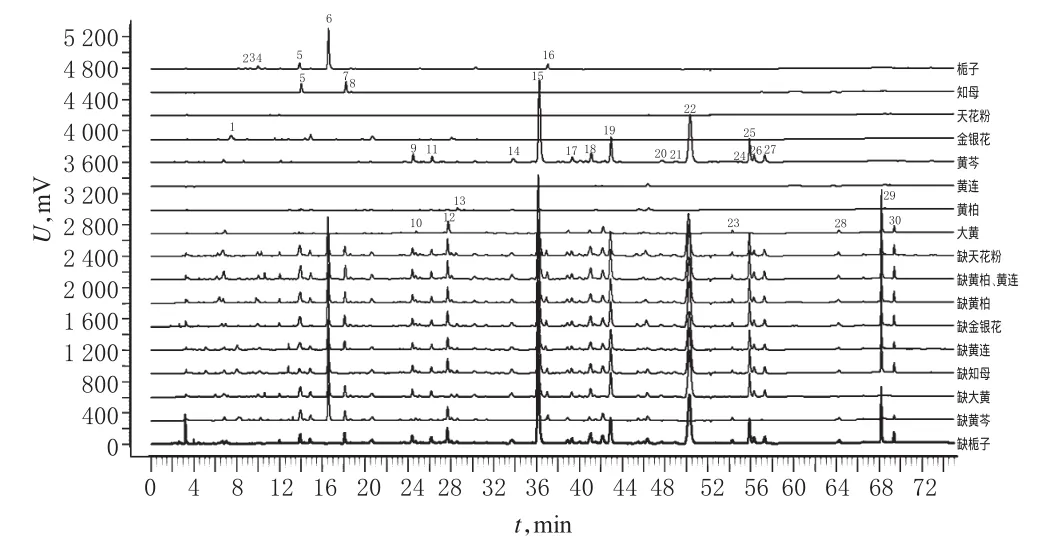
图3 各单味药材及缺味阴性溶液色谱图Fig 3 Chromatogram of single herb and negative solution
2.6体外抗氧化试验[11-12]
2.6.1DPPH溶液的制备取DPPH 10.0 mg,精密称定,置于25 ml棕色量瓶中,加无水乙醇适量,超声使其完全溶解,定容,作为贮备液。精密吸取上述贮备液6.0 ml,置于50 ml棕色量瓶中,无水乙醇定容,摇匀,即得。
2.6.2DPPH自由基清除率的测定精密量取按“2.2.2”项下方法制备的12批供试品溶液各2.0 ml,置于25 ml量瓶中,无水乙醇定容,摇匀。精密吸取上述溶液0.6、0.8、1.0、1.5、2.0 ml,分别置于10 ml棕色量瓶中,再分别加入4.0 ml DDPH溶液,无水乙醇定容,摇匀,避光放置40 min。在517 nm波长下测定吸光度Ai(供试品溶液+DPPH溶液),同法测得Aj(供试品溶液+无水乙醇溶液)和Ac(无水乙醇溶液+DPPH溶液)。以相同质量浓度的VC作为阳性对照。计算DPPH自由基清除率:清除率(%)=[1-(Ai-Aj)]/Ac×100%。以药物质量浓度为横坐标、清除率为纵坐标进行对数回归,根据回归方程计算半数抑制浓度(IC50)。不同批次栀子金花丸及VC抗氧化能力结果见图4。

图4 不同批次栀子金花丸及VC抗氧化能力比较Fig 4 Comparison of antioxidant ability between different batches of ZZJHW and VC
由图4可见,不同批次栀子金花丸的体外抗氧化能力有明显差别,其中样品S7的IC50最大,表明其抗氧化能力最弱;样品S8的IC50最小,表明其抗氧化能力最强,但弱于VC。
2.7指纹图谱与抗氧化活性谱-效关系分析
为了研究栀子金花丸指纹图谱中各共有峰对抗氧化活性的贡献大小,以12批次栀子金花丸各共有峰的峰面积作为X矩阵,以各批药材的IC50作为Y变量,利用SIMCA 13.5进行偏相关分析,并建立IC50预测值与实际值之间的回归模型,结果见图5。
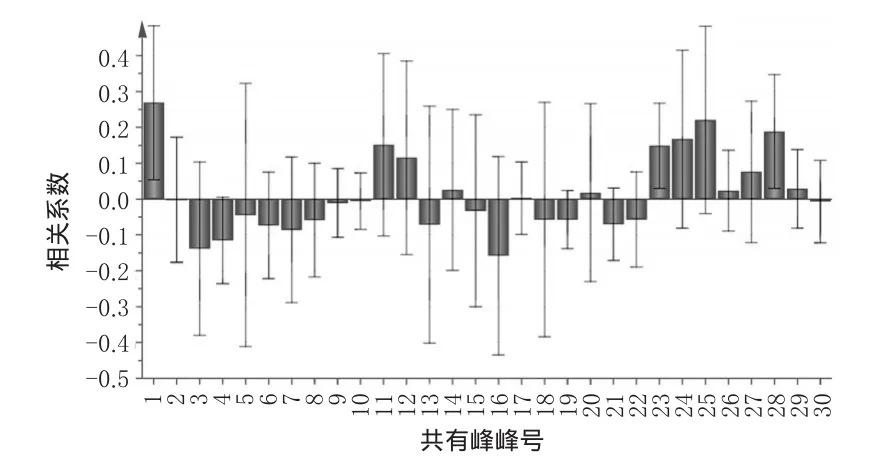
图5 各共有峰与IC50之间的相关性Fig 5 The correlation between common peak and antioxidant activity IC50
由图5可知,指纹图谱中30个共有峰对药物体外抗氧化活性贡献程度存在差异,其中有13个共有峰与抗氧化活性呈正相关,1、25、28号峰与IC50正相关性比较大。但由于试验条件原因,未能对1号峰定性,即在已知成分中与IC50正相关关系比较大的为汉黄芩素和大黄素。在17个共有峰与抗氧化活性呈负相关的色谱峰中,3、16号峰与IC50相关性比较大,但由于试验条件原因,未能对3、16号色谱峰定性。
通过建立IC50预测值与实际值之间的关系,验证偏相关分析所建模型的合理性,见图6。
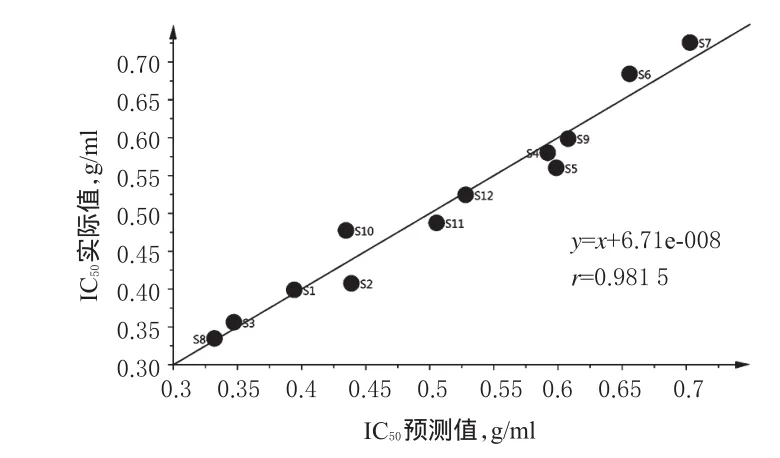
图6 抗氧化活性IC50预测值与实际值之间的关系Fig 6 The relationship between the predicted value and the actual value of antioxidant activity IC50
从图6可以看出,12批栀子金花丸均匀地分布于回归线两侧,表明12批栀子金花丸抗氧化活性的实际值与预测值间呈良好的线性关系(r=0.981 5),同时验证了谱-效关系分析过程中所建立的偏相关模型的合理性。
3 讨论
中药制剂多为复方制剂,化学组成比较复杂,为尽可能在同一张色谱图上显示更多的信息,本试验在供试品溶液制备过程中对多种提取方法进行了考察和优化,并分别对提取溶剂(甲醇、乙醇)、提取方式(超声、加热回流)及提取时间进行了考察。最终选用75%甲醇回流提取2次,第1次1 h、第2次40 min;滤渣再用75%乙醇回流提取1次,时间为30 min。结果表明,经此方法制备的供试品溶液不仅色谱峰强度较好而且数量较多,并且试验过程操作简便。
在流动相的选择上,笔者分别考察了用0.1%磷酸溶液-甲醇、0.2%磷酸溶液-乙腈、0.2%磷酸溶液(含3 mmol/L庚烷磺酸钠溶液)-乙腈等作为流动相进行梯度洗脱。结果显示,当采用0.2%磷酸溶液(含3 mmol/L庚烷磺酸钠溶液)-乙腈洗脱时,得到的色谱峰峰形和分离度较好、基线较平,故在本试验中以其为流动相。在检测波长的选择上,笔者分别在220、230、240、254、278、300、326 nm 7个波长下分别记录并比较HPLC图,结果在254 nm波长下检测到的色谱峰数量较多、强度适中,并且基线平稳,所以选定254 nm作为栀子金花丸指纹图谱测定的检测波长。除此之外,笔者还分别对柱温、流速、进样量进行了优化,通过比较色谱图,最终确定柱温为38℃、流速为0.8 ml/min、进样量为10 μl。在缺味阴性溶液的制备过程中,由于黄连和黄柏均含有小檗碱,为了对其进行定性分析,除了制备正常的缺味阴性溶液外,还制备了同时缺黄连和黄柏的阴性溶液。
通过对不同批次的栀子金花丸的色谱图比较分析,确定了30个共有峰,并以黄芩苷峰作为参照计算了各共有峰的相对保留时间和相对峰面积,并进行了方法学研究,利用国家药典委员会的指纹图谱相似度评价软件对12批样品色谱图进行了相似度评价。通过研究指纹图谱与各批次药品抗氧化活性之间的谱-效关系,首次联合评价了指纹图谱共有模式中的30个共有峰与活性的关系。结果显示,栀子金花丸中抗氧化活性的成分主要集中在金银花、黄芩和大黄3味药材中,而栀子、知母中含有的一些化学成分与栀子金花丸的抗氧化活性呈负相关。但本研究未对指纹图谱共有模式中与抗氧化活性相关性较大的化学成分进行定性及定量,缺少对活性成分与药效之间的量-效关系研究,这也将成为笔者今后研究工作的重点。
[1]国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:1 165.
[2]严安定,张永,高建.RP-HPLC法同时测定不同品种栀子及栀子金花丸中栀子苷[J].中成药,2012,34(5):965.
[3]林辉.HPLC法测定栀子金花丸中黄芩苷的含量[J].海峡药学,2012,24(11):79.
[4]高晓燕,卢建秋.栀子金花丸中栀子苷、黄芩苷、番泻苷A和番泻苷B的含量测定方法研究[J].中国中药杂志,2009,34(20):2 649.
[5]温金莲,周清,宋粉云.RP-HPLC测定栀子金花丸中芒果苷的含量[J].中国实验方剂学杂志,2011,17(17):65.
[6]蒋范任,蔡洪鲲,周翀,等.反相高效液相色谱法同时测定栀子金花丸中栀子苷、小檗碱、黄芩苷、大黄酸、大黄素、大黄酚的含量[J].中南药学,2015,13(2):172.
[7]陈晓虎,苏晶,王慧,等.UPLC法同时测定栀子金花丸中11种成分[J].中草药,2014,45(6):955.
[8]李正国,孙兆伟,刘琳琳.栀子金花丸中黄连、黄柏薄层鉴别方法研究[J].中国药事,2010,24(11):1 122.
[9]孙国祥,胡玥珊,智雪枝.用复杂性科学原理揭示中药指纹图谱的本质特征[J].中南药学,2008,6(5):600.
[10]罗志江,徐彦,吴建英,等.虎杖指纹图谱及其抗氧化活性的“谱-效”关系研究[J].西南大学学报:自然科学版,2012,34(1):138.
[11]曹玉娜,宋志前,魏征,等.抗氧化剂的抗氧化活性测定方法研究进展[J].中国药房,2013,24(1):86.
[12]陈帅,王慧竹,钟方丽,等.葫芦巴总黄酮提取工艺及其体外抗氧化活性[J].青岛科技大学学报:自然科学版,2015,36(6):628.
(编辑:林静)
Analysis of the Relationship of HPLC Fingerprint of Zhizi Jinhua Pills with Its in vitro Antioxidant Activity
CHEN Shuai1,2,WANG Huizhu1,XUE Jianfei1,ZHONG Fangli1,LI Lingli1
(1.School of Chemistry and Pharmaceutical Engineering,Jilin Institute of Chemical Technology,Jilin Jilin 132022,China;2.School of Pharmacy,Shenyang Pharmaceutical University,Shenyang 110016,China)
OBJECTIVE:To establish fingerprint of Zhizi jinhua pills(ZZJHW)and analyze the relationship of it with in vitro antioxidant activity,in order to provide the basis for the quality control of them.METHODS:HPLC method was adopted.The separation was performed on a Sinochrom ODS-BP C18(200 mm×4.6 mm,5 μm)column with mobile phase consisted of 0.2%acetic acid(containing 3 mmol/L sodium heptanesulfonate solution)-acetonitrile(gradient elution)at the detection wavelength of 254 nm and flow rate of 0.8 ml/min.The column temperature was controlled at 38℃,and injection volume was 10 μl.The“Chromatographic Fingerprint Similarity Evaluation System for TCM”(2012.130723 edition)issued by Chinese Pharmacopoeia Commission was used to evaluate the similarity of the 12 batches of ZZJHW using baicalin as reference peak so as to attribute the common peak of fingerprint.DPPH free radical scavenging assay was used to investigate the in vitro antioxidant activity of 12 batches of ZZJHW,and the relationship between its fingerprint and antioxidant activity was studied.RESULTS:The fingerprint of 12 batches of ZZJHW was established and the similarity between the fingerprint of ZZJHW with their reference fingerprint were all above 0.9 (except S1,S2,S3,S12).30 common peaks were marked,all of which were assigned to the herbs.Antioxidant experiment result showed the differences in the antioxidant capacity among different batches of ZZJHW;spectrum effect relationship showed that 13 common peaks were positively related with oxidation activity and 17 common peaks negatively related with it;among known components,oxidation activity components were mainly from Lonicera japonica,Scutellaria baicalensis and Rheum palmatum.CONCLUSIONS:The spectrum effect relationship of established fingerprint with its antioxidant activity can provide reference for the quality control of ZZJHW.
Zhizi jinhua pills;Fingerprint;HPLC;Antioxidation
R927.1
A
1001-0408(2016)22-3077-04
10.6039/j.issn.1001-0408.2016.22.16
*讲师,硕士。研究方向:中药制剂分析。E-mail:chenshuai2011 @163.com
教授,博士。研究方向:天然产物化学及应用。电话:0432-62183130。E-mail:fanglizhong@sina.com
2016-01-10
2016-04-14)

