FeM nOx和等离子体对苯的协同降解
陈 睿,王升高,崔丽佳,刘星星,张 维,皮晓强
(武汉工程大学 湖北省等离子体化学与新材料重点实验室,武汉 430074)
FeM nOx和等离子体对苯的协同降解
陈睿,王升高,崔丽佳,刘星星,张维,皮晓强
(武汉工程大学 湖北省等离子体化学与新材料重点实验室,武汉430074)
为提高介质阻挡放电对空气中苯的降解效率,以硫酸锰和过硫酸铵为原料,采用水热法制备出β-MnO2载体,并用浸渍烧结法制备出FeMnOx复合型催化剂。结合等离子体对模拟空气中的苯进行了降解研究,分析了β-MnO2和FeMnOx在不同条件下对苯的降解率的影响。结果表明,FeMnOx复合型催化剂与等离子体结合能有效提高模拟空气中苯的降解率和二氧化碳选择比;苯的降解率和二氧化碳选择比随功率的增加而增加,但随气体流速的增加而减少。苯的降解率可达到73.4%,二氧化碳选择比升至86.5%。
介质阻挡放电;催化;降解
0 引言
苯为挥发性有机化合物[1],在充足阳光下可与氧化剂发生化学反应,产生有毒的光化学烟雾[2]、破坏臭氧层;不仅如此,一旦苯的含量达到一定浓度,通过呼吸道吸入人体,在很短时间内人会产生乏力、头痛、恶心等症状,长期吸入一定量的高浓度苯蒸气,可损害造血系统和神经系统而发生慢性苯中毒[3]。目前对挥发性有机化合物的降解方法主要有冷凝法、液体吸收法、吸附法、光催化法等[4-11],但这些传统方法都存在一些缺点。低温等离子体[12]的电子温度高于背景气体温度,能保证大部分能量被用来产生高能电子、离子和活性自由基,从而促进降解反应的进行。但是,在分解过程中,单一等离子体在放电过程中存在对副产品难以控制,处理不完全等问题[13],调查表明[14-20],采用将低温等离子体协同不同种类的催化剂的方法,在处理废气的时候,其在降低反应能耗跟提高降解率等方面都有着相当不俗的表现[21-22],目前国内外研究者在铜系、锰系、镍系[23]等催化剂都有相关的研究。
利用硫酸锰和过硫酸铵为基本原料,采用浸渍烧结法制备FeMnOx粉末,比较了β-MnO2和FeMnOx在不同功率和不同气体流速对苯的降解率的影响,分析了FeMnOx复合催化剂的催化效果。
1 实验部分
1.1主要实验试剂
实验中使用的主要化学试剂如表1所列。
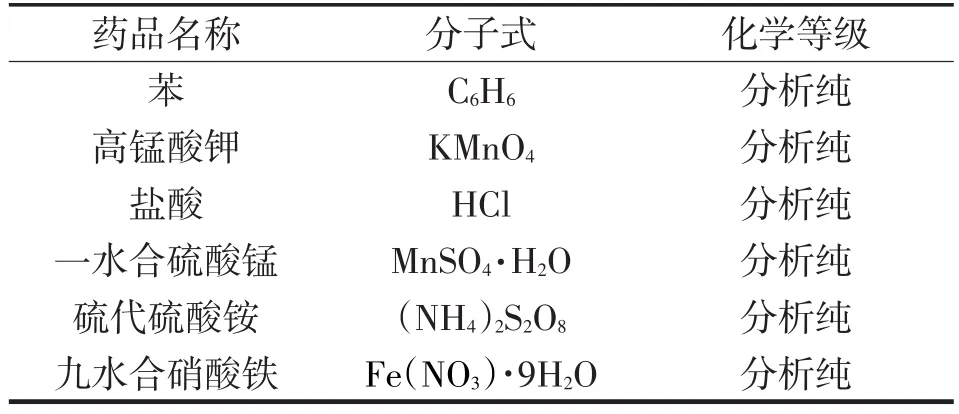
表1 实验试剂表
1.2主要实验装置
实验中使用的主要实验装置如表2所列。

表2 实验仪器表
1.3β-MnO2的制备
称取2.7 g MnSO4·H2O、3.7 g(NH4)2S2O8粉末,用40 mL去离子水溶解,磁力搅拌30 min后冷却至室温,将溶液转移至50 mL高压釜,控制温度120℃反应48 h后冷却至室温。用去离子水过滤洗涤至pH值为7,在真空干燥箱中70℃干燥24 h,得到二氧化锰黑色粉末。
1.4FeMnOx的制备
称取4.1 g Fe(NO3)·9H2O和2.6 gβ-MnO2,用40 mL去离子水溶解,在90℃下旋转蒸发,将样品放入管式炉中并在600℃下焙烧4 h制备出铁锰复合催化剂。
1.5介质阻挡放电与结合催化剂对苯的降解
实验装置[24]由等离子体反应器和分析系统、供气系统组成。DBD等离子体反应器由具有同心圆结构的双石英管组成,外层石英管外径为45 mm,壁厚为2 mm,内石英管外径为33 mm,壁厚2 mm,采用聚四氟乙烯将双石英管完全密封。石英管外壁缠有作为放电电极的铜胶纸,放电间隙为5 mm,放电长度为50 mm。最内层直径6 mm的玻璃管作为催化剂床。
使用的模拟气体流速为120 mL/min,初始浓度为3 500 mg/L。将所制备的催化剂粉末放入最内层玻璃管中通气,分别改变功率为20、24、28、32、36 W,测得不同条件下降解后苯的浓度。
1.6苯降解率测量
苯标准溶液的配制:将2 mL分析纯苯溶于一定量丙酮中,再把溶液移入100 mL定容瓶中定容。分别将0.1、0.2、0.3、0.4、0.5μL含微量苯的丙酮依次注入气相色谱仪获得对应的峰面积,式(1)为色谱峰面积与苯含量的关系。苯降解率的测定通过式(2)进行计算。
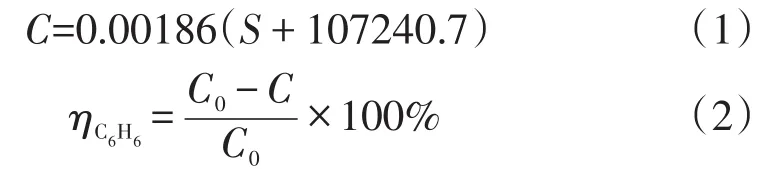
式中:S为检测样品的峰面积,C0为苯的起始浓度,mg/L,C为反应后苯的浓度,mg/L,为苯的降解率,%。
以苯的标液量为横坐标,以峰面积为纵坐标,绘制浓度标准曲线。
1.7碳氧化物的测定
本实验气相色谱仪装配有十通阀和六通阀分析气体中CO和CO2含量,柱箱温度为80℃,TCD温度为80℃。气体样品先通过TDX-01填充柱将CO2与其他气体成分分离并被保留在TDX-01填充柱中,然后其他气体成分经过5A分子筛填充柱进一步分离,并进入TCD检测器,而后再切换六通阀使载气反冲TDX-01填充柱中将CO2带入TCD检测器中。通过TCD图谱中各成分峰面积采用归一法计算样品气体CO和CO2的含量。其计算如式(3):
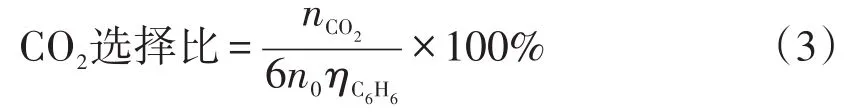
2 结果与讨论
图1为FeMnOx催化剂的XRD图,通过比对PDF卡片,FeMnOx催化剂中含有两种晶体,一种是MnO2(JCPDS No.24-0735),另一种是(Mn0.98Fe0.017)2O3(JCPDSNo.24-0507)。说明β-MnO2反应以后得到(Mn0.98Fe0.017)2O3。
图2为FeMnOx催化剂的SEM照片,由图可知,粉末的分散性较好,均以纳米棒的形式存在,通过氮吸附测得其比表面积为74.5 m2/g,通常来说,催化剂的比表面积越大,催化剂表面的活性基团的分散状态也就越好,能更好的和气体分子进行反应。
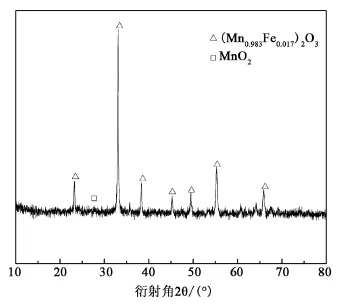
图1 FeMnOX的衍射图谱

图2 FeMnOx的SEM图
图3为苯的降解率随功率的变化。根据Hyun等[25]的理论,随着功率的增大苯的降解率逐步增加,随着气体流速的增大而逐步减小。其主要原因是,当功率增大时,等离子区的电场强度增强,气体分子运动加剧,分子间作用力增大,苯的降解程度加大;而当流速加快时,气体分子在放电区域反应的时间相对减少,有机气体分子与活性粒子间发生碰撞降解程度降低。对比(a)、(b)图可知,只用单一等离子体对苯的有机气体进行降解时,苯的降解率为43%~57%;当MnO2和等离子体协同降解时,苯的降解率为60%~70%,可见在MnO2催化剂的作用下,苯的降解率有很大的提高;而(c)中FeMnOx催化降解时,苯的降解率提高到65%~75%。这可能是由于等离子体中活性离子和自由基气体放电时,一些高能激发粒子向下跃迁产生紫外光,紫外光能更好的激发Fe里面的电子,使电子从价带跃迁到了导带,形成具有很强活性的电子空穴对,并诱捕一系列氧化还原反应的进行,提高了对苯的降解率[26-28]。
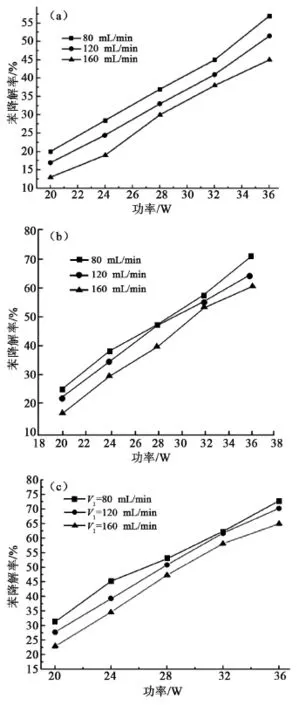
图3 苯的降解率随功率的变化曲线图
图4为降解产物中CO2的选择比随功率的变化,二氧化碳选择比随功率的增大而增加,随气体流速的增大而减小。其主要原因是,当功率增大时,苯的降解程度加大,降解更完全,一氧化碳转变成二氧化碳的量增加;而当流速加快时,气体分子在放电区域反应的时间相对减少,降解程度减弱,反应不完全,一氧化碳的量增加。对比(a)、(b)图可知,在单一等离子体的处理下,二氧化碳选择比为38%~55%;在等离子体和MnO2协同催化下,二氧化碳选择比为45%~75%;而在(c)等离子体和FeMnOx催化降解下,二氧化碳选择比明显提高至76%~87%。可能是因为Fe作为金属粒子,是氧运输和保存的载体,可以加快活性氧的反应,因此将Fe负载在MnO2上能大大提高氧的存储能力和释放转换能力,同时氧的活性也得以提高,增加了对二氧化碳的选择性[29-30]。
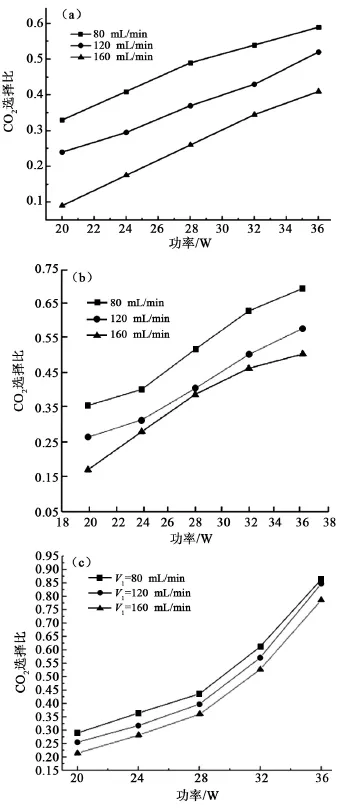
图4 降解产物中CO2的选择比随功率的变化曲线图
3 结论
利用硫酸锰和过硫酸铵反应,成功制备出β-MnO2,采用浸渍烧结制备铁锰氧化物催化剂,结合DBD对含苯的有机废气进行降解分析发现,苯的降解率和二氧化碳选择比均随功率的增加而增加,随气体流速的增大而减小。
分析发现,利用浸渍烧结生成的(Mn0.98Fe0.017)2O3催化性能比β-MnO2好,对苯的降解率可达到73.4%,二氧化碳选择比升至86.5%。
[1]DirectiveC.CouncilDirective1999/30/ECof22April1999 relating to limitvalues forsulphurdioxide,nitrogen dioxide and oxidesofnitrogen,particulatematterand lead inambientair[J]. JournaloftheEuropeanCommunities,1999,50(163):41-60.
[2]Duncan BN,Yoshida Y,Olson JR,etal.Application ofOMI observations toa space-based indicatorofNOxand VOC controlson surfaceozone formation[J].Atmospheric Environment,2010,44(18):2213-2223.
[3]赵琳,肖燕,金润铭.再生障碍性贫血发病机制研究进展[J].中国实用儿科杂志.2011,26(7):545-547.
[4]岑超平,陈定盛,蓝如辉,等.吸收法脱除废气的实验研究[J].环境工程,2007,25(6):40-42.
[5]李湘凌,林岗,周元祥,等.复方液吸收法处理低浓度苯类废气[J].合肥工业大学学报,2002,25(5):794-796.
[6]闰勇.有机废气中VOC的回收方法[J].化工环保,1997,17 (6):332-335.
[7]Khan F I,GhoshalAK.Removalofvolatileorganic compounds from polluted air[J].Journal of loss prevention in the process industries,2000,13(6):527-545.
[8]GhoshalAK,Manjare SD.Selection ofappropriateadsorption technique for recoveryofVOCs:an analysis[J].Journalof Loss prevention in theProcess Industries,2002,15(6):413-421.
[9]曹耀华,杨绍文,金梅,等.纳米二氧化钛降解有机污染物的试验研究[J].矿产保护与利用,2002(3):37-40.
[10]孙珮石,王洁,吴献花,等.生物法净化处理低浓度挥发性有机及恶臭气体[J].环境工程,2006,24(3):38-41.
[11]刘媛,王鸯鸯,杨威.浅析挥发性有机废气治理技术[J].中国环保产业,2012(11):40-43.
[12]李天鸣,闫光绪,郭绍辉.低温等离子体放电技术应用研究进展[J].石油技术,2014,14(2):59-64.
[13]TangX,Feng F,Ye L,etal.RemovalofdiluteVOCsinairby post-plasma catalysis over Ag-based composite oxide catalysts[J].CatalysisToday,2013,211:39-43.
[14]倪章松,李国强,高超.介质挡板面放电等离子体流动控制研究进展[J].真空与低温,2014,20(1):9-16.
[15]ChenW M,Qie L,ShaoQG,etal.Controllable Synthesisof Hollow Bipyramidβ-MnO2and Its High Electrochemical Performance for Lithium Storage[J].ACSappliedmaterials& interfaces,2012,4(6):3047-3053.
[16]ZhangDE,XieQ,Chen AM,etal.Fabricationand characterisation ofMnOOH andβ-MnO2nanorodswith rectangular cross-sections[J].Journal of Experimental Nanoscience,2013,8(1):77-83.
[17]Boppana V BR,Jiao F.Nanostructured MnO2:an efficient and robustwateroxidation catalyst[J].ChemicalCommunications,2011,47(31):8973-8975.
[18]LiY,LiD,Li J,etal.Pretreatmentof cyanided tailingsby catalytic ozonation with Mn2+/O3[J].Journalof EnvironmentalSciences,2015,28:14-21.
[19]CastaoM H,Molina R,Moreno S.Cooperative effectof the Co-Mnmixed oxides for the catalytic oxidation ofVOCs:Influenceof the synthesismethod[J].Applied Catalysis AGeneral,2015(492):48-59.
[20]LiY,LiD,Li J,etal.Pretreatmentof cyanided tailings by catalytic ozonation with Mn2+/O3[J].Journalof EnvironmentalSciences,2015,28:14-21.
[21]Vandenbroucke A M,Morent R,De Geyter N,etal.Nonthermal plasmas fornon-catalytic and catalytic VOC abatement[J].Journalofhazardousmaterials,2011,195:30-54.
[22]KirkpatrickM J,Odic E,ZinolaS,etal.Plasmaassisted heterogeneous catalytic oxidation:HCCIDieselengine investigations[J].Applied Catalysis B:Environmental,2012,117: 1-9.
[23]Chen CY,Liu T,Wang H,etal.Removalofhexane by nonthermal plasma and MnO2/γ-Al2O3combination[J].Chinese JournalofCatalysis,2012,33(6):941-951.
[24]王升高,刘翔,孔垂雄,等.介质阻挡放电结合二氧化锰对空气中苯的降解[J].武汉工程大学学报,2014,36(7): 48-52.
[25]Hyun-Ha H,Seung-Min O,AtsushiO,etal.Decompotion ofgas-phase benzene using plasma-driven catalyst(PDC)reactorpackedwith Ag/TiO2catalyst[J].Applied CatalysisB: Environmental,2005,56(3):213-220.
[26]宁晓宇,陈红,耿静,等.低温等离子体-催化协同空气净化技术研究进展[J].科技导报,2009,27(6):97-101.
[27]都基峻,季学李.低温等离子体处理气态有机物[J].污染防治技术,2000,13(1):33-34.
[28]陈砺,区瑞锟,严宗诚,等.放电等离子体驱动下甲醛的光催化降解丰[J].华南理工大学学报(自然科学版),2011,39(1)68-73.
[29邱作志,叶代启.放电等离子体驱动光催化降解甲苯研究[J].工业催化,2008,16(6):69-74.
[30]TangW X,Wu X F,Liu G,etal.Preparation ofhierarchical layer-stackingMn-Cecompositeoxide forcatalytic totaloxidationofVOCs[J].JournalofRareEarths,2015,33:62-69.
SYNERGY OFFeM nOXANDPLASMA FOR THEREMOVAL OFBENZENE
CHEN Rui,WANG Sheng-gao,CUILi-jia,LIU Xing-xing,ZHANGWei,PIXiao-qiang
(Provincial Key Laboratory of Plasma Chem istry and Advanced M aterialsof HubeiProvince,Wuhan Instituteof Technology,Wuhan430074,China)
To improve the degradation capability of the dielectric barrier discharge technology on benzene,using sulfateand ammonium persulphateas raw materials,β-MnO2are prepared by hydrothermalmethod,FeMnOx catalystare prepared by impregnationmethod,and used to degrade the benzene in the simulated air combined w ith plasma.The effects of β-MnO2and FeMnOx on the different conditionswas evaluated.The result indicates that the degradation ratio of benzene and the selectivity of carbon dioxide are improved when the plasma degradation andmanganese dioxide catalytic degradation are simultaneously used,the degradation efficiency of benzene and the selectivity of carbon dioxide are both improved w ith the increasing of power,butdecreasew ith the increasing of gas velocity.The degradation ratio of benzene increases to 73.4%and the selectivity of carbon dioxide growsup to 86.5%.
dielectric barrier discharge;catalysis;degradation
O53
A
1006-7086(2016)03-0173-05
10.3969/j.issn.1006-7086.2016.03.011
2016-01-04
国家自然科学基金(No.51272187和No.51442003)、湖北省自然科学基金(No.2013CFA012和No.2015CFB229)及湖北省科技厅(No.2015BAA093)
陈睿,(1993-),男,湖北武汉人,硕士研究生,主要从事等离子体技术与应用。E-mail:2334156911@qq.com。

