鸭瘟病毒单抗的制备及胶体金试纸条检测方法的建立
赵丹丹,杨国平,刁有祥,陈 浩,提金凤,张 璐,张 英,李川川
(山东农业大学动物科技学院,山东泰安 271000)
鸭瘟病毒单抗的制备及胶体金试纸条检测方法的建立
赵丹丹,杨国平,刁有祥,陈 浩,提金凤,张 璐,张 英,李川川
(山东农业大学动物科技学院,山东泰安 271000)
【目的】鸭瘟(DP)是由鸭瘟病毒(DPV)引起的一种急性、败血性传染病,以头颈肿胀、食道黏膜和泄殖腔黏膜出血、黄白色溃疡,头颈部皮下有黄白色胶冻样渗出为特征。该病一旦发生,发病急、死亡快、死亡率高,对养鸭业危害严重。快速诊断是控制鸭瘟的重要措施之一,可以及时确定病原,以便采取有效的防制手段。试验旨在建立鸭瘟病毒(DPV)胶体金快速检测方法。【方法】利用生物学软件Protean分析,选择鸭瘟病毒抗原表位较多的一段序列设计引物,PCR扩增目的基因。连接到载体pMD-18T上,测序正确后再连接到原核表达载体pET-28a上。将获得的重组质粒转化至Rosetta感受态细胞中进行诱导表达。表达的蛋白经纯化后测其浓度并经Western blotting鉴定分析。以表达的DPV-gB蛋白作为抗原,免疫7周龄BALB/c小鼠,取其脾细胞与SP2/0骨髓瘤细胞进行融合,经间接ELISA筛选及亚克隆,获得DPV-gB特异性单克隆抗体。采用柠檬酸三钠还原法制备胶体金颗粒,以制备的 H6F6单抗作为标记抗体(标记的最适pH为8.0—8.5,最佳标记浓度为15倍原液稀释),将纯化的A8D7单抗(浓度为2倍原液稀释)和羊抗鼠IgG(浓度为10倍稀释)包被在硝酸纤维素膜(NC)上,分别作为检测线和质控线,经条件优化建立了鸭瘟病毒胶体金试纸条检测方法。【结果】共获得4株能稳定分泌抗DPV-gB蛋白抗体的杂交瘤细胞株,命名为A8D7、E6C3、H11F8、H6F6。间接ELISA检测腹水效价分别为1∶103、1∶103、1∶105、1∶103。亚类鉴定结果分别为IgG2b、IgG2a、IgG2b、IgG1,轻链均为kappa链。Western blotting结果显示4株单抗均能与DPV-gB蛋白特异性结合。IFA结果显示制备的4株单抗是针对DPV产生的。建立的胶体金试纸条方法能够特异性地检测鸭瘟病毒,与鸭坦布苏病毒、H9N2亚型禽流感病毒、呼肠孤病毒、减蛋综合征病毒无反应。阳性尿囊液稀释50倍后用该试纸条检测依然为阳性;用不同批次的试纸条重复检测,结果无差异。利用制备的胶体金试纸条和PCR方法对38份临床样品进行检测比较,结果显示两者符合率为91.6 % 。【结论】本研究建立的试纸条检测方法具有良好的特异性、敏感性、重复性和稳定性,可用于DPV的快速检测。
鸭瘟病毒;gB蛋白;原核表达;单克隆抗体;胶体金试纸条
0 引言
【研究意义】鸭瘟(duck plague,DP)是由鸭瘟病毒(duck plague virus,DPV)引起的一种急性、败血性传染病[1],以头颈肿胀、食道黏膜和泄殖腔黏膜出血、头颈部皮下有淡黄色胶冻样渗出为特征。该病一旦发生,发病急、死亡快、死亡率高,对养鸭业危害严重。快速诊断是控制鸭瘟的重要措施之一,可以及时确定病原,以便采取有效防制手段。【前人研究进展】目前已建立了PCR、ELISA、间接免疫荧光技术、微量中和试验等检测鸭瘟的方法[2],但上述检测方法均需特殊的仪器设备,且耗时长,不适于在基层推广应用。胶体金免疫层析技术是近年来发展起来的集胶体金标记技术、蛋白层析技术于一体的新型快速免疫检测技术[3-4]。该技术操作简便、耗时短,不需要特殊的仪器设备[5-6],特别适合在基层推广应用[7-8]。【本研究切入点】鸭瘟对养鸭业危害严重,目前已建立了PCR、ELISA、间接免疫荧光技术、微量中和试验等检测鸭瘟的方法,但上述检测方法均需特殊的仪器设备,且耗时长,不适于在基层推广应用。胶体金免疫层析技术是近年来发展起来的集胶体金标记技术、蛋白层析技术于一体的新型快速免疫检测技术。该技术操作简便、耗时短,不需要特殊的仪器设备,特别适合在基层推广应用。且目前关于鸭瘟病毒胶体金试纸条检测方法的研究尚未见报道,本研究意义较大。【拟解决的关键问题】原核表达DPV-gB蛋白,制备抗DPV-gB蛋白单克隆抗体,从中选取2株单抗分别用于胶体金的标记及检测线的包被,采用柠檬酸三钠还原法制备胶体金颗粒,建立鸭瘟病毒胶体金试纸条检测方法。
1 材料与方法
1.1材料
1.1.1毒株、细胞株和试验动物 鸭瘟病毒(SD-Y)、鸭呼肠孤病毒(DRV)、减蛋综合征病毒(EDS-76V)、H9亚型禽流感病毒(AIV-H9N2)、坦布苏病毒(TMUV)由山东农业大学禽病学研究室分离并保存。SP2/0骨髓瘤细胞由山东农业大学禽病学研究室保存;6~8周龄SPF级BALB/c雌性小鼠购自山东省实验动物中心。
1.1.2主要试剂 原核表达载体 pET-28a、大肠杆菌DH5α和Rosetta由山东农业大学禽病学研究室保存;DNA 凝胶回收试剂盒、T4 DNA连接酶、IPTG、pMD18-T 载体等购自宝生物工程(大连)有限公司;弗氏完全佐剂、弗氏不完全佐剂、HAT、HT、PEG4000购自Sigma公司;HRP标记的羊抗鼠IgG、HRP标记的羊抗鸭IgG、FITC标记的羊抗鼠IgG、DMEM培养基、胎牛血清购自全式金生物技术(北京)有限公司;Rapid Mouse Isotyping Kit-Gold Series购 自RayBiotech;氯金酸(HAuCl4·3H2O)、二氯二甲基硅烷、正辛酸购自Aladdin公司;牛血清白蛋白(BSA)购自北京索莱宝科技有限公司;胶体金卡式套装系列购自上海杰一生物技术有限公司;超敏性辣根过氧化物酶 DAB显色试剂盒购自上海生工生物工程股份有限公司。其他试剂均为分析纯。
1.1.3试验时间与地点 2012年10月至2015年3月在山东农业大学禽病学研究室完成。
1.2DPV-gB蛋白的制备及纯化
根据GenBank发表的DPV gB基因序列,设计一对引物,上游为gB-f :5′-CCGGAATTCTGGGATTG GATGCCTAA-3′,含有EcoR1酶切位点;下游为gB-r:5′-CCGCTCGAGTATTGTACCGCCGTCTTT-3′,含有XhoL1酶切位点,PCR扩增gB,回收目的基因,将其连接到 pMD-18T载体上,鉴定正确后再经双酶切、与pET-28a载体连接,构建重组质粒pET-28a-gB。
将重组质粒pET-28a-gB转化入Rosetta感受态细胞,加入IPTG诱导表达gB蛋白。按文献[9]介绍的方法纯化表达的蛋白,并进行SDS-PAGE及Western blotting分析。
1.3DPV-gB蛋白单抗的制备
按照常规方法进行动物免疫[10]。三免后14 d,尾静脉采血,间接ELISA测定血清效价。选择效价最高的小鼠进行加强免疫,采用gB蛋白腹腔注射,80 μg/只。注射后第3天,进行细胞融合。
按照常规方法进行细胞融合[11]。采用间接ELISA对杂交瘤细胞上清进行筛选。阳性孔再经过3次有限稀释法进行亚克隆[12],待阳性率达到 100%时扩大培养,用于制备腹水,并保存于液氮。参照文献[13]进行腹水的制备,待小鼠腹部膨大后抽取腹水,离心取上清。
1.4单抗的鉴定
1.4.1单抗的纯化及亚类的鉴定 将制备的腹水从1∶100开始做倍比稀释,采用间接ELISA方法检测腹水效价。利用HiTrapTMProtein G 亲和层析柱纯化腹水,进行SDS-PAGE电泳分析;同时利用紫外分光光度法测定 260 nm和 280 nm的吸光值 A260和A280,按照蛋白质浓度=1.45×A280-0.74×A260公式计算抗体浓度。
按照Rapid Mouse Isotyping Kit-Gold Series说明书对单抗的亚类进行鉴定。
1.4.2Western blotting 鉴定 将纯化的 gB蛋白和含 pET28a 空质粒的菌体蛋白进行 SDS-PAGE 电泳后,转印至硝酸纤维素膜上,5%脱脂乳封闭过夜,以阳性单克隆细胞上清为一抗,二抗为 HRP 标记的羊抗鼠IgG(1∶5 000稀释),DAB 试剂盒显色,进行Western blotting鉴定[14]。
1.4.3间接免疫荧光(IFA)鉴定 按照常规方法[15]制备鸭胚成纤维细胞(DEF),传代后将其转到24孔细胞培养板上继续培养。待细胞长成单层,且面积为底部面积的70 %—80 %时,用DPV感染DEF细胞,同时设空白对照。待出现细胞病变后,用丙酮与甲醇按照1∶1的体积比进行固定,以鉴定为阳性的杂交瘤细胞上清为一抗,二抗为FITC标记的羊抗鼠IgG抗体(1∶200稀释),荧光显微镜下观察结果。
1.4.4单抗的特异性 分别用 DPV、TMUV、AIVH9N2、EDS-76V、DRV作为抗原包被酶标板,一抗为杂交瘤细胞上清液,二抗为HRP标记的羊抗鼠IgG (1∶5 000稀释),利用间接ELISA方法检测单克隆抗体细胞上清。
1.4.5单抗的稳定性 在杂交瘤细胞冻存3个月、6个月时,取出冻存的细胞进行复苏,并对细胞培养上清进行间接ELISA检测,以检测阳性杂交瘤细胞的稳定性。
1.5胶体金试纸条的研制
1.5.1标记条件的确定 利用棋盘法[16-17]将溶液的pH分别调为6.5、7.0、7.5、8.0、8.5、9.0、9.5和10.0,以确定胶体金标记抗体的最适pH;用0.01 mol·L-1PB (pH 7.0)将单抗按照1 mL胶体金标记抗体的量分别为30、35、40、45、50、55和60 μg,以确定抗体最适标记量。
1.5.2胶体金探针的制备 采用柠檬酸三钠还原法[18-19]制备粒径约为30 nm的胶体金颗粒,以制备的一株单克隆抗体H6F6标记胶体金,采用差速离心法[20]对胶体金探针进行纯化。
1.5.3试纸条的组装 将制备的另一株单克隆抗体A8D7和羊抗鼠IgG包被于硝酸纤维素膜(NC膜)上,分别作为检测线和质控线,按照胶体金试纸条常规构造,在PVC底板上按照NC膜、金标垫、样品垫和吸水垫的顺序粘贴[21],组装试纸条,优化反应条件,于4℃保存备用。
1.6试纸条性能的评价
1.6.1特异性试验 用制备的胶体金试纸条分别检测DPV、TMUV、AIV- H9N2、EDS-76V、DRV,观察是否出现交叉反应。
1.6.2敏感性试验 将半数致死量为 10-4.33的 DPV阳性尿囊液分别按照1∶10、1∶50、1∶100、1∶200、1∶500稀释,观察试纸条检测结果。
1.6.3重复性试验 用前后制备的 3个批次的试纸条对阳性鸭瘟病毒尿囊液进行检测,验证试纸条检测结果的重复性。
1.6.4稳定性试验 每隔一个月用保存的试纸条对阳性鸭瘟病毒尿囊液进行检测,观察其检测结果是否稳定。
1.6.5试纸条的初步应用 对实验室保存的24份疑似感染鸭瘟病毒的临床样品和 14份阳性尿囊液分别进行试纸条和PCR检测,验证二者的符合率。
2 结果
2.1DPV-gB蛋白单抗的制备
2.1.1重组质粒的构建及鉴定 PCR扩增gB基因后进行凝胶电泳,结果显示,在915 bp处可见到特异性条带(图1)。
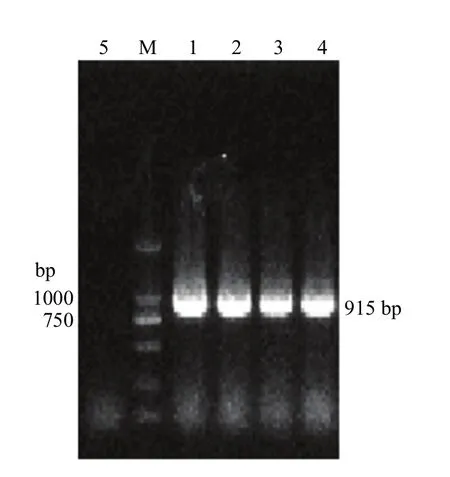
图1 重组表达载体的PCR鉴定Fig.1 The PCR identification of recombinant expression vector
2.1.2gB蛋白的纯化与鉴定 将表达及纯化后的蛋白经 SDS-PAGE 电泳后,转印到NC膜上,用鸭瘟阳性血清进行 Western blotting 鉴定。结果显示,表达的蛋白在约34kD处可见特异性条带,而菌体蛋白无条带(图2)。
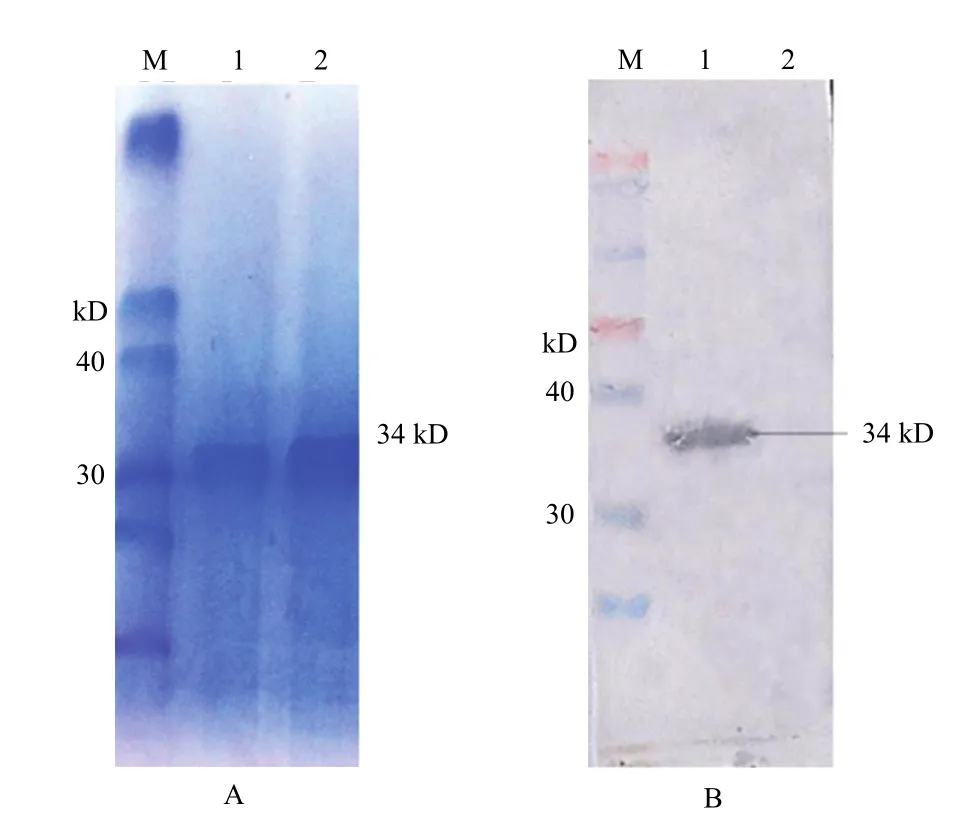
图2 诱导表达DPV-gB蛋白SDS-PAGE及Western blotting分析Fig.2 SDS-PAGE(A)and Western blotting(B)analysis of DPV-gB protein
2.1.3阳性杂交瘤细胞的筛选 细胞融合后观察,细胞融合率达90%以上,经间接ELISA检测及有限稀释法克隆至阳性率达100%,共获得4株稳定分泌抗gB蛋白的杂交瘤细胞株,分别命名为 A8D7,E6C3,H11F8,H6F6。
2.1.4单抗效价的测定 间接ELISA方法测定腹水的效价分别为 A8D7(1∶103)、E6C3(1∶103)、H11F8(1∶105)、H6F6(1∶103)。
2.1.5单抗的纯化及浓度测定 利用 HiTrapTMProtein G 亲和层析柱对准备试验的两株腹水进行纯化,SDS-PAGE蛋白质电泳结果显示,纯化的单抗有两条明显的重链和轻链,效果较好(图3)。
同时,利用紫外分光光度法计算4株单抗的浓度分别为:A8D7(2.0 mg·mL-1)、E6C3(1.8 mg·mL-1)、H11F8(1.65 mg·mL-1)、H6F6(1.93 mg·mL-1)
2.1.6单抗亚类的鉴定 获得的 4株单抗经亚类鉴定分别为:A8D7(IgG2b)、E6C3(IgG2a)、H11F8(IgG2b)、H6F6(IgG1),轻链均为kappa链。
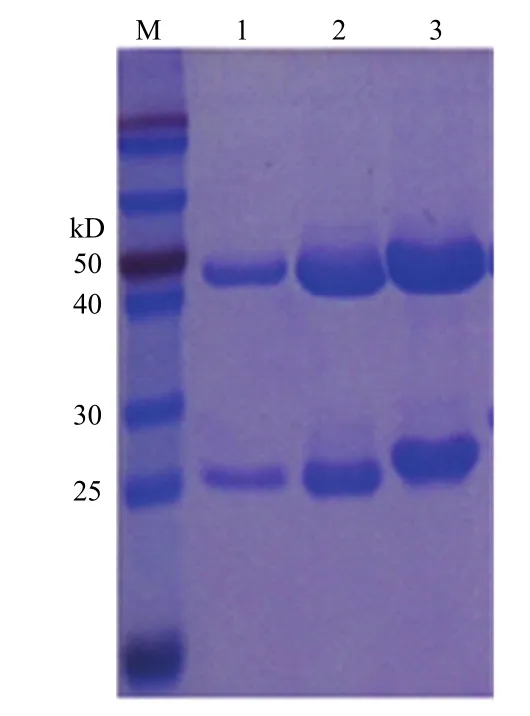
图3 单抗的纯化Fig.3 Purification of monoclonal antibodies
2.1.7Western blotting 鉴定 4株单抗均可特异性识别gB蛋白,在约34kD处出现特异性条带,而不与含空质粒表达的菌体蛋白反应(图4)。

图4 4株单抗的Western blotting 分析Fig.4 Western blotting analysis of four monoclonal antibodies
2.1.8IFA鉴定结果 DPV感染DEF细胞,出现病变后,对4株单抗进行IFA检测,结果显示,4株单抗均可显现特异性的绿色荧光,未感染的细胞未显现绿色荧光(图5)。
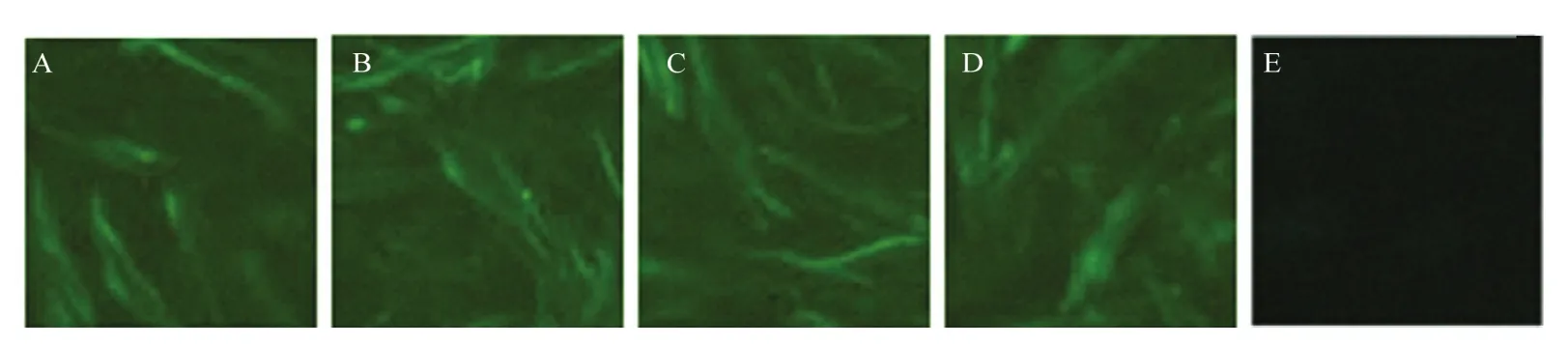
图5 单抗与感染的DPV的DEF细胞的IFA试验Fig.5 The indirect immunofluorescence assay of DPV in DEF cells with the four monoclonal antibodies
2.1.9单抗的特异性 利用间接 ELISA方法用DPV、TMUV、AIV- H9N2、EDS-76V、DRV对杂交瘤细胞上清进行检测。结果表明,本试验制备的单抗仅与DPV反应,与TMUV、AIV- H9N2、EDS-76V、DRV不发生反应。
2.1.10单抗的稳定性 在杂交瘤细胞冻存后 3个月,6个月时,取出冻存的细胞进行复苏,并对细胞培养上清进行间接ELISA检测。结果表明,冻存后的杂交瘤细胞仍能稳定的分泌抗体。
2.2胶体金试纸条的制备
2.2.1胶体金溶液的制备 制备的胶体金溶液肉眼观察为酒红色或偏紫红色,液面上无油状物质。在日光下观察,溶液为均匀的介质,颜色清亮,静置后底部无杂质,无死金现象。
2.2.2胶体金标记条件的确定 当pH为8.0—8.5、1 mL胶体金溶液中单抗标记量为50 μg时,胶体金溶液稳定,保持红色不变。由此确定胶体金标记单抗的最适pH为8.0—8.5,单抗的最佳标记量为50 μg·mL-1。
2.3试纸条性能的评价
2.3.1特异性试验 用胶体金试纸条分别检测DPV、TMUV、AIV- H9N2、EDS-76V、DRV,该试纸条仅与DPV反应,与其他病毒不发生反应(图6)。

图6 特异性检测Fig.6 Detection of specificity
2.3.2敏感性试验 敏感性试验结果显示,半数致死量为10-4.33的DPV阳性尿囊液稀释50倍后仍能用试纸条检测出来(图7)。

图7 敏感性检测Fig.7 Detection of sensitivity
2.3.3重复性试验 用不同批次的试纸条对DPV尿囊液进行检测,结果无明显差异,表明该试纸条具有较好的重复性。
2.3.4稳定性试验 稳定性试验结果显示,研制的试纸条4℃保存5个月、室温下保存3个月后依然有效。
2.3.5试纸条的初步应用 用制备的胶体金免疫层析试纸条对实验室保存的 24份疑似感染鸭瘟病毒的临床样品和14份阳性尿囊液进行检测,同时做PCR对照检测,检测结果表明,其中21份临床样品及12份尿囊液可在1—5min内得出检测结果;PCR可检测出22份临床样品及14份尿囊液(表1);二者符合率为91.6 %,适用于DPV的快速检测与筛选。

表1 比较试验结果Table 1 Comparative experiment of the result
3 讨论
3.1gB蛋白是鸭瘟病毒最为保守的囊膜蛋白之一,在促进病毒吸附细胞及在细胞间的扩散,诱导机体产生中和抗体,介导体液免疫和细胞免疫应答等方面发挥重要作用,具有良好的免疫原性及免疫保护性[22]。本研究采用原核表达系统Rosetta E. coli,表达了鸭瘟病毒 gB蛋白,原核表达系统相对于真核表达系统具有成本低、操作简便、表达量高等优点,省去了传统方法中的繁琐步骤,可大大节省时间。单克隆抗体具有高度均一、生物活性单一和与抗原结合特异性强等优点[23],可以为建立更加快速、特异性强的检测方法提供有利的工具。本研究利用表达的 gB蛋白免疫小鼠制备的单抗,检测结果显示,仅与鸭瘟病毒反应,而与其他病毒不发生反应,表明制备的单抗具有较高的特异性。
3.2多种因素会影响胶体金标记的效果,如胶体金颗粒的大小、标记蛋白的浓度、溶液的 pH值以及所用容器的纯净程度等[24-25]。胶体金颗粒的大小与制备胶体金反应的时间及所用容器的洁净度有较大关系。反应时间小于5 min时,氯金酸还原不彻底,胶体金颗粒大小不一;反应时间超过 10 min时,胶体金溶液容易形成大的颗粒甚至沉淀。同时,进入胶体金溶液内的污物都会干扰胶体金颗粒的生成或使生成的胶体金出现聚积现象。所以,反应时间一般控制在5—10min,容器最好经酸洗和硅化处理。溶液的pH可影响胶体金与单抗的结合效率,pH接近和稍高于蛋白质的等电点时,胶体金蛋白质的吸附力最强。pH偏低破坏胶体金表面静电荷,易导致胶体金发生自身聚合,出现变色,静置后有肉眼可见的颗粒性沉淀;pH偏高时,金粒子与单抗间作用力不足,结合蛋白量少,试纸条检测显色明显减弱,灵敏度降低。胶体金溶液与被标蛋白的用量是否合适也是影响标记成功的一个重要因素。蛋白浓度过高,造成浪费的同时引起试纸的拖带现象;蛋白浓度过低,导致胶体金标记不完全,从而降低试纸条的灵敏度及假阳性现象的出现。本研究采用柠檬酸三钠还原法制备胶体金溶液,通过条件优化,以反应时间为 5 min、单抗标记量为 50 μg·mL-1、溶液的pH为8.0—8.5时获得了较好的标记效果。
3.3对鸭瘟病料及阳性尿囊液检测结果显示,胶体金试纸条检测方法与PCR方法的阳性符合率为91.6 %,胶体金试纸条的检出率稍低于PCR法,但胶体金试纸条检测方法具有检测速度快,在10 min左右即可得到检测结果;无需特殊仪器设备;操作简单,便于基层临床检测等优点。
4 结论
本研究制备的DPV-gB蛋白单克隆抗体,特异、稳定。以此为基础建立的DPV胶体金检测方法,特异性强、敏感性高、重复性好,可用于鸭瘟的临床快速诊断。
References
[1] GUO Y F,SHEN C J,CHENG A C,WANG M S,ZHANG N,CHEN S,ZHOU Y. Anatid herpesvirus 1 CH virulent strain induces syncytium and apoptosisin duck embryo fibroblast cultures. Veterinary Microbiology,2009,138: 258-265.
[2] 徐晓娟,郭霄峰,魏平华. 鸭瘟病毒研究进展. 养禽与禽病防治,2012(10): 8-12. XU X J,GUO X F,WEI P H. Research progress of duck plague virus. Poultry Husbandry and Disease Control,2012(10): 8-12. (in Chinese)
[3] WANG Y H,X R LI,WANG G X,YIN H,CAI X P,FU B Q,ZHANG. D L. Development of an immunochromatographic strip for the rapid detection of Toxoplasmagondii circulating antigens. Parasitology International,2011,60: 105-107.
[4] WANG H L,FENG N,YANG S T,WANG C Y,WANG T C,GAO Y W,SU J Q,ZHENG X X,HOU X Q,HUANG H N,YANG R M,ZOU X H,HUANG G,XIA X Z. A rapid immunochromatographic test strip for detecting rabies virus antibody. Journal of Virological Methods,2010,170: 80-85.
[5] KUSANO N,IWANAMI T,NARAHARA K,TANAKA M. Production of monoclonal antibodies specific for the recombinantviral coat protein of Apple stem grooving virus-citrus isolate and theirapplication for a simple,rapid diagnosis by animmunochromatographicassay. Journal of Virological Methods,2014,195: 86-91.
[6] 王建科,易立,罗彬,杨莘,程世鹏. 胶体金免疫层析技术在动物病毒性传染病诊断中的应用. 动物医学进展,2011,32(1): 93-98. WANG J K,YI L,LUO B,YANG S,CHENG S P. Application of gold immunochromatographic Technique in the diagnosis of animal viral infectious disease. Progress in Veterinary Medicine,2011,32(1): 93-98. (in Chinese)
[7] LI Y M,HOU L D,YE J,LIU X Q,DAN H B,JING M L,CHEN H C,CAO S B. Development of a convenient immunochromatographic strip for diagnosis of infection with Japanese encephalitis virus in swine. Journal of Virological Methods,2010,168: 51-56.
[8] LI J F,ZOU M Q,CHEN Y,XUE Q,ZHANG F,LI B B,WANG Y F,QI X H,YANG Y. Gold immunochromatographic strips for enhanced detection of Avian influenza and Newcastle disease viruses. Analytica Chimica Acta,2013,782: 54-58.
[9] 吴晓平,吴异健,韩典霖,吴宝成,黄一帆. 原核表达番鸭呼肠孤病毒 σC与 σB蛋白对雏番鸭的免疫保护. 中国农业科学,2013,46(14): 3040-3045. WU X P,WU Y J,HAN D L,WU B C,HUANG Y F. Protection ofmusovy duck reovirus by immunization with the recombinant σC and σB protein expressed in E. coli. Scientia Agricultura Sinica,2013,46(14): 3040-3045. (in Chinese)
[10] 王洪海,苏敬良,曹振,田克恭. 鸭肠炎病毒单克隆抗体的制备.中国兽医科技,2004,34(11): 13-17. WANG H H,SU J L,CAO Z,TIAN K G. Preparation of monoclonal antibodies against duck enteritis virus. Chinese Journal of Veterinary Science and Technology,2004,34(11): 13-17. (in Chinese)
[11] 周艳君,华荣虹,王云峰,安同庆,刘金霞,杨金雨,华玉卓,童光志. SARS-CoV单克隆抗体的制备及抗原表位的初步鉴定. 生物工程学报,2005,21(2): 211-215. ZHOU Y J,HUA R H,WANG Y F,AN T Q,LIU J X,YANG J Y,HUA Y Z,TONG G Z. Development of monoclonal antibodies against SARS-CoV and identification of antigenic epitopes. Chinese Journal of Biotechnology,2005,21(2): 211-215. (in Chinese)
[12] 孙建慧,黄立平,危艳武,吴洪丽,王一平,张辉,刘丹,陈冬杰,张智慧,刘长明.猪细小病毒1型VP2蛋白的表达与单克隆抗体的制备及应用. 中国兽医科学,2014,44(12): 1279-1285. SUN J X,HUANG L P,WEI Y W,WU H L,WANG Y P,ZHANG H,LIU D,CHEN D J,ZHANG Z H,LIU C M. Expression of porcine parvovirus type 1 VP2 protein and preparation and application of monoclonal antibody against VP2 protein. Chinese Veterinary Science,2014,44(12): 1279-1285. (in Chinese)
[13] 王莹,郑浩,何成华,张爱华,冯璐璐,皇超英,张海彬. 伏马菌素B1单克隆抗体的制备及鉴定. 中国农业科学. 2011,44(20): 4302-4308. WANG Y,ZHENG H,HE C H,ZHANG A H,FENG L L,HUANG C Y,ZHANG H B. Generation and identification of the monoclonal antibody against fumonisin B1. Scientia Agricultura Sinica,2011,44(20): 4302-4308. (in Chinese)
[14] 贠炳岭,李德龙,胡晓亮,刘在斯,秦立廷,吴关,刘文,祁小乐,王永强,高宏雷,高玉龙,王笑梅. 禽白血病病毒群特异性抗原单克隆抗体的制备与鉴定. 中国预防兽医学报,2012,34(10): 782-785. YUAN B L,LI D L,HU X L,LIU Z S,QIN L T,WU G,LIU W,QI X L,WANG Y Q,GAO H L,GAO Y L,WANG X M. Preparation and identification of monoclonal antibodies against the group specific antigen of avian leukosisvirus. Chinese Journal of Preventive Veterinary Medicine,2012,34(10): 782-785. (in Chinese)
[15] 许静,李世军,熊胜,陈黎,杨倩,卢立志. 鸭胚成纤维细胞培养、传代及保存方法的研究. 中国家禽,2012,34(13): 9-13. XU J,LI S J,XIONG S,CHEN L,YANG Q,LU L Z. Culture subculture and cryopreservation of embryo fibroblast of duck. China Poultry,2012,34(13): 9-13. (in Chinese)
[16] 李向梅,王战辉,肖希龙,王照鹏,温凯,吴小平,夏.曦,武晋孝,江海洋. 同时检测牛奶中喹诺酮类和庆大霉素残留的胶体金免疫层析方法研究. 中国农业科学,2014,47(19): 3883-3889. LI X M,WANG Z H,XIAO X L,WANG Z P,WEN K,WU X P,XIA X,WU J X,JIANG H Y. Development of a colloidal gold immunochromatographic technique for simultaneous detection of quinolones and gentamicin in milk. Scientia Agricultura Sinica,2014,47(19): 3883-3889. (in Chinese)
[17] 蒋韬,梁仲,陈涓,何继军,吕律,马维民,刘在新,刘湘涛. 口蹄疫病毒 O、A、AsiaI型定型诊断胶体金免疫层析方法的建立. 中国农业科学 2008,41(11): 3801-3808. JIANG T,LIANG Z,CHEN J,HE J J,LÜ L,MA W M,LIU Z X,LIU X T. Development of a rapid gold immunochromatographic strip test for the diagnosis of Foot-and-Mouth disease virus O,A and Asiatype. IScientia Agricultura Sinica,2008,41(11): 3801-3808. (in Chinese)
[18] 宋万杰,胡伯里,金玉兰,阮系真,邵敬霞,周继勇.猪圆环病毒 2型抗体胶体金免疫层析方法的建立. 中国兽医科学,2014,44(7): 710-714. SONG W J,HU B L,JIN Y L,RUAN X Z,SHAO J X,ZHOU J Y. Establishment of a method for detection of the antibody against porcine circovirus type 2 based on colloidal gold immunochromatographic assay. Chinese Veterinary Science,2014,44(7): 710-714. (in Chinese)
[19] 张鑫宇,左伟勇,朱善元,夏晓莉,孙怀昌. 非洲猪瘟病毒 p54 抗体胶体金试纸检测方法的建立. 中国预防兽医学报,2014,36(4): 281-285. ZHANG X Y,ZUO W Y,ZHU S Y,XIA X L,SUN H C. Establishment of colloidal gold strip for detecting antibody against African swine fever virus. Chinese Journal of Preventive Veterinary Medicine,2014,36(4): 281-285. (in Chinese)
[20] ZHOU P,LU Y T,ZHU J,HONG J B,LI B,ZHOU J,GONG D,MONTOYA A. Nanocolloidal gold-based immunoassay for the detection of the N-Methylcarbamate pesticide carbofuran. Journal of Agricultural and Food Chemistry,2004,52: 4355-4359.
[21] JIANG T,LIANG Z,REN W W,CHEN J,ZHI X Y,QI G Y,LIU X T,CAI X P. A simple and rapid colloidal gold-based immunochromatogarphic strip test for detection of FMDV serotype A. Virologica Sinica,2011,26 (1): 30-39.
[22] GRIFFIN A. M. The nucleotide sequence of the glycoprotein gB gene of infectious laryngotracheitisvirus: analysis and evolutionary relationship to the homologous gene from other herpesviruses.Journal of General Virology,1991,72(2): 393-398.
[23] 夏兴霞,王永山,孟祥升,朱国强,张雪寒,何孔旺. 大肠杆菌0157: H7单克隆抗体胶体金免疫层析检测试纸条的研制. 中国动物传染病学报,2010,18(4): 47-53. XIA X X,WANG Y S,MENG X S,ZHU G Q,ZHANG X H,HE K W. Development of a gold immunochromatogarphic strip for the detection of the E.Coli0157: H7. Chinese Journal of Animal Infectious Diseases,2010,18(4): 47-53.(in Chinese)
[24] 孙园园,王云龙,李玉林,王继创,程蕾,邓黎黎.pH 值对胶体金标记单克隆抗体性能的影响. 细胞与分子免疫学杂志,2014,30(11): 1170-1173. SUN Y Y,WANG Y L,LI Y L,WANG J C,CHENG L,DENG L L. Effects of pH on the properties of colloidal gold labeling monoclonal antibody. Chinese Journal of Cellular and Molecular Immunology,2014,30(11): 1170-1173. (in Chinese)
[25] 顾菲菲,高海岗,陆建荣.不同粒径大小胶体金的制备. 中国畜牧兽医文摘. 2013,29(10): 45-46. GU F F,GAO H G,LU J R. Different sizes of colloidal gold preparation. Chinese Abstracts of Animal Husbandry and Veterinary Medicine. 2013,29(10): 45-46.(in Chinese)
(责任编辑 林鉴非)
Preparation of Monoclonal Antibodies Against DPV and Development of Colloidal Gold Strip for DPV Detection
ZHAO Dan-dan,YANG Guo-ping,DIAO You-xiang,CHEN Hao,TI Jin-feng,ZHANG Lu,ZHANG Ying,LI Chuan-chuan
(College of Animal Science and Technology,Shandong Agricultural University,Tai’an 271000,Shandong)
【Objective】 Duck plague (DP) is an acute,septic contagion,caused by duck plague virus (DPV),with the characteristics of head and neck swelling,the mucosa of esophageal and cloacal bleeding and yellowish-white ulcer,head and neck skin has a yellowish-white gelatin sample. Once an outbreak of this disease manifested by with high morbidity and high mortality,it would cause serious harm to the duck industry. The aim of this assay is to establish a method of colloidal gold strip for the detection of duck plague virus (DPV) rapidly. 【Method】 The main antigenic domain of DPV was chosen and analyzed by using of theProtean Biology software to design a pair of primer to amplify the aim gene by PCR. Then the fragment was inserted into prokaryotic expression vector pET-28a to construct recombinant plasmid. Then it was transformed into Rosetta for expression. During the experiment,the authors have groped the concentration of the IPTG and the induction time. After purification,the concentration of the aim protein was tested and was also analyzed and identified by Western blotting. Hybridoma cell lines stably secreting monoclonal antibody against gB protein of DPV were generated by fusing SP2/0 myeloma cells with splenocytes from the immunized mice,which used the gB protein of DPV,expressed and purified with prokaryotic,as the antigen. The monoclonal antibody-based colloidal gold immunochromatography strip was developed for the detection of DPV. The purified DPV-gB monoclonal antibody,named H6F6,was labeled with colloidal gold,with the appropriate pH between 8.0 and 8.5 and the concentration was 15 times dilution. The purified A8D7 monoclonal antibody,with the concentration of twice dilution,and the goat anti-mouse immunoglobulin G (IgG)antibody,with the concentration of ten times dilution,were blotted on nitrocellulose membrane as test line and control line,respectively. 【Result】 Hybridoma cell lines designated as A8D9,E6C3,H11F8,H6A10,stably secreting monoclonal antibody against gB protein of DPV. The titres of ascitic fluid was1:103,1:103,1:105,1:103,respectively by indirect ELISA and the immunoglobulin subtype of the monoclonal antibodies was IgG2b,IgG2a,IgG2b,IgG1,with the light chain of kappa. The result of western blot showed that the four monoclonal antibodies were able to specifically recognize gB protein of DPV. The result of IFA showed that the four monoclonal antibodies were specific to DPV. The detection results indicated that the strip was specific to DPV and had no cross reaction with DRV,EDS-76V,AIV-H9N2,and TMUV. The detection limit of DPV were 50 times dilution. 38 clinical suspected samples were simultaneously detected by immunochromatography strip and PCR while the results showed 91.6 % accuracy between them. The monoclonal antibodies-based colloidal gold strip was highly specific and sensitive and more convenient for the clinical diagnosis of DPV. 【Conclusion】 The colloidal gold strip was highly specific and sensitive and more convenient for the clinical diagnosis of DPV.
duck plague virus; glycoprotein B; Prokaryotic expression; monoclonal antibody; colloidal gold strip
2015-05-13;接受日期:2016-03-10
国家现代农业产业技术体系项目(CARS-43-10)
联系方式:赵丹丹,Tel:17863963319;E-mail:zhaodandan_0925@163.com。通信作者刁有祥,Tel:13605386443;E-mail:yxdiao@163.com

