螺纹钢表面锈蚀的实验研究
谷征满,李艳杰,邓 倩,陈 义,刘相华
(1.东北大学冶金学院,沈阳110819 ;2.东北大学材料科学与工程学院,沈阳110819;3.东北大学研究院,沈阳110819)
螺纹钢表面锈蚀的实验研究
谷征满1,李艳杰1,邓倩2,陈义2,刘相华3
(1.东北大学冶金学院,沈阳110819 ;2.东北大学材料科学与工程学院,沈阳110819;3.东北大学研究院,沈阳110819)
为解决螺纹钢加速冷却后容易生锈的问题,结合其生产工艺现状,在其穿水冷却过程中提供加速氧化气氛,以形成致密氧化膜.利用氧化膜的防护作用,控制螺纹钢基体氧化,达到防锈目的.螺纹钢加热快速冷却后通过喷射雾化的H2O2处理,电子探针分析观察到钢筋表面致密氧化膜从3~4 μm增加到17~18 μm.样品经过干湿交替加速腐蚀试验,结果表明:经过H2O2处理后的螺纹钢开始生锈时间从2 d延长至14 d,防锈性能得到大幅度提升.
螺纹钢; 防锈; 致密氧化膜
螺纹钢广泛使用在各类建筑中,建筑工地上随处可见生了锈的螺纹钢筋.生了锈的钢筋会削弱它与混凝土的结合程度,严重时可影响到钢筋强度,甚至影响建筑物寿命[1].为了提高我国建筑安全标准,国家已明确规定要以高强度的Ⅲ级螺纹钢取代Ⅱ级螺纹钢.与微合金强化钢筋相比,采用轧后水冷强化成本低,很多钢铁企业采用轧后穿水冷却工艺[2].但穿水冷却后的钢筋更容易生锈[3],影响外观和强度,导致销售困难,成为加速冷却钢筋的一个瓶颈问题.本文针对这一问题,结合现场生产工艺,在避免大幅度增加成本、不增加专门工序环节的前提下,找到一种提高螺纹钢防锈性能的方法.
1 实验研究
1.1实验材料
选取钢种为400 MPa级的Ф16 mm螺纹钢筋(成分见表1),削去表面氧化皮,切割成四组 100 mm 长的试样;选取体积分数为3%的H2O2水溶液作为氧化剂.
1.2实验过程
对表2所示的4组螺纹钢试样编号,1号试样不作任何处理,2-4号试样装入充满氮气的石英管中密封后,送入加热炉加热.2、3号试样加热温度为900 ℃,4号试样加热温度为 1 100 ℃.设置上述加热温度时,考虑了实际生产过程中穿水前温度为900~1 000 ℃,穿水后温度为700~800 ℃,及实验中从出炉到喷水过程试件产生的温降问题.

表1 400 MPa级螺纹钢的化学成分(质量分数)
把石英管中密封的试样放入炉中,加热到指定温度并恒温20 min后依次取出,立刻敲碎石英管并淬水,瞬间将试样的表面温度降低到320 ℃,试样停止淬水9 s后,表面反红至约700 ℃,再将2号试样喷洒雾化水,3、4号试样喷洒3%H2O2雾化试剂,持续约2 s,之后自然冷却.喷雾处理的工艺条件见表2.
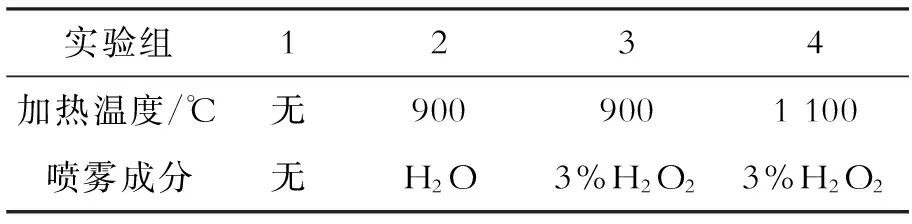
表2 喷雾处理工艺条件
喷雾处理24 h后对4组试样进行干湿交替加速腐蚀试验:每天中午 13∶00 开始喷水,15∶00 停喷,晾干后放置在室内常温环境.每天喷水之前观察螺纹钢锈蚀情况并记录.当全部试样均发现出现锈蚀时,把2-4号试样用环氧树脂镶嵌,经磨抛机抛光处理后,用酒精清洗试样表面,吹风机吹干,表面进行喷碳处理,做电子探针分析,观察氧化皮厚度,分析氧化层成分分布状况.
2 结果与讨论
2.1试样锈斑观察
经2个循环周期(2 d)后1号试样开始出现锈斑,14个循环周期(14 d)后,防锈性能最好的一组(4号试样)最后一个出现了锈斑,4组试样锈迹有明显差异,如图1所示.未经处理的1号试样已布满一层黄锈(羟基氧化铁,FeOOH),2号试样也已锈迹斑斑,3号试样锈斑明显,但远少于1号试样和2号试样.对比之下,4号试样锈迹最少,螺纹钢本体外观呈蓝黑色.通过对比可以看出,经过3%H2O2水溶液处理的4号试样防锈性能最佳.

图1 不同实验条件下螺纹钢防锈试验照片
2.2电子探针分析
试样切割后,用电子探针观察氧化铁皮厚度,发现2号试样在放大10,000倍下观测到氧化皮厚度为3.8~4.3 μm,见图2(a);3号试样在5000倍下观察,氧化层厚度为3.0~5.4 μm, 见图2(b); 4号试样在3000倍下观察,氧化皮厚度为17.0~18.0 μm, 见图2(c).显然在不同温度下喷洒不同冷却剂对氧化皮厚度的影响很显著,氧化皮厚度相差达6倍,极差达15 μm;同一试样上氧化皮厚度也不均匀,但是偏差一般不超过2~3 μm,其原因可能与试样成分的均匀性、温度的均匀性及喷洒冷却剂的均匀性有关.
图2(c)中还发现有岛状析出物,初步分析认为是共析反应的残余物:FeO、Fe等,不会对螺纹钢防锈性能造成影响;在氧化铁皮与基体之间,可见有宽度为纳米级的间隙.

图2 氧化铁皮的电子探针照片
2.3氧化铁皮结构分析
氧化铁皮的结构比较固定,一般由三层组成,最外层是Fe2O3,中间层是Fe3O4,最内层是FeO.由于氧化条件不同,氧化铁皮的组成和厚度也不同,各层厚度也会因生成条件的改变而不同[4].在加热过程中,钢的氧化可用Wanger理论进行分析,初始时符合抛物线增厚规律[5],此时氧化反应由铁原子的扩散及接触金属的氧化性气体控制;而穿水过后,由于水中游离氧含量较少,水冷速度较快,生成氧化皮中致密的Fe3O4较少,而生成疏松多孔的FeO较多,这是造成穿水螺纹钢容易生锈的重要原因.氧化皮中的Fe3O4主要通过共析反应由FeO 转变而来[6],反应方程式如下:
4Fe1-yO=Fe3O4+(1-4y)Fe
(1)
当温度在570 ℃ 以下,FeO 层发生共析反应时,其反应产物的形成与含氧量有关,在贫氧区形成Fe 晶核,在富氧区形成Fe3O4晶核,两者共同形成了一个共析反应产物的晶核(片层状的Fe3O4/Fe)[6].由此说明Fe3O4形成与FeO层中的氧含量有关,在富氧区即供氧相对充足时促使Fe3O4的形成[7].实验中H2O2在螺纹钢表皮氧化过程中提供了相对充足的氧,促使形成致密的Fe3O4.
对4号试样的氧化皮做电子探针分析,在同一直线上从内到外选取3个点,如图3所示.氧化铁皮中这3个点处Fe与O的物质的量比见表3.

图3 氧化铁皮结构测试照片
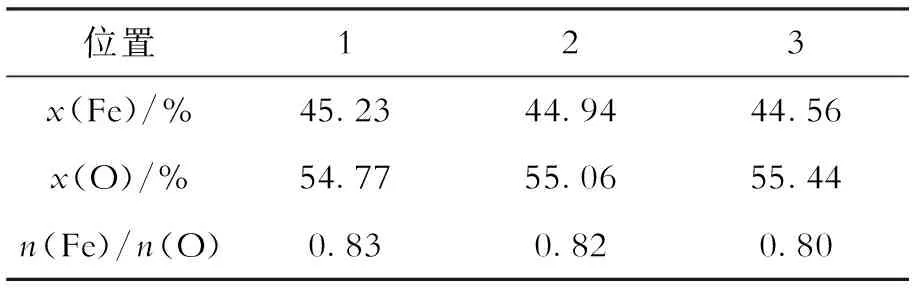
位置123x(Fe)/%45.2344.9444.56x(O)/%54.7755.0655.44n(Fe)/n(O)0.830.820.80
FeO、Fe3O4和Fe2O3的n(Fe)/n(O)分别为1.0、0.75和0.66,经分析可知所取3个点均在Fe3O4组成层内(17~18 μm).这与分析结果基本一致,氧化皮中含致密的Fe3O4层确实得到增厚而且比魏凤玉等人[8]关于缓蚀剂研究所得到的致密氧化膜更厚.Fe3O4阻止了部分氧气渗入,起到了防锈作用.本实验改变传统加入缓蚀剂防锈的思路,通过加入氧化剂增加致密氧化膜的厚度来达到防锈的目的,为解决螺纹钢防锈难题提供新途径.
3 结 论
(1)选用环境友好型化学试剂H2O2作为氧化剂,促进螺纹钢表面生成致密Fe3O4氧化膜,实现了以氧化铁皮保护控制基体的氧化.
(2)经3%H2O2喷雾处理,可生成厚度为17.0~18.0 μm 的致密氧化膜,经干湿交替加速腐蚀实验,所生成的致密氧化膜起到了防止基体生锈的作用.
(3)在现有螺纹钢的加速冷却后增加H2O2喷雾处理的技术路线,能解决螺纹钢易生锈的问题.
[1]Novak P,Mala R,Joska L.Influence of pre-rusting on steel corrosion in concrete[J].Cement and Concrete Research,2001,31(4): 589-593.
[2]曹树卫,王新江.穿水冷却工艺对HRB400热轧带肋钢筋性能的影响[J].钢铁研究,2010,01: 18-20.
(Cao Shuwei,Wang Xinjiang.Effect of accelerated cooling on properties of HRB400 hot-rolled ribbed bars[J].Research on Iron & Steel,2010,01: 18-20.)
[3]Abdullah A, Almusallam.Effect of degree of corrosion on the properties of reinforcing steel bars[J].Construction and Building Materials,2001,15(8): 361-368.
[4]冷茂林,于浩,孙卫华,等.热轧低碳钢氧化铁皮的变形行为研究[J].新技术新工艺,2008,12: 100-102+3.
(Leng Maolin,Yu Hao,Sun Weihua,etal.Deformation behavior study of low-carbon steel iron oxide scale during hot rolled[J].New Technology & New Process,2008,12: 100-102+3.)
[5]蒋柯,韩静涛.20MnSi氧化铁皮成分和结构研究[J].塑性工程学报,2000,03: 40-43.
(Jiang Ke,Han Jingtao.Scale component and microstructure of 20MnSi steel[J].Journal of Plasticity Engineering,2000,03: 40-43.)
[6]孙彬,刘振宇,邱以清,等.低碳钢表面FeO层空气条件下等温转变行为的研究[J].钢铁研究学报,2010,02: 34-40.
(Sun Bin,Liu Zhengyu,Qiu Yiqing,etal.Isothermal eutectic decomposition of FeO formed on a low carbon steel in air[J].Journal of Iron and Steel Research,2010,02: 34-40.)
[7]张娟娟,魏连启,仉小猛,等.高温防锈剂对螺纹钢耐腐蚀性能的影响研究[J].计算机与应用化学,2011,11: 1362-1366.
(Zhang juanjuan,Wei Lianqi,Zhang Xiaomeng,etal.Study on corrosion resistance of high temperature anti-rust agent on rebar[J].Computers and Applied Chemistry,2011,11: 1362-1366.)
[8]魏凤玉,李武林.一种新型螺纹钢低温缓蚀淬火剂[J].腐蚀与防护,2015,02: 166-169+181.
(Wei Fengyu,Li Wulin.A new type of low temperature corrosion inhibition quenched agent for rebar[J].Corrosion and Protection,2015,02: 166-169+181.)
An Experimental investigation on rust-eaten of rebar surface
Gu Zhengman1,Li Yanjie1,Deng Qian2,Chen Yi2,Liu Xianghua3
(1.School of Metallurgy,Northeastern University,Shenyang 110819,China; 2 School of Materials Science and Engineering,Northeastern University,Shenyang 110819,China;3 Research Institute of Science and Technoligy,Northeastern University Shenyang 110819,China )
It is easy for the rebar to rust-eaten after the water cooling process.In order to solve the problem,an experiment was carryed where a strongly oxidative atmosphere was provided to produce a dense layer of the oxide,so that base metal can be prevented from further rust-eaten.After heated,the rebar was sprayed by atomized H2O2.The electron probe analysis showed that the oxide layer increases from 3~4 μm to 17~18 μm.After several times of dry and wet corrosion test,it was showed that the time for the rebar to be rusted changes the from 2 days to 14 days.It is believed that the authors method is feasible.
rebar,antirust,tightly oxide layer
10.14186/j.cnki.1671-6620.2016.02.013
TG 178
A
1671-6620(2016)02-0143-04

