山茱萸果肉化学成分研究*
任亚硕,许凤清,马凤爱
(1 安徽中医药大学药学院,安徽 合肥 230012;2 安徽省现代中药重点实验室,安徽 合肥 230012)
山茱萸果肉化学成分研究*
任亚硕1,2,许凤清1,2,马凤爱1,2
(1 安徽中医药大学药学院,安徽合肥230012;2 安徽省现代中药重点实验室,安徽合肥230012)
研究了山茱萸(Cornusofficinalis)果肉的化学成分,分离得到单体化合物。对山茱萸成熟果实渗漉提取,利用硅胶、Sephadex LH-20柱色谱和重结晶等方法分离纯化化合物,通过理化性质和现代波谱分析技术鉴定化合物结构。结果表明:从山茱萸果肉中分离并鉴定得到6个单体化合物。化合物分别鉴定为槲皮素(Quercetin, 1)、咖啡酸(Caffeic acid, 2)、没食子酸(Gallic acid, 3)、没食子酸乙酯(Ethyl gallate, 4)、齐墩果酸(Oleanoic acid, 5)、β-谷甾醇(β-Sitosterol, 6)。
山茱萸;化学成分;提取分离;结构鉴定
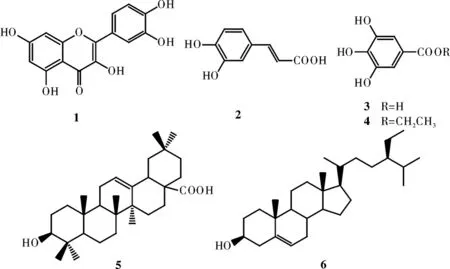
图1 化合物1~6的结构式Fig.1 The structure of compounds 1~6
山茱萸(CornusofficinalisSieb.et Zucc)为山茱萸科(Cornaceae)植物[1]。药用部位是除去果核的干燥成熟果肉,始载于《神农木草经》,又名蜀枣、 药枣、山萸肉、枣皮、肉枣等,具有补益肝肾、涩精固脱的功效[2]。作为临床常用中草药,山茱萸含有多种活性成分,为了进一步阐明其药理活性的化学基础,本文对新鲜的山茱萸果肉进行了化学成分研究,分离得到6个单体化合物。
1 实 验
1.1仪器与材料
AV-500核磁共振仪,Bruker BioSpin GmbH, Rheinstetten, Germany;EYELA SB-1100旋转蒸发仪,东京理化器械株式会社;SHB-III循环水式多用真空泵,郑州长城科工贸有限公司;ZF-2型三用紫外仪,上海市安亭电子仪器厂;HH-S2恒温水浴锅,江苏金坛市环宇科学仪器厂;DZF-6050真空干燥箱,上海博讯实业有限公司医疗设备厂;AB135-S十万分之一分析天平,瑞士METTLER TOLEDO;大孔树脂AB-8型,天津光复精细化工有限公司;柱色谱用硅胶(100~200目,200~300目)、薄层色谱用硅胶G、GF254,青岛海洋化工厂生产;凝胶为Sephadex LH-20(50 μm),GE 公司;乙醇为食用酒精;水为蒸馏水;其它试剂均为市售分析纯。
山茱萸药材采自安徽省岳西县石关乡,由安徽中医药大学中药资源系杨青山鉴定为山茱萸科植物山茱萸(CornusofficinalisSieb.et Zucc)。
1.2提取与分离
山茱萸成熟果实6.0 kg,人工去核,得到山茱萸果肉,95%乙醇50 L浸渍2次,续用70% 乙醇50 L 浸渍1次,每次2天,合并3次浸渍液,回收溶剂,得到无醇味稠浸膏,加水混悬,依次以乙酸乙酯、正丁醇进行萃取,合并萃取液,减压回收溶剂,分别得到乙酸乙酯部位浸膏127.9 g,正丁醇部位浸膏521.3 g。水相经AB-8大孔树脂柱,水洗2个柱体积,后续用70%乙醇洗脱,回收洗脱液,得到水相部位。
取山茱萸乙酸乙酯部位浸膏,加乙醇溶解,吸附于350 g硅胶(200~300目),经硅胶柱色谱(1.65 kg, 13×80 cm),二氯甲烷-甲醇(95:5, 9:1, 85:15, 4:1, each 20 L, V/V)系统梯度洗脱,经TLC检识,合并相近的流份,得到12个洗脱部位(Fr 1~Fr 12)。取Fr 1、Fr 2、Fr 3、Fr 7经硅胶柱色谱和Sephadex LH-20葡聚糖凝胶色谱反复纯化,从Fr 1中分离得到化合物6(38 mg),Fr 2中分离得到化合物5(16 mg),Fr 3中分离得到化合物4(2 mg),Fr 7中分离得到化合物1(626 mg),2(12 mg),3(6 mg)。
2 结果与讨论
2.1结构鉴定结果
化合物1:黄色针状结晶(甲醇)。1H-NMR (500 MHz, DMSO-d6) δH: 12.48 (1H, s, OH-5), 7.65 (1H, d,J=2.2 Hz H-2′), 7.51 (1H, dd,J=8.4, 2.2 Hz, H-6′), 6.85 (1H, d,J=8.4 Hz, H-5′), 6.38 (1H, d,J=2.0 Hz, H-8), 6.16 (1H,d,J=2.0Hz,H-6), 10.80 (1H,s,3′-OH), 9.6 (1H,s,4′-OH), 9.36(1H,s,7-OH), 9.31(1H,s,3-OH);13C-NMR (125 MHz, DMSO-d6) δ: 175.8 (s, C-4), 163.9 (s, C-7), 160.7 (s, C-5), 156.1 (s, C-9), 147.3 (s, C-4′), 146.8 (s, C-2), 145.0 (s, C-3′), 135.7 (s, C-3), 121.9 (s, C-1′), 120.0 (d, C-6′), 115.6 (d, C-5′), 115.0 (d, C-2′), 103.0 (s, C-10), 98.2 (d, C-6), 93.4 (d, C-8)。以上波谱数据与文献[3]一致,故鉴定化合物1为槲皮素(Quercetin)。
化合物2:黄色针状结晶(甲醇)。1H-NMR (500 MHz, DMSO-d6) δH: 7.37 (1H, d,J=15.8 Hz, H-7), 7.00 (1H, d,J=2.0 Hz, H-2), 6.91 (1H, dd,J=8.2, 2.0 Hz, H-6), 6.73 (1H, d,J=8.2 Hz, H-5), 6.13 (1H, d,J=15.8 Hz, H-8).13C-NMR (125 MHz, DMSO-d6) δC: 167.9 (s, C-9), 148.1 (s, C-4), 145.5 (s, C-3), 144.6 (s, C-7), 125.0 (s, C-1), 121.2 (d, C-6), 115.7 (d, C-5), 115.1 (d, C-2), 114.6 (s, C-8)。以上波谱数据与文献[4]一致,故鉴定化合物2为咖啡酸(Caffeic acid)。
化合物3:无色针状结晶(甲醇)。1H-NMR (500 MHz, acetone-d6) δH: 7.13 (2H, s, H-2, 6)。13C-NMR (125 MHz, acetone-d6) δC: 167.7 (s, C-7), 145.9 (s × 2, C-3,5), 138.6 (s, C-4), 121.9 (s, C-1), 110.0 (d × 2,C-2, 6)。以上波谱数据与文献[5]一致,故鉴定化合物3为没食子酸(Gallic acid)。
化合物4:无色针状结晶(氯仿)。1H-NMR (500 MHz, DMSO-d6) δH: 7.13 (2H, s, H-2, 6)。13C-NMR (125 MHz, DMSO-d6) δC: 167.7 (s, C-7), 145.9 (s×2, C-3,5), 138.6 (s, C-4), 121.9 (s, C-1), 110.0 (d×2, C-2, 6)。以上波谱核磁数据与文献[6]报道一致,故鉴定化合物4为没食子酸乙酯(Ethyl gallate)。
化合物5:无色针状结晶(甲醇)。1H-NMR (400 MHz,DMSO-d6) δH:0.7~1.2之间出现7个甲基氢质子峰,1.0~2.1(m)为多个CH、CH2上的H信号,5.28(1H,br.s,H-12)为烯氢信号。13C-NMR (100 MHz, DMSO-d6) δC:38.4(C-1),27.7(C-2),79.1(C-3),38.7(C-4),55.2(C-5),18.2(C-6),32.4(C-7),39.6(C-8),47.6(C-9),37.0(C-10),23.3(C-11),122.6(C-12),143.6(C-13),41.5(C-14),28.1(C-15),23.9(C-16),46.8(C-17),41.9(C-18),46.5(C-19),29.6(C-20),33.8(C-21),32.6(C-22),30.6(C-23),15.9(C-24),15.5(C-25),17.2(C-26),26.9(C-27),182.8(C-28),34.0(C-29),23.9(C-30)。以上波谱数据与文献[7]所报道的一致,故鉴定化合物5为齐墩果酸(Oleanoic acid)。
化合物6:白色无定形粉末(氯仿)。经TLC 检识与β-谷甾醇对照,薄层行为一致;后经HPLC验证,保留时间与β-谷甾醇对照品相同,故确定化合物6为β-谷甾醇。
2.2讨论
本实验以安徽大别山区的山茱萸新鲜果肉为研究对象,为防止植物中的某些化学成分遇热会被破坏,采用渗漉的方式提取,并在实验过程中严格控制实验温度在60 ℃以下,通过系统溶剂萃取法将提取浸膏进行极性分段,并利用多种色谱技术对乙酸乙酯萃取部位的化学成分进行初步分离,分得6个化合物,经薄层检识、1H-NMR,13C-NMR等方法对分离得到的6个单体化合物进行结构鉴定。
后期进一步对比山茱萸果肉与果核中化学成分的异同,深入探讨山茱萸炮制前后化学成分的改变,将会对山茱萸的综合开发与应用起到促进作用。
3 结 论
山茱萸是目前中医临床常用的传统中药,本研究对其乙酸乙酯萃取部位化学成分进行系统分离,后期实验还将对其石油醚、正丁醇萃取进行研究。山茱萸因含有丰富的活性成分,确切的保健功效,成为研究热点,随着山茱萸在医药和保健品等方面的广泛应用,其药效机制的研究也在不断深入。本课题组也将继续进行系统实验,以期为山茱萸的进一步研究提供有益参考。
[1]中科院中国植物志中国植物志编委会. 《中国植物志》. 北京:科学出版社,1990: 56, 84.
[2]国家药典委员会. 中华人民共和国药典(第一部)[S]. 北京:中国医药科技出版社,2015: 27.
[3]宋丽,臧志和,廖洪利,等. 槲皮素三种化学结构修饰方法的研究[J]. 成都医学院学报, 2007, 2(2): 115-117.
[4]段营辉,戴毅,高昊,等. 草珊瑚的化学成分研究[J]. 中草药, 2010, 41(1): 29-32.
[5]杨小凤,付宏征. 栾树的化学成分[J]. 药学学报, 1999, 34(6): 457-462.
[6]程琛舒. 山茱萸化学成分的研究[D]. 合肥:安徽大学, 2011.
[7]李娟,毕志明,肖雅洁,等. 怀牛膝的三萜皂苷成分研究[J]. 中国药学杂志,2007, 42(3): 178-180.
Study on the Chemical Constituents from the Fruit ofCornusofficinalis*
RENYa-shuo1,2,XUFeng-qing1,2,MAFeng-ai1,2
(1 School of Pharmacy, Anhui University of Chinese Medicine, Anhui, Hefei 230012;2 Anhui Key Laboratory of Modernized Chinese Materia Medica, Anhui Hefei 230012, China)
To study the chemical constituents from the fruit ofCornusofficinalis, the chemical constituents were separated and purified by a variety of chromatographic methods such as silica gel, Sephadex LH-20 and recrystallization. Their structures were elucidated on the basis of extensive spectroscopic methods and physico-chemical characters. Results showed that six compounds were isolated from the fruit ofCornusofficinalis. Compounds 1~6 were identified as Quercetin, Caffeic acid, Gallic acid, Ethyl gallate, Oleanoic acid and β-Sitosterol.
CornusofficinalisSieb.et Zucc; chemical constituents; extraction and isolation; structure establishment
安徽中医药大学自然科学研究基金项目(No: 2015zr008)。
任亚硕(1987-),男,助教。
许凤清,女,副教授。
R931.6
A
1001-9677(2016)08-0076-02

