以矿粉制备纳米吸附剂及其吸附性能研究
封羽涛
(宝钢发展有限公司,上海 201999)
以矿粉制备纳米吸附剂及其吸附性能研究
封羽涛
(宝钢发展有限公司,上海201999)
铅离子由于会富集在生物体重要器官,造成严重的生物毒性。本文以矿渣为原料采用共沉淀法制备纳米羟基磷灰石(HA)颗粒。结果表明:合成的低结晶度的HA纳米颗粒呈现球形,粒径分布在50~80 nm。纳米HA对铅离子具有良好的吸附性能,其吸附机制为溶解-沉积反应。纳米HA置于铅离子溶液后发生溶解反应,释放出的磷酸根离子与溶液中的铅离子反应生成棒状铅磷灰石(PbHA)。纳米HA颗粒对铅离子吸附性能的影响因素包括溶液铅离子浓度、溶液pH值和吸附温度。铅离子浓度越高、pH值越小、吸附温度越高,则纳米HA对铅离子的平衡吸附量越高。因此,纳米HA在吸附重金属铅离子领域具有重要的应用前景。
纳米羟基磷灰石;化学吸附;铅离子
近年来,由于社会的不断进步和工业的持续发展,污水、污泥、土壤中重金属含量的超标对环境造成了潜在的危害。重金属的污染与其它化合物的污染不同,即使浓度很低,也不易在环境中净化,并易造成不断蓄积,常对环境带来联合污染[1-2]。尤其是,铅离子不仅会与蛋白中的-SH基团形成键合作用,从而抑制酶,而且还可以改变骨细胞对功能[3]。此外,在土壤、水体中经微生物作用,可转化为毒性更强的有机金属,甚至还可以通过食物链逐级富集,使其侵入人体的剂量成倍地增长[3]。
目前,去除重金属离子的常用方法包括以下几种:化学法、离子交换法、生物法、吸附法、溶剂萃取法、蒸发浓缩法、表面活性剂法、磁分离法等[4-7]。最新研究发现:羟基磷灰石(Ca10(PO4)6(OH)2,简写为HA)对铅、铬、铜等重金属离子具有优良的吸附性能,其原因主要取决于HA独体的结构特征[8-10]。HA晶胞是由2个分子组成的六方晶系结构,钙和氢氧根离子围成的柱状体形成了一个平行c 轴的螺旋六重对称性通道。羟基能被氟离子、氯离子和碳酸根离子代替,生成氟基磷灰石、氯基磷灰石或含碳酸根的磷灰石。而Ca2+很容易被Cd2+,Hg2+等有害金属离子和Pb2+,Cu2+,Zn2+,Co2+,Sr2+等重金属离子发生交换作用,故可以作为这类离子的吸附剂进行废水等的净化,并可以根据需要制备成具有较大比表面积的颗粒以提高吸附效果[8-10]。
本文以宝钢集团钢铁冶炼后排放的矿渣微粉为原料制备HA纳米颗粒,深入探讨纳米HA的结构、形貌,以及对重金属铅离子的吸附性能和吸附机制。
1 实 验
1.1材料
矿渣,上海宝钢发展有限公司;磷酸氢二胺,国药集团化学试剂有限公司;浓盐酸,上海润捷化学试剂有限公司;浓氨水,江苏强盛功能化学有限公司。
1.2实验方法
室温下,称取10 g矿渣(组成含量如表1所示)溶于1 mol/L盐酸中,过滤除去产生的沉淀。用1 mol/L氨水(氢氧化钠、氢氧化钾)将滤液调节至pH=10。过滤除去沉淀,得到的滤液中主要是钙离子。测定滤液中钙离子的浓度,按HA的化学计量比Ca/P=1.67称取磷酸氢二铵,并用1.0 mol/L氨水调节pH=10。搅拌下,将磷酸氢二铵溶液逐滴滴入到钙离子溶液中,并继续搅拌1 h,陈化12 h。最后,经过过滤、用去离子水洗涤、干燥和研磨得到纳米HA颗粒。

表1 矿渣微粉化学分析Table 1 Chemical Analysis of slag powder
1.3材料的表征
用扫描电镜(SEM; JEOJ, JSM-6380LV)观察纳米HA以及吸附铅离子前后的晶体形貌。采用X射线衍射光谱(XRD; D/max-Ⅲ C)和傅里叶红外变换(FITR; Nicolet 5DX)表征纳米HA吸附铅离子前后的结晶结构及组成。
1.4HA对铅离子的吸附实验
将硝酸铅溶解在去离子水中配制1 L不同浓度的铅离子溶液(400 mg/L、600 mg/L、800 mg/L、1000 mg/L)。用HNO3(0.1 M)和NaOH(0.1 M)溶液调节铅离子溶液的pH=2.5~5.5。称取0.5 g HA粉末加入到铅离子溶液中,20 ℃、30 ℃、40 ℃下搅拌,定时取样,测定溶液中残留铅离子的浓度。
2 结果与讨论
2.1纳米HA的结构和形貌

图1 纳米HA的SEM照片



图2 HA的结构表征
2.2纳米HA颗粒对铅离子的吸附性能和吸附机理

图3 纳米HA在不同离子浓度的铅溶液中的吸附曲线
为了研究纳米HA的铅吸附性能,将HA置于不同浓度的铅离子溶液中,并采用ICP测试铅离子在不同时间点的溶液离子浓度。由图3可知,吸附2 h前HA纳米颗粒对铅离子具有快速吸附速率,随后离子浓度逐渐达到吸附平衡。溶液中的离子浓度对纳米HA的平衡吸附量具有较大的影响。铅离子浓度由400 mg/L增加到800 mg/L,平衡吸附量由589 mg/L随之增大到1426 mg/L。当铅离子浓度达到1000 mg/L时,平衡吸附量反而降到902 mg/L(图3)。
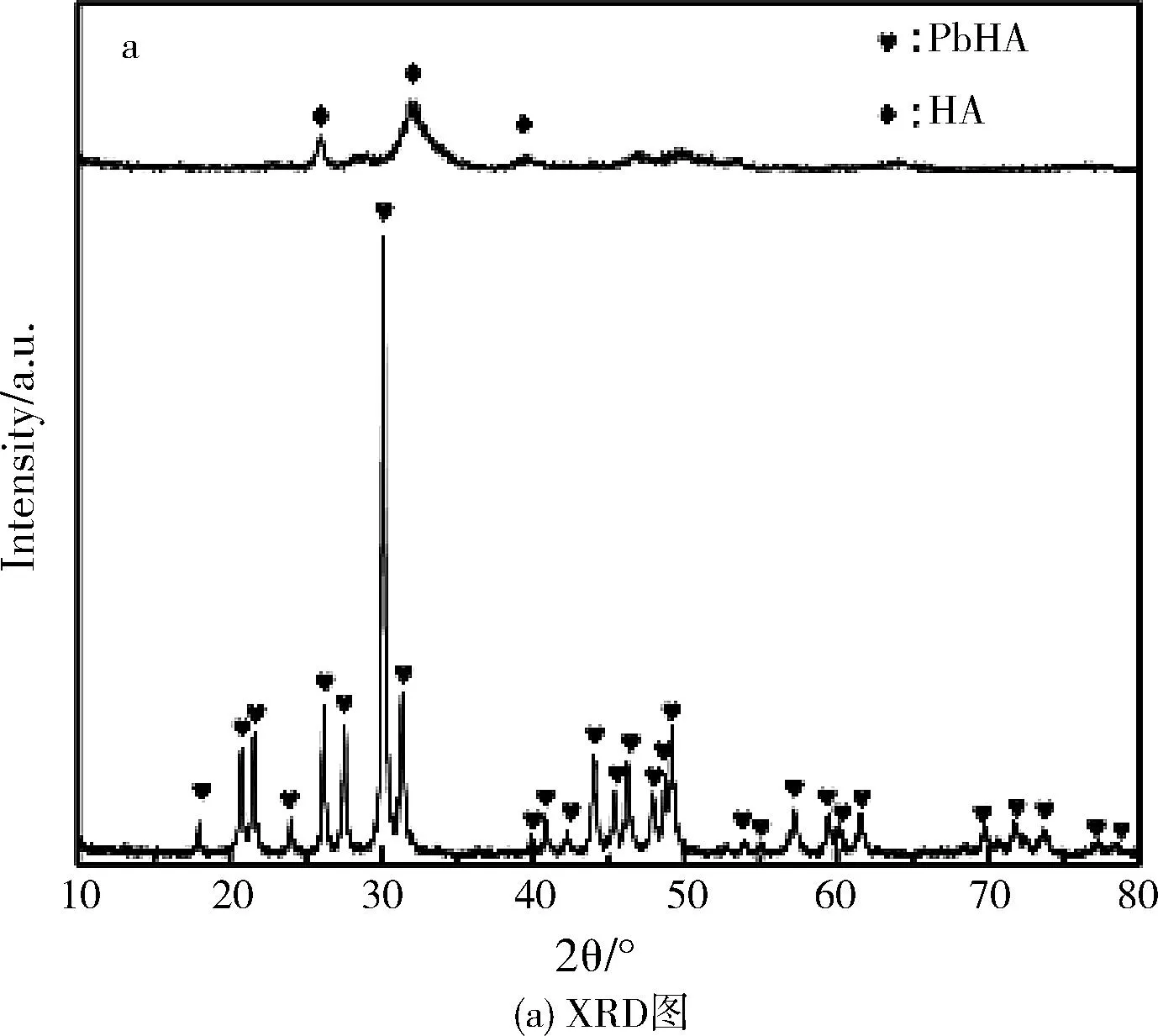
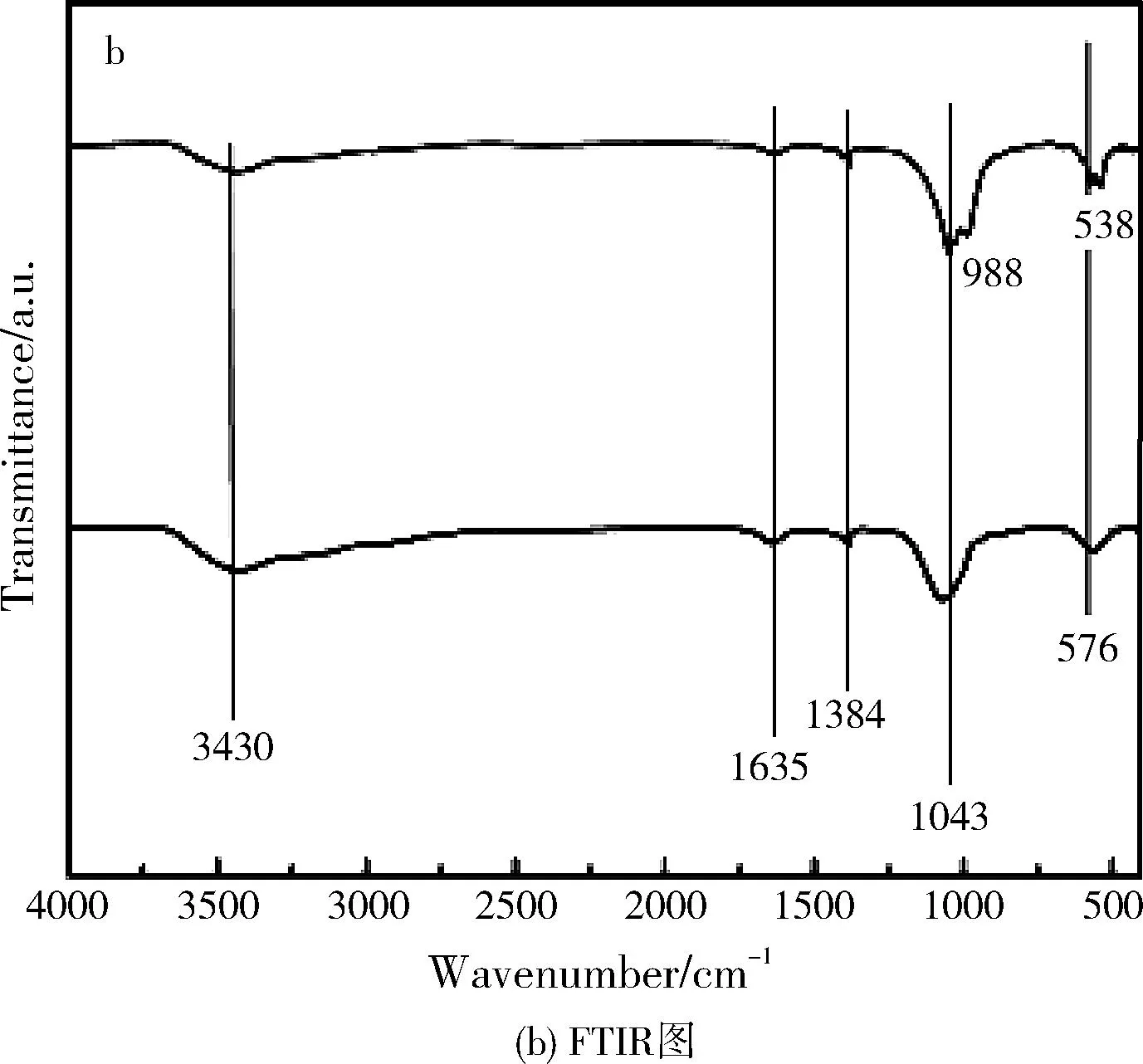
图4 纳米HA吸附铅离子前后的结构表征
图4为纳米HA对铅离子吸附前后的XRD图和FTIR图。由XRD图可知,HA纳米颗粒吸附后出现铅磷灰石(PbHA)晶体的特征衍射峰,而归属与HA的特征衍射峰强度减弱,甚至消失(图4a)。由FTIR图(图4b)可知,HA和PbHA具有相同的波谱特征,其原因取决于两种晶体拥有相同的官能团包括磷酸根和羟基。

图5 纳米HA在不同浓度铅离子溶液中吸附24 h后的SEM图
从SEM图中可以看出,HA纳米颗粒吸附铅离子24 h后,其形貌发生重大变化。由球形纳米颗粒转化成棒状颗粒物(图5)。从EDS图中可以看出Pb元素均匀分布在整个颗粒上,而Ca元素消失(图6)。根据XRD图、FTIR图和SEM图可知,HA纳米颗粒吸附铅离子的机理为溶解-沉积反应,HA颗粒在铅离子溶液中发生溶解反应,游离出的磷酸根离子与铅离子、氢氧根离子反应转化成PbHA颗粒。PbHA颗粒的沉积速率与溶液浓度呈现正向关系,浓度越高,则越有利于PbHA的沉积,因此随着铅离子浓度由400 mg/L增加到800 mg/L,平衡吸附量随之提高 (图7a)。但是,过高的铅离子浓度会导致PbHA的快速形核并包覆HA纳米颗粒物,抑制内部HA颗粒物的溶解,从而降低平衡吸附量(图5d和图7a)。

图6 纳米HA颗粒吸附铅离子后的面扫描图和EDS图
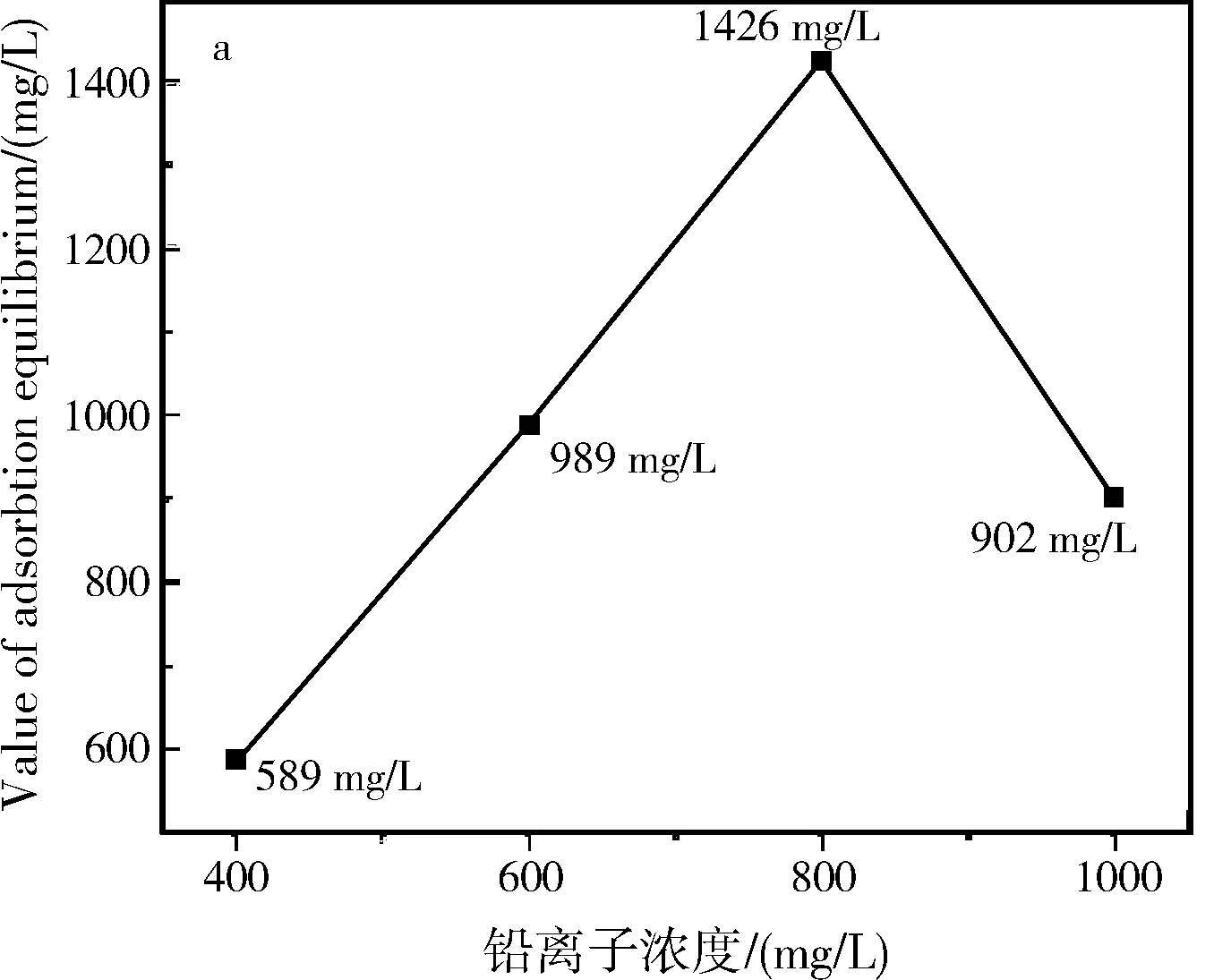
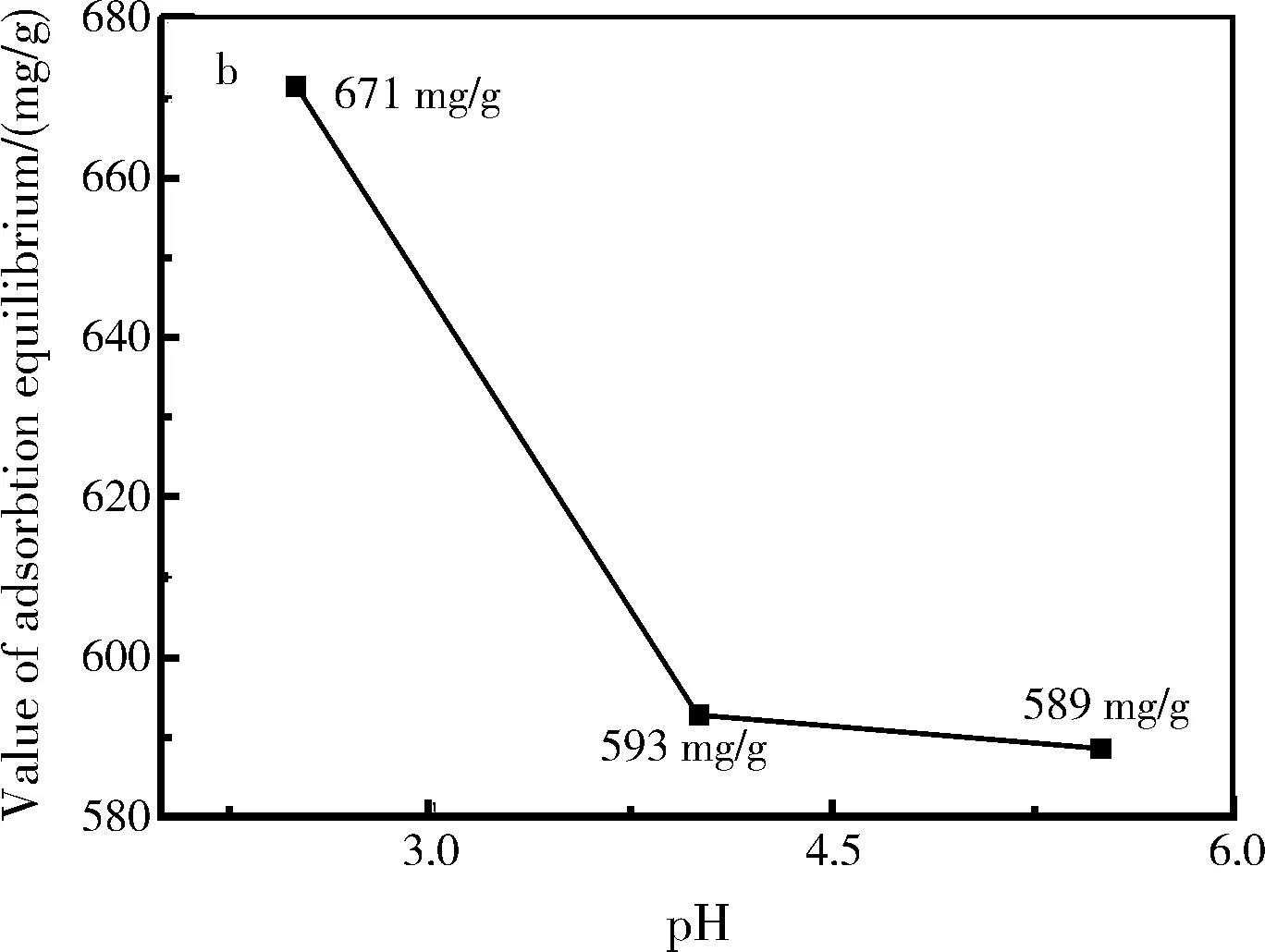

图7 纳米HA对铅离子的平衡吸附量曲线
此外,铅离子溶液的pH值和吸附温度对纳米HA颗粒的平衡吸附量也造成重大影响,如图7b和图7c所示。铅离子溶液的pH值越低,则平衡吸附量越高。当pH值由5.5降低到2.5时,铅离子的平衡吸附量则由589 mg/L增大到671 mg/L。其原因是:酸性条件下,HA溶解的速率加快,从而加快PbHA的沉积速率和沉积量。图7c为铅离子平衡吸附量与温度的关系曲线。随着吸附温度从20 ℃提高到40 ℃时,对应的平衡吸附量则由597 mg/L增大到667 mg/L。
基于上述分析可知:HA纳米颗粒对铅离子具有优良的吸附性能;HA纳米颗粒对铅离子吸附性能的影响因素包括溶液铅离子浓度、溶液pH值和吸附温度。铅离子浓度越高、pH值越小、吸附温度越高,则HA对铅离子的平衡吸附量越高。
3 结 论
(1)本文以矿渣微粉为原料制备出具有低结晶度的纳米HA颗粒,其平均直径约为50~80 nm;
(2)纳米HA颗粒对铅离子具有优良的吸附性能,其吸附机理为溶解-沉积反应。增大溶液铅离子浓度,降低溶液pH值和提高吸附温度均能够有效增大纳米HA颗粒的平衡吸附量;
(3)以矿渣为原料制备的纳米HA颗粒在吸附重金属离子领域具有宽阔的应用前景。
[1]Amini M, Younesi H, Bahramifar N. Statistical modeling and optimization of the cadmium biosorption process in an aqueous solution using Aspergillus niger [J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2009, 337(1-3): 67-73.
[2]Mureseanu M, Reiss A, Stefanescu I, David E, Parvulescu V, Renard G, Hulea V. Modified SBA-15 mesoporous silica for heavy metal ions remediation [J]. Chemosphere, 2008, 73(9): 1499-1504.
[3]Pounds JG, Long GJ, Rosen JF. Cellular and molecular toxicity of lead in bone [J]. Environmental Health Perspectives, 1991, 91: 17-32.
[4]Donat R, Akdogan A, Erdem E, Cetisli H. Thermodynamics of Pb2+and Ni2+adsorption onto natural bentonite from aqueous solutions [J]. Journal of Colloid and Interface Science, 2005, 286(1): 43-52.
[5]Bailey SE, Olin TJ, Bricka RM, Adrian DD. A review of potentially low-cost sorbents for heavy metals [J]. Water Research, 1999, 33(11): 2469-2479.
[6]Bhatnagar A, Minocha AK. Biosorption optimization of nickel removal from water using Punica granatum peel waste [J]. Colloids and Surfaces B: Biointerfaces, 2010, 76(2): 544-548.
[7]Sun XF,Liu CY, Ma Y,Wang SG,Gao BY,Li XM. Enhanced Cu(II) and Cr(VI) biosorption capacity on poly(ethylenimine) grafted aerobic granular sludge [J]. Colloids and Surfaces B: Biointerfaces, 2011, 82(2): 456-462.
[8]Stotzel C, Muller FA, Reinert F, Niederdraenk F, Barralet JE, Gbureck U. Ion adsorption behaviour of hydroxyapatite with different crystallinities [J]. Colloids and surfaces. B, Biointerfaces, 2009, 74(1):91-95.
[9]A Corami, Mignardi S, Ferrini V. Cadmium removal from single- and multimetal(Cd + Pb + Zn + Cu) solutions by sorption on hydroxyapatite [J]. Journal of Colloid and Interface Science, 2008, 317(2): 402-408.
[10]Xenidis A, Stouraiti C, Papassiopi N. Stabilization of Pb and As in soils by applying combined treatment with phosphates and ferrous iron [J]. Journal of Hazardous Materials, 2010, 177(1-3): 929-937.
[11]Walsh D, Furuzono T, Tanaka J. Preparation of porous composite implant materials by in situ polymerization of porous apatite containing ε-caprolactone or methyl methacrylate [J]. Biomaterials,2011, 22(11):1205-1212
[12]Chen W, Long T, Guo YJ, Zhu ZA, Guo YP. Magnetic hydroxyapatite coatings with oriented nanorod arrays: hydrothermal synthesis, structure and biocompatibility [J]. Journal of Materials Chemistry B, 2014, 2(12): 1653-1660.
Fabrication and Pb2+Ions Adsorption of Hydroxyapatite Nanoparticles Using Slag Powders as Raw Materials
FENG Yu-tao
(Baosteel Development Co., Ltd., Shanghai 201999, China)
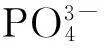
hydroxyapatite nanoparticles; Chemical adsorption; lead ions
封羽涛(1986-),男,毕业于北京大学,宝钢发展技术中心主任助理(主持工作),主要研究固废循环综合利用。
X592
A
1001-9677(2016)014-0113-04

