常压碳热还原含铟渣中三氧化二铟的动力学
谢富春,尹周澜,丁治英,谭 军,刘常青,张平民
(1. 中南大学 化学化工学院,长沙 410083;2. 湖南工程学院 机械工程学院,湘潭 411101)
常压碳热还原含铟渣中三氧化二铟的动力学
谢富春1, 2,尹周澜1,丁治英1,谭 军1,刘常青1,张平民1
(1. 中南大学 化学化工学院,长沙 410083;2. 湖南工程学院 机械工程学院,湘潭 411101)
在常压下研究碳热还原氧化铟的动力学。结果表明:增大碳与含铟渣的质量比或提高反应温度,铟还原率增大。当反应温度为 1523 K,碳与含铟渣质量比为 0.5、反应时间为 60 min时,含铟渣铟的还原挥发率达到85.21%;在常压下,碳与含铟渣质量比达到0.5,含铟渣平均粒度是80μm,石墨颗粒平均度约为30μm,反应温度在1373~ 1523 K区间内,碳热还原含铟渣的还原挥发速率由界面化学反应所控制,其表观活化能为168.67 kJ/mol。
碳热还原;含铟渣;动力学;铟;熔池熔炼
在铅锌冶炼废渣中含有大量铅锌金属、黑色金属以及多种稀贵金属。作为稀贵金属之一的铟,在这些铅锌矿的冶炼过程中逐步富集。通过对含铟渣中铟的物相分析发现,大部分铟主要是以 In2O3的形式存在[1]。因此,可以通过还原挥发的方法将含铟渣中的铟还原挥发出来。而在In-C-O体系中,碳还原三氧化二铟的过程中主要包括三氧化二铟与碳热直接发生还原反应(1)、间接还原反应(2)以及碳的气化反应(3)等反应过程。
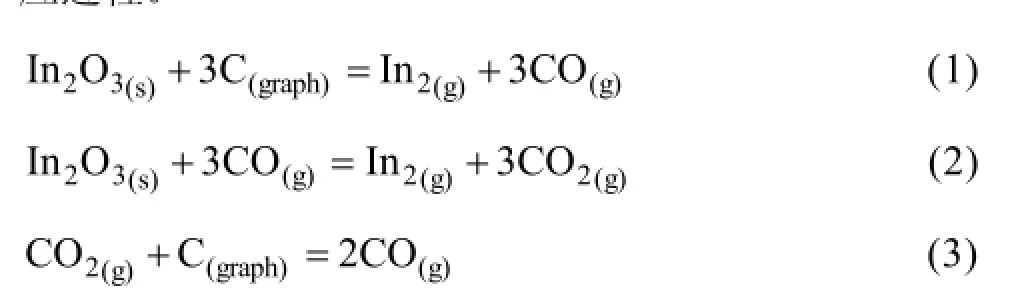
关于从各种富铟渣中回收铟的研究已有较多报道[2-4],如罗虹霖等[5]针对含有多种有价金属的还原挥发氧化锌烟尘,对各元素的挥发特性进行热力学计算,实验室回转窑挥发和中试试验,验证铟镉铅选择性挥发效果,获得高铟物料和脱除氟氯的高锌焙砂的工艺路线;宁顺明等[6]根据从黄钾铁矾渣中回收锌铟的焙解条件,采用热分析法确定黄钾铁矾渣焙解的温度范围,对焙解前后黄钾铁矾渣中的锌、铁进行物相分析,得出铁酸锌的转化率与焙解温度和时间之间的关系,从而获得回收铟的工艺参数;吕伯康等[7]在高温条件下进行锌浸出渣高温挥发富集铟锗的实验,得到锌浸出渣高温挥发富集铟的工业参数;吴文伟等[8]对回转窑火法还原挥发富集火法炼铅锑弃渣中的铟及其他有价金属进行热力学分析,计算出渣中相关化合物最低还原温度及蒸气压与温度的关系表明了工艺的可行性。这些都是通过热力学分析计算或者实验来证明相关工艺参数是可行的,工艺性或工程性的意识比较强,而针对三氧化二铟的还原动力学研究文献较少。
本文作者在考虑常压下碳热还原含铟渣的还原挥发机理及其产物的可能性的基础上,主要引进时间变量(或时间因素),考察碳与含铟渣的质量比对铟还原率的影响、反应温度对铟还原率的影响,从而可以求算出反应速率,运用动力学模型分析还原率对时间的关系,确定含铟渣还原挥发过程的控制步骤,计算出碳热还原含铟渣反应的活化能,从而获得常压下碳热还原氧化铟的相关动力学参数,为含铟渣的处理提供理论依据。
1 实验
1.1 实验原料
实验所用二氧化硅、三氧化二铁、硫化亚铁和氧化钙均为分析纯,西陇化工股份有限公司生产,三氧化二铟分析纯和石墨粉均为国药集团化学试剂有限公司提供,石墨平均粒径约为30μm。
实验采用的原料为平均粒度是 80μm的自制原料,根据某冶炼公司的沉铁渣成分以及 FeO-SO2-CO系三元相图进行沉铁渣的熔炼配制,其主要成分的配置比为 m(Fe)/m(SiO2)=1.2、m(CaO)/m(SiO2)=0.6,该渣系熔点低于1200 ℃[9],将In2O3按照一定配比加入渣中,采用XRF分析该含铟渣中各元素的含量(见表1)。
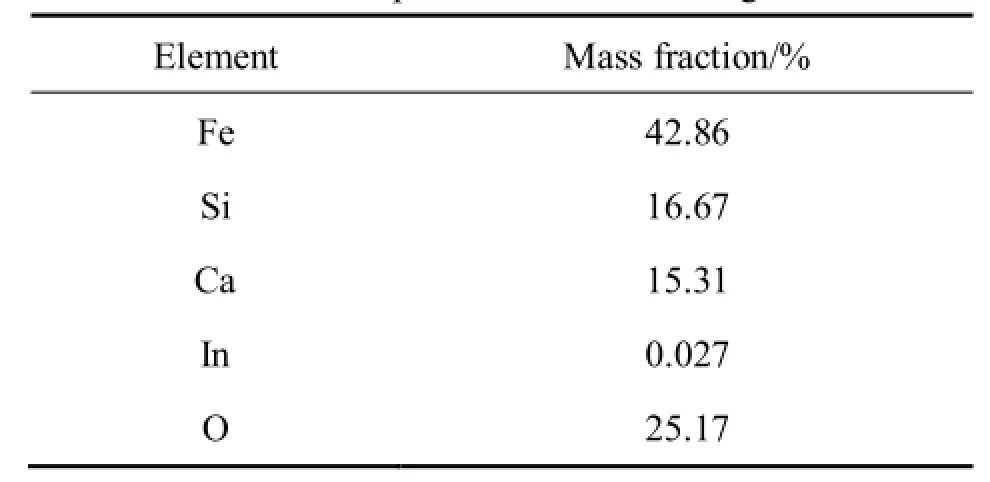
表1 含铟渣的化学成分Table 1 Chemical composition of In oxide slag
1.2 实验设备
实验主要设备为长沙科辉炉业有限公司生产的SG-6-16Q升降式高温气氛炉(见图1),其配套的智能温控柜型号为RSY-12-T。采用快速升降炉,能够保证熔融物瞬间降温,形成玻璃体混合物;当含铟渣中的铟被还原预定的时间后,在瞬间下降过程中,通氮气保护还原出来的铟以防铟再次氧化。

图1 SG-6-16Q升降式高温气氛炉Fig. 1 SG-6-16Q automatic elevator shaft high temperature experimental furnace
1.3 实验过程
将含铟渣和石墨粉按照一定的比例混合置于刚玉坩埚中,升降炉升温到一定温度后,放置刚玉坩埚。当炉温达到试验温度时开始计时,反应结束后,通入氮气,打开升降炉瞬间冷却,取出被还原后的含铟渣,以分析渣中铟的含量。
1.4 分析方法
采用电感耦合等离子体发射光谱法(ICP-OES)分析含铟渣中铟和钙的含量。分析仪器为全谱直读发射光谱仪,型号SPECTROBLUE SOP(德国生产),波长范围165~770 nm,CCD检测器。
2 结果与分析
铟的还原率α按式(4)进行计算。

考虑到反应过程中的样品有质量损失,但由于体系中CaO没有被还原,且刚玉坩埚中Al2O3在本试验温度区间(1373~1523 K)稳定存在,几乎不与CaO发生反应,即使考虑刚玉坩埚或者其他物质与氧化钙反应,其反应产物不挥发,不会有Ca的损失,所以,Ca在体系中的质量保持不变。因此,可以用Ca作为参照对象来计算反应后样品中剩余的铟质量,具体见式(5)。
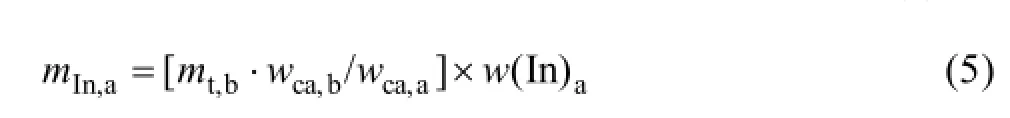
式中:mIn,b为试样中初始铟的质量;mIn,a为试样产物铟的质量;w(In)a为试样产物铟的质量含量;mt,b为试样反应前总质量;wCa,b为试样中初始钙的质量含量;wCa,a为反应产物钙的质量含量。
2.1 碳热还原含铟渣的热力学分析
在碳热还原 In2O3过程中,还可能存在以下几个反应。

廖春发等[10]分析和讨论反应(6)、(7)进行的可能性。反应(6)能够自发进行的温度是 1780 K,反应(7)能够自发进行的温度是1417 K,当温度低于1831 K时,反应(7)比反应(6)更容易进行;在可能的还原条件下,In2O3以还原成液态金属铟为主。张银堂等[11]研究反应(6)、(8)和(9)进行的可能性,当T>974 K时,反应(8)比反应(6)更容易进行;当T>800 K时 ,反应(9)比反应(8)更容易进行。
因此,In2O3还原挥发的主要产物是 In2(g)和In2O(g)。当773 K<T<1529 K时,pIn2(g)>pIn2O(g);当T>974 K时,C和CO相比较,In2O3更容易被前者还原,In2O3被还原为In2(g)比还原为In2O(g)容易。
炉渣中铟的挥发还原程度取决于单质In2(g)及In2O(g)的蒸汽压的大小,其中张银堂等[11]已经推算出该体系中In2(g)和In2O(g)的分压和温度的关系如式(10)和式(11)。
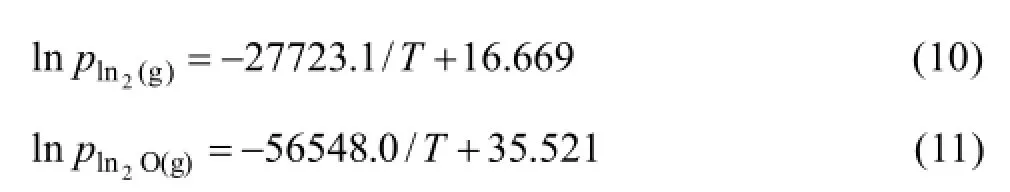
因此,依据式(10)和(11),In-C-O体系中 In2(g)和In2O(g)分压和温度的关系如图2所示。和关系图

图2 In-C-O体系的
由图2 可知,在In-C-O体系中,随着温度的升高,In2(g)和In2O(g)分压逐步增大;当温度低于1529 K时,In2(g)的分压大于 In2O(g)的分压,因此,该体系中的还原产物主要是In2(g)。
2.2 碳与含铟渣的质量比对铟还原率的影响
当系统压强为1.01×105Pa,温度为1523 K时,在碳与含铟渣的质量为 0.2~0.6时进行实验。不同碳与含铟渣的质量比对含铟渣中铟还原率的影响见图3。总体来说,随着碳渣质量比增大,铟还原率增大。由于碳渣质量比较高时,熔体中C含量高,增加了C 与In2O3和CO2接触面积,使式(1)和式(3)的界面反应向正方向进行,利于更多CO的生成,从而使得铟还原速率提高。在同一碳渣质量比的前提下,随着反应时间的延长,呈现出铟的还原率先增大而后缓慢增加的趋势。由图3 可知,在1.01×105Pa、1523 K、反应时间大于60 min的反应条件下,铟的还原率趋于某一个稳定值。这与文献[12]中对氧化铟还原研究较一致。
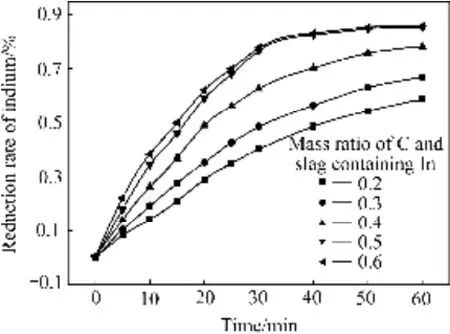
图3 碳与含铟渣的质量比对铟还原率的影响Fig. 3 Effect of mass ratio of C and slag containing In on reduction rate of In
2.3 反应温度对铟还原率与反应速率的影响
图4所示为碳与含铟渣的质量比为0.5、系统压强为1.01×105Pa时,利用自制的含铟渣、石墨作还原剂,温度在1373~1523 K之间,还原温度对渣中铟的还原率的影响。但从图4可知,在反应时间小于30 min时,不同反应温度同一时刻下的还原率对时间的微分(dα/dt—即反应速率)随温度升高而增大。即温度升高,含铟渣中铟的还原率与反应速率提高较快。如在温度低于1423 K时,含铟渣中铟的还原率与反应速率明显提高较慢,但当温度高于1473 K时,含铟渣中的铟的还原率与反应速率明显提高较快。

图4 反应温度对铟还原率的影响Fig. 4 Effect of reaction temperature on reduction ratio of In
2.4 动力学分析
综上所述,常压下碳还原含铟渣体系的反应为
(1)、(2)和(3),这3个反应都涉及到固/气的界面化学反应过程和气体的扩散过程。下面分别应用动力学模型处理还原率对时间关系的数据,从而判断过程的控制步骤。
2.4.1 界面化学反应步骤控制时的动力学模型的应用若含铟渣还原为界面化学反应控制,则动力学方程可由Mckwan方程(12)表达[13],即有

根据Mckwan方程,利用不同温度下的还原率对时间关系数据,可得到1-(1-α)1/3与时间t的关系曲线及其线性相关性如图5所示。

图5 不同温度下 1 - (1-α)1/3与时间t的关系曲线Fig. 5 Relationship between 1 - (1-α)1/3and time (t) at different reaction temperatures
由图5可见,在温度1373~1523K范围内,数据的线性关系比较好,表明还原过程很可能受界面反应步骤控制[14-15]。
2.4.2 扩散步骤控制时的动力学模型应用
若含铟渣还原为气相扩散控制,且扩散符合菲克(Fick)定律,则动力学方程可分别用杨德尔(Jander)方程(13)和金斯特林格(Ginstling)方程(14)来表示,即有
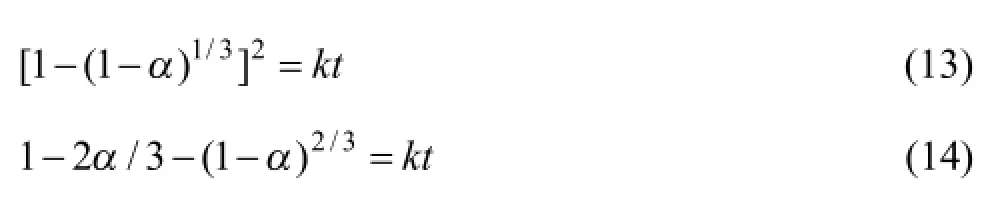
根据式(13)和(14),利用不同温度下还原率对时间关系数据,可以得到[1-(1-α)1/3]2或1-2α/3-(1-α)2/3与时间t的关系曲线如图6所示。
由图6可知,当温度为1473 K和1523 K时,即温度比较高时,数据的线性关系不太好,而在低温时,数据的线性关系却比较好。按照通常的规律,高温时,应该是扩散步骤控制,这一反常现象充分表明还原过程不受扩散步骤控制,而受界面反应步骤控制。同时,当温度为1373~1523 K时,图5中数据的线性相关性明显好于图6中数据的线性相关性,更加能表明还原过程受界面反应步骤控制[16-17]。
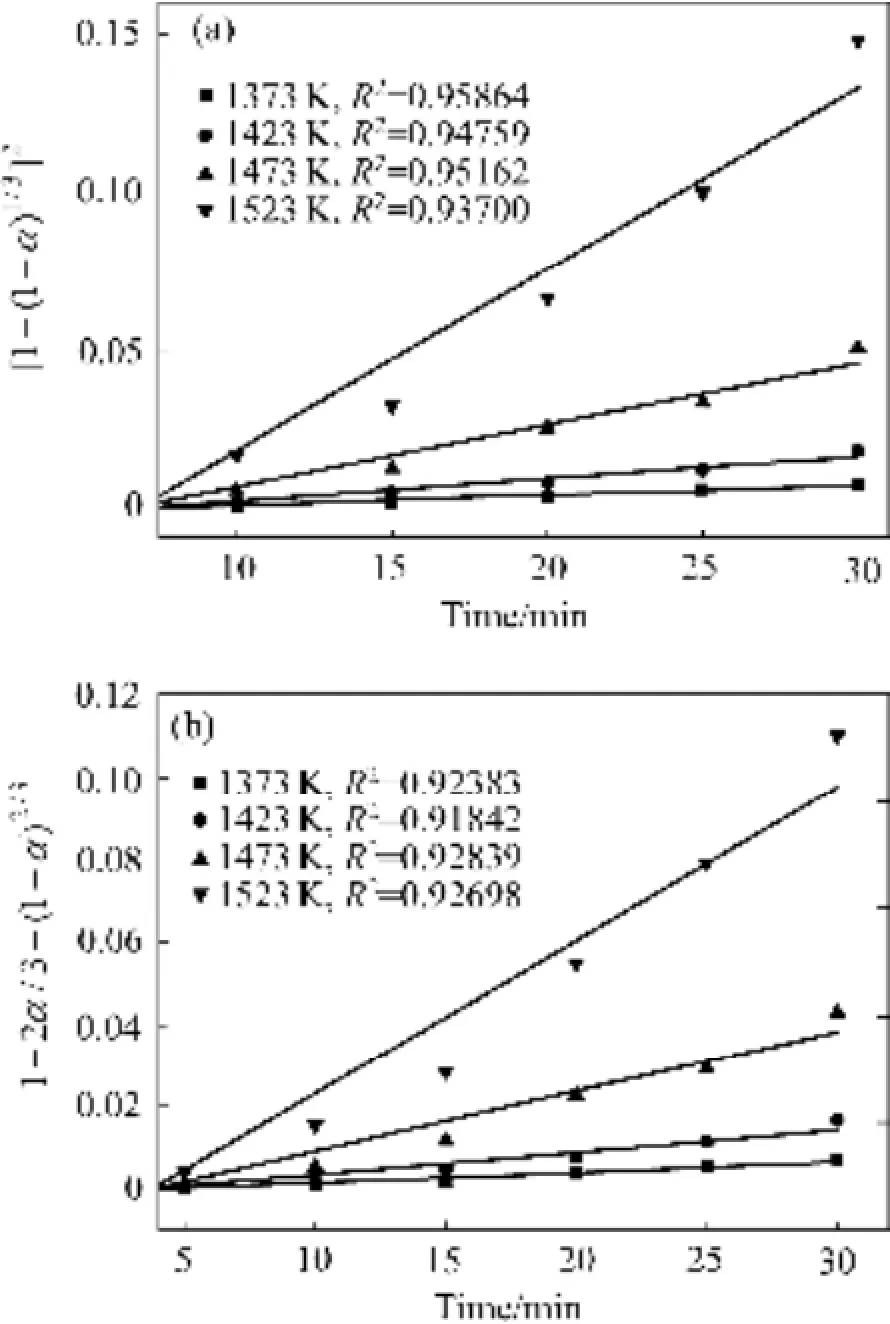
图6 不同温度下 [1- (1-α)1/3]2和 1-2α /3-(1-α)2/3与时间t的关系曲线Fig. 6 Relationships among [1- (1-α)1/3]2(a),1-2α /3-(1-α)2/3(b) and time (t) at different reaction temperatures
2.4.3 活化能计算
由上面分析可知,常压下碳热还原含铟渣反应温度在1373~1523 K时,界面化学反应是还原过程的控制步骤。因此,可以利用图5所示数据,即各直线的斜率视为在1373 K、1423 K、1473 K和1523 K温度下的表观反应速率常数(严格意义讲是表观速率常数与这些直线的斜率直接相关),然后根据Arrhenius经验方程的一般形式: lnk=lnA-E/(RT)得到-lnk与1/T关系的回归方程及反应的活化能[18](见表2)。
由表2可知,常压下碳热还原含铟渣,碳与含铟渣的质量比为0.5,系统压强为标准大气压,渣的粒度为 80μm,石墨的粒度平均为 30μm,反应温度为1373~1523 K时,还原反应速率是由界面化学反应所控制,其表观活化能为168.67 kJ/mol。
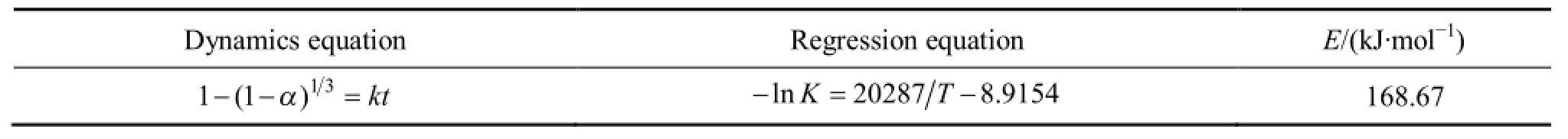
表2 碳热还原含铟渣的表面反应活化能Table 2 Estimated activation energy of surface reaction of carbothermal reduction of In bearing residue
3 结论
1) 碳与含铟渣质量比越大,还原反应速率越大;反应温度愈高,铟的还原反应速率愈大,铟的还原挥发的有效总压力愈大。当反应温度达到1523 K,碳与含铟渣质量比达到0.5,反应时间为60 min时,含铟渣中铟的还原挥发率达到85.21%。
2) 在常压下,当碳与含铟渣质量比达到 0.5,含铟渣平均粒度约是 80μm,石墨颗粒平均度约为 30μm,反应温度在1373~1523 K,碳热还原含铟渣的还原速率是由界面化学反应所控制,其表观活化能为168.67 kJ/mol。
REFERENCES
[1]ФEOPOB Д И, AКЧPИH P X. 铟化学手册[M]. 张启运, 徐克敏, 译. 北京: 北京大学出版社, 2005: 150-165. ФEOPOB Д И, AКЧPИH P X. Indium chemical handbook[M]. ZHANG Qi-yun, XU Ke-min, transl. Beijing: Beijing University Press, 2005: 150-165.
[2]周智华, 莫红兵, 徐国荣, 唐安平. 稀散金属铟富集与回收技术的研究进展[J]. 有色金属, 2005, 57(1): 71-76. ZHOU Zhi-hua, MO Hong-ging, XU Guo-rong, TANG An-ping. Progress in indium and pre-concentration technology[J]. Nonferrous Metals, 2005, 57(1): 71-76.
[3]刘大春, 杨 斌, 戴永年, 杜国山, 唐万启, 韩 龙. 从富铟渣提取金属铟的研究[J]. 稀有金属, 2005, 29(4): 574-577. LIU Da-chun, YANG Bin, DAI Yong-nian, DU Guo-shan,TANG Wan-qi, HAN Long. Extracting indium metal from Indiums enriched slag[J]. Chinese Journal of Rare Metals, 2005,29(4): 574-577.
[4]王树楷. 铟的应用与提取进展[J]. 中国工程科学, 2008, 10(5): 85-94. WANG Shu-kai. Progress of extraction and application of indiun[J]. Chinese Engineering Science, 2008, 10(5): 85-94.
[5]罗虹霖, 刘 维, 覃文庆, 刘瑞增, 郑永兴, 杨 康, 韩俊伟.氧化锌烟尘中铟的挥发富集[J]. 中国有色金属学报, 2014,24(11): 2892-2899. LUO Hong-lin, LIU Wei, QIN Wen-qing, LIU Rui-zeng,ZHENG Yong-xing, YANG Kang, HAN Jun-wei. Volatilization of indium from zinc oxide fly ash[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(11): 2892-2899.
[6]宁顺明, 陈志飞. 从黄钾铁矾渣中回收锌铟[J]. 中国有色金属学报, 1997, 7(3): 56-58. NING Shun-ming, CHEN Zhi-fei. Recovery of zinc and indium from jarosite residues[J]. The Chinese Journal of Nonferrous Metals, 1997, 7(3): 56-58.
[7]吕伯康, 刘 洋. 锌渣浸出渣高温挥发富集铟锗试验研究[J].南方金属, 2007, 156(3): 7-9. LÜ Bo-kang, LIU Yang. An experimental study of the enrichment of indnun and germaniun via high temperature volatilization of zinc residue[J]. Southern Metals, 2007, 156(3): 7-9.
[8]吴文伟, 赖水彬, 廖 森. 还原挥发富集火法炼铅锑渣中铟及其他有价金属的热力学分析[J]. 有色金属, 2008, 60(1): 67-70. WU Wen-wei, LAI Shui-bin, LIAO Sen. A thermodynamic analysis enriching Indium and other valuable matals pyrometallurgical slag via reduction-volatilization[J]. Nonferrous Metals Engineering, 2008, 60(1): 67-70.
[9]李洪桂, 冶金原理[M]. 北京: 科学出版社, 2005: 32-42. LI Hong-gui. Metallurgy principle[M]. Beijing: Science Press,2005: 32-42.
[10] 廖春发, 聂华平, 王秀红. 基夫塞特工艺中铟的富集规律和机理探讨[J]. 中国有色冶金, 2006(4): 29-34. LIAO Chun-fa, NIE Hua-ping, WANG Xiu-hong. An approach to enrichment law and mechanism of indium in the KIVCET process[J]. China Nonferrous Metallurgy, 2006(4): 29-34.
[11] 张银堂, 陈志飞, 宁顺明. In2O3还原挥发的热力学计算[J]. 中国有色金属学报, 2002, 12(3): 592-595. ZHANG Yin-tang, CHEN Zhi-fei, NING Shun-ming. Thermodymical calculation of deoxidization and volatilization of In2O3[J]. The Chinese Journal of Nonferrous Metals, 2002, 12(3): 592-595.
[12] 沈丽娟, 吴克明, 高耀文. 用还原挥发法从铁铟渣中回收铟的试验研究[J]. 湿法冶金, 2013, 32(1): 35-36. SHEN Li-juan, WU Ke-ming, GAO Yao-wen. Study on recovery of indium from In-Fe by reduction volatilization[J]. Hydrometallurgy of China, 2013, 32(1): 35-36.
[13] MEZ-BAREA G, LECKNER B, PERALES A L V, CAMPOY M. Analytical solutions of sharp interface models with nth order kinetics. Application to char conversion[J]. Chemical Engineering Journal, 2012, 183(4): 408-421.
[14] 隋丽丽, 翟玉春. 硫酸氢铵焙烧高钛渣反应动力学[J]. 中国有色金属学报, 2014, 24(2): 542-546. SUI Li-li, ZHAI Yu-chun. Kinetics on reaction of roasting high titanium slag with ammonium bisulfate[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(2): 542-546
[15] 潘自维, 王大卫, 杜 浩, 陈 刚, 郑诗礼, 王少娜, 张 懿.活性炭强化钒渣中钒、铬提取技术[J]. 中国有色金属学报,2014, 24(8): 2171-2180. PAN Zi-wei, WANG Da-wei, DU Hao, CHEN Gang, ZHENG Shi-li, WANG Shao-na, ZHANG Yi. Extraction technology of vanadium and chromium from vanadium slags in presence of activated carbon[J]. The Chinese Journal of Nonferrous Metals,2014, 24(8): 2171-2180.
[16] TJANDRA D, LADE M, WAGNER O, SCHOM01CKER R. The kinetics of an interfacial reaction in a microemulsion[J]. Chemical Engineering & Technology, 1998, 21(8): 666-670.
[17] 李 鹏, 毕学工, 张慧轩, 周进东. 武钢球团矿还原反应动力学[J]. 钢铁研究学报, 2015, 27(11): 8-13. LI Peng, BI Xue-gong, ZHANU Hui-xuan, ZHOU Jin-dong. Reduction kinetics of pellets from Wuhan Iron and Steel Corporation[J]. Journal of Iron and Steel Research, 2015, 27(11): 8-13.
[18] CAIRO C A A, FLORIAN M, GRA M L A, CCEDIL,BRESSIANI J C. Kinetic study by TGA of the effect of oxidation inhibitors for carbon-carbon composite[J]. Materials Science and Engineering A, 2003, 358(1/2): 298-303.
(编辑 李艳红)
(编辑 李艳红)
Atmospheric carbon thermoreduction kinetics of In2O3of slag containing In
XIE Fu-chun1, 2, YIN Zhou-lan1, DING Zhi-ying1, TAN Jun1, LIU Chang-qing1, ZHANG Ping-min1
(1. College of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China;2. Department of Mechanical Engineering, Hunan Institute of Engineering, Xiangtan 411101, China)
The kinetics of atmospheric carbothermic reduction of indium oxide slag was investigated. The results indicate that the reduction volatilization ratio of indium increases with the quality ratio of mass ratio of C and slag containing In or the reaction temperature increasing, the highest indium reduction 85.21% was realized under the condition of the mass ratio of C and slag containing In of 0.5 at 1523 K after 60 min. The interface reaction is the controlling step of the overall reduction process and the activation energy is estimated to be 168.67 kJ/mol when the mass ratio of C and slag containing In is o.5, the average size of slag is 80μm, the average size of graphite is 30μm and the reaction temperature is from 1273 to 1523 K.
carbon thermoreduction; indium oxide slag; kinetics; indium; bath smelting
Project(2011AA061003) supported by the National High Research Development Program of China
date: 2015-08-25; Accepted date: 2016-01-19
DING Zhi-ying; Tel: +86-731-88879616; E-mail: zy.ding@csu.edu.cn
TF843.1;TD983
A
1004-0609(2016)-06-1350-06
国家高技术研究发展计划资助项目(2011AA061003)
2015-08-25;
2016-01-19
丁治英,讲师;博士;电话:0731-88879616;E-mail: zy.ding@csu.edu.cn

