无机碳对SNAD工艺硝氮积累问题恢复的影响
李 冬,田海成,梁瑜海,苏庆岭,张 杰,2
(1.水质科学与水环境恢复工程北京市重点实验室(北京工业大学),北京 100124;2.城市水资源与水环境国家重点实验室(哈尔滨工业大学),哈尔滨 150090)
无机碳对SNAD工艺硝氮积累问题恢复的影响
李冬1,田海成1,梁瑜海1,苏庆岭1,张杰1,2
(1.水质科学与水环境恢复工程北京市重点实验室(北京工业大学),北京 100124;2.城市水资源与水环境国家重点实验室(哈尔滨工业大学),哈尔滨 150090)
摘要:为研究充足的无机碳对同步亚硝化-厌氧氨氧化与反硝化(SNAD)工艺的恢复与稳定运行的影响,向硝酸盐氮积累而崩溃的SNAD反应器中投加过量无机碳,对反应器的运行情况进行研究.结果表明:在无机碳质量浓度为理论需要量的350%~410%的条件下运行36 d后,出水硝酸盐氮由12.1 mg/L下降至3.47 mg/L,特征比由2.31升高至20.77;继续投加无机碳至理论需要量的200%~310%,运行42 d后,总氮去除负荷由0.176 g/(L·d)升高至0.299 g/(L·d);投加无机碳前后,好氧氨氧化活性(AOR,RAO)与厌氧氨氧化活性(ANR,RAN)分别由0.061 4和0.040 6 g/(g·d)升高至0.081 1和0.065 9 g/(g·d).结果表明,充足的无机碳投加在有效解除SNAD工艺硝酸盐氮积累问题的同时,可以促进好氧氨氧化菌(AOB)和厌氧氨氧化菌(AnAOB)的活性.
关键词:同步亚硝化-厌氧氨氧化与反硝化工艺;无机碳;好氧氨氧化菌;厌氧氨氧化菌;亚硝酸盐氧化菌
同步亚硝化-厌氧氨氧化与反硝化工艺(simultaneous partial nitrification, anaerobic ammonium oxidation and denitrification,SNAD)(反应式(3))是在全程自养脱氮工艺(completely autotrophic nitrogen removal over nitrite,CANON)(反应式(1))的基础上,引入异养反硝化(反应式(2)),即
0.01C5H7NO2+0.028CH2O0.5N0.15,
(1)
(2)
0.49N2+1.05H2CO3+3.31H2O+0.017C5H7NO2+
0.028CH2O0.5N0.15,
(3)
从而实现自养厌氧氨氧化菌和异养反硝化菌耦合脱氮的新型工艺.解决了传统全程硝化反硝化工艺能源消耗量高、需外加有机碳源、污泥产量高等问题,也解决了CANON工艺出水硝酸盐氮含量高(理论上占氨氮去除量的11%)、无法去除有机物的缺点,成为研究热点.目前,SNAD工艺已经在污泥消化液、垃圾渗滤液、养猪废水、光电废水、化工废水等高温、高氨氮废水处理领域得到应用[1-5],并且实现了较高的总氮去除率和总氮去除负荷.对于城市生活污水处理,国际上研究的主流趋势是采用厌氧消化与SNAD的工艺流程实现脱氮除碳,该工艺可有效提高污水处理厂的能源自给率[6],然而,目前关于将SNAD工艺应用于城市生活污水领域的研究报道很少.在SNAD工艺运行过程中,常常面临由于亚硝酸盐氧化菌(NOB)活性升高致使出水硝酸盐氮积累的难题,同时有机物的存在会抑制好氧氨氧化菌(AOB)和厌氧氨氧化菌(AnAOB)的活性,导致AOB缺乏溶解氧,AnAOB缺乏足够的基质亚硝酸盐氮,使得AnAOB的竞争优势逐渐被反硝化菌取代直至系统崩溃[3, 7].当SNAD系统向全程硝化反硝化途径转变时,采用常规手段难以有效恢复[4, 8-10].
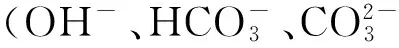
1实验
1.1实验装置
实验采用由有机玻璃精加工而成的SBR反应器(如图1),有效容积5.4 L,高100 cm,内径9 cm.底部安装直径为7 cm的微孔曝气环,使用气泵和气体流量计控制表观气速为0.091 7 cm/s,反应器内溶解氧为0.1~1.0 mg/L.反应器内部安装搅拌机,转速为150 r/min.反应器通过水浴控制在(30±1)℃.pH、DO、温度通过在线测定仪监测.
1、2、3、4分别为进水、排水、搅拌、曝气时序控制器;5、6分别为pH、DO测定仪;7为机械搅拌机;8为微孔曝气环;A、B、C分别为控制进水、排水、曝气的电磁阀
图1实验装置示意
Fig.1Laboratory reactor
1.2实验水质与污泥
实验前,反应器在生活污水中稳定运行,出水达一级A标准.但由于仪器故障等原因导致反应器内NOB大量增殖,出水硝酸盐氮大幅增加,系统脱氮性能显著下降.本实验在前期运行的基础上,对反应器的脱氮性能进行恢复.初始污泥质量浓度2.74 g/L,污泥粒径305.6 μm.
整个实验过程以某大学生活小区化粪池出水为原水(水质见表1,对于其他氨氮质量浓度的生活污水,可以通过调节容积交换率的方式,使得各反应周期初始氨氮质量浓度与本实验相近).反应器采用间歇运行模式,容积交换率为50%,每周期包括进水(3 min)、反应(反应时间根据周期实验结果确定)、沉淀(5 min)、排水(2 min)等4个阶段.每周期结束后,洗泥3次以去除上一周期反应结束残留的物质.实验共进行91 d,分为崩溃阶段、恢复阶段、稳定运行3个阶段.其中崩溃阶段完全以生活污水为进水,恢复阶段和稳定运行通过外加NaHCO3的方式提高无机碳质量浓度.各阶段参数见表2.

表2 实验各阶段水质及操作参数
注:无机碳理论需要量根据反应式(3)计算,无机碳理论上需要的质量浓度为氨氮质量浓度的90%.
1.3分析项目与方法
NH4+-N:纳氏试剂分光光度法;NO2--N:N-(1-萘基)-乙二胺分光光度法;NO3--N:紫外分光光度法;COD:5B-3B型COD测定仪;粒径:Mastersize2000型激光粒度仪;MLSS:重量法;TIC:非色散红外吸收TOC测定仪;DO、pH、t:WTW在线测定仪.脱氮途径计算时依据模型[8, 19-20]假定:1)硝化过程氧化的NH4+-N全部转化为NO2--N;2)厌氧氨氧化过程消耗的NH4+-N与NO2--N比为1∶1.32,同时每消耗1 mg/L NH4+-N生成0.26 mg/L NO3--N,生成的NO3--N可用于反硝化;3)反硝化过程每消耗1 mg/L NO3--N需要消耗2.86 mg/L的COD(模型假设中未考虑细胞合成作用).涉及的计算公式如下:

总氮去除量
Δρ(TN)=ρinf(TN)-ρeff(TN),
反硝化途径氮去除量


厌氧氨氧化途径氮去除量
Δ2=Δρ(TN)-Δ1,

好氧氨氧化活性
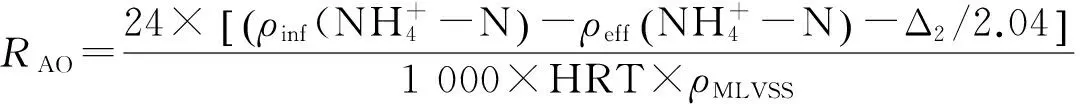
厌氧氨氧化活性

特征比
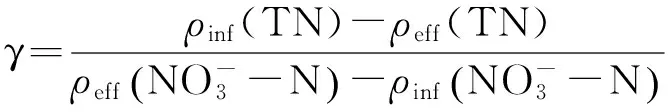

表观气速
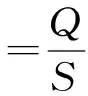
式中:ρinf(NH4+-N)、ρinf(NO2--N)、ρinf(NO3--N)分别表示进水氨氮、亚硝酸盐氮和硝酸盐氮质量浓度,mg/L;ρeff(NH4+-N)、ρeff(NO2--N)、ρeff(NO3--N)分别表示出水氨氮、亚硝酸盐氮和硝酸盐氮质量浓度,mg/L;HRT为水力停留时间,h;ρMLVSS为挥发性固体悬浮物质量浓度,g/L;Q为曝气量,cm3/s;S为反应器横截面积,cm2.
2结果与讨论
实验采用的反应器前期曾在生活污水条件下稳定运行,但是由于实验室仪器故障未对反应器的运行状况进行监测,待故障排除后反应器出水硝酸盐氮大幅升高,总氮去除负荷降低,若不及时恢复SNAD系统将向全程硝化反硝化路径转变.仪器故障排除后反应器经历了崩溃阶段(I)、恢复阶段(II)以及稳定运行阶段(III)3个过程.各反应周期开始前氨氮质量浓度始终维持在40 mg/L左右, COD维持在90 mg/L左右.
2.1投加无机碳前后SNAD反应器脱氮除碳性能的变化
投加无机碳前后SNAD反应器运行效果如图2所示.从仪器故障排除后的第1~13天为崩溃阶段,此阶段完全以生活污水为进水基质,反应开始前无机碳质量浓度介于30~50 mg/L(图2(c)).第1~5天,依然按照先前的参数运行反应器,设置HRT为100 min(图2(d)),发现总氮去除率仅为23.9%(图2(a)),COD去除率为45%(图2(b)),出水无机碳质量浓度约10 mg/L;为提高总氮去除率,在第6~13天将HRT延长至190 min.由于反应时间的增加,总氮去除率也随之升高至53.0%,COD去除率升高至65%,但是作为自养菌细胞合成碳源的无机碳质量浓度已经不足5 mg/L,这可能会影响自养菌的脱氮效果.接下来的第14~49天为恢复阶段,在生活污水中投加100 mg/L的无机碳以促进AOB和AnAOB的活性,从而逐渐形成AOB和AnAOB对NOB的竞争优势,并将NOB淘汰出反应器.投加无机碳后的第15~28天,总氮去除率迅速由53.2%升至69.7%,总氮去除负荷也由崩溃阶段的0.178 g/(L·d)升至0.224 g/(L·d);随后的第29~49天缩短HRT至160 min以继续提高总氮去除负荷,至第49天结束时总氮去除负荷已达0.299 g/(L·d),总氮去除率达73.9%,COD去除率为61%.此阶段反应周期结束时,反应器内始终保持着40 mg/L以上的无机碳质量浓度,以避免无机碳源缺乏对反应器脱氮性能的限制.第50~91天为稳定运行阶段,将外加无机碳质量浓度降为60 mg/L,研究降低无机碳质量浓度后反应器能否稳定运行.此阶段,反应器出水无机碳始终保持在25 mg/L以上,反应器的脱氮除碳效果稳定,通过不断降低HRT以提高总氮去除负荷,最终在HRT=150 min的情况下,总氮去除率达74.9%, COD去除率为51%,总氮去除负荷达0.307 g/(L·d).目前已有应用于高氨氮废水领域的SNAD工艺(见表3),本实验无需高氨氮淘洗NOB,而是借助于高无机碳所形成的AOB对于NOB的竞争优势,实现了SNAD反应器在低氨氮条件下的稳定运行,且实现了较高的总氮去除负荷和总氮去除率.

图2 投加无机碳前后SNAD反应器运行效果
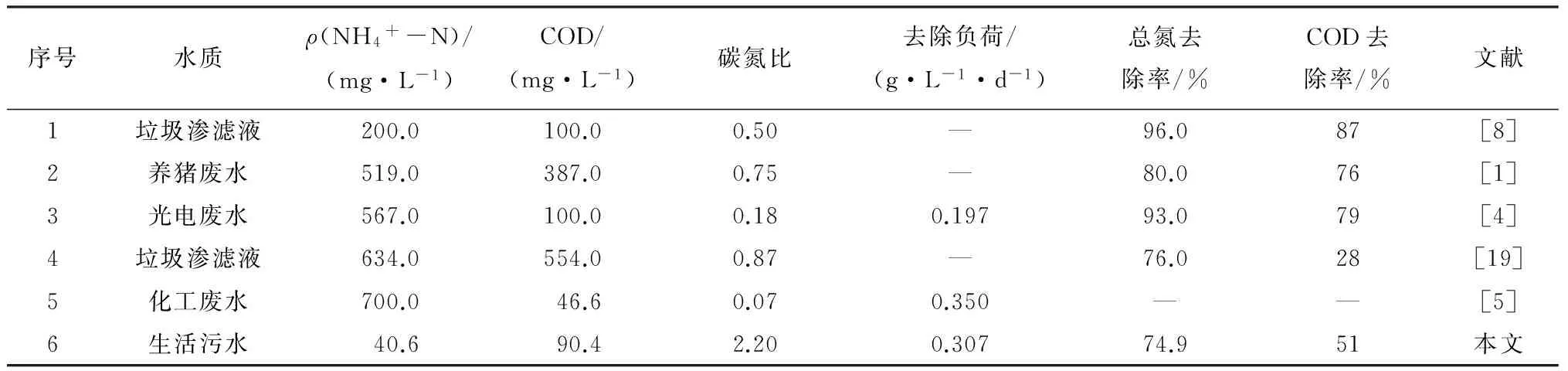
序号水质ρ(Nh1+-N)/(mg·L-1)COD/(mg·L-1)碳氮比去除负荷/(g·L-1·d-1)总氮去除率/%COD去除率/%文献1垃圾渗滤液200.0100.00.50—96.087[8]2养猪废水519.0387.00.75—80.076[1]3光电废水567.0100.00.180.19793.079[4]4垃圾渗滤液634.0554.00.87—76.028[19]5化工废水700.046.60.070.350——[5]6生活污水40.690.42.200.30774.951本文
2.2无机碳对SNAD反应器内各菌群活性的影响
异养菌在降低SNAD出水硝氮过程中有重要作用,但是影响异养菌活性的主要因素是COD与氮比,而实验过程中COD与氮比几乎不变,因此,反硝化菌对于SNAD脱氮性能的提升影响不大.无机碳对于SNAD系统的影响主要是AOB、NOB以及AnAOB等自养菌的活性.
2.2.1无机碳对AOB和NOB的影响
实验期间AOR的变化如图3所示.阶段Ⅰ中进水无机碳仅为30~50 mg/L(为理论需要量的80%~130%),致使出水无机碳不足,AOB的活性受到限制, AOR平均值仅为0.061 4 g/(g·d),AOR较低导致亚硝化过程受阻,氨氮转化率仅为68.2%(图4),中间产物亚硝酸盐氮生成量不足,无法为厌氧氨氧化反应提供足够的基质,这将严重制约反应器的脱氮效果.阶段II中将无机碳源质量浓度升高至120~150 mg/L(为理论需要量的350%~410%),AOB的活性得到提高,平均值升至0.073 7 g/(g·d),氨氮转化率也随之升至78.3%.阶段Ⅲ中降低无机碳源质量浓度至90~110 mg/L(为理论需要量的250%~310%),由于出水中依然保有25 mg/L以上的无机碳,AOB活性依然很高,AOR平均值达0.081 1 g/(g·d),氨氮转化率也升至83.1%,反应器脱氮效果稳定.Guisasola A等[14]的研究表明,无机碳对于AOB活性的影响服从莫诺方程式,而无机碳对于NOB的活性几乎无影响.因此,利用无机碳对于AOB和NOB活性影响的差异,通过供给充足的无机碳促进AOB的活性,以形成AOB对NOB的竞争优势,从而将NOB不断淘汰使得硝化反应控制在亚硝酸盐氮阶段.

图3 无机碳对各菌群活性的影响
出水硝酸盐氮和特征比可以有效揭示反应器内的NOB是否大量繁殖.阶段Ⅰ,反应器出水硝酸盐氮质量浓度平均值高达9.63 mg/L,占出水总氮的55%(图5),特征比(图3)平均为2.18,表明无机碳质量浓度不足时,反应器内的AOB活性较低,无法形成对于NOB的竞争优势,导致出水硝酸盐氮大幅升高.阶段II,随着充足无机碳的加入,出水硝酸盐氮不断下降至5.23 mg/L,仅占出水总氮的33%,仅仅36 d内特征比快速升高至20以上,表明AOB活性的升高导致其对于NOB的竞争优势不断增强,使得出水硝酸盐氮大幅减少.阶段Ⅲ,继续保持充足的无机碳质量浓度,在HRT=150 min情况下,反应器出水硝酸盐氮进一步降低至2.89 mg/L,特征比最终稳定在20左右并持续运行31 d,由此表明反应器在长期充足无机碳条件下运行后,AOB对NOB的竞争优势使得NOB被淘洗出反应器.

图4 无机碳对氨氮去除效果的影响

图5 无机碳对出水硝氮的影响
阶段Ⅰ中游离氨质量浓度平均为0.41 mg/L,阶段II与Ⅲ中游离氨质量浓度平均分别为0.54和0.31 mg/L,而Anthonisen A C等[21]认为游离氨对NOB抑制而对AOB不抑制的范围是1~10 mg/L,因此,游离氨在NOB淘汰过程中的作用并不大;此外,整个实验期间温度和表观气速维持稳定,对于NOB活性的影响并不大.反应器性能恢复前后,只有无机碳质量浓度的增加,表明充足无机碳对于SNAD工艺中NOB的有效抑制具有显著作用.Ma Yiwei等[22]在无机碳质量浓度为理论需要量350%时实现了对NOB的有效抑制,当无机碳质量浓度降为理论需要量40%时,反应器内NOB大量繁殖,总氮去除率由78%下降至46%,经过长时间的恢复,系统内依然存有较高比例的NOB,上述实验结果进一步证明了无机碳对于形成AOB对NOB竞争优势的重要作用.相关研究[23-26]表明,亚硝化过程是整个脱氮过程的限制步骤,通过投加无机碳以提高AOB活性有助于降低亚硝化反应对于整个脱氮过程的限制作用,从而提高总氮去除能力.
2.2.2无机碳对AnAOB的影响
实验期间ANR的变化如图3所示.阶段Ⅰ中由于无机碳质量浓度较低,限制了AnAOB的活性,ANR平均值仅为0.040 6 g/(g·d);阶段II与Ⅲ中,随着无机碳的加入,ANR的平均值分别升高至0.051 5和0.065 9 g/(g·d).AnAOB活性的升高使得其与异养菌竞争基质的能力提升,有利于减轻反应器内COD对于自养菌活性的抑制,维持自养菌在反应器内的竞争优势.Yang Jiachun等[15]通过向厌氧氨氧化反应器中投加充足的无机碳,使得短短32 d内总氮去除负荷由5.2 g/(L·d)迅速升高至11.8 g/(L·d).廖德祥[27]在厌氧氨氧化反应器中研究了无机碳对于AnAOB的影响,结果表明,无机碳为1.0 g/L时,AnAOB活性受到抑制,氨氮和亚硝酸盐氮去除率仅为41.6%和46.2%,当无机碳升高至1.5 g/L时,氨氮和亚硝酸盐氮去除率迅速提高至83.6%和100%.上述研究成果均进一步表明无机碳对于AnAOB活性的促进作用.
2.3无机碳对SNAD工艺恢复与稳定运行的意义
实现SNAD工艺稳定运行的关键在于将硝化反应控制在亚硝酸盐氮阶段,即抑制NOB的活性,避免短程硝化反应向全程硝化方向转变.对于如何抑制NOB的活性,研究者们主要采用高游离氨(FA)或亚硝酸(FNA)、低溶解氧或高温等手段,但是以上方法在实际应用中均有其局限性:如高游离氨依赖于较高的氨氮质量浓度和较高的温度,常温低氨氮时难以实现,而且微生物会对游离氨产生适应性[28];可以利用AOB比NOB对氧亲和力强的特点,采用低溶解氧实现AOB对NOB的竞争优势,但是低溶解氧也同时限制了AOB的活性,导致氨氧化率降低;高温需要消耗巨大的能源,对于实际污水处理并不现实.对NOB长久有效抑制策略的缺失,导致SNAD工艺在实际运行中出水硝酸盐氮不断增加进而崩溃的现象时有发生,且采用常规手段难以迅速有效地恢复[4, 8-10, 29].
本实验在低氨氮条件下通过投加充足的无机碳抑制NOB,实现了生活污水SNAD工艺的恢复与稳定运行(稳定运行阶段实际无机碳质量浓度为理论需要量的250%~310%).投加无机碳的恢复成本为0.9元/t水(NaHCO3价格以1 300元/t计);采用投加高氨氮恢复方式的成本为1.45元/t水(按游离氨质量浓度提高至10 mg/L计,(NH4)2SO4价格以1 100元/t计);采用高温恢复方式的成本为9.2元/t水(按水温升高10 ℃计算,电费按0.8元/(kW·h)计).显然与高游离氨或高温的恢复方式相比,投加无机碳的恢复方式可以省去投加高氨氮造成的恢复费用,还可以大幅削减恢复过程中排入水体的氮负荷以及因加热水体而造成的巨大能源消耗.鉴于高游离氨、高温、低溶解氧等抑制策略在常温低氨氮污水处理领域的局限性,通过供给充足的无机碳实现AOB对NOB的竞争优势,继而将NOB淘洗的策略对于SNAD工艺应用于实际工程具有一定的经济价值和环保效益.
3结论
1)向由于NOB增殖、出水硝酸盐氮升高而导致崩溃的SNAD反应器中投加无机碳,使得实际无机碳质量浓度为理论需要量的250%~410%.经78 d的恢复与稳定运行,总氮去除率由53%升高至75%,总氮去除负荷由0.176 g/(L·d)升至0.299 g/(L·d),表明充足的无机碳有利于提高反应器的去除能力.
2)投加无机碳前后,好氧氨氧化活性(AOR)与厌氧氨氧化活性(ANR)分别由0.061 4和0.040 6 g/(g·d)升至0.081 1和0.065 9 g/(g·d),表明无机碳可以有效促进AOB和AnAOB的活性.
3)在无机碳质量浓度为理论需要量的350%~410%的条件下运行36 d后,出水硝酸盐氮由12.1 mg/L下降至3.47 mg/L,特征比由2.31升高至20.77,表明充足的无机碳可以有效恢复由于出水硝酸盐氮升高而导致崩溃的SNAD系统.
参考文献
[1] DAVEREY A, HUNG N, DUTTA K, et al. Ambient temperature SNAD process treating anaerobic digester liquor of swine wastewater[J]. Bioresource Technology, 2013, 141: 191-198.
[2] XU Zhengyong, ZENG Guangming, YANG Zhaohui, et al. Biological treatment of landfill leachate with the integration of partial nitrification, anaerobic ammonium oxidation and heterotrophic denitrification[J]. Bioresource Technology, 2010, 101(1): 79-86.
[3] ZHANG Zhaoji, LI Yuanyuan, CHEN Shaohua, et al. Simultaneous nitrogen and carbon removal from swine digester liquor by the canon process and denitrification[J]. Bioresource Technology, 2012, 114: 84-89.
[4] DAVEREY A, SU S, HUANG Y, et al. Nitrogen removal from opto-electronic wastewater using the simultaneous partial nitrification, anaerobic ammonium oxidation and denitrification (SNAD) process in sequencing batch reactor[J]. Bioresource Technology, 2012, 113: 225-231.
[5] KELUSKAR R, NERURKAR A, DESAI A. Development of a simultaneous partial nitrification, anaerobic ammonia oxidation and denitrification (SNAD) bench scale process for removal of ammonia from effluent of a fertilizer industry[J]. Bioresource Technology, 2013, 130: 390-397.
[6] 彭永臻, 邵和东, 杨延栋, 等. 基于厌氧氨氧化的城市污水处理厂能耗分析[J]. 北京工业大学学报, 2015, 41(4): 621-627.
PENG Yongzhen,SHAO Hedong,YANG Yandong, et al. Energy consumption of the municipal wastewater treatment plant with anammox process[J]. Journal of Beijing University of Technology,2015,41(4):621-627.
[7] DU Rui, PENG Yongzhen, CAO Shenbin, et al. Advanced nitrogen removal with simultaneous anammox and denitrification in sequencing batch reactor[J]. Bioresource Technology, 2014, 162: 316-322.
[8] LAN C, KUMAR M, WANG C, et al. Development of simultaneous partial nitrification, anammox and denitrification (SNAD) process in a sequential batch reactor[J]. Bioresource Technology, 2011, 102(9): 5514-5519.
[9] JOSS A, DERLON N, CYPRIEN C, et al. Combined nitritation-anammox: advances in understanding process stability[J]. Environmental Science & Technology, 2011, 45(22): 9735-9742.
[10]CHO S, FUJII N, LEE T, et al. Development of a simultaneous partial nitrification and anaerobic ammonia oxidation process in a single reactor[J]. Bioresource Technology, 2011, 102(2): 652-659.
[11]张子健, 王舜和, 王建龙, 等. 利用碱度控制SBR中短程硝化反应的进程[J]. 清华大学学报(自然科学版), 2008, 48(9): 1475-1478.
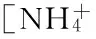
[12]陈建伟, 郑平, 陈小光, 等. 短程硝化过程碱度变化规律与控制对策研究[J]. 中国给水排水, 2011, 27(21): 105-108.
CHEN Jianwei,ZHENG Ping,CHEN Xiaoguang, et al. Study on change and control of alkalinity in SHARON process[J]. China Water & Wastewater, 2011, 27(21): 105-108.
[13]张肖静, 李冬, 周利军, 等. 碱度对常低温处理生活污水亚硝化的影响[J]. 哈尔滨工业大学学报, 2013, 45(4): 38-43.
ZHANG Xiaojing,LI Dong,ZHOU Lijun, et al. Effect of alkalinity on partial nitrification of domestic sewage at ordinary and low temperatures[J]. Journal of Harbin Institute of Technology, 2013, 45(4): 38-43.
[14]GUISASOLA A, PETZET S, BAEZA J A, et al. Inorganic carbon limitations on nitrification: experimental assessment and modelling[J]. Water Research, 2007, 41(2): 277-286.
[15]YANG Jiachun, ZHANG Li, FUKUZAKI Y, et al. High-rate nitrogen removal by the Anammox process with a sufficient inorganic carbon source[J]. Bioresource Technology, 2010, 101(24): 9471-9478.
[16]ZEKKER I, RIKMANN E, TENNO T, et al. Effect of concentration on anammox nitrogen removal rate in a moving bed biofilm reactor[J]. Environmental Technology, 2012, 33(20): 2263-2271.
[17]鲍林林, 茹祥莉, 郭守德, 等. 无机碳对厌氧氨氧化反应的影响[J]. 河南师范大学学报(自然科学版), 2013, 41(4): 90-93.
BAO Linlin,RU Xiangli,GUO Shoude, et al. Effect of inorganic carbon on anaerobic ammonia oxidation reaction[J]. Journal of Henan Normal University(Natural Science Edition) , 2013, 41(4): 90-93.
[18]李捷, 张杰, 周少奇. TOC与IC对厌氧氨氧化反应的影响研究[J]. 给水排水, 2008, 34(11): 157-160.
LI Jie,ZHANG Jie,ZHOU Shaoqi. Effect of TOC and IC on anaerobic ammonia oxidation reaction[J]. Water & Wastewater Engineering, 2008, 34(11): 157-160.
[19]WANG C, LEE P, KUMAR M, et al. Simultaneous partial nitrification, anaerobic ammonium oxidation and denitrification (SNAD) in a full-scale landfill-leachate treatment plant[J]. Journal of Hazardous Materials, 2010, 175(1/2/3): 622-628.
[20]李冬, 杨卓, 梁瑜海, 等. 耦合反硝化的CANON生物滤池脱氮研究[J]. 中国环境科学, 2014, 34(6): 1448-1456.
LI Dong,YANG Zhuo,LIANG Yuhai, et al. Nitrogen removal performance by CANON biological filtration with denitrification[J]. China Environmental Science,2014,34(6):1448-1456.
[21]ANTHONISEN A C, LOEHR R C, PRAKASAM T B S, et al. Inhibition of nitrification by ammonia and nitrous acid[J]. Water Pollution Control Federation, 1976,48(5): 835-852.
[22]MA Yiwei, SUNDAR S, PARK H, et al. The effect of inorganic carbon on microbial interactions in a biofilm nitritation-anammox process[J]. Water Research, 2015, 70: 246-254.
[23]SLIEKERS A O, DERWORT N, GOMEZ J L C, et al. Completely autotrophic nitrogen removal over nitrite in one single reactor[J]. Water Research, 2002, 36(10): 2475-2482.
[25]AHN Y, CHOI H. Autotrophic nitrogen removal from sludge digester liquids in upflow sludge bed reactor with external aeration[J]. Process Biochemistry, 2006, 41(9): 1945-1950.
[26]SLIEKERS A O, THIRD K A, ABMA W, et al. CANON and Anammox in a gas-lift reactor[J]. FEMS Microbiology Letters, 2003, 218(2): 339-344.
[27]廖德祥. 全程自养生物脱氮基础研究及其污泥颗粒化培养[D]. 长沙: 湖南大学, 2008.
LIAO Dexiang.Fundamental study of completely autotrophic nitrogen removal and its granulation in SBR reactor[D].Changsha: Hunan University,2008.
[28]DS M. Stability of nitrite build-up in an activated sludge system[J]. Water Pollution Control Federation,1989, 61(8):1440-1448.
[29]BLACKBURNE R, YUAN Zhiguo, KELLER J. Partial nitrification to nitrite using low dissolved oxygen concentration as the main selection factor[J]. Biodegradation, 2008, 19(2): 303-312.
(编辑刘彤)
doi:10.11918/j.issn.0367-6234.2016.08.003
收稿日期:2015-06-20
基金项目:北京市青年拔尖团队项目(2014000026833TD02)
作者简介:李冬(1976—),女,教授,博士生导师;
通信作者:李冬,lidong2006@bjut.edu.cn
中图分类号:X703.1
文献标志码:A
文章编号:0367-6234(2016)08-0017-07
Effect of inorganic carbon for sewage SNAD process nitrate accumulation restore problems
LI Dong1,TIAN Haicheng1,LIANG Yuhai1,SU Qingling1,ZHANG Jie1,2
(1.Key Laboratory of Beijing for Water Quality Science and Water Environment Recovery Engineering(Beijing University of Technology), Beijing 100124, China;2.State Key Laboratory of Urban Water Resource and Environment (Harbin Institute of Technology), Harbin 150090, China)
Abstract:In order to assess the impact of the inorganic carbon on the recovery and stability of SNAD process, excessive inorganic carbon was added to the SNAD reactor, which has collapsed due to the nitrate accumulation. The reactor was operated for 36 d under the conditions with a 370%-430% of theoretical inorganic carbon additive, and the effluent nitrate decreased from 12.1 mg/L to 3.47 mg/L under steady-state operation, simultaneously the feature ratio increased from 2.31 to 20.77. Then reduced the inorganic carbon additive to 260%-320% of the theoretical inorganic carbon concentration, the total nitrogen removal load increased from 0.176 g/(L·d) to 0.299 g/(L·d) after 42 d operation, the aerobic ammonia oxidation activity (AOR) and anaerobic ammonia oxidation activity (ANR) also increased from 0.061 4 g/(g·d) to 0.081 1 g/(g·d), and 0.040 6 g/(g·d) to 0.065 9 g/(g·d), respectively. Thus, sufficient inorganic carbon source not only released the problem of nitrate build-up, but also enhanced the activity of AOB and AnAOB.
Keywords:SNAD; inorganic carbon; AOB; AnAOB; NOB
张杰(1938—),男,博士生导师,中国工程院院士

