一种快速检测水体中氨氮含量的双波长光谱法
吴慧玲,胡湛波*,柴欣生,王 璀,杨瓯蒙
1.广西大学环境学院,广西 南宁 530004 2.华南理工大学制浆造纸工程国家重点实验室,广东 广州 510641
一种快速检测水体中氨氮含量的双波长光谱法
吴慧玲1,胡湛波1*,柴欣生2,王 璀1,杨瓯蒙1
1.广西大学环境学院,广西 南宁 530004 2.华南理工大学制浆造纸工程国家重点实验室,广东 广州 510641
氨氮是衡量地表水质量状况的重要指标之一。在现行的纳氏试剂分光光度法(HJ535—2009)检测氨氮含量过程中,水样预处理(絮凝沉淀法)、剩余浊度与仪器基线漂移等因素给检测过程带来不确定影响。据此,提出一种双波长(420和650 nm)光谱的改进方法,通过扣除由剩余浊度与仪器基线漂移引入的吸光度,以消除检测干扰。先确定水样在420 nm处的浊度修正系数k,后以420 nm处的吸光度减去650 nm处吸光度与k值的乘积,得到氨氮显色反应的净吸收值,从而实现对氨氮含量的准确定量检测,并对该方法的精确度与准确性进行评价。结果表明:在单波长法中,仅由絮凝沉淀法过滤过程引入的相对偏差可达8.67%,而双波长法无絮凝沉淀步骤,不受该偏差影响。双波长法5次重复实验的精度标准差低至1.58%,回收率在98.5~103%之间,因此更为准确、可靠。与现行的纳氏试剂分光光度法相比,该方法既省略了水样预处理的步骤,又扣除了剩余浊度的干扰,显著提高了实验的效率,特别适用于大批量地表水样中氨氮含量的快速检测。
氨氮; 纳氏试剂分光光度法; 双波长光谱法
引 言
氨氮是衡量水体富营养化程度的重要指标,也是水质监测分析的基本指标之一。目前,检测氨氮的主要方法有纳氏试剂分光光度法、苯酚-次氯酸盐光度法、气相分子吸收光谱法、电化学分析法等,其中,纳氏试剂分光光度法(HJ535—2009)因具有检测快速、操作简单、反应灵敏等特点,被广泛用于地表水中氨氮含量的测定[1-3]。然而,在实际检测过程中,这种方法容易受到实验因素(如实验环境、试剂的配制与保存、实验用水等)的影响,使检测结果与实际值相差较大,影响检测结果的可靠性与精确度。近年来,针对如何提高纳氏试剂分光光度法检测结果的准确性进行了许多的改进研究,主要集中于水样的预处理、纳氏试剂的使用量、氨氮标准溶液的配置方法与保存、标准曲线的绘制与操作过程、显色时间与温度等方面[4]。尽管以上研究在很大程度上减小了由于试剂和实验操作方面所引入的误差,但都忽略了剩余浊度与仪器本身基线漂移对检测结果的影响。另外,该法采用絮凝沉淀法对水样进行预处理步骤繁琐、耗时长,容易造成样品污染,不能快速准确检测氨氮的含量[5]。因此,为保证纳氏试剂光度法快速测定地表水中氨氮含量的准确性以达到国家相关检测部门的要求,对该方法提出改进尤为必要。
本文在纳氏试剂分光光度法(单波长法)测定氨氮含量的实验条件与步骤的基础上,探讨絮凝沉淀法、细小悬浮颗粒物与仪器基线漂移对氨氮检测过程产生的不确定性影响,提出了采用双波长光谱法[6-8]对纳氏试剂分光光度法进行改进的方法,并对该方法的精度与准确性进行评价。
1 实验部分
1.1 仪器与试剂
(1)仪器:岛津UV-1800型紫外-可见分光光度计。
(2)试剂的配置:
根据《水与废水监测分析方法》[1]中纳氏试剂分光光度法的标准步骤配置铵标准使用液(10 mg·L-1)、10%的硫酸锌溶液、25%氢氧化钠溶液、纳氏试剂、酒石酸钾钠溶液。
1.2 方法
(1)氨氮标准曲线的绘制
取铵标准使用液0.00,0.50,1.00,3.00,5.00,7.00和10.00 mL于50 mL比色管中,加无氨水稀释至标线,即可得浓度为0.00,0.10,0.20,0.60,1.00,1.40和2.00 mg·L-1的氨氮标准溶液。加1.0 mL酒石酸钾钠溶液,摇匀。加1.5 mL纳氏试剂,混匀,放置10 min后,用20 mm比色皿,以无氨水为参比,扫描全光谱,以420 nm处的吸光度绘制标准曲线。
(2)水样预处理
取100 mL水样于烧杯中,加入1.0 mL 10%硫酸锌溶液和0.1~0.2 mL 25%氢氧化钠溶液,调节pH至10.5左右,混匀,静置使沉淀,用经无氨水充分洗涤过的中速滤纸过滤,弃去前20 mL后所得溶液为预处理后的水样。
(3)单波长法测定水样中氨氮含量
取适量经过预处理后的水样于50 mL比色管中,稀释至标线,按上述氨氮标准曲线的测定步骤测定氨氮的吸光度,最后根据标准曲线计算氨氮含量。
(4)双波长法测定水样中氨氮含量
取适量不经过预处理的水样于50 mL比色管中,稀释至标线,加1.0 mL酒石酸钾钠溶液与加1.5 mL纳氏试剂,混匀,放置10 min后,用20 mm比色皿测定420和650 nm处的吸光度。根据建立的双波长法计算氨氮的含量。
2 结果与讨论
2.1 氨氮检测原理与标准曲线的建立
氨氮显色反应原理是碘化汞和碘化钾的碱性溶液与氨反应生成淡红棕色胶态化合物,此颜色在410~425 nm范围内具有强烈吸收,通常取420 nm处吸光度作为水样中氨氮的吸收值。根据纳氏试剂分光光度法(HJ535—2009)的操作步骤测得不同浓度的氨氮标准溶液(0~2.00 mg·L-1)对应的吸光度,同时扫描其全光谱,得到标准曲线如图1所示,氨氮的浓度与对应的吸光度呈正比关系,即符合Lamber-Beer定律。当需要检测干扰较少的水样氨氮浓度时,可以采用上述方法准确检测水样中氨氮的浓度。
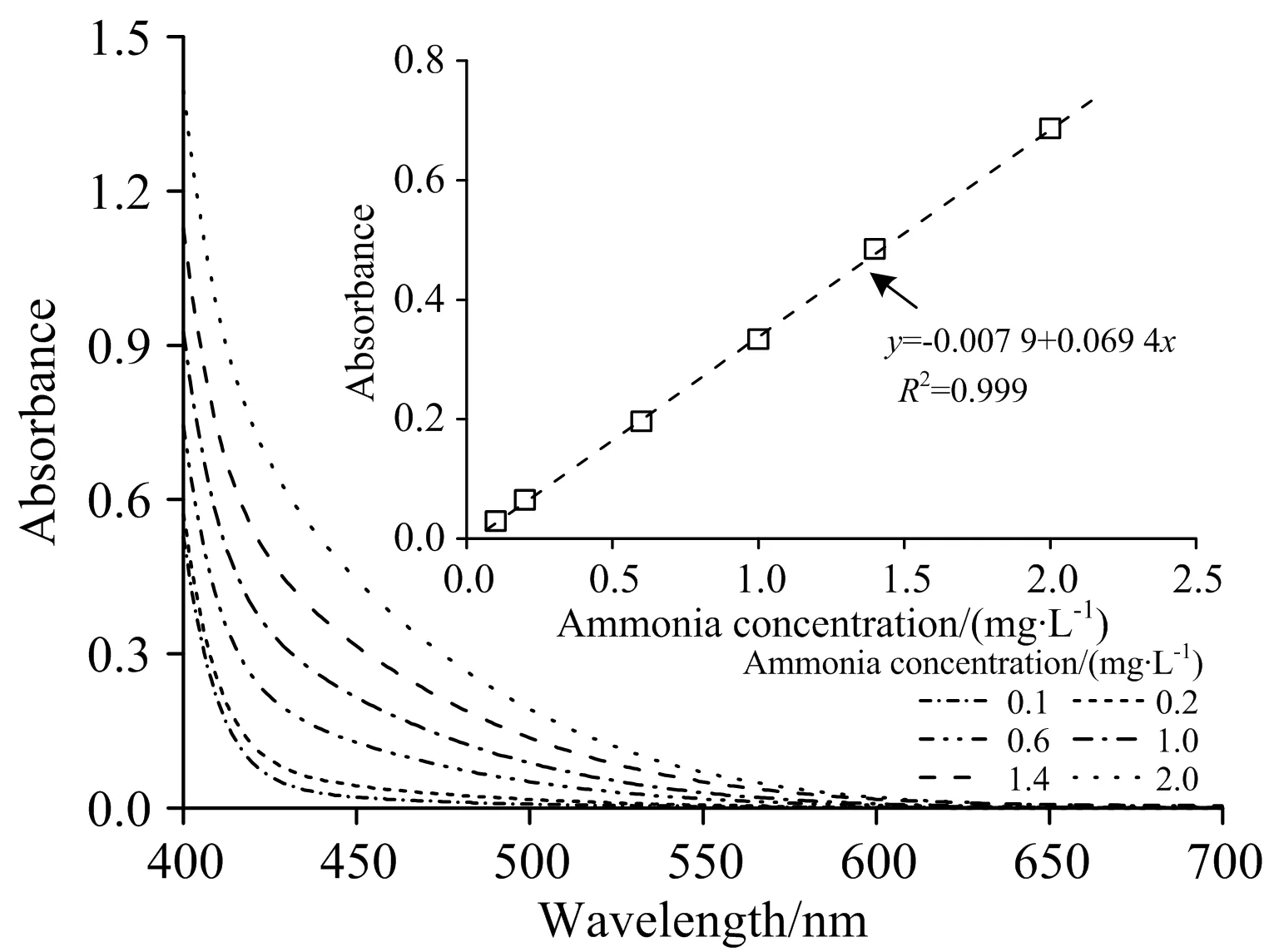
图1 氨氮标准溶液显色后的可见光谱
2.2 影响氨氮检测准确性的干扰因素
图2为不经过预处理与经过预处理的氨氮标准溶液(1-1,1-2)、实际水样(2-1,2-2)显色后的光谱图。由于地表水样来源成分复杂,水样中的有机化合物、无机离子、悬浮颗粒物等会产生浑浊或异色而引起干扰,通常采用絮凝沉淀法对污染程度较轻的水样进行预处理,但未能完全去除肉眼难以察觉的细小悬浮颗粒物质(剩余浊度),从而造成如图2内置图中水样由悬浮颗粒物质的光散射或吸收作用引起的基线显著上移,即使是空白溶液也难以避免该现象,给检测结果带来正偏差。同时,又因絮凝沉淀法过滤步骤所用中速滤纸中有少量铵盐溶出,导致所测水样中氨氮浓度普遍偏高,如图2中1-2在420 nm处的吸光度稍高于1-1。表2为采用市售5种不同品牌的滤纸分别过滤经絮凝沉淀后的标准溶液(1.00 mg·L-1)所测得的氨氮浓度值。相对误差在1.16%~8.67%之间,对低浓度氨氮的检测尤其不利。所以,采用絮凝沉淀法的预处理方式虽能消除大部分浊度影响但随之也带来误差,加之剩余浊度与基线漂移的影响,无疑将直接降低检测结果的准确性。因此,针对污染程度较轻的地表水样,可不进行水样预处理而直接采用以浊度的吸收波长为基准的双波长光谱法简化氨氮的检测步骤,以达到快速准确、节时省力的目的。
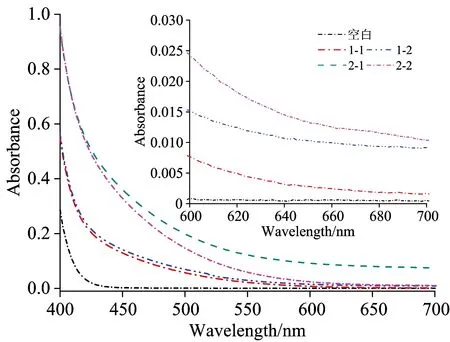
图2 水样显色后光谱

表1 不同品牌滤纸过滤后氨氮实测值
注:相对误差以标准浓度1.00 mg·L-1为基准计算。
2.3 双波长光谱法的建立与推导
从图2可以看出氨氮光谱从波长为640 nm后基线趋于稳定,所以本文选取650 nm处的吸光度表示浊度的吸收值。由于在420与650 nm处由浊度引起的吸光度的比值是一个恒定常数,为此,引入420 nm处浊度的修正系数k,即
(1)
式中:k为浊度修正系数;Aa, 420和Aa, 650分别为不同种类的水样在420与650 nm波长处的吸光度。
纳氏试剂分光光度法(HJ535—2009)单波长检测氨氮含量基于如下计算公式
A420=As, 420-Ad, 420
(2)
式中:As, 420和Ad, 420分别为试验水样、空白水样显色后420 nm波长处的吸光度。
将420 nm波长处的吸光度减去由浊度引起的吸光度,即可得出水样中氨氮的净吸光值。具体推导公式如下
(3)
(4)
式中:As, 650和Ad, 650分别为试验水样、空白水样显色后650 nm波长处的吸光度。
将式(3)和式(4)代入式(2)中可得
(5)
基于上述推导,获得水样中氨氮显色后的净吸光值,再代入由Lamber-Beer定律确定的氨氮标准工作曲线,经变形后水样中氨氮含量的计算公式可写为
(6)
式中:c氨氮为水样中氨氮的浓度,mg·L-1;a1和b1为氨氮标准工作曲线的斜率与截距;V1和V2为水样体积与定容体积,mL。
2.4 浊度修正系数k值的确定
k值可根据地表水的类型而确定。本文以广西大学校园内不同地点的生活污水为例,不加纳氏试剂直接测定其420与650 nm处的吸光度,代入式(1)中计算k值,结果如表2所示。各个水样的k值十分接近,其平均值为2.10。因此,可取2.10为计算所用浊度校正系数。
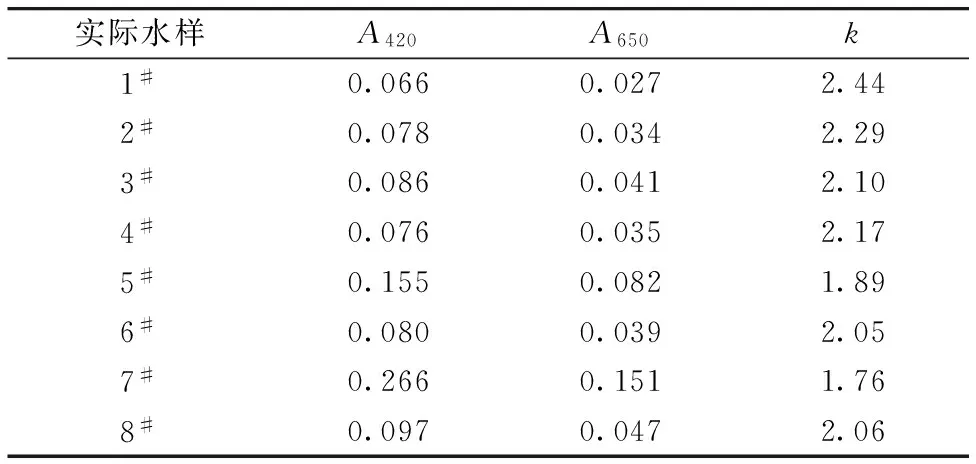
表2 不同水样的k值
2.5 方法的评价
2.5.1 方法的精度分析
为了验证双波长光谱法的精确度,在相同环境下按照单波长法与双波长法的实验步骤分别对同一水样重复测定5次,其k值为2.1,计算氨氮的含量与标准差。从表3可知,单波长法检测氨氮的含量大于双波长法,两种方法的标准差分别为7.09%和1.58%,说明双波长法的检测精度高于国标法。

表3 两种方法的精度比较
2.5.2 方法的准确性
为验证双波长法的准确性,将一系列氨氮标准溶液加入上述水样中,按照双波长法实验步骤对样品进行测定,并计算回收率,结果如表4所示,回收率在98.5%~103%之间,符合回收率的要求。因此,本方法完全可以实现氨氮检测的高准确性。
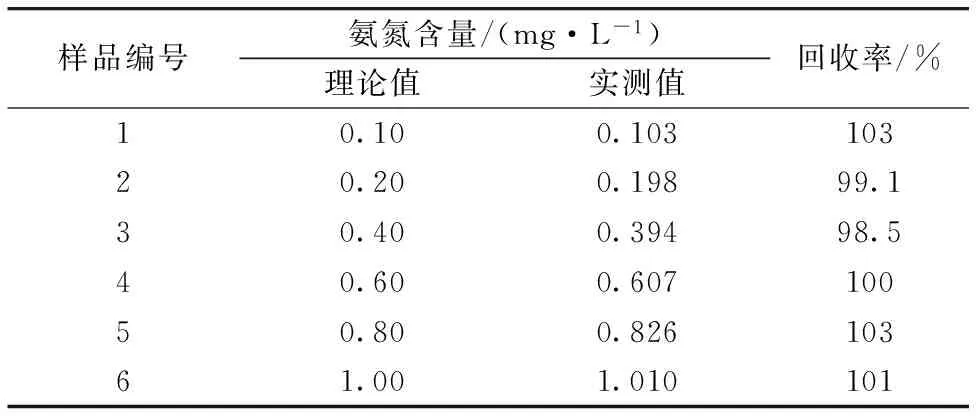
表4 方法的回收率
3 结 论
对纳氏试剂分光光度法检测氨氮过程中由絮凝沉淀法与剩余浊度引起的影响进行讨论,提出一种基于双波长光谱法的快速检测水样中氨氮含量的改进方法,并对方法的精确度及准确性进行评价。结果表明,该方法检测精度的标准偏差仅为1.58%,回收率在98.5%~103%之间,因此该方法不仅准确、可靠,同时还克服了水样预处理的缺陷,简化了操作过程,大大提高了检测效率,非常适用于地表水样中氨氮含量的批量化快速分析。
[1] National Environmental Protection Bureau(国家环境保护总局).Monitoring and Analysis Method of Water and Waster Water(Edition 4)(水和废水检测分析方法)(第4版).Beijing: China Standard Press(北京: 中国环境科学出版社), 2002.276.
[2] Sonia Senra-Ferreiro, Francisco Pena-Pereira, Isabel Costas-Mora.Talanta, 2011, 85(3): 1448.
[3] Shoji T, Nakamura E.Analytical Sciences,2010, 26(7): 779.
[4] FU Jiao-feng, CHEN Shi-jian, ZHANG Ting(傅娇凤, 陈世俭, 张 婷).Environmental Science & Technology(环境科学与技术),2013, 27(1): 92.
[5] ZHANG Bang-xi, XIA Pin-hua, LI Cun-xiong(张邦喜, 夏品华, 李存雄).Environmental Monitoring in China(中国环境监测),2012, 28(1): 37.
[6] Nesrine T Lamie.Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy,2015, 149: 201.
[7] Ahmed S Saad.Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy,2015, 147: 257.
[8] CHEN Hai-xiang, HU Hui-chao, ZENG Jia-xin(陈海翔, 胡会超, 曾嘉欣).Spectroscopy and Spectral Analysis(光谱学与光谱分析), 2013, 33(9): 2566.
(Received Feb.2, 2015; accepted May 18, 2015)
*Corresponding author
Rapid Detection of Ammonia Nitrogen in Water with Dual-Wavelength Spectroscopy
WU Hui-ling1, HU Zhan-bo1*, CHAI Xin-sheng2, WANG Cui1, YANG Ou-meng1
1.School of Environment, Guangxi University, Nanning 530004, 2.State Key Laboratory of Pulp and Paper Engineering, South China University of Technology, Guangzhou 510641, China
Ammonia nitrogen is an important indicator to measure the quality of surface water.In the process of detecting ammonia nitrogen content with Nessler’s reagent spectrophotometry method (HJ535—2009), water sample pretreatment (flocculation method), residual turbidity and instrument baseline drifting will bring uncertainty to the process.Accordingly, a spectroscopic method based on dual-wavelength (420 and 650 nm) measurement is proposed, so as to subtract the absorbance of residual turbidity and instrument baseline-drifting to eliminate such interference.We first figure out k, the turbidity correction coefficient of the water sample at the wavelength 420 nm, then divide the product of absorbance of 650 andkby the absorbance of 420, and finally obtain the net absorption of ammonia nitrogen chromogenic reaction.Thus we can make accurate quantitative detection of ammonia nitrogen content and evaluate the precision and accuracy of dual-wavelength spectrometry.The results shows that, with single-wavelength method, the relative deviation can be up to 8.67% caused by the filtration process of flocculation and sedimentation, while the dual-wavelength method would not be affected by the deviation, since dual-wavelength method includes no filtration process.The accuracy standard deviation of dual-wavelength method could be as low as 1.58%, and the recovery is between 98.5% and 103%, which shows that the method is more accurate and reliable.Compared with the current Nessler’s reagent spectrophotometric method, the present method not only omits the process of water sample pretreatment, but also avoids the interference of residual turbidity, which could significantly improve the efficiency of the experiment.Therefore, it is more suitable for rapid determination of ammonia nitrogen in large quantities of surface water samples.
Ammonia nitrogen; Nessler’s reagent spectrophotometry method; Dual-wavelength spectroscopy
2015-02-02,
2015-05-18
国家自然科学基金项目(51409287),南宁市科学研究与技术开发计划项目(20143105),广西自然科学基金项目(2013GXNSFAA019278)资助
吴慧玲,女,1990年生,广西大学环境学院硕士研究生 e-mail: whl415899@126.com *通讯联系人 e-mail: hzb2005@126.com
O657.3
A
10.3964/j.issn.1000-0593(2016)05-1396-04
- 光谱学与光谱分析的其它文章
- Pb(Ⅱ)印迹磁性复合吸附剂在水溶液中吸附行为的FAAS法分析
- Study on the Multi-Spectral True Temperature Pyrometer for Explosion Transient of Thermo-Baric Explosives
- 蛋白饲料原料粗蛋白含量近红外光谱模型转移研究
- Native Defect Luminescence of Zinc Oxide Films and Its Potential Application as White Light Sources
- 增强的UV-B辐射对高粱幼苗光合和抗氧化系统的影响
- Spectrum Quantitative Analysis Based on Bootstrap-SVM Model with Small Sample Set

