光聚合壳聚糖基絮凝剂及其絮凝性能
孙永军 任梦娇 徐炎华 马江雅 张鹏 朱国成 肖雪峰 吴慧芳 尤朝阳 朱成雨

摘要:壳聚糖是一种天然碱性氨基多糖物质,其分子上分布着许多功能性的氨基和羟基,使其能成为潜在的高效絮凝剂。采用紫外光引发壳聚糖(CS)与丙烯酰胺(AM)、丙烯酰氧乙基三甲基氯化铵(DAC)接枝共聚制备P(CS-AD)絮凝剂,探讨了单体浓度、壳聚糖百分比、阳离子度、光引发剂浓度、光照时间对P(CS-AD)的特性粘度的影响,确定了合成的优化条件:单体浓度为30%~40%、壳聚糖百分比为10%~20%、阳离子度为30%~40%、光引发剂浓度为0.3%~0.5%、光照时间为120 min,优化后的制备的P(CS-AD)的特性粘度最高可达1 865 mg/L。同时,采用红外光谱、扫描电镜(SEM)、差热热重分析(TG-DTA)对其进行表征。采用模拟硅藻土水样验证其絮凝性能,试验结果表明:P(CS-AD)的絮凝性能显著优于市售聚丙烯酰胺(PAM)。
关键词:壳聚糖;絮凝剂;紫外光;接枝共聚;絮凝
中图分类号:X703.5;TU991.22
文献标志码:A 文章编号:1674-4764(2016)03-0058-07
Abstract:Chitosan is a natural basic amino polysaccharide substance with many functional amino and hydroxyl groups on the molecular chain. So that it can become a potential flocculant.
P(CS-AD) flocculant is graft copolymerized by chitosan (CS) and acrylamide (AM), acryloyloxyethyl trimethyl ammonium chloride (DAC) with UV irradiation. The effects of key factors on the intrinsic viscosity such as monomer concentration, chitosan percentage, cationic degree, photoinitiator concentration, and illumination time are discussed. The optimal synthesis conditions are determined: monomer concentration 30% to 40%, the percentage of chitosan 10%~20%, cationic degree 30%~40%, photoinitiator concentration 0.3%~0.5%, illumination time 120 min. The maximum intrinsic viscosity is 1 865 mg/L after optimization. Infrared spectroscopy, scanning electron microscopy (SEM), and differential thermal analysis (TG-DTA) are used to characterize the graft copolymer. Diatomite water samples are used to verify its flocculation performance, and flocculation test results show that P (CS-AD) flocculation performance is significantly better than the commercially available polyacrylamide (PAM).
Keywords:chitosan; flocculant; ultraviolet light; graft copolymerization; flocculation
随着工业化和城市化进程的加快,湖泊和水库接纳了大量工业和生活污水,为藻类的生长和繁殖提供了大量营养,使得天然水体富营养化日益严重。湖泊与水库的富营养化使得水中的藻类等浮游生物大量生长、过度繁殖,导致水质恶化,严重威胁了安全饮用水工程[1-2]。絮凝法在给水处理方法中是最经济、常用、重要的方法之一,作为给水处理的重要的操作单元之一不可或缺,而絮凝剂则是影响絮凝效果的关键因素[3]。
近年来,具有无毒无害、来源广泛、投加量少、受pH值影响小的天然有机高分子絮凝剂受到普遍关注。其中,壳聚糖是一种天然碱性氨基多糖物质,其分子上分布着许多功能性的氨基和羟基,对重金属离子和难降解有机物具有一定的络合和吸附作用,使其能够成为一种潜在的高效絮凝剂[4]。但由于壳聚糖的溶解性较差,通常只溶于弱酸性溶液,以及分子量较低等不足,使其作为絮凝剂的应用受到限制。而对壳聚糖接枝改性获得高效的壳聚糖基絮凝剂则是一种克服以上缺陷的高效方法。Yang等[5]以硝酸铈铵为引发剂采用热引发聚合3 h合成接枝率约为212%的壳聚糖和丙烯酰胺的接枝共聚物。朱贝贝等[6]采用热引发反相乳液法需要在一定温度下反应数个小时方可制备壳聚糖甲基丙烯酰氧乙基三甲基氯化铵接枝共聚物。传统的热引发接枝共聚应用较多,但其存在着引发聚合反应时间过长的不足。而紫外光引发是一种高效、节能、环保的引发方式,具有聚合反应时间短、效率高、能耗低等优势而越来越受到重视[7-8]。壳聚糖大分子链上具有两种可用于接枝反应的活性基团:氨基、C-3和C-6位置上的羟基。通过紫外光辐射光引发剂分解产生自由基引发接枝反应,可在壳聚糖主链上接入不同的活性基团或功能性单体,从而增加其分子量和溶解性[9]。但是将其应用于壳聚糖的接枝改性制备壳聚糖基絮凝剂却鲜有研究。
笔者采用紫外光引发壳聚糖(CS)与丙烯酰胺(AM)、丙烯酰氧乙基三甲基氯化铵(DAC)接枝共聚制备P(CS-AD)絮凝剂,探讨了单体浓度、壳聚糖百分比、阳离子度、光引发剂浓度、光照时间对P(CS-AD)的特性粘度的影响,并采用红外光谱、扫描电镜、差热热重分析对其进行表征,最后将其应用于硅藻土模拟水样的絮凝试验,考察其絮凝性能。
1 试验部分
1.1 材料与仪器
丙烯酰胺(AM:工业级);丙烯酰氧基乙基三甲基氯化铵(DAC:分析纯);壳聚糖(CS:生化试剂);光引发剂2,2-偶氮双(2-甲基丙脒)二盐酸盐(V50:分析纯);氮气(纯度99.9%)。
1.2 合成方法
将一定质量的AM、DAC、CS于1%的醋酸溶液中溶解,采用磁力搅拌器搅拌使之充分溶解,然后通入氮气驱氧30 min后加入光引发剂,密封并置于紫外光下照射(高压汞灯主波长为365 nm,功率为500 W),连续光照一定时间后获得胶体状接枝共聚物。将胶体剪碎后进行提纯干燥,再碾磨制成粉状,以备用。
1.3 合成产物表征
按照《水处理剂 阳离子型聚丙烯酰胺的技术条件和试验方法》(GB/T 31246—2014)测定其特性粘度。分别采用Nicolet Nexus 670红外拉曼光谱仪(ATR附件,美国Thermo Nicolet公司)、VEGAII LMU扫描电子显微镜(北捷克TES-CAN公司)、热重差热分析仪(DTG-60H、日本岛津公司)对聚合产物进行红外光谱、表面形态、差热热重表征。
1.4 絮凝试验
试验采用硅藻土配制1 g/L的模拟水样,硅藻土在配制模拟水样前过400目筛网(孔径为38 μm)使其粒度小于38 μm,模拟水样的浊度为187.8 NTU。将聚合产品以及市售聚丙烯酰胺(市售聚丙烯酰胺为阳离子聚丙烯酰胺,阳离子为20%,分子量为500万)配制成5‰的水溶液备用。投加一定量的絮凝剂以快搅速度为250 rpm搅拌2 min、慢搅速度为60 rpm搅拌10 min进行絮凝试验,静沉15 min,考察投加量和pH对絮凝剂絮凝性能的影响。
2 试验结果与讨论
2.1 壳聚糖基絮凝剂的合成
2.1.1 总单体浓度对特性粘度的影响
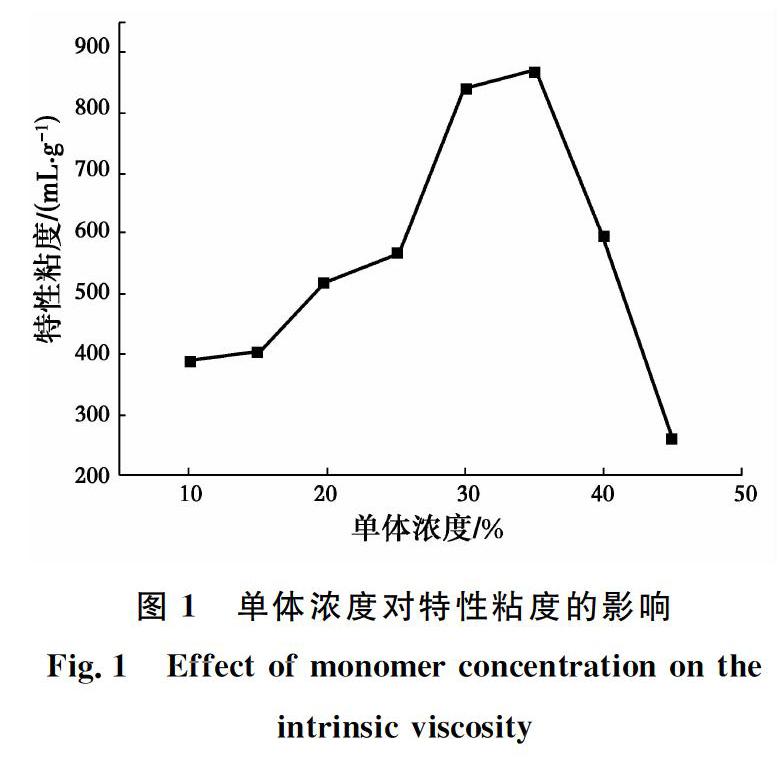
总单体浓度为所有单体的质量之和占总单体水溶液的质量百分比。总单体浓度对特性粘度的影响如图1所示。随着总单体浓度的增加,特性粘度是先缓慢逐步增加,然后急剧减小。在总单体浓度为35%时,P(CS-AD)的特性粘度达到最大,最大值为865 mL/g。当总单体浓度较低时,单体分子之间发生接触及碰撞的概率较低,因而发生反应的概率较低,反应生成的P(CS-AD)特性粘度较低。随着总单体浓度的增加,P(CS-AD)特性粘度逐渐增加。当总单体浓度超过35%时,由于反应体系内壳聚糖浓度增加,使得反应体系的浓度增加,反应溶液变得粘稠,不利于聚合反应。同时,由于总单体浓度的增加,也导致大量的壳聚糖在反应体系中溶解性降低,降低了聚合反应的有效性,从而导致P(CS-AD)特性粘度降低。因此,合成P(CS-AD)的最佳总单体浓度为30%~40%。
2.1.2 壳聚糖百分比对特性粘度的影响
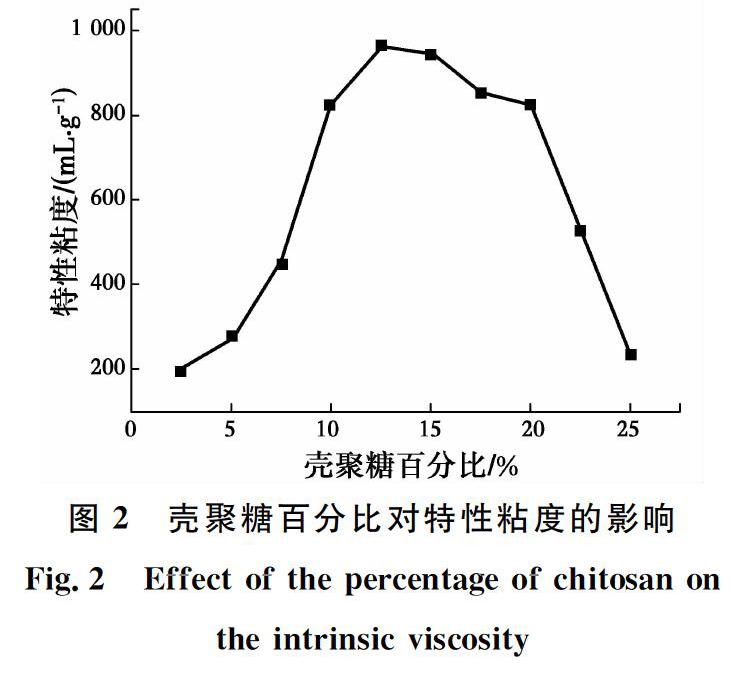
壳聚糖百分比对特性粘度的影响如图2所示。随着壳聚糖百分比的增加,P(CS-AD)的特性粘度先增加,然后减小。当壳聚糖百分比达到12.5%时,P(CS-AD)的特性粘度达到最大值为965 mL/g,当壳聚糖百分比超过12.5%时,P(CS-AD)的特性粘度开始逐渐下降。当壳聚糖含量较低时,壳聚糖大分子上的反应活性点能够有效地与AM、DAC单体发生反应,随着壳聚糖的浓度增加,壳聚糖大分子上的反应活性点位逐渐增加,但AM、DAC单体逐渐减少,使得可在壳聚糖大分子上的反应活性点位发生反应的聚合单体减少,导致P(CS-AD)的特性粘度降低[10]。同时,壳聚糖百分比增加导致部分壳聚糖未溶解,从而导致总反应单体有效浓度较低,进而导致分子量降低。综上,较佳的壳聚糖百分比为10%~20%。
2.1.3 阳离子度对特性粘度的影响
阳离子度对特性粘度的影响如图3所示。随着阳离子度的增加,P(CS-AD)的特性粘度逐渐增加,当阳离子度达到35%,P(CS-AD)的特性粘度达到最大值。当阳离子度超过35%时,P(CS-AD)的特性粘度开始降低。当阳离子度较低时,由于AM的竞聚率较高,AM发生的反应速率较快,聚合物链节上AM单体较多,形成的聚合产物的特性粘度较高[11]。随着阳离子度的增加,P(CS-AD)的特性粘度逐渐减小,是由于DAC携带的带正电荷的阳离子铵基基团与壳聚糖的氨基之间产生静电斥力,降低了反应活性,并且产生空间位阻效应,
降低了产物的特性粘度。当DAC含量较高时,降低反应体系的扩散碰撞速率,降低反应效率,从而使特性粘度降低。综上,较佳的阳离子度范围30%~40%。
2.1.4 光引发剂浓度对特性粘度的影响
光引发剂浓度对特性粘度的影响如图4所示。随着光引发剂浓度的增加,P(CS-AD)的特性粘度逐渐增加,当光引发剂浓度达到0.4%时,P(CS-AD)特性粘度达到最大,最大值为1 506 mL/g。当光引发剂浓度超过0.4%时,其特性粘度逐渐减小。当光引发剂的浓度较低时,产生的自由基较少,不足以使得全部的壳聚糖大分子产生活性点位和AM、DAC发生完全聚合,故聚合产物特性粘度较低。当光引发剂浓度较高时,在紫外光作用下引发剂快速分解产生大量的自由基,易使聚合单体发生爆聚和交联,从而降低聚合产物的溶解性[12]。同时,也会导致壳聚糖大分子产生的聚合反应点位远大于可反应的单体数量,从而导致产生一定程度的自聚,降低聚合物的特性粘度。综上,较佳的光引发剂浓度范围为0.3%~0.5%。
2.1.5 光照时间对特性粘度的影响
光照时间对特性粘度的影响如图5所示。随着光照时间的增加,P(CS-AD)的特性粘度逐渐增加,当光照时间超过120 min时,P(CS-AD)的特性粘度略有下降。当光照时间为120 min时,特性粘度达到最大,最大值为1 865 mL/g。随着光照时间增加,光引发剂被紫外光辐照吸收能量而分解产生自由基,使反应速率增加,P(CS-AD)特性粘度增加。但随着光照时间进一步增加,光引发剂被分解完全,特性粘度趋于平稳,但继续增加光照时间时,由于紫外光的辐照使得部分聚合单体发生一定程度的交联,以及聚合体系变得粘稠逐渐呈胶体状,降低自由基以及壳聚糖反应活性点位的运动速率,从而降低反应活性,使P(CS-AD)的特性粘度降低[13]。综上,较佳的光照反应时间为120 min。
2.2 壳聚糖基絮凝剂的表征
2.2.1 红外光谱表征
P(CS-AD)的红外光谱如图6所示,3 175 cm-1和3 299 cm-1处的吸收峰为壳聚糖中的-OH(包括NH2)和AM中的酰胺基(-CONH2)的-NH2的伸缩性振动吸收峰,由于氢键作用导致该处吸收峰较宽且强。1 648 cm-1处为AM中的-COOCH2和壳聚糖中的C=O的伸缩振动吸收峰,表明壳聚糖已经和AM及DAC发生了聚合反应[14-15]。1 602 cm-1为壳聚糖中的N-H的弯曲振动吸收峰,聚合物中1 404 cm-1处为DAC中的-CH2-N+(CH3)3亚甲基的弯曲振动吸收峰。1 160 cm-1处为-COOCH2-中C-O-C的不对称伸缩振动吸收峰,也是壳聚糖中糖苷键的吸收峰。1 072 cm-1为壳聚糖中的伯醇C-OH拉伸振动吸收峰,947 cm-1处为季铵基的吸收峰。在聚合物的红外光谱中出现了壳聚糖的特征吸收峰,表明CS与AM、DAC成功发生接枝共聚反应。
2.2.2 扫描电镜表征
P(CS-AD)的扫描电镜照片如图7所示,图7中分别展示了1 000倍、3 000倍、5 000倍的放大倍数下的P(CS-AD)的表面形态照片。从图7(a)可以看出P(CS-AD)絮凝剂的表面存在大量不规则的凸起结构,从图7(b)中可进一步看出表明的凸起结构是由细小的片层状结构引起的,经过5 000倍放大后,从图7(c)中可以看出表面是由于壳聚糖的接入引起的表面凸起。与文献[16]中的关于紫外光引发P(AM-DAC)的扫面电镜相对比,P(CS-AD)的表面形态比P(AM-DAC)更加不平整,这导致P(CS-AD)比表面积更大。
2.2.3 差热热重表征(TG-DTA)
P(CS-AD)的差热热重图谱如图8所示,P(CS-AD)在30~600 ℃的范围内存在3个阶段的失重。第1阶段失重温度范围为30~190 ℃,在此范围内样品失重为4.71%,该范围内的失重是由于P(CS-AD)吸湿,在加热干燥的条件下脱去吸附水和结晶水,因而出现了较为轻微的失重现象。第2阶段失重温度范围为190~330 ℃,此范围内样品失重约24.89%,样品失重的原因可能是酰胺基团(-CO-NH-)和壳聚糖的氨基受热分解以及酰胺基团(-CO-NH-)的亚胺反应和季铵基上(-C(CH3)3N+Cl-)的甲基脱离,同时脱去氯化氢。第3阶段失重温度范围为330~480 ℃,聚合物主链和壳聚糖开始发吸热降解,迅速失重40.26%,最终分解完全的温度约在480 ℃。480 ℃以后,热重曲线趋于平缓,无失重产生,最终残余重量30.14%左右。从图8中的DTA曲线可以看出,30~190 ℃范围有吸热峰,对应于第1阶段失重;190~330 ℃的吸热峰对应于第2阶段失重;330~480 ℃范围的吸热峰对应于第3阶段失重[17]。P(CS-AD)的TG-DSC曲线分析表明:紫外光引发接枝共聚合成的P(CS-AD)在常温下性质稳定,不会发生分解。
2.3 絮凝性能
2.3.1 投加量对絮凝性能的影响
P(CS-AD)的絮凝能力随投加量的变化如图9所示。絮凝后上清液的剩余浊度被用于表征絮凝剂的絮凝性能,浊度越低,P(CS-AD)絮凝性能越好。P(CS-AD)絮凝后上清液剩余浊度随着投加量的增加而处于一个相对稳定的较低值,即2~3 NTU,当投加量超过4 mg/L时,上清液浊度才逐渐略有升高。市售PAM絮凝后的上清液剩余浊度随着投加量的增加先迅速增加,当投加量超过4 mg/L时,上清液剩余浊度趋于平缓。从图中可明显看出,P(CS-AD)在1~6 mg/L投加量范围内,P(CS-AD)絮凝后上清液剩余浊度显著小于PAM絮凝后上清液剩余浊度,说明P(CS-AD)具有较为宽的絮凝剂投加量范围,且相比于市售PAM,P(CS-AD)具有更加优异的絮凝性能[18]。
2.3.2 pH值对絮凝性能的影响
pH值对絮凝性能的影响如图10所示。随着pH值的增加,P(CS-AD)絮凝后上清液剩余浊度急剧减小,当pH大于7后上清液剩余浊度趋于平缓,当pH值为8时,上清液剩余浊度最小,最小值为2.25 NTU。PAM絮凝后上清液剩余浊度随着pH值的增加先缓慢减小后逐渐增加,当pH值为7时,絮凝后上清液剩余浊度最小,最小值为6.55 NTU。由图10可知,在pH值1~10的范围内,P(CS-AD)絮凝后上清液剩余浊度均小于市售PAM絮凝后的上清液剩余浊度,P(CS-AD)的絮凝性能显著优于市售PAM。同时,P(CS-AD)对pH值的敏感性显著高于PAM,P(CS-AD) 在酸性条件下(pH值1~6)絮凝效果相对较差,但在pH值7~10的范围内具有较好的絮凝性能,这与P(CS-AD)自身特性有关,由于P(CS-AD)中含有壳聚糖,壳聚糖在酸性条件下易于溶解和水解,从而使得P(CS-AD)在酸性条件下发生降解,故进一步导致P(CS-AD)在酸性条件下絮凝效果变差[19]。综上,P(CS-AD)的较佳的适用pH值范围7~10。
3 结 论
采用紫外光引发接枝共聚成功制备了壳聚糖、AM、DAC三元共聚物,即壳聚糖基絮凝剂。研究结果表明,紫外光引发壳聚糖、AM、DAC三元接枝共聚的优化制备条件为:单体浓度30%~40%、壳聚糖百分比10%~20%、阳离子度30%~40%、光引发剂浓度0.3%~0.5%、光照时间120 min,优化后制备的P(CS-AD)的特性粘度最高可达1 865 mg/L。红外光谱分析表明合成出的产物为壳聚糖、AM、DAC三元接枝共聚合物P(CS-AD)。SEM照片表明P(CS-AD)絮凝剂表面存在大量不规则的凸起结构。TG-DSC曲线分析表明:紫外光引发接枝共聚合成的P(CS-AD)在常温下性质稳定,不会发生分解。絮凝试验表明:P(CS-AD)的絮凝性能显著优于市售PAM,P(CS-AD)的优化絮凝条件为:投加量为1~4 mg/L、pH值为7~10,絮凝后上清液剩余浊度低于3.0 NTU。
参考文献:
[1] SUN Y J, ZHENG H L, XIONG Z P, et al. Algae removal by flocculation process from algae-containing raw water and the fractal characteristic of flocs [J]. Desalination and Water Treatment, 2015, 56(4): 894-904.
[2] MA X X, WANG Y A, FENG S Q, et al. Comparison of four flocculants for removing algae in Dianchi Lake [J]. Environmental Earth Sciences, 2015, 74: 3795-3804.
[3] Dao V H, CAMERON N R, SAITO K. Synthesis, properties and performance of organic polymers employed in flocculation applications [J]. RSC Advance, 2016, 7: 11-25.
[4] 仲米贵,王郑. 壳聚糖絮凝性能及其在微污染源水中的应用研究[J].应用化工,2015,44(4):702-706.
ZHONG M G, WANG Z. The flocculation efficiency of chitosan and its application research in micro-polluted source water [J]. Applied Chemical Industry, 2015, 44(4): 702-706.(in Chinese)
[5] YANG Z, YUAN B, HUANG X, et al. Evaluation of the flocculation performance of carboxymethyl chitosan-graft-polyacrylamide, a novel amphoteric chemically bonded composite flocculant [J]. Water Research, 2012, 46: 107-114.
[6] 朱贝贝,姚春才,许丽,等. 壳聚糖-甲基丙烯酰氧乙基三甲基氯化铵接枝共聚物的制备与絮凝性能研究[J]. 生物质化学工程,2013,47(2):15-18.
ZHU B B, YAO C C, XU L, et al. Preparation and flocculation performance of chitosan-methacryloyloxyethyl trimethyl ammonium chloride graft copolymer [J]. Biomass Chemical Engineering, 2013, 47(2): 15-18.(in Chinese)
[7] 谢龙,邵自强. 紫外光直接引发AM反相微乳液聚合及其机理[J]. 高分子材料科学与工程,2012,28(5):41-43.
XIE L, SHAO Z Q. Polymerization of AM Inverse microemulsion initiated directly by UV radiation [J]. Polymer Materials Science & Engineering, 2012, 28(5): 41-43.(in Chinese)
[8] ZHENG H L, SUN Y J, ZHU C J, et al. UV-initiated polymerization of hydrophobically associating cationic flocculants: Synthesis, characterization, and dewatering properties [J]. Chemical Engineering Journal, 2013, 234: 318-326.
[9] RENAULT F, SANCEY B, BADOT P M, et al. Chitosan for coagulation/flocculation processes-An eco-friendly approach [J]. European Polymer Journal, 2009, 45: 1337-1348.
[10] 杜凤龄,王刚,徐敏,等. 新型高分子螯合絮凝剂制备条件的响应面优化[J]. 中国环境科学,2015,35(4):1116-1122.
DU F L, WANG G, XU M, et al. Optimization of preparation conditions of novel macromolecule chelating-flocculant by response surface methodology [J]. China Environmental Science, 2015, 35(4): 1116-1122.(in Chinese)
[11] 李万捷,李春,陈庆柏. 紫外光照射下光敏引发丙烯酰胺聚合动力学 [J]. 高分子材料科学与工程,2011,27(4):5-8.
LI W J, LI C, CHEN Q B. Polymerization kinetics of acrylamide initiated by photosensitizer under UV lamp [J]. Polymer Materials Science & Engineering, 2011, 27(4):5-8.(in Chinese)
[12] 郑怀礼,熊祖平,孙永军,等. 疏水缔合阳离子聚丙烯酰胺污泥脱水剂的合成及其表征[J]. 土木建筑与环境工程,2014,36(4):104-108.
ZHENG H L, XIONG Z P, SUN Y J, et al. Synthesis and characterization of hydrophobic associating cationic polyacrylamide flocculant for sludge dewatering [J]. Journal of Civil, Architectural & Environmental Engineering, 2014, 36(4): 104-108.(in Chinese)
[13] 郑怀礼,尤艳飞,邓晓莉,等. 高分子量高纯度阳离子聚丙烯酰胺的合成[J].环境工程学报, 2012, 6(4): 1075-1080.
ZHENG H L, YOU Y F, DENG X L, et al. Synthesis of a cationic polyacrylamide with high molecular weight and high purity [J]. Chinese Journal of Environmental Engineering, 2012, 6(4): 1075-1080.(in Chinese)
[14] 孙永军,梁建军,郑怀礼,等. 紫外光引发阳离子聚丙烯酰胺的红外光谱研究[J]. 光谱学与光谱分析,2014,34(5):1234-1239.
SUN Y J, LIANG J J, ZHENG H L, et al. Study on infrared spectroscopy of cationic polyacrylamide initiated by ultraviole [J]. Spectroscopy and Spectral Analysis, 2014,34(5):1234-1239.(in Chinese)
[15] 黄朋,叶林. 壳聚糖/蒙脱土复合絮凝剂的结构及污泥脱水性能[J]. 高分子材料科学与工程, 2014,30(4):119-123.
HUANG P, YE L. Structure and sludge dewatering property of chitosan/montmorillonite composite [J]. Polymer Materials Science & Engineering, 2014, 30(4): 119-123.(in Chinese)
[16] ZHENG H L, SUN Y J, GUO J S, et al. Characterization and evaluation of dewatering properties of PADB, a highly efficient cationic flocculant [J]. Industrial & Engineering Chemistry Research, 2014, 53: 2572-2582.
[17] WANG J P, CHEN Y Z, GE X Z, et al. Gamma radiation-induced grafting of a cationic monomer onto chitosan as a flocculant [J]. Chemosphere, 2007, 66: 1752-1757.
[18] ZHU J R, ZHENG H L, Jiang Z Z, et al. Synthesis and characterization of a dewatering reagent: cationic polyacrylamide(P(AM-DMC-DAC)) for activated sludge dewatering treatment [J]. Desalination and Water Treatment, 2013, 51(13/14/15): 2791-2801.
[19] 张文轩,尚亚波,袁博,等. 壳聚糖改性絮凝剂絮凝性能的研究[J]. 高分子通报,2010(4):49-54.
ZHANG W X, SHANG Y B, YUAN B, et al. Study on the flocculating properties of chemical modified chitosan flocculants [J]. Polymer Bulletin, 2010(4): 49-54.(in Chinese)
(编辑 胡英奎)

