用数学方法解决盖斯定律
袁寄华

【摘要】 高考时,好多学生有比较大的心理压力,那么如何化难为简是我们一线教师一直在探讨的问题.以盖斯定律为例, 它并没有多少知识点,可是每年考试好多学生都做错,如果说这类题目是送分题,那么我们就要做到如何让我们的学生能省时省力省脑筋轻松地拿到这个分。
【关键词】 数学方法 盖斯定律
【中图分类号】 G633.8 【文献标识码】 A 【文章编号】 1992-7711(2016)06-037-01
下面以一些比较典型的习题为例详谈解该类题目的解决办法。
例题1.已知相同条件下:
①4Ca5(PO4)3F(s)+3SiO2(s)===6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g) ΔH1
②2Ca3(PO4)2(s)+10C(s)===P4(g)+6CaO(s)+10CO(g) ΔH2
③SiO2(s)+CaO(s)===CaSiO3(s) ΔH3
由磷灰石[主要成分Ca5(PO4)3F]在高温下制备黄磷(P4)的热化学方程式为:
④4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)===3P4(g)+20CaSiO3(s)+30CO(g)+ SiF4(g)H4
用ΔH1、ΔH2和ΔH3表示ΔH4 , ΔH4=________。
解析:分别将①方程式左右两边同时乘以a;
将②方程式左右两边同时乘以b;
将③方程式左右两边同时乘以c;
观察最右侧的列式这一栏,我们发现,不必要把所有的步骤都写出来再列式,因为重复严重,所以我们的作法是只需要挑选其中的3步,计算得出结果。
所以: a=1; b=3; c=18;
答案 (1) ΔH4=ΔH1+3ΔH2+18ΔH3
例题2. 已知下列热化学方程式:
①Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH1=-26.7 kJ·mol-1
②3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g) ΔH2=-50.75 kJ·mol-1
③Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH3=-36.5 kJ·mol-1
则反应④FeO(s)+CO(g)===Fe(s)+CO2(g)的焓变ΔH4为( )
A.+7.28 kJ·mol-1 B.-7.28 kJ·mol-1
C.+43.68 kJ·mol-1 D.-43.68 kJ·mol-1
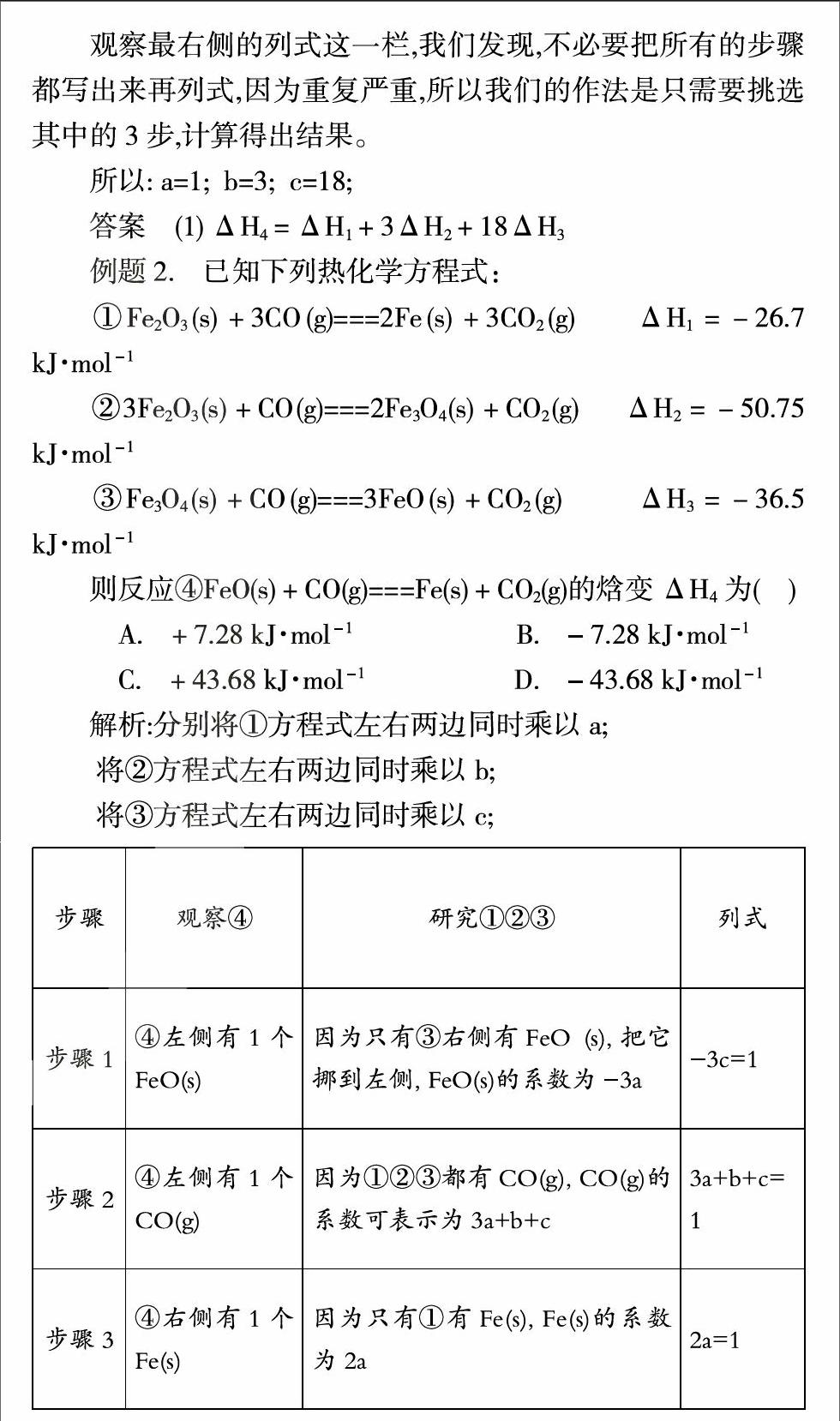
解析:分别将①方程式左右两边同时乘以a;
将②方程式左右两边同时乘以b;
将③方程式左右两边同时乘以c;
因为是要求出a b c 是一个三元一次方程,所以只挑选了前三步,就可以得出结果。所以a=1/2; b=-1/6; c=-1/3;
ΔH4=1/2ΔH1 - 1/6ΔH2 - 1/3ΔH3 答案为 A
该方法采用数学方法解决盖斯定律,方法具有普遍性,尤其适用于大多数化学方程式较长的反应和多个方程式计算获得一个方程式的反应,可以解决较难的盖斯定律问题。

