盾叶薯蓣中薯蓣皂苷元生物合成途径研究进展
毕淮龙,乔亚茹,化文平
(陕西学前师范学院生物科学与技术系,陕西西安 710100)
盾叶薯蓣中薯蓣皂苷元生物合成途径研究进展
毕淮龙,乔亚茹,化文平*
(陕西学前师范学院生物科学与技术系,陕西西安 710100)
摘要综述了薯蓣皂苷元生物合成途径的研究进展及相关酶的研究进展,对其生物合成途径进行了推断,以期为盾叶薯蓣皂苷元合成相关的研究以及利用生物工程进行生产奠定基础。
关键词盾叶薯蓣;薯蓣皂苷元;合成途径;关键酶
盾叶薯蓣(DioscoreazingiberensisC.H.Wright)是薯蓣属多年生草本植物,俗称黄姜,是目前世界上薯蓣皂苷元含量最高的种。该物种是我国特有种,主要分布在湖北、湖南、陕西秦岭以南、河南南部、甘肃天水以及四川等省海拔100~1 500 m的区域[1],在湖北、陕西南部等地也有大面积的种植。盾叶薯蓣以根状茎入药,能祛风、利湿,主治风湿顽痹、腰膝疼痛等症[2],在《山海经》《神农本草经》《图经本草》《本草纲目》等医药典籍中均有记载[3]。自20世纪40年代发现盾叶薯蓣根状茎中含有丰富的薯蓣皂苷元以来,薯蓣皂苷元已被应用于300多种避孕药及甾体激素类药物的合成,已成为重要的甾体激素类药源植物[4]。笔者综述了薯蓣皂苷元生物合成途径及相关酶的研究进展,以期为盾叶薯蓣皂苷元生物合成相关的研究以及利用生物工程进行生产奠定基础。
1薯蓣皂苷元及应用价值
薯蓣皂苷,俗称黄姜皂素,为螺甾烷类甾体化合物。由薯蓣皂苷元(diosgenin)(图1)通过糖苷键与植物纤维素结合,在C3位通过皂苷键与糖链相连形成。皂苷在植物细胞壁中,与细胞壁紧密连接包裹。在酸、热等条件下水解可得到薯蓣皂苷元[5]。薯蓣皂苷元在盾叶薯蓣块茎中的含量达1.1%~16.15%。
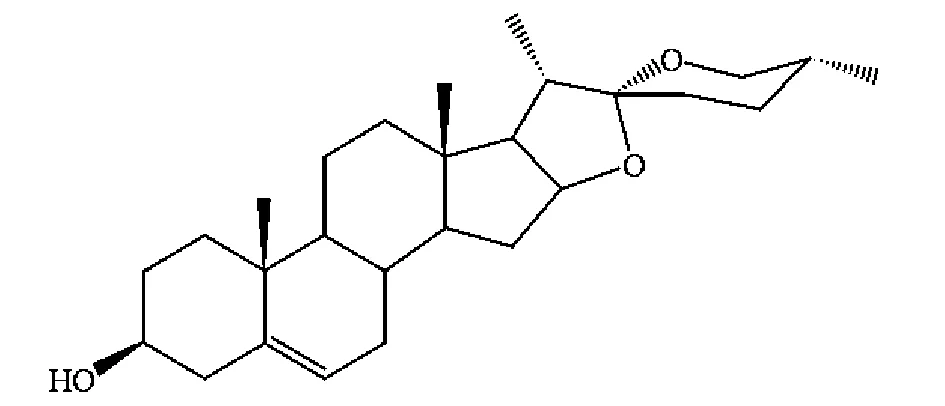
图1 薯蓣皂苷元化学结构Fig.1 Chemical structure of diosgenin
薯蓣皂苷元和甾体激素类药物在结构上非常相近,是合成性激素、肾上腺皮质激素和蛋白同化激素三大类甾体激素药物最理想的前体原料。目前以薯蓣皂苷元为原料生产的甾体类激素产品已近300种[6],全球对薯蓣皂苷元的需求量仅次于抗生素,薯蓣皂苷元加工已成为医药工业中的第二大药品生产领域。薯蓣皂苷元亦被誉为“药用黄金”。
2薯蓣皂苷元生物合成途径
目前对薯蓣皂苷元生物合成途径的研究尚处于初级阶段,其合成途径中的很多步骤(或路线),尤其是后期的步骤,尚不清晰。一般认为,薯蓣皂苷元属于甾醇类化合物,由三萜类化合物衍生而来。三萜类化合物在植物体中主要通过类异戊二烯生物合成途径合成。在高等植物中萜类物质是以5C骨架的IPP(3-isopentenyl pyrophosphate,C5)和 DMAPP(dimethylallyl pyrophosphate,C5)为前体衍生而来。在植物细胞内存在甲羟戊酸(MVA)途径(主要在细胞质中)和2-甲基-D-赤藻糖醇-4-磷酸(MEP)途径(主要在质体中)2条IPP合成途径[7]。研究表明,植物体内三萜类物质(如人参皂苷等)合成的前体IPP主要来源于细胞质中的MVA途径[8-10]。IPP与DMAPP(IPP的同分异构体)首尾相连逐级缩合,逐渐合成鲨烯(squalene),经鲨烯环氧酶(squalene epoxydase)催化合成2,3-氧化角鲨烯(2,3-oxidosqualene),再在环阿屯醇合酶(cycloartenol synthase,CAS)的环化下生成环阿屯醇合酶(cycloartenol);或者在羊毛甾醇合酶(lanosterol synthase)作用下生成羊毛甾醇(lanosterol)[11]。 Mehrafarin 等[12]研究认为在植物Trigonellafoenum-graecumL.中胆固醇的合成可以由环阿屯醇或羊毛甾醇分别合成。研究表明,在Dioscoreafloribunda和Dioscoreadeltoidea中以14C- 或3H 标记的胆固醇可以转化为放射性标记的薯蓣皂苷元[13-15]。随后在D.deltoidea细胞中发现,呋喃甾醇(furostanol)是胆固醇向薯蓣皂苷元转化合成的中间物[16];Stohs等[17]指出胆固醇经呋喃甾醇(furostanol)和原薯蓣皂苷元等多步转化过程,最后合成薯蓣皂苷元。但在悬浮培养的D.deltoidea细胞中发现同位素标记的谷甾醇sitosterol也可以转化为可放射性检测的薯蓣皂苷元。胆固醇和谷甾醇在结构上的差异仅在于胆固醇在侧链C24位无烷基,而谷甾醇的侧链C24位有一个乙基基团;两者都由环阿屯醇衍化而来,其中在甾醇 C24 甲基转移酶(sterol C24-methyltransferase;SMT)作用下在C24位加一个乙基生成谷甾醇[18-19]。在植物中,胆固醇由环阿屯醇在CAS催化下生成[20]。
依据上述研究,推测盾叶薯蓣中从2,3-氧化角鲨烯到薯蓣皂苷元的生物合成可能经过2条不同的途径:由环阿屯醇cycolartenol在CAS或LSS催化合成的胆固醇合成薯蓣皂苷元;由谷甾醇sitosterol合成薯蓣皂苷元[21]。具体合成步骤见图2。
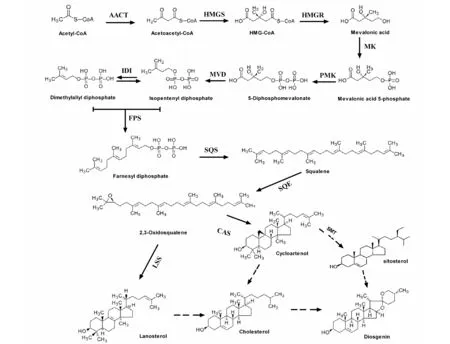
注:AACT.Acetoacetyl-CoA thiolase;HMGS.3-Hydroxy-3-methylglutaryl-CoA synthase;HMGR.3-Hydroxy-3-methylglutaryl-CoA reductase;MK.Mevalonate kinase;PMK.Phosphomevalonate kinase;MVD.Mevalonate diphospate decarboxylase;IDI.Isopentenyl diphosphate isomerase;FPS.Farnesyl pyrophosphate synthase;SQS.Squalene synthase;SQE.Squalene epoxydase;CAS.Cycloartenol synthase;LSS.Lanosterol synthase;SMT.sterol C24-methyltransferase.Note:AACT.Acetoacetyl-CoA thiolase;HMGS.3-Hydroxy-3-methylglutaryl-CoA synthase;HMGR.3-Hydroxy-3-methylglutaryl-CoA reductase;MK.Mevalonate kinase;PMK.Phosphomevalonate kinase;MVD.Mevalonate diphospate decarboxylase;IDI.Isopentenyl diphosphate isomerase;FPS.Farnesyl pyrophosphate synthase;SQS.Squalene synthase;SQE.Squalene epoxydase;CAS.Cycloartenol synthase;LSS.Lanosterol synthase;SMT.Sterol C24-methyltransferase.图2 盾叶薯蓣中薯蓣皂苷元生物合成途径Fig.2 Synthesis route of diosgenin in D.zingiberensis
目前,薯蓣皂苷元合成途径的前期步骤已经明确,但自胆固醇合成薯蓣皂苷元的具体步骤尚不清晰。推测主要是通过一系列的氧化、环化等步骤完成,可能需要细胞色素P450 单加氧酶、糖基转移酶和糖苷酶等多种酶参与[22]。
3薯蓣皂苷元生物合成途径关键酶及其编码基因
目前,对盾叶薯蓣中薯蓣皂苷元生物合成途径中酶及其编码基因的研究尚处于起步阶段,仅有CAS、HMGR、SQS、FPS、sterol24-C-methyltransferase1(STM)等少数关键酶编码基因被克隆或被验证其编码蛋白功能。陈迪等[23]和涂碧梦等[24]先后克隆得到2条环阿屯醇合酶(cycloartenol synthase,CAS)基因,并在酵母缺陷菌株中验证了DzCAS2基因的编码蛋白功能。Ye等[25]从盾叶薯蓣中克隆得到鲨烯合酶(squalene synthase)基因DzSQS,并在大肠杆菌中表达验证发现其编码蛋白具有鲨烯合酶活性。但Diarra等[26]研究发现,乙烯在显著提高盾叶薯蓣中薯蓣皂苷元含量的同时,DzSQS的表达变化不明显;而且环阿屯醇合酶(cycloartenol synthase,CAS)基因和甲羟戊酸(MVA)途径HMGR基因的表达量明显上调。Diarra等[26]推测CAS和HMGR是盾叶薯蓣中薯蓣皂苷元合成的关键酶。
虽然很多植物体内甾醇、三萜类等物质合成的前体IPP主要来源于细胞质中的MVA途径[8-10],但研究表明在一些物种中MVA合成的IPP(细胞质中)和MEP合成的IPP(质体中)之间存在“交流”[27]。有些研究者也将研究集中在MEP通路中关键酶上,以期通过该类关键酶基因的研究明确MEP通路在薯蓣皂苷元合成中的作用。如王润发[28]、杨婷[29]分别克隆得到盾叶薯蓣中MEP通路中的HDR基因、 1-脱氧-木酮糖-5-磷酸还原异构酶(1-Deoxy-D-xylulose5-phosphate reductoisomerase,DXR)和2-C-甲基赤藓醇-2,4-环焦磷酸合成酶(2-C-Methy-D-erythritol2,4-cyclodiphosphate synthase,MDS)等基因的全长,并验证其编码蛋白在大肠杆菌中的催化功能[28-29]。
4展望
目前关于盾叶薯蓣的研究主要集中于其有效成分薯蓣皂苷元提取技术改良、药理作用和栽培技术等方面,关于盾叶薯蓣中薯蓣皂苷元的合成途径研究近年来进展较慢。但近2年关于盾叶薯蓣中薯蓣皂苷元的合成途径中涉及酶的编码基因研究正在兴起。笔者认为,今后关于薯蓣皂苷元合成途径的研究主要集中在以下2个方面:① 进一步通过基因工程手段,研究已明确的合成途径中酶及其编码基因在薯蓣皂苷元合成中的作用;②借鉴人参等药用植物研究经验,通过表达谱筛选等手段筛选与薯蓣皂苷元合成密切相关的、参与后期合成步骤的细胞色素P450 单加氧酶、糖基转移酶等的编码基因,通过基因功能的研究阐明薯蓣皂苷元生物合成路线后期可能的合成步骤。
参考文献
[1] 赵毓棠.中国植物志:薯蓣科:16 卷第1分册[M].北京:科学出版社,1985:64.
[2] 李祥,马建中,史云东.盾叶薯蓣薯蓣皂素研究进展及展望[J].林产化学与工业,2010,30(2):107-112.
[3] 丁志遵.甾体激素药源植物[M].北京:科学出版社,1983.
[4] SAUTOUR M,MITAINE-OFFER A C,LACAILLE-DUBOIS M A.TheDioscoreagenus:A review of bioactive steroid saponins[J].J Nat Meds,2007,61(2):91-101.
[5] PENG Y,YANG Z,WANG Y,et al.Pathways for the steroidal saponins conversion to diosgenin during acid hydrolysis ofDioscoreazingiberensisCH Wright[J].Chem Eng Res,2011,89(12):2620-2625.
[6] QIU L,NIU H,HUANG W.Ultrasonic and fermented pretreatment technology for diosgenin production fromDiosoreazingiberensisCH Wright[J].Chem Engg Res,2011,89(2):239-247.
[7] ZULAK K G,BOHLMANN J.Terpenoid biosynthesis and specialized vascular cells of conifer defense[J].J Integra Plant Biol,2010,52(1):86-97.
[8] NES W D.Biosynthesis of cholesterol and other sterols[J].Chem Rev,2011,111(10):6423-6451.
[9] CHAPPELL J.The genetics and molecular genetics of terpene and sterol origami[J].Curr Opinion Plant Biol,2002,5(2):151-157.
[10] KIRBY J,KEASLING J D.Biosynthesis of plant isoprenoids:Perspectives for microbial engineering[J].Annu Rev Plant Biol,2009,60:335-355.
[11] OHYAMA K,SUZUKI M,KIKUCHI J,et al.Dual biosynthetic pathways to phytosterol via cycloartenol and lanosterol inArabidopsis[J].PNAS,2009,106(3):725-730.
[12] MEHRAFARIN A,GHADERI A,REZAZADEH S,et al.Bioengineering of important secondary metabolites and metabolic pathways in fenugreek(Trigonellafoenum-graecumL.)[J].J Med Plants,2010,9(35):1-18.
[13] STOHS S J,KAUL B,STABA E J.The metabolism of14C-cholesterol byDioscoreadeltoideasuspension cultures[J].Phytochemistry,1969,8(9):1679-1686.
[14] JOLY R A,BONNER J,BENNETT R D,et al.The biosynthesis of steroidal sapogenins inDioscoreafloribundafrom doubly labelled cholesterol[J].Phytochemistry,1969,8(9):1709-1711.
[15] BENNETT R D,HEFTMANN E,JOLY R A.Biosynthesis of diosgenin from 26-hydroxycholesterol inDioscoreafloribunda[J].Phytochemistry,1970,9(2):349-353.
[16] TAL B,TAMIR I,ROKEM J,et al.Isolation and characterization of an intermediate steroid metabolite in diosgenin biosynthesis in suspension cultures ofDioscoreadeltoideacells[J].Biochem J,1984,219(2):619.
[17] STOHS S J,SABATKA J J,ROSENBERG H.Incorporation of 4-14C-22,23-3H-sitosterol Into diosgenin byDioscoreadeltoideatissue suspension cultures[J].Phytochemistry,1974,13(10):2145-2148.
[18] DIENER A C,LI H,ZHOU W X,et al.Sterol methyltransferase 1 controls the level of cholesterol in plants[J].Plant cell,2000,12(6):853-870.
[19] SCHAEFFER A,BRONNER R,BENVENISTE P,et al.The ratio of campesterol to sitosterol that modulates growth inArabidopsisis controlled bySTEROLMETHYLTRANSFERASE2;1[J].Plant J,2001,25(6):605-615.
[20] SUZUKI M,XIANG T,OHYAMA K,et al.Lanosterol synthase in dicotyledonous plants[J].Plant cell physiol,2006,47(5):565-571.
[21] VAIDYA K,GHOSH A,KUMAR V,et al.De Novo transcriptome sequencing inTrigonellafoenum-graecumL.to identify genes involved in the biosynthesis of diosgenin[J].Plant Gen,2013,6(2):1-11.
[22] 雷彩燕,李静静,闫凤鸣.植物皂苷生物合成及调控研究进展[J].中国农业科技导报,2014, 16(4):50-58.
[23] 陈迪,陈永勤,杨之帆,等.盾叶薯蓣环阿屯醇合酶基因克隆与表达(英文)[J].西北植物学报,2009,29(2):221-228.
[24] 涂碧梦,陈永勤,杨之帆.盾叶薯蓣环阿屯醇合酶全长基因的克隆与分析[J].西北植物学报,2010(1):8-13.
[25] YE Y,WANG R,JIN L,et al.Molecular cloning and differential expression analysis of a squalene synthase gene fromDioscoreazingiberensis,an important pharmaceutical plant [J].Molecular biology reports,2014,41(9):6097-6104.
[26] DIARRA S T,HE J,WANG J,et al.Ethylene treatment improves diosgenin accumulation in in vitro cultures ofDioscoreazingiberensisvia up-regulation of CAS and HMGR gene expression [J].Electronic journal of biotechnology,2013,16(5):9.
[27] LAULE O,FÜRHOLZ A,CHANG H S,et al.Crosstalk between cytosolic and plastidial pathways of isoprenoid biosynthesis inArabidopsisthaliana[J].Proceedings of the national academy of sciences,2003,100(11):6866-6871.
[28] 王润发.盾叶薯蓣 DXR 基因和 MDS 基因的克隆与功能验证[D].武汉:湖北大学,2014.
[29] 杨婷.盾叶薯蓣 4-羟基-3-甲基-2-丁烯基焦磷酸还原酶基因克隆与功能分析[D].武汉:湖北大学,2014.
Research Progress of Diosgenin Biosynthesis Route ofDioscoreazingiberensisC. H. Wright
BI Huai-long, QIAO Ya-ru, HUA Wen-ping*
(Department of Biological Science and Technology, Shaanxi Normal University, Xi’an, Shaanxi 710100)
AbstractWe reviewed the research progress of diosgenin biosynthesis route of Dioscorea zingiberensis C. H. Wright, as well as the research progress of related enzymes. The biosynthetic route was deduced, which laid foundation for the research on diosgenin biosynthesis of D. zingiberensis, and its production by bioengineering.
Key wordsDioscorea zingiberensis C. H. Wright; Diosgenin; Biosynthesis route; Key enzyme
基金项目大学生创新项目(2015DC031,201514390767);陕西学前师范学院基金项目(2013KJ033)。
作者简介毕淮龙(1994- ),男,陕西安康人,本科生,专业:生命科学。*通讯作者,副教授,博士,从事药用植物次生代谢调控研究。
收稿日期2016-03-30
中图分类号R 284.3
文献标识码A
文章编号0517-6611(2016)11-142-03

