固体直接进样-原子荧光法测定土壤中的镉
郑 波,刘潇威*,穆 莉,徐亚萍,戴礼洪,冯 礼(.农业部环境保护科研监测所,环境质量监督检验测试中心,天津3009;.北京吉天仪器有限公司,北京0005)
固体直接进样-原子荧光法测定土壤中的镉
郑波1,刘潇威1*,穆莉1,徐亚萍1,戴礼洪1,冯礼2
(1.农业部环境保护科研监测所,环境质量监督检验测试中心,天津300191;2.北京吉天仪器有限公司,北京100015)
摘要:采用固体进样原子荧光镉分析仪测定土壤中的镉无需进行样品的消解前处理,避免了元素损失,提高了检测效率。研究表明,采用Pauwels公式和相对均匀度因子(HE)估算实际样品的最小取样量在3 mg前提下,研磨粒径小于0.3 mm(60目)即可满足仪器微量进样要求;采用归一化方法得出干燥灰化功率为50 W、30 s,70 W、40 s,仪器的Ar-H2(9:1,V/V)载气流量为800 mL·min-1时,仪器检出限为0.016 ng、方法检出限为0.005 3 mg·kg-1,试验验证相对标准偏差小于10%,分析时间小于3 min,且与ICP-MS法测定结果无显著性差异(P>0.05)。该仪器检测方法操作简便、耗时短,适用于田间土壤中Cd的分析测定。
关键词:直接进样;原子荧光光谱;土壤;镉;电热蒸发
郑波,刘潇威,穆莉,等.固体直接进样-原子荧光法测定土壤中的镉[J].农业环境科学学报, 2016, 35(5):1016-1020.
ZHENG Bo, LIU Xiao-wei, MU Li, et al. Determination of cadmium in soil by using direct solid sampling-atomic fluorescence spectrometry method[J]. Journal of Agro-Environment Science, 2016, 35(5): 1016-1020.
镉是环境和工业污染物中对人体健康具有毒性的重金属元素之一[1]。同其他重金属相比,镉表现出较强的传播性和潜伏性[2]。当人体长期暴露于镉环境,摄入被镉污染严重的食品时,将会出现镉慢性中毒,对肺、肾、心血管系统、生殖系统造等成不良影响[2-3]。近几年,土壤镉污染已严重威胁到人体的健康,使得土壤中镉的测定方法研究具有更为重要的现实意义。
土壤中镉元素的检测方法很多,广泛应用的有石墨炉原子吸收分光光度法(GFAAS)[4]、火焰原子吸收分光光度法(FAAS)[5]、原子荧光分光光度法(AFS)[6]、电感耦合等离子体原子发射光谱法、质谱法(ICP-AES、ICP-MS)[7-9]等。上述方法通常需要复杂的样品前处理,增大了样品被污染和分析元素损失的风险。采用固体直接进样技术则能很好地解决这些问题,其检测取样量少,可避免可能出现的污染和损失,简化样品前处理过程,缩短分析时间,提高检测效率[10-11]。近年来,固体直接进样技术有很大的发展,如美国利曼公司固体直接进样测汞仪在土壤[12]和食品[10]检测中的应用,德国耶拿公司固体直接进样石墨炉原子吸收在土壤[13]分析、激光烧蚀[14]固体进样技术领域的应用等。北京吉天仪器有限公司研发的固体进样原子荧光镉分析仪DCD-AFS,结合原子捕获阱技术的电热蒸发固体直接进样方法,将样品灰化除去水分和有机质后,利用特异性原子捕获阱高选择性地捕获电热蒸发出的待测元素,同时实现了与蒸发基体的分离,从而减少了基体带来的光谱和非光谱干扰,既发挥了固体直接进样的优势,又避免了电热蒸发带来的严重的基体干扰,成为新的研究热点,已成功用于测定苹果、菠菜[15]、大米[16]和常见农产品[17]中的镉。
为达到田间土壤快速检测的目标,本文采用原子捕获阱技术和电热蒸发技术与原子荧光相结合,通过归一化方法和控制变量法对仪器条件、最小取样量和样品粒径大小进行了优化选择。
1 试验部分
1.1仪器及试剂
固体进样原子荧光镉分析仪DCD-AFS(北京吉天仪器有限公司),Ar-H2混合发生器(北京吉天仪器有限公司)。GSS系列土壤成分分析标准物质(中国地质科学院物化探所),超纯水(18.24 MΩ·cm-1)。
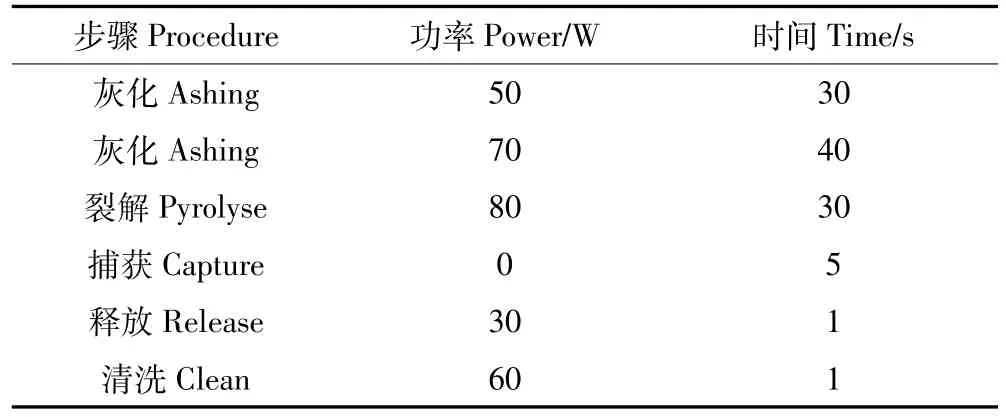
表1 控温程序Table 1 Temperature-controlling programme
1.2仪器条件
控温程序见表1。其中除捕获?步骤无加热外,其余均采用阶梯升温方式。
原子荧光条件见表2,仪器原理如图1所示。

图1 检测原理示意图Figure 1 Schematic diagram of analytical procedures for SS-ETV-AFS

表2 原子荧光条件参数Table 2 Operating parameters for atomic fluorescence spectrometry
2 结果与讨论
2.1灰化和蒸发程序优化
对于基体复杂程度不同的固体样品,测量所需的灰化蒸发温度和时间不同。高功率条件能够使样品短时间充分灰化,但功率过高时,可能造成Cd元素的损失,降低回收率。添加100 μg·L-1的Cd标准溶液,比较不同灰化温度下响应值的变化,以功率为50 W 和70 W的响应值定为100,其他做归一化处理,结果表明:随着功率的增加,响应值逐渐增加,两步灰化功率分别在50 W和70 W达到最大响应值,且稳定性良好,如图2所示。
梯度升温可以防止温度骤升导致的爆沸,保持灰化平缓且充分。综合图2和表3,根据响应值和相对标准偏差选择最优的干燥灰化条件是50 W、30 s,70W、40 s。本试验最终选择梯度升温灰化条件为:初步灰化50 W、30 s,充分灰化70 W、40 s。
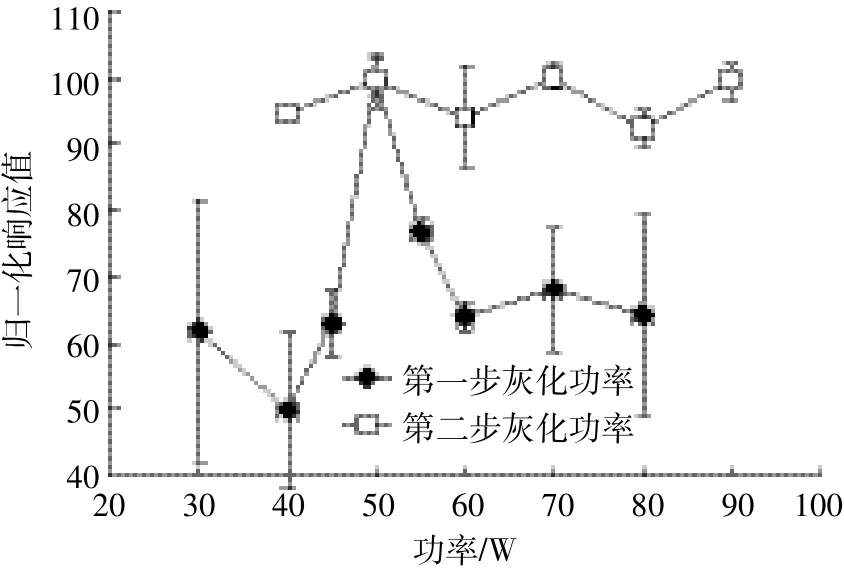
图2 灰化功率对响应值的影响Figure 2 Effect of vaporizing power on normalized intensity
2.2载气流速
本研究使用Ar-H2混合发生器产生载气,通过测定100 μg·L-1的Cd标液,比较载气流速对测定结果的影响,发现在载气流速达到800 mL·min-1时响应值最高,稳定性也较好,相对标准偏差为5.2%。载气流速继续增大,响应值逐渐降低,可能是流速过高产生稀释效应所致(图3)。
2.3测试样品粒径和最小取样量的选择
当前所用的土壤标准物质,证书标识最小取样量为0.2 g,无法满足本实验微量进样要求,因此利用相对均匀度因子(HE)[18]和Pauwels[19]公式对测定土壤中Cd的最小取样量(M)进行评价,并对土壤样品粒径的选择进行评估。
均匀度因子:HE=RSD×m1/2
式中:RSD为n个测定值的相对标准偏差;m为n个样品的平均质量,mg。
Pauwels公式:M=(k2′×RSD/UNC)2×m
式中:M为最小取样量,mg;k2′为正态分布常数;UNC为总体相对不确定度。
根据《土壤环境质量标准》(HJ/T 166—2004)[20],采集四川地区田间土壤样品,经风干研磨后,分别过20、40、60、100目筛,对于田间土壤样品的测定,10%的不确定度完全可以接受。按以上公式进行估算,结果如表4所示。
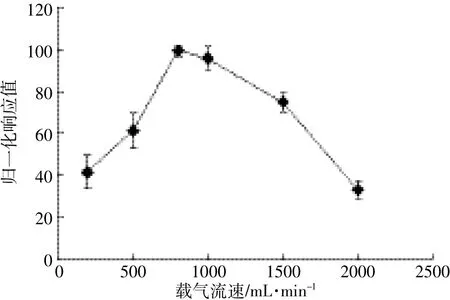
图3 载气流速对响应值的影响Figure 3 Effect of carrier gas flow rates on normalized intensity
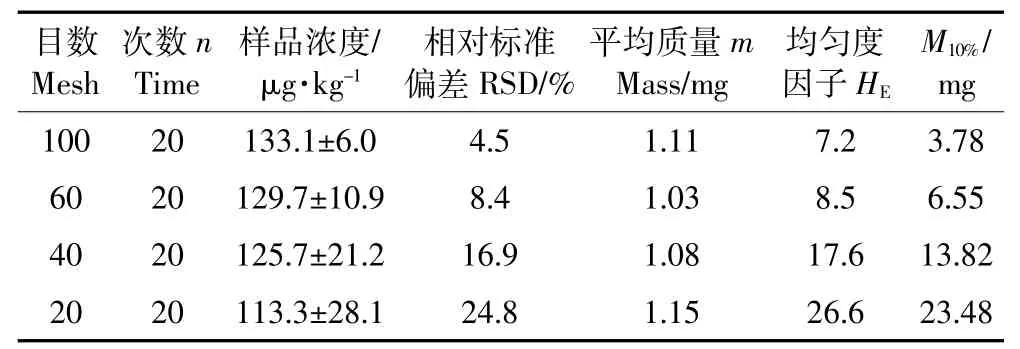
表4 不同研磨目数下测定Cd含量时的HE和最小取样量MTable 4 HEand M values of soil samples for Cd analysis at different sample particle sizes

表3 灰化时间优化Table 3 Optimization of ashing time

?
由表4可以看出,60、100目样品的HE小于10,表明均匀度良好;20、40目样品的HE大于10,表明均匀度较差不能保证其准确性。因此,研磨目数大于60目时,用ETV-AFS测定土壤样品的最小取样量范围为3~6 mg,符合进样和测定要求。
2.4标准曲线及检出限
测定土壤中重金属含量,采用测定标准参考物质的方法能更好地反映准确度,因此选用不同基质的国家土壤标准物质建立曲线。由于各类型土壤中Cd含量不同,为了得到更好的峰形,不同标准曲线的建立采用了不同的仪器条件(灯电流40~60 mA和负高压250~270 V),选用GSS-2和GSS-5。称取土壤标准物质(Cd计),建立以Cd质量(ng)为横坐标,荧光值为纵坐标的标准曲线。对0.09、0.15、0.24、0.31、0.37 ng低浓度Cd标准物质测定得线性回归方程为:
Y=1 980.5X+89.2,R2=0.997 9
对0.42、0.77、0.94、1.04、1.62 ng高浓度Cd标准物质测定得线性回归方程为:
Y=252.475 6X+8.629 1,R2=0.996 3
以上结果表明,荧光值与Cd含量线性良好。使用进样专用的特制石墨舟,连续测定11次空白值,空白标准偏差SD,确定3倍标准偏差为仪器检出限,得到该值为0.016 ng。称取3 mg土壤样品,重复测定10次,统计测定结果的标准偏差,3倍标准偏差得到该方法检出限为0.005 3 mg·kg-1。
2.5国家标准物质的测定
使用本方法对多种土壤标准物质进行了测定,以考查分析结果的准确性。选用的土壤来自我国不同地域,具有不同性质和广泛代表性。测试结果见表5,所测值均在标物的不确定度范围内。
2.6实际样品检测与验证
将本研究方法检测结果与ICP-MS进行对比(表6),方差分析显示两者检测结果无显著性差异(P>0.05)。
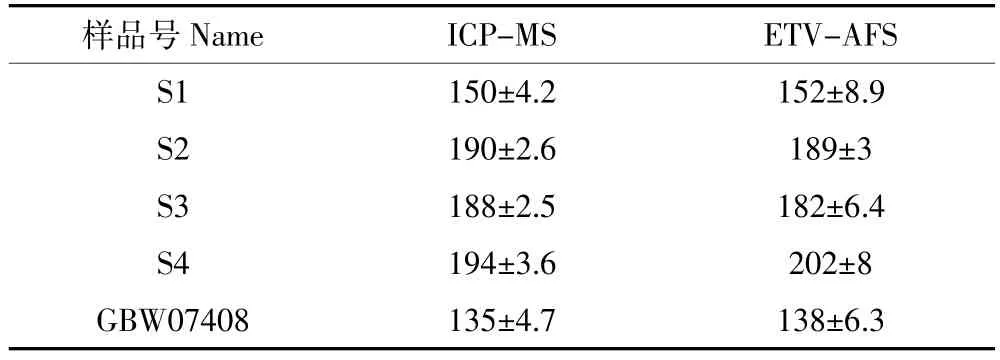
表6 ETV-AFS与ICP-MS测定值比对(μg·kg-1)Table 6 Comparisons of ETV-AFS and ICP-MS
3 结论
本文建立了固体进样原子荧光测定田间土壤中镉含量的方法,采用干燥灰化功率为50 W、30 s和70 W、40 s,在Ar-H2(9:1,V/V)载气流量为800 mL·min-1的条件下,方法标准曲线相关系数R在0.995以上,方法检出限为0.005 3 mg·kg-1(进样量3 mg),实际样品和国家标准土壤样品测定的相对标准偏差RSD<10%,分析时间不超过3 min。该方法进样量小,适合于痕量分析,并且污染少,简便快速,符合环境可持续性发展的要求,具有很强的实用性和广阔的发展前景。

表5 标准物质测量结果Table 5 Test results of standard soil samples(n=3)
参考文献:
[1]Jackson L S. Chemical food safety issues in the United States:Past, present, and future[J]. Journal of Agricultural and Food Chemistry, 2009, 57(18):8161-8170.
[2]Tang X Y, Zhu Y G, Cui Y S, et al. The effect of ageing on the bioaccessibility and fractionation of cadmium in some typical soils of China[J]. Environment International, 2006, 32(5):682-689.
[3]Davis A C, Wu P, Zhang X F, et al. Determination of cadmium in biological samples[J]. Applied Spectroscopy Reviews, 2006, 41(1):35-75.
[4]邵文军,张激光,刘晶晶.石墨炉原子吸收光谱法测定岩石和土壤中痕量镉[J].岩矿测试, 2008, 27(4):310-312. SHAO Wen-jun, ZHANG Ji-guang, LIU Jing-jing. Determination of trace cadmium in rock and soil samples by graphite furnace atomic absorption spectrometry[J]. Rock and Mineral Analysis, 2008, 27(4):310-312.
[5]景丽洁,马甲.火焰原子吸收分光光度法测定污染土壤中5种重金属[J].中国土壤与肥料, 2009(1):74-77. JING Li-jie, MA Jia. Determination of 5 kinds of heavy metals in contaminated soil by flames atomic absorption spectrophotometry[J]. Soils and Fertilizers Sciences in China, 2009(1):74-77.
[6]赖冬梅,邓天龙.抗坏血酸-磺胺增效氢化物发生-原子荧光光谱法测定土壤中镉[J].分析化学, 2010, 38(4):542-546. LAI Dong-mei, DENG Tian-long. Determination of cadmium in soil samples with ascorbic acid and sulfanilamide as enhanced reagent using hydride generation atomic fluorescence spectrometry[J]. Chinese Journal of Analytical Chemistry, 2010, 38(4):542-546.
[7]徐爱列. ICP-AES测定海娜植物及土壤中镉、铜、铅、锌[J].安徽农业科学, 2007, 35(21):6353-6354. XU Ai-lie. Determination of Cd, Cu, Pb and Zn in henna plant and the soil with ICP-AES[J]. Journal of Anhui Agricultural Sciences, 2007, 35 (21):6353-6354.
[8]Waterlot C, Douay F. The problem of arsenic interference in the analysis of Cd to evaluate its extractability in soils contaminated by arsenic[J]. Talanta, 2009, 80(2):716-722.
[9]Guo W, Hu S, Xiao Y, et al. Direct determination of trace cadmium in environmental samples by dynamic reaction cell inductively coupled plasma mass spectrometry[J]. Chemosphere, 2010, 81(11):1463-1468. [10]Barst B D, Hammerschmidt C R, Chumchal M M, et al. Determination of mercury speciation in fish tissue with a direct mercury analyzer[J]. Environmental Toxicology and Chemistry, 2013, 32(6):1237-1241.
[11]张英,王金玉,毛雪飞,等.固体进样等离子体光谱技术在食品元素分析中的应用[J].食品工业科技, 2015(12):353-357. ZHANG Ying, WANG Jin-yu, MAO Xue-fei, et al. Applications of solid sampling plasma spectrometric technology for elemental analysis in food[J]. Science and Technology of Food Industry, 2015(12):353-357.
[12]王永强,冯敏洪.自动固体测汞仪测定土壤中的汞[J].资源节约与环保, 2015(4):50. WANG Yong-qiang, FENG Min-hong. Determination of mercury in soil by automatic solid mercury measurement instrument[J]. Resource Savingand Environmental Protection, 2015(4):50.
[13]徐鹏,王青柏,姜雅红.固体进样-石墨炉原子吸收光谱法测定土壤中重金属[J].分析试验室, 2015(5):554-557. XU Peng, WANG Qing-bo, JIANG Ya-hong. Direct determination of heavy metals in soil by graphite furnace atomic absorption spectrometry with solid sampling[J]. Chinese Journal of Analysis Laboratory, 2015 (5):554-557.
[14]Bu K, Cizdziel J V, Reidy L. Analysis of herbal supplements for selected dietary minerals and trace elements by laser ablation- and solutionbased ICP-MS[J]. Microchemical Journal, 2013, 106:244-249.
[15]黄亚涛,毛雪飞,刘霁欣,等.电热蒸发钨丝在线捕获原子荧光光谱法直接测定菠菜中痕量镉[J].分析化学, 2013, 41(10):1587-1591. HUANG Ya-tao, MAO Xue-fei, LIU Ji-xin, et al. Direct determination of ultratrace cadmium in spinach by electrothermal vaporization atomic fluorescence spectrometry using on-line atom trap of tungsten coil[J]. Chinese Journal of Analytical Chemistry, 2013, 41(10):1587-1591.
[16]Mao X, Liu J, Huang Y, et al. Assessment of homogeneity and minimum sample mass for cadmium analysis in powdered certified reference materials and real rice samples by solid sampling electrothermal vaporization atomic fluorescence spectrometry[J]. Journal of Agricultural and Food Chemistry, 2013, 61(4):848-853.
[17]Feng L, Liu J. Solid sampling graphite fibre felt electrothermal atomic fluorescence spectrometry with tungsten coil atomic trap for the determination of cadmium in food samples[J]. Journal of Analytical Atomic Spectrometry, 2010, 25(7):1072-1078.
[18]Kempenaers L, Janssens K, Jochum K P, et al. Micro-heterogeneity study of trace elements in USGS, MPI-DING and NIST glass reference materials by means of synchrotron micro-XRF[J]. Journal of Analytical Atomic Spectrometry, 2003, 18(4):350-357.
[19]Pauwels J, Hofmann C, Grobeeker K H. Homogeneity determination of Cd in plastic CRMs using solid sampling atomic absorption spectrometry[J]. Fresenius Journal of Analytical Chemistry, 1993, 345(7):475-477.
[20]中华人民共和国环境保护行业标准. HJ/T 166—2004土壤环境监测技术规范[S].北京:中国环境科学出版社, 2005. Environmental Protection Industry Standard of the People′s Republic of China. HJ/T 166—2004 The technical specification for soil environmental monitoring[S]. Beijing:China Environmental Science Press, 2005.
中图分类号:X833
文献标志码:A
文章编号:1672-2043(2016)05-1016-05
doi:10.11654/jaes.2016.05.028
收稿日期:2015-11-05
基金项目:国家重大科学仪器设备开发专项(2011YQ14014905)
作者简介:郑波(1991—),内蒙古赤峰人,男,硕士研究生,从事土壤重金属检测。E-mail:616312122@163.com
*通信作者:刘潇威E-mail:xwliu2006@163.com
Determination of cadmium in soil by using direct solid sampling-atomic fluorescence spectrometry method
ZHENG Bo1, LIU Xiao-wei1*, MU Li1, XU Ya-ping1, DAI Li-hong1, FENG Li2
(1.Agro-Environmental Protection Institute Ministry of Agriculture, Quality Supervision and Testing Center, MOA, Tianjin 300191, China; 2.Beijing Titan Instruments Company Limited , Beijing 100015, China)
Abstract:The current methods for determining soil cadmium(Cd)require complicated pretreatments. Here we developed a method to determine soil Cd by using solid sample-atomic fluorescence spectrometry. The method avoided element loss and improved the analysis efficiency. Estimates by the Pauwels formula and Homogeneity(HE)showed that minimum of 3 mg sample with particle size less than 0.3 mm(60 mesh)met the trace sampling requirements of the instrument. The power and time of sample drying were 50 W and 30 s, and those for sample ashing 70 W and 40 s, respectively. The Ar-H2(9:1, V/V)flow rate was controlled at 800 mL·min-1. The instrument detection limit and method detection limit were 0.016 ng and 0.005 3 mg·kg-1, respectively, with the relative standard deviations less than 10%. The analysis time was less than 3 min. The results obtained by the present method was not significantly different(P>0.05)from those of ICP-MS. In conclusion, the present method is quick, simple, and sensitive, and can meet the requirements of cadmium determination in soils.
Keywords:direct solid sampling; atomic fluorescence spectrometry; soil; cadmium; electrothermal vaporization

