长江中游湖泊柱状沉积物的垂直污染特征
罗明科,田学达,余 辉,杨 超,牛 远,刘 鹏,牛 勇(.湘潭大学化工学院,湖南湘潭405;.中国环境科学研究院,环境基准与风险评估国家重点实验室,北京000;.环境保护部环境与经济政策研究中心,北京0009)
涂 汉,吴 攀*,韩志伟,曹星星,张 水(贵州大学资源与环境工程学院,贵阳550025)
刘 梦1,2,王华静1,王鲲鹏2,杨金燕2*(1.四川师范大学地理与资源科学学院,成都610101;2.四川大学建筑与环境学院,成都610065)
长江中游湖泊柱状沉积物的垂直污染特征
罗明科1,2,田学达1,余辉2*,杨超3,牛远2,刘鹏1,2,牛勇2
(1.湘潭大学化工学院,湖南湘潭411105;2.中国环境科学研究院,环境基准与风险评估国家重点实验室,北京100012;3.环境保护部环境与经济政策研究中心,北京100029)
摘要:为研究长江中游湖泊沉积物污染的变化规律和主要来源,采集了武汉东湖、黄石海口湖、钟祥南湖3个不同类型湖泊的柱状沉积物,研究总有机碳(TOC)、总氮(TN)和重金属(Zn、Cu、Ni、Cr、Pb)的垂直分布特征。结果表明:3个湖泊沉积物TOC、TN含量从底层到表层总体呈增加趋势,30~10 cm增加速度较大,与各湖泊环境演变时间一致,其中TOC含量最大的是黄石海口湖,TN含量最大的是武汉东湖。研究区Zn、Cu、Pb受人为影响较大,Cr主要来自土壤环境,5种金属污染程度为武汉东湖>黄石海口湖>钟祥南湖。主成分分析和相关性分析表明,三个湖泊污染人为贡献率大于自然贡献率,营养盐和重金属Pb是共有的污染问题,重金属的污染来源受多种因素控制。
关键词:柱状沉积物;TOC;TN;重金属;相关分析;主成分分析
罗明科,田学达,余辉,等.长江中游湖泊柱状沉积物的垂直污染特征[J].农业环境科学学报, 2016, 35(5):955-962.
LUO Ming-ke, TIAN Xue-da, YU Hui, et al. Vertical pollution characteristics of sediments from lakes in middle reaches of Yangtze River[J]. Journal of Agro-Environment Science, 2016, 35(5): 955-962.
长江中下游是我国浅水型湖泊分布最密集的地区,水域面积大于1 km2的湖泊总数超过650个,其中大约有1/3的湖泊位于中游湖北,此类湖泊多属浅平宽广型,湖底泥沙淤积较厚,平均水深1~2 m,是整个长江中下游湖泊群中一个重要组成部分,研究该地区的湖泊对整个长江游流域有重要意义[1]。
近年来我国水体污染与富营养化问题日益突出,尤其是河流、湖泊等地表水。城市湖泊水环境质量不断下降,部分区域已出现水体黑臭、沉积物大量堆积等现象,导致水体功能严重丧失,给人类的健康、社会的发展带来了长久的危害[2]。沉积物是湖泊一系列复杂物理、化学、生物过程的产物,能直接反映出湖泊污染的现状及湖泊环境演变的过程[3-5]。目前,长江流域湖泊的沉积物研究不少,如王玲玲等[6]通过研究梁子湖沉积物确定了该区域重金属污染种类,王毛兰等[7]分析了鄱阳湖三江口柱状沉积物的主要污染来源,李辉等[8]根据滇池柱状沉积物的总氮变化特征得出其历史变化规律。但目前的研究大部分针对单个湖泊,城市湖泊与郊区湖泊环境变化有何关联,湖泊开发种植对湖泊环境具体有何影响,尚待深入研究。有学者研究了长江中游部分湖泊沉积物的营养盐形态特征[9]和重金属的变化规律[10],但针对的仅仅是表层沉积物,这对恢复长江流域湖泊古环境研究显然不够,因为除了要掌握近几年环境污染状况外,还必须了解历史演变进程、历史含量丰度等。本文基于这一角度,选取长江中游三个典型的湖泊——武汉市东湖(城市内湖)、黄石市海口湖(种植型湖泊)、钟祥市南湖(郊区型湖泊),通过分析其柱状沉积物的重金属和营养盐垂直变化特征,揭示其环境演变规律和污染来源,以期为长江流域环境保护和时代变化特征提供一定参考。
1 材料与方法
1.1样品采集
2014年10月对武汉东湖、黄石海口湖、钟祥南湖进行了调查,三个湖泊均为浅水型湖泊,淤泥较厚,湖盆平坦,故采样点设在人为影响较少,且能最大程度反映整个湖泊汇水情况的湖中心。武汉东湖是我国第二大城市内湖,由五大湖区构成,周边主要为风景区和居住区,人员流量大,水域面积32 km2,平均水深约2 m,位于长江南岸,由长江淤塞而形成,采样点布在郭郑湖区;黄石海口湖,水域面积为12.9 km2,平均水深1.3 m,位于长江右岸,属沉溺谷经积水而成的滞积湖,周边以农田为主,湖区内被围格开发种植莲藕,采样船无法达到主湖中心,采样点设在较靠近湖中心处;钟祥南湖为郊区湖泊,水域面积13.7 km2,平均水深1.5 m,毗邻汉江,属于河湖相沉积的泻湖,周边工业较少,湖泊水质清澈,采样点设在湖中心。各湖泊采样点位[11]如图1所示。

图1 各湖泊采样点位示意图Figure 1 Sampling sites in three lakes
以GPS定位,柱状重力采泥器采样。沉积物柱长不少于50 cm,现场以2 cm为一层切割,将样品装入聚乙烯封口袋中低温保存,带回实验室冷冻。
1.2样品处理与分析
柱状沉积物样品先用冷冻干燥机干燥(-50℃以下,5 d以上),待干燥完全选出石块、动植物残体等杂物,经玛瑙研钵研磨处理后,过100目尼龙筛,存放于样品袋中待用。
称取0.3 g上述样品,加HNO3-HCl-HF混酸使用微波消解仪(CEM Mars6)消解[12],消解完全后采用等离子发射光谱仪ICP-OES(Optima 8000DV)检测样品中Cu、Zn、Pb、Cr、Ni的含量,标准样由国家标准物质中心提供;TOC、TN采用元素分析仪Organic Elemental Analyzer(FLASH 2000)测定。所用数据为3个平行样品均值,相对标准偏差均保持在10%以内,分析结果均以沉积物干重计。数据采用IBM SPSS Statistics 21与Origin 8.0处理,包括数据统计、相关分析(显著P<0.05,极显著P<0.01)、主成分分析。
1.3营养盐评价
有机指数和有机氮常用来衡量一个水体沉积物环境污染的指标[13]。计算方法:有机指数=有机碳(%)×有机氮(%);有机氮(%)=总氮(%)×0.95。水体沉积物有机指数评价标准见表1。
1.4重金属污染评价
地累积指数(Igeo)法是评价沉积物中重金属污染状况常用的方法之一,以相应天然含量或背景值为参比,得到因人为活动所造成的重金属总富集程度[14]。
Igeo=log2[Cn/(1.5×Bn)]
式中:Cn为沉积物中重金属的实测值,mg·kg-1;Bn为沉积岩中重金属的环境背景值mg·kg-1,本研究采用湖北省土壤背景值进行评价(Zn、Cu、Ni、Cr、Pb分别为83.6、30.7、37.3、86.0、26.7 mg·kg-1)。
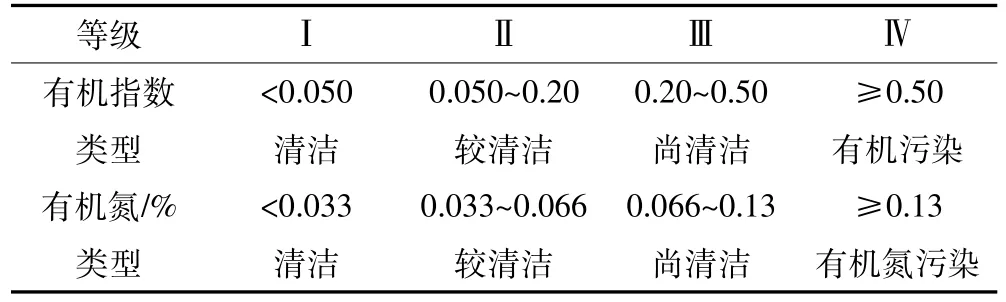
表1 水体沉积物有机指数评价标准Table 1 Evaluation criterion of organic indexes in sediments
地累积指数所对应的污染级别和程度见表2。
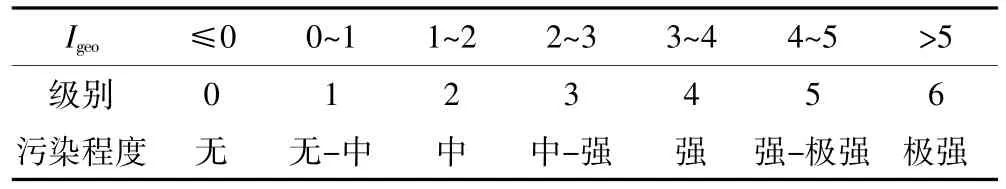
表2 地累积指数(Igeo)与污染级数Table 2 Index of geo-accumulation and pollution grades
沉积物中重金属污染具有伴生性或综合性的特点,单个金属污染因子评价往往难以概括整个湖泊沉积物的重金属污染程度。内梅罗指数是一种兼顾结合最大值的计权型多因子环境质量指数,是应用较多的多因子环境质量指数的综合评价方法[15]。

式中:Pi为单个元素污染指数;Ci为单个元素实测值,mg·kg-1;Si为单个元素在该区域的基线值或评价标准值,mg·kg-1;PN为内梅罗污染指数;Piave为所有元素污染指数的平均值;Pimax为所有元素污染指数的最大值。
内梅罗污染指数所对应的污染等级和程度见表3。
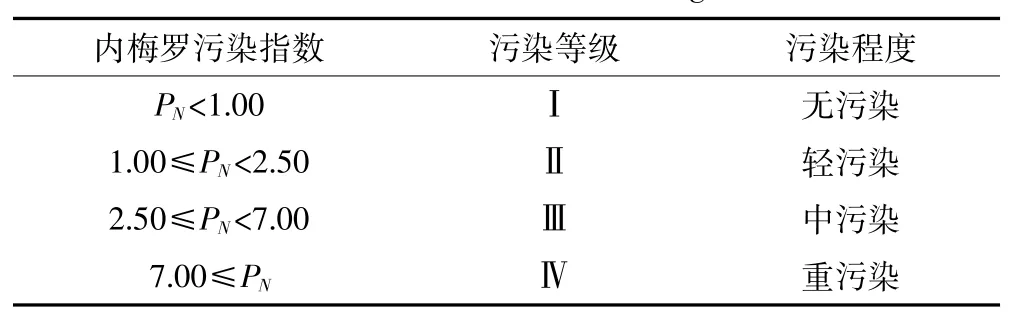
表3 内梅罗污染指数Table 3 Index of Nemerow integrated
2 结果与讨论
2.1沉积物环境因子垂直分布特征
2.1.1营养盐分布特征
从柱状底泥TOC、TN垂直变化图(图2)发现,武汉东湖、黄石海口湖和钟祥南湖柱状沉积物的TOC含量范围分别为9.03~41.7、26.1~55.7、7.14~21.9 mg· g-1,平均值分别为26.0、38.5、13.6 mg·g-1;TN含量范围分别为1.49~5.22、1.85~5.41、0.60~2.81 mg·g-1,平均值分别为3.34、3.08、1.64 mg·g-1。
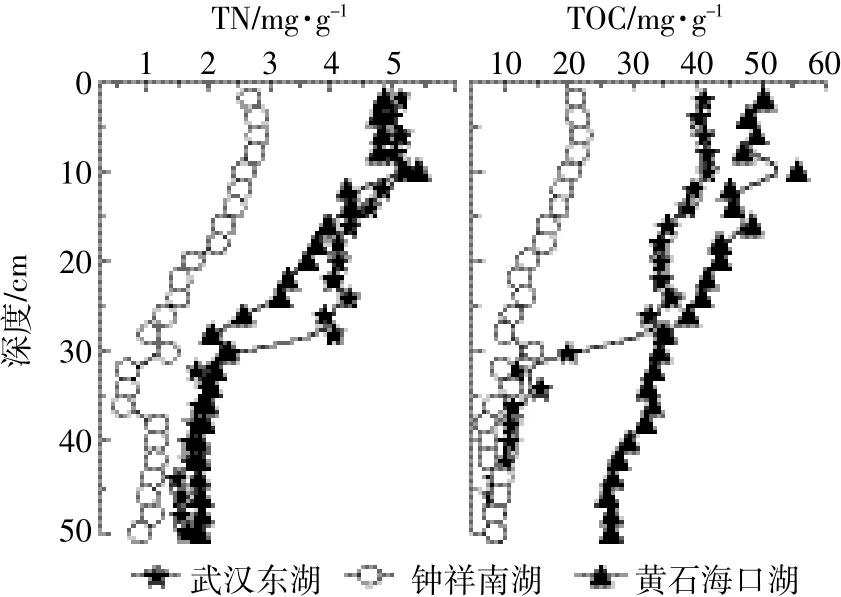
图2 湖泊柱状沉积物TOC、TN含量的垂直变化Figure 2 Vertical characteristics of TOC and TN in lake sediments
武汉东湖、黄石海口湖、钟祥南湖柱状沉积物的TOC和TN,从底层到表层基本呈增加的趋势。一般沉积物表层氧化还原电位较高,所含有机质也较高,表层沉积物中有机质还未完全矿化或还原,被后来的沉积物覆盖并积累,随着深度的增加,氧化还原电位降低,总有机质含量减少;总体上TOC和TN在30~10 cm增加速度较快,50~30、10~0 cm趋于平缓。由此可得30 cm与10 cm处各湖泊环境发生较大变化,根据文献[16]提供的武汉东湖在该点位附近的平均沉积速率值5.8 mm·a-1计算,分别得出变化时间为1962年和1996年,与武汉东湖周边20世纪60年代至90年代大建钢铁冶炼厂导致环境污染时间点吻合。该结果与刘碧波等[17]研究结果一致。
2.1.2重金属分布特征
三个湖泊重金属含量的垂直变化情况如图3所示。Zn、Cu和Ni平均含量最大的是武汉东湖,分别为121、44.7、43.5 mg·kg-1;Pb平均含量最大的是黄石海口湖,为37.8 mg·kg-1;武汉东湖和钟祥南湖的Cr平均含量与背景值基本一致。武汉东湖的Zn、Cu和Pb从底层到表层总体上呈增加的趋势,三者与深度极显著负相关(表4,P<0.01),其中Zn与Cu均在30 cm附近急剧增加;Ni总体上为递减,与深度极显著正相关;Cr变化无明显特征,在背景值附近波动,变异系数为6.47%,与深度相关性不显著(P>0.05)。黄石海口湖的Zn、Cu、Pb变化趋势及相关性(表5)与武汉东湖接近,三者均在30 cm附近急剧增加;Ni和Cr在均值附近波动,变异系数分别为4.64%和7.18%,与深
度相关性不显著。钟祥南湖的Zn、Cu、Ni和Cr四种金属变化特征不明显,变异系数分别为20.4%、15.7%、12.1%和5.55%;Zn、Cu和Ni均与深度相关性不显著(表6);Cu、Ni与Cr显著正相关;Pb在30 cm附近快速增加,6 cm附近达到最大值,与其他金属相关性均不显著,与深度极显著负相关。
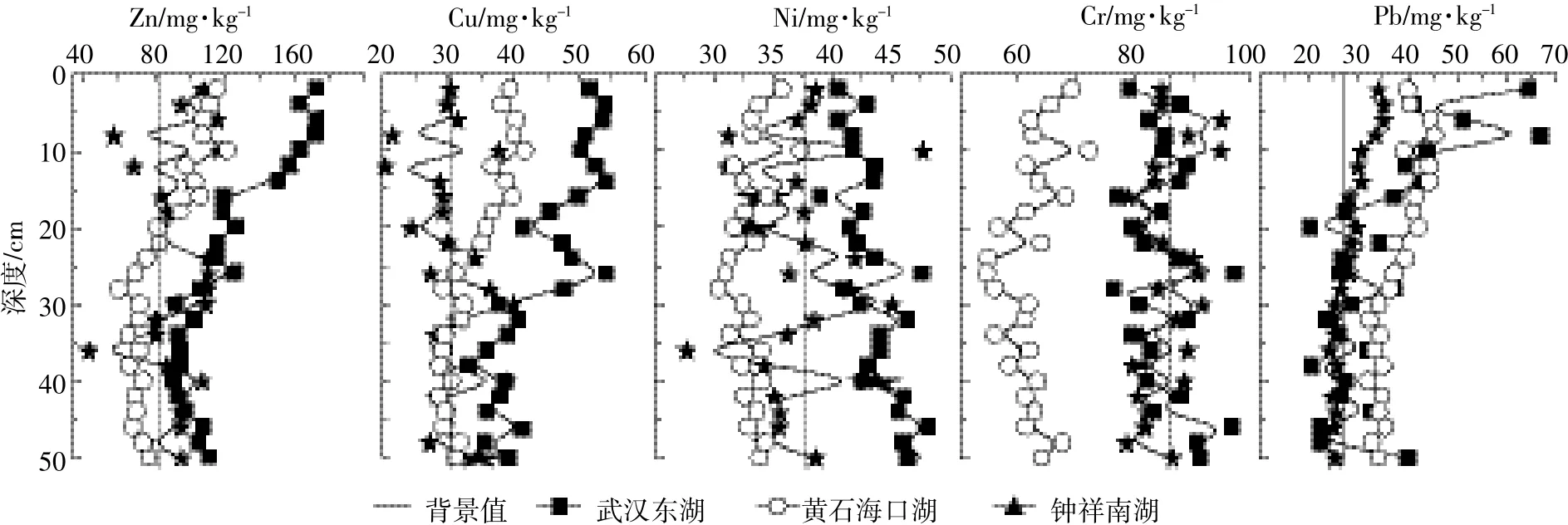
图3 湖泊重金属含量的垂直变化Figure 3 Vertical distribution characteristics of heavy metals in lake sediments
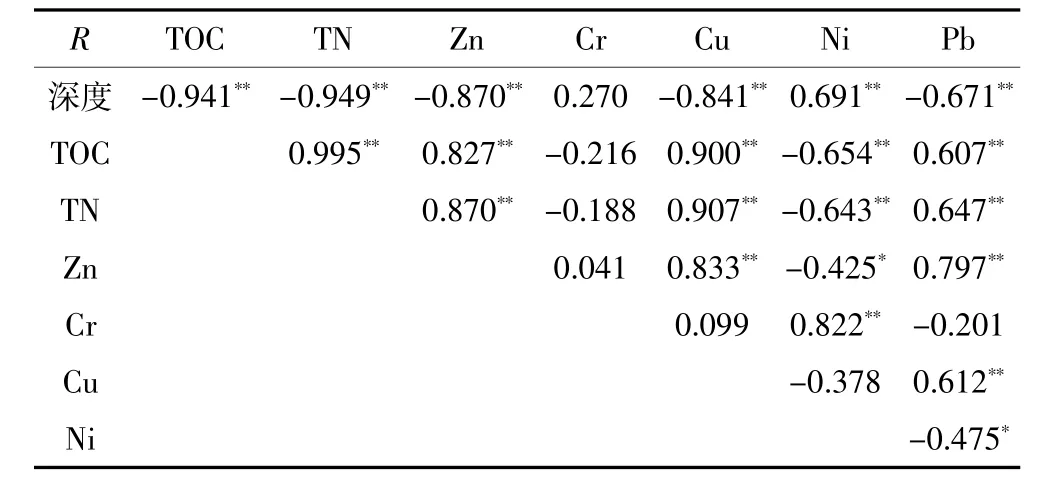
表4 武汉东湖柱状沉积物环境因子相关性矩阵Table 4 Correlation matrix for pollution factors of WDH sediments
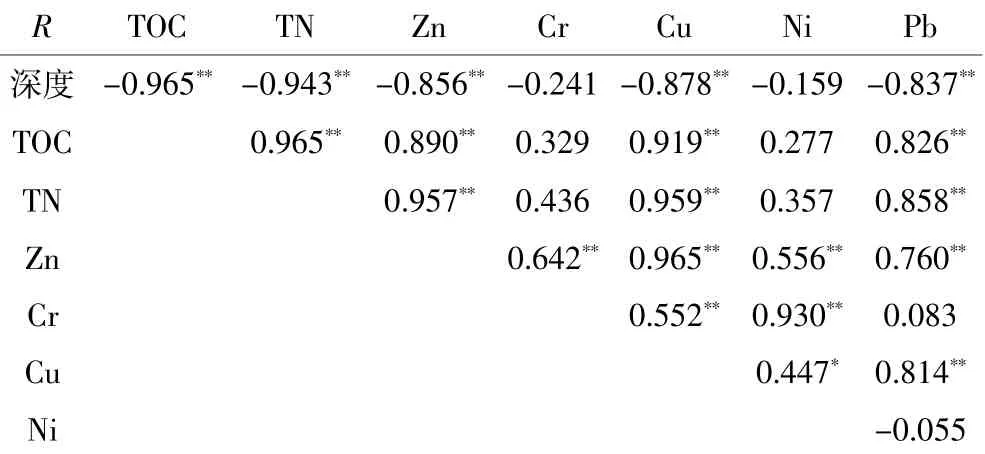
表5 黄石海口湖柱状沉积物环境因子相关性矩阵Table 5 Correlation matrix for pollution factors of HKH sediments
2.2沉积物污染评价与来源分析
2.2.1营养盐评价
根据相关性结果(表4、表5、表6),武汉东湖的TOC-TN(0.995,P<0.01)、黄石海口湖TOC-TN(0.965,P<0.01)和钟祥南湖TOC-TN(0.946,P<0.01)均为极显著正相关,说明各湖泊相应的TOC与TN可能具有同源性。
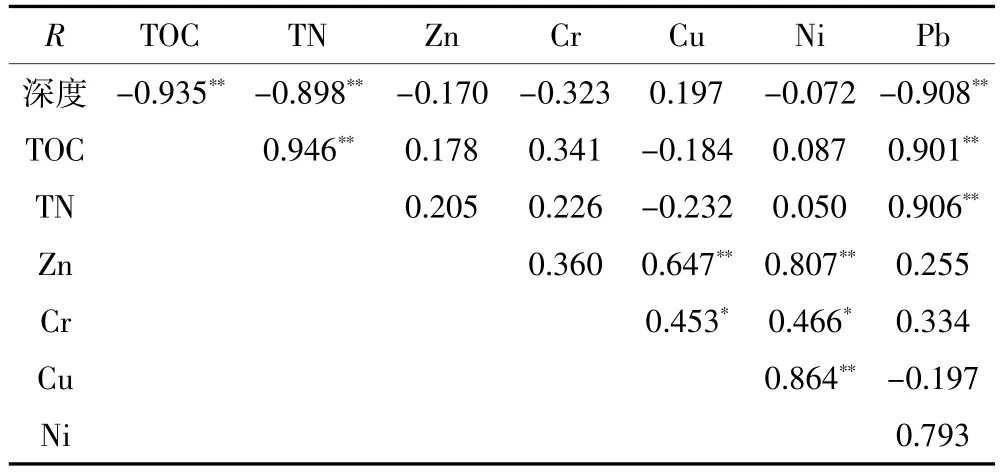
表6 钟祥南湖柱状沉积物环境因子相关性矩阵Table 6 Correlation matrix for pollution factors of ZNH sediments
结合表1和图4可得,武汉东湖、黄石海口湖柱状沉积物的有机指数范围分别为0.12~2.07、0.46~2.86,平均值分别为1.00、1.22。武汉东湖30 cm与黄石海口湖40 cm以下部分处于等级Ⅲ,尚清洁,30 cm 与40 cm以上部分均达到等级Ⅳ,有机污染严重,二者整体上为等级Ⅳ,均属于严重污染范畴。有机氮范围分别为0.14%~0.50%、0.18%~0.51%,均值分别为0.32%、0.29%,均超过等级Ⅳ控制线,沉积物氮污染较重,与有机指数结论一致。因武汉东湖为城市内湖,周边生活、娱乐、工业用水的直接排放导致相应污染较重。黄石海口湖在改革开放至21世纪初,水草植被覆盖率为96%[18],此次现场采样发现,水草植被几乎消失,底泥含有大量植物残体,因沉积物表层新鲜植物残体还没有充分氧化,其所含的营养物质又会被后来的植物所吸收,在这个循环过程中,TOC、TN含量在各层逐渐累积并快速增加[19]。
钟祥南湖柱状沉积物的有机指数范围为0.05~0.59(图4),均值为0.25。20 cm以下部分处于等级Ⅱ,较清洁,20~10 cm处于等级Ⅲ,尚清洁,总体上处于等级Ⅲ,尚清洁。有机氮范围为0.06%~0.27%,均值0.16%,20 cm以上达到等级Ⅳ,有机氮污染严重,可能是近几十年周边农田过多施氮肥导致。20 cm以下总体处于等级Ⅲ,但32~36 cm出现断层现象,等级为Ⅱ,较清洁,可能原因是20世纪50年代初期钟祥南湖出现超长冰冻期,低温导致底泥中有机污染物被释放[20]。
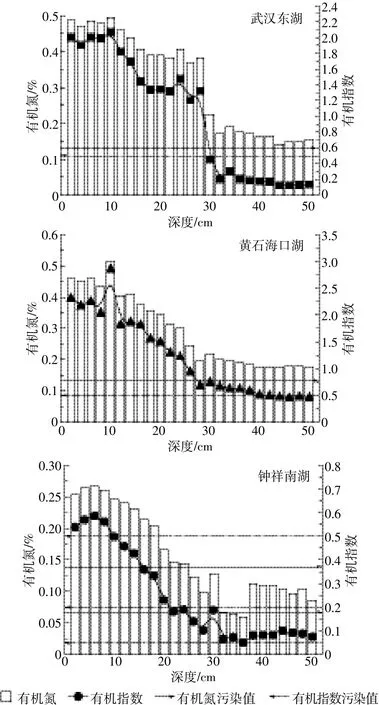
图4 各湖泊沉积物的有机指数和有机氮含量Figure 4 Organic index and organic nitrogen in lake sediments
2.2.2重金属评价
地累积指数评价结果见表7。武汉东湖Zn和Cu 在0~28 cm与Pb在0~14 cm地累积指数均为1,属于无-中污染水平,Zn、Cu和Pb平均地累积指数均为1,属于无-中污染水平,Ni与Cr地累积指数为0,未受到污染。黄石海口湖0~20 cm层Pb地累积指数为1,属于无-中污染水平,其他五种金属地累积指数为0,未受到污染。钟祥南湖五种金属地累积指数均为0,污染较少。Ni与Cr在三个湖泊中地累积指数均为0,基本属于无污染状态。在研究区三个湖泊柱状沉积物的Zn、Cu、Ni、Cr和Pb在30~50 cm层地累积指数均为0,表明在该阶段受到各金属污染较少。在研究区内武汉东湖主要污染重金属是Zn、Cu和Pb,黄石海口湖主要污染重金属为Pb,钟祥南湖五种金属污染相对较少。五种重金属污染总程度为武汉东湖>黄石海口湖>钟祥南湖。
2.2.3污染来源分析
沉积物来源因素较复杂,主要分为两大类,一类是人为活动过程中产生的污染物质,包括生活废水、工业污水及农业活动产生的污染物;另一类是自然环境来源,如地壳活动,地表岩石水流侵蚀、风化等[21-22]。通常利用相对稳定、主要来源于环境的重金属作为参考元素,与目标元素的相关性判别来源是自然因素和人为因素[23-24]。前人研究表明,Cr在研究区主要来源于自然环境[25-27],Cu和Zn主要来源于生活垃圾焚烧及工业废水,Pb主要来源于矿物(煤、石油)燃烧及农业化肥、药物[27-29]。为了探讨沉积物中污染物的可能来源,对三个湖泊的重金属Cu、Zn、Ni、Cr、Pb与TOC、TN、深度采用了相关性和主成分分析[30-31]。
武汉东湖柱状沉积物的营养盐(TOC和TN)与除Cr以外的重金属均达到极显著相关水平(表4),说明沉积物中TOC和TN污染的同时,可能伴随重金属的污染;Zn、Cu、Pb三者之间极显著正相关性,Cr与Ni极显著正相关性,说明重金属来源具有一定的相似性。主成分分析(表8)表明,第一主成分载荷较大的是TOC、TN、Zn、Cu、Ni、Pb。根据重金属垂直分布情况(图3),Zn、Cu、Ni、Pb总体上从底层到表层为增加的趋势,含量均高于背景值,显然受到人为污染。近几十年来,武汉东湖周边人口的急剧增长,一定程度上造成交通堵塞,汽车尾气使得Pb含量增加,大量生活、工业废水及垃圾焚烧排放使得Zn、Cu增多。第二主成分载荷较大的主要是Cr和Ni。Cr均值含量与背景值基本一致,空间上在背景值附近波动,变异系数6.47%,说明其受人为影响较少,因此Cr主要来源于自然环境。Ni在两主成分中均载荷量较大,表明其受冶炼[32]等人为活动影响外,还受自然环境支配。
黄石海口湖柱状沉积物的TOC、TN、Zn、Cu、Pb两两之间极显著正相关(表5),表明TOC、TN与Zn、Cu、Pb可能具有一定的同源性或受某种因子共同控制;Zn-Cu(0.965,P<0.01)、Ni-Cr(0.930,P<0.01)均为极显著正相关,说明他们可能具有同源性。黄石海口湖第一主成分(表8)主要载荷因子为TOC、TN、Zn、Cu、Pb,其中Zn、Cu、Pb均在30 cm处急剧增加(图3),Zn、Cu在30 cm以下低于背景值,有研究[33]发现莲藕对底泥重金属具有富集浓缩作用,导致相应金属含量变低。Zn、Cu和Pb在30 cm处含量开始急剧增加,且20 cm以上含量均大于背景值,说明人为污染增加。由于黄石海口湖属于远郊湖泊,工业污染源相对较少,周边农田分布较广,农业生产大量使用的肥料、农药含有Zn、Cu、Pb等重金属,这些重金属随大气沉降、地表径流进入湖泊,并逐渐累积。第二主载荷较大的为Cr和Ni,垂直变异系数分别为7.18%、4.64%,说明外界影响不大,来源可能为自然环境,但二者均低于背景值,可能与研究区域土壤母质含量低及历史输入量少有关,具体原因较复杂。
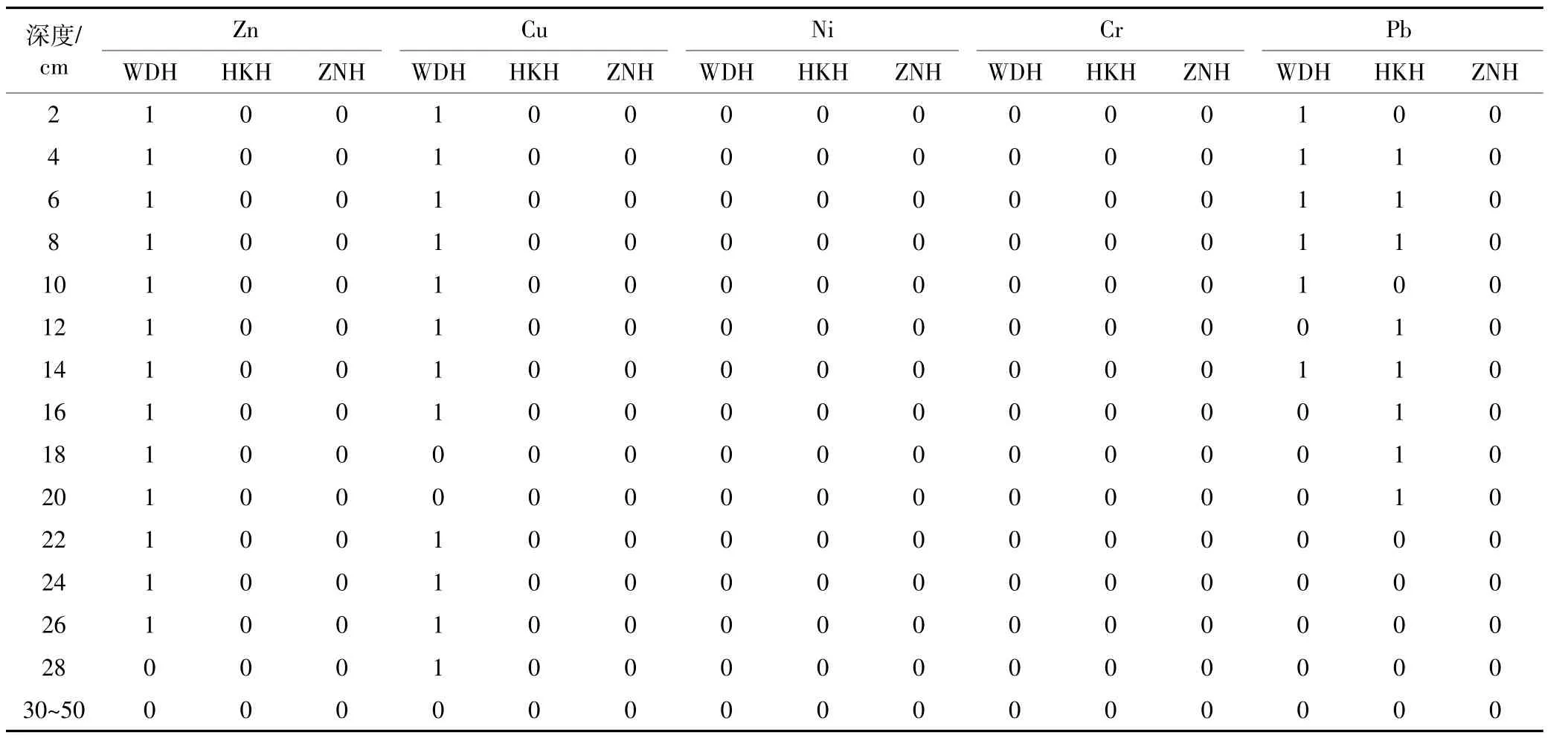
表7 湖泊沉积物重金属地累积污染级数Table 7 Index of geoaccumulation(Igeo)values for metals in lake sediments

表8 湖泊柱状沉积物环境因子主成分矩阵Table 8 Component matrices for pollution factors of lake sediments

?
钟祥南湖柱状沉积物的TOC-Pb(0.901,P<0.01)、TN-Pb(0.906,P<0.01)极显著正相关(表6),表明TOC、TN与Pb具同源性或Pb与TOC、TN存在络合关系[34]。Zn、Cu、Ni三种金属之间极显著正相关,Cu-Cr、Ni-Cr显著正相关,说明重金属来源可能相近。第一主成分载荷较大的是TOC、TN、Pb,其中Pb在30 cm处开始增加,均值28.0 mg·kg-1大于背景值,说明人类活动产生Pb污染。第二主成分载荷量较大的是Zn、Cu、Ni,其中Cu、Ni含量均值分别为30.3、37.1 mg·kg-1,与背景值基本一致。图3中Cu、Ni在背景值附近波动,变异系数分别为15.7%、12.1%,说明人为影响相对较小,因此Cu、Ni主要来源于自然环境。第二主成分中Zn载荷相对较大,均值含量略大于背景值83.6 mg·kg-1,变异系数为20.4%,表明Zn除来源于自然环境外,还受到人为活动影响。钟祥南湖西北角为市区,北面至西南角沿江为高速公路,Zn是改善汽车轮胎硬度的添加剂,轮胎磨损过程会产生含Zn粉尘,Pb的累积与交通密集程度有密切关系,周边的农业有机肥料含有Zn、Pb等元素,也可能随着降雨导致沉积物重金属含量增多[35]。
3 结论
(1)武汉东湖、黄石海口湖和钟祥南湖研究区的柱状沉积物中营养盐总体变化趋势是增加,地域性差异不太显著;TOC含量最大的是黄石海口湖,TN含量最大的是武汉东湖。
(2)各湖泊重金属污染有增加的风险,Zn、Cu、Pb受到人为影响较大,Cr主要来源于自然因素,Ni受环境与人类活动共同影响,5种重金属污染程度为武汉东湖>黄石海口湖>钟祥南湖。
(3)人为影响较大的营养盐及重金属均与深度显著相关,在30 cm与10 cm附近含量出现较大变化;TOC、TN与Pb是三个湖泊共同污染问题;武汉东湖污染可能主要来自工业及生活废水,黄石海口湖污染来源是人工种植,钟祥南湖污染来源是生活与农业废水。
应用SPSS 14.0统计软件分析本次研究数据,其中计数资料采用百分率(%)来表示,运用χ2检验组间并发症发生率和治疗有效率对比,而计量资料则运用均数±标准差来表示,组间比较采用t检验,以P<0.05表示存在显著差异。
参考文献:
[1]张敏.长江中下游浅水湖泊富营养化机制与重金属污染研究[D].武汉:中国科学院水生生物研究所, 2005. ZHANG Min. The mechanisms of eutrophication and heavy metal pollution in shallow lakes along the Yangtze River[D]. Wuhan:Institute of Hydrobiology, Chinese Academy of Sciences, 2005.
[2]郭子军,田学达,余辉,等.微电解-电极生物膜法在污水深度处理中的应用[J].环境科学研究, 2015, 28(6):1001-1007. GUO Zi-jun, TIAN Xue-da, YU Hui, et al. Advanced treatment of polluted water using micro-electrolysis biofilm-electrode process[J]. Research of Environmental Sciences, 2015, 28(6):1001-1007.
[3]薛滨,姚书春,夏威岚.长江中下游典型湖泊近代环境变化研究[J].地质学报, 2008, 82(8):1135-1141. XUE Bin, YAO Shu-chun, XIA Wei-lan. Modern environmental changes of typical lakes along the middle and lower reaches of Yangtze River basin[J]. Acta Geological Sinica, 2008, 82(8):1135-1141.
[4]Lukawska-Matusaewska K, Kielczewska J, Bolalek J. Factors controlling spatial distributions and relationships of carbon, nitrogen, phosphorus and sulphur in sediments of the stratified and eutrophic Gulf of Gdansk[J]. Continental Shelf Research, 2014, 85:168-180.
[5]Dennis T, David P, Hamilton C A P. Evaluating the influence of lake morphology, tropic status and digenesis on geochemical profiles in lake sediments[J]. Applied Geochemistry, 2010, 25(5):621-632.
[6]王玲玲,吴卫菊,张斌,等.梁子湖沉积物中重金属及营养盐分布特征研究[J].环境科学与技术, 2015, 38(6):197-203. WANG Ling-ling, WU Wei-ju, ZHANG Bin, et al. Distribution characteristic of heavy metals and nutrient in sediments of Liangzi Lake[J]. Environmental Science & Technology, 2015, 38(6):197-203.
[7]王毛兰,艾永平,张丁苓.鄱阳湖三江口柱状沉积物有机氮同位素特征及其环境指示意义[J].中国环境科学, 2015, 35(2):558-564. WANG Mao-lan, AI Yong-ping, ZHANG Ding-ling. Stable organic nitrogen isotope in core sediments of the Three Rivers Estuary, Poyang Lake and its environmental implications[J]. China Environmental Science, 2015, 35(2):558-564.
[8]李辉.滇池柱状沉积物中氮赋存形态及其分布特征研究[D].昆明:昆明理工大学, 2012. LI Hui. Nitrogen forms and distribution in the sediment cores of Dianchi Lake[D]. Kunming:Kunming University of Science and Technology, 2012.
[9]王圣瑞,焦立新,金相灿,等.长江中下游浅水湖泊沉积物总氮、可交换态氮与固定态铵的赋存特征[J].环境科学学报,2008,28(1):37-43. WANG Shen-rui, JIAO Li-xin, JIN Xiang-can, et al. Distribution of total exchangeable and fixed nitrogen in the sediments from shallow lakes in the middle and lower reaches of the Yangtze River[J]. Acta Scientiae Circumstantiae, 2008, 28(1):37-43.
[10]李德亮,张婷,余建波.长江中游典型湖泊重金属分布及其风险评价:以大通湖为例[J].长江流域资源与环境, 2010, 19(Z1):183-189. LI De-liang, ZHANG Ting, YU Jian-bo. Distribution and risk evolution of heavy metals in typical lakes in middle reaches of the Yangtze River:Taking the Datong Lake for example[J]. Resources and Environments in the Yangtze Basin, 2010, 19(Z1):183-189.
[11]朱志龙,周梦雷,柯航.湖北省城中湖泊调查分析[J].人民长江, 2013, 44(1):155-157. ZHU Zhi-long, ZHOU Meng-lei, KE Hang. Investigation of urban lakes in Hubei Province[J]. Yangtze River, 2013, 44(1): 155-157.
[12]王毛兰,赖劲虎,倪妍,等.微波消解-GFAAS测定浅水湖泊底泥中重金属元素[J].分析试验室, 2012, 31(2):51-54. WANG Mao-lan, LAI Jin-hu, NI Yan, et al. A microwave digestion method for determination of heavy metals in shallow lake sediments by graphite furnace atomic absorption spectrometry[J]. Chinese Journal of Analysis Laboratory, 2012, 31(2):51-54.
[13]隋桂荣.太湖表层沉积物中OM, TN, TP的现状与评价[J].湖泊科学, 1996, 8(4):319-324. SUI Gui-rong. Statement and evaluation of organic matter, total nitrogen and total phosphate in surface layer sediments in Taihu Lake[J]. Journal of Lake Science, 1996, 8(4):319-324.
[14]Muller G. Index of geo-accumulation in sediments of the Rhine River [J]. Geo Journal, 1969, 2(3):108-118.
[15]李晓燕,陈同斌,雷梅,等.不同土地利用方式下北京城区土壤的重金属累积特征[J].环境科学学报, 2010, 30(11):2285-2293. LI Xiao-yan, CHEN Tong-bing, LEI Mei, et al. Accumulation of heavy metals in urban soils under different land uses in Beijing[J]. Acta Scientiae Circumstantiate, 2010, 30(11):2285-2293.
[16]杨洪,易朝路,邢阳平,等.210Pb和137Cs法对比研究武汉东湖现代沉积速率[J].华中师范大学学报:自然科学版, 2004, 38(1):109-113. YANG Hong, YI Chao -lu, XING Yang -ping, et al. A comparative study on recent sedimentation rates in Lake Donghu, Wuhan with210Pb and137Cs dating techniques[J]. Journal of Central China Normal University(Nat Sci), 2004, 38(1):109-113.
[17]刘碧波,丰民义,刘剑彤.东湖典型区域沉积物总氮的空间分布和季节变化[C].武汉:环境污染与大众健康学术会议, 2011:1063-1065. LIU Bi-bo, FENG Min-yi, LIU Jian-tong. Vertical distribution and seasonal variation of nitrogen in sediment pore water of typical area in East Lake[C]. Wuhan:Conference on Environmental Pollution and Public Health, 2011:1063-1065.
[18]简永兴,王建波,何国庆,等.湖北省海口湖、太白湖与武山湖水生植物多样性的较研究[J].生态学报, 2001, 21(11):1815-1824. JIAN Yong-Xing, WANG Jian-Bo, HE Guo-Qing, et al. A comparative study of aquatic plant diversity of Haikou, Taibai and Wushan Lake in Hubei Province of China[J]. Acta Ecological Sinica,2001, 21(11):1815-1824.
[19]秦伯强.长江中下游浅水湖泊富营养化发生机制与控制途径初探[J].湖泊科学, 2002, 14(3):193-201. QIN Bo-qiang. Approaches to mechanisms and control of eutrophication of shallow lakes in the middle and lower reaches of the Yangze River[J]. Journal of Lake Sciences, 2002, 14(3):193-201.
[20]李剑超,朱光灿,刘伟生,等.沉积时间和温度对底泥间隙水有机污染物的影响[J].农业环境科学学报, 2004, 23(4):723-726. LI Jian-chao, ZHU Guang-can, LIU Wei-sheng, et al. Effect of formation time and environmental temperature on organic contaminant in pore water of bottom sediment[J]. Journal of Agro-Environment Science, 2004, 23(4):723-726.
[21]刘伟,陈振楼,许世远,等.上海市小城镇河流沉积物重金属污染特征研究[J].环境科学, 2000, 27(3):535-543. LIU Wei, CHEN Zhen-lou, XU Shi-yuan, et al. Pollution character of heavy metals in river sediments from small towns, Shanghai[J]. Environmental Science, 2000, 27(3):535-543.
[22]Spencer K J, De Carlo E H, McMurtry G M. Isotopic clues to source natural and anthropogenic lead in sediments and soils from O′ahu Hawai′i[J]. Pacific Science, 1995, 49(4):492-510.
[23]Tkalin A V, Presley B J, Boothe P N. Spatial and temporal variations of trace metals in bottom sediments of Peter the Great Bay, the Sea of Japan[J]. Environ Pollution,1996, 92(1):73-78.
[24]李建芬,王福,商志文,等.天津市潮间带柱状沉积物中重金属的污染历史及来源判别[J].地质调查与研究, 2012, 33(1):55-62. LI Jian-fen, WANG Fu, SHANG Zhi-wen, et al. Pollution history and source discrimination for the heavy metals in core sediments of Tianjin intertidal zone[J]. Ecological Survey and Research, 2012, 33(1):55-62.
[25]于瑞莲,张伟芳,胡恭任,等.晋江河口沉积物重金属污染历史与来源[J].环境科学研究, 2015, 28(6):907-914. YU Rui-lian, ZHANG Wei-fang, HU Gong-ren, et al. Pollution history and source analysis of heavy metals in sediments from Jinjiang River estuary[J]. Research of Environmental Sciences, 2015, 28(6):907-914.
[26]魏荣菲,庄舜尧,杨浩,等.苏州河网区河道沉积物重金属的污染特征[J].湖泊科学, 2010, 22(4):527-537. WEI Rong-fei, ZHUANG Shun-yao, YANG Hao, et al. Pollution characteristics of heavy metals in sediments from the river network of Suzhou City[J]. Journal of Lake Sciences, 2010, 22(4):527-537.
[27]乔胜英,蒋敬业,向武,等.武汉地区湖泊沉积物重金属的分布及潜在生态效应评价[J].长江流域资源与环境, 2005, 14(3):353-357. QIAO Sheng-ying, JIANG Jing-ye, XIANG Wu, et al. Distribution of heavy metals in sediments in lakes in Wuhan with assessment on their potential ecological risk[J]. Resources and Environments in the Yangtze Basin, 2005, 14(3):353-357.
[28]唐阵武,程家丽,岳勇,等.武汉典型湖泊沉积物中重金属累积特征及其环境风险[J].湖泊科学, 2009, 21(1):61-68. TANG Zhen-wu, CHENG Jia-li, YUE Yong, et al. Accumulations and risks of heavy metals in the sediments from 8 typical lakes in Wuhan, China[J]. Journal of Lake Sciences, 2009, 21(1):61-68.
[29]杜臣昌,刘恩峰,羊向东,等.巢湖沉积物重金属富集特征与人为污染评价[J].湖泊科学, 2012, 24(1):59-66. DU Chen-chang, LIU En-feng, YANG Xiang-dong, et al. Characteristics of enrichment and evaluation of anthropogenic pollution of heavy metals in the sediments of Lake Chaohu[J]. Journal of Lake Sciences, 2012, 24(1):59-66.
[30]马立杰,崔迎春,王海荣.运用因子分析评价山东黑泥湾沉积物重金属污染来源[J].海洋地质前沿, 2012, 28(4):57-61. MA Li-jie, CUI Ying-chun, WANG Hai-rong. Souce of heavy metal contamination in Heini Bay sediments:A case study using factor analysis[J]. Marine Geology Frontier, 2012, 28(4):57-61.
[31]Elisangela A P, Jeferson C A, Izaias S S, et al. Assessment of trace metals contamination in estuarine sediments using a sequential extraction technique and principal component analysis[J]. Microchemical Journal, 2010, 96(1):50-57.
[32]王金瑾,鲍建国,李立青.东湖沉积物重金属来源与人类活动相关性分析[J].环境科学与技术, 2010, 33(4):84-90. WANG Jin-jin, BAO Jian-guo, LI Li-qing. Sources of heavy metal pollutions in sediments of Lake Donghu and their relationship with anthropogenic activities[J]. Environmental Science & Technology, 2010, 33 (4):84-90.
[33]胡文勇,马陶武,易浪波,等.受污藕塘中莲藕对重金属的生物富集特征[J].贵州农业科学, 2010, 38(3):229-231. HU Wen-yong, MA Tao-wu, YI Lang-bo, et al. Biological enrichment characteristics of heavy metals in lotus root in polluted lotus ponds[J]. Guizhou Agricultural Sciences, 2010, 38(3):229-231.
[34]石陶然,张远,于涛,等.滇池沉积物不同分子量溶解性有机质分布及其与Cu和Pb的相互作用[J].环境科学研究, 2013, 26(2):137-144. SHI Tao-ran, ZHANG Yuan, YU Tao, et al. Distribution of different molecular weight fractions of dissolved organic matters and their complexation with Cu and Pb in the sediment from Dianchi Lake, China[J]. Research of Environmental Sciences, 2013, 26(2):137-144.
[35]戴彬,吕建树,战金成,等.山东省典型工业城市土壤重金属来源、空间分布及潜在生态风险评价[J].环境科学, 2015, 36(2):507-515. DAI Bin, LÜ Jian-shu, ZHAN Jin-cheng, et al. Assessment of sources, spatial distribution and ecological risk of heavy metals in soils in a typical industry-based city of Shandong Province, Eastern China[J]. Environmental Science, 2015, 36(2):507-515.
贵州草海上覆水与沉积物中砷的分布特征及扩散通量估算
涂汉,吴攀*,韩志伟,曹星星,张水
(贵州大学资源与环境工程学院,贵阳550025)
摘要:对草海不同区域沉积物上覆水及孔隙水、附近河流和雨水中砷的含量与分布特征进行了分析,并利用一维孔隙水扩散模型估算了砷在沉积物-水界面的扩散通量。结果表明:草海出口砷含量为1.59 μg·L-1,明显高于流入草海的水体端元(平均值0.32 μg·L-1)和雨水(0.37 μg·L-1)中砷浓度;草海上覆水中砷的空间分布表现为挺水植物区(2.99~3.45 μg·L-1)>沉水植物区(1.79~2.34 μg·L-1),垂直分布上无明显变化,挺水植物区上覆水体中的砷以As(Ⅲ)(H3AsO3)形态存在,沉水植物区上覆水体中的砷以As(Ⅴ)(HAsO2-4)形态存在;而沉积物和孔隙水中总砷含量垂直方向上波动较大,规律与上覆水相似,均表现为挺水植物区>沉水植物区,其中挺水植物区沉积物砷含量为19.86~36.45 mg·kg-1,平均值27.84 mg·kg-1,沉水植物区沉积物砷含量为13.05~32.32 mg·kg-1,平均值19.79 mg·kg-1;草海挺水植物区和沉水植物区三处取样点在沉积物-水界面的扩散通量分别为73.84 μg·m-2·d-1和18.99、11.45 μg·m-2·d-1,均表现为沉积物孔隙水中的砷向上覆水释放,揭示沉积物可能是草海水体中砷重要的输入源。
关键词:草海;砷;沉积物;孔隙水;扩散通量
中图分类号:X522文献标志码:A文章编号:1672-2043(2016)05-0963-06doi:10.11654/jaes.2016.05.021
涂汉,吴攀,韩志伟,等.贵州草海上覆水与沉积物中砷的分布特征及扩散通量估算[J].农业环境科学学报, 2016, 35(5):963-968.
TU Han, WU Pan, HAN Zhi-wei, et al. Distribution and diffusion flux of arsenic in sediment and overlying-water of Lake Caohai, Guizhou Province[J]. Journal of Agro-Environment Science, 2016, 35(5): 963-968.
收稿日期:2015-10-24
基金项目:贵州大学研究生创新基金项目(研理工2015064)
作者简介:涂汉(1990—),男,研究生,主要从事水污染控制研究。E-mail:tuhan0603@163.com
*通信作者:吴攀E-mail:pwu@gzu.edu.cn
Distribution and diffusion flux of arsenic in sediment and overlying-water of Lake Caohai, Guizhou Province
TU Han, WU Pan*, HAN Zhi-wei, CAO Xing-xing, ZHANG Shui
(College of Resources and Environmental Engineering, Guizhou University, Guiyang 550025, China)
Abstract:This paper investigated the distribution and concentration of arsenic in overlying water and sediment pore water of Caohai as well as the nearby rivers and rainwater in different areas. Utilizing one-dimensional pore water diffusion model, we estimated arsenic diffusion flux across the sediment-water interface. Results indicated that arsenic concentrations at the Caohai exit was 1.59 μg·L-1, obviously higher than at the entry of Caohai(averagely 0.32 μg·L-1)as well as rainwater(0.37 μg·L-1). The spatial distribution of arsenic concentrations in the overlying water was as follows:emergent plant zone(2.99~3.45 μg·L-1)>submerged plant zone(1.79~2.34 μg·L-1). The arsenic in the overlying water existed as H3AsO3form in emergent plant zone but as HAsO2-4form in submerged plant zone. The total arsenic concentrations in sediments and pore water showed large vertical variation and were emergent plant zone>submerged plant zone. The arsenic in the sediments in emergent plant zone was between 19.86 mg·kg-1and 36.45 mg·kg-1, with average value of 27.84 mg·kg-1, while in submerged plant zone arsenic concentrations ranged from 13.05 mg·kg-1to 32.32 mg·kg-1, averaging 19.79 mg·kg-1. The diffusion flux across the sediment-water interface in emergent plant and submerged plant zons were 73.84 μg·m-2·d-1and 18.99~11.45 μg·m-2·d-1, respectively, showing that arsenic stored in sediment pore water released into the overlying water and that sediment might thus be significant source of arsenic in Lake Caohai water.
Keywords:Caohai; arsenic; sediment; pore water; diffusion flux
沉积物-水界面砷的分布情况备受国内外学者的广泛关注[1-4]。进入湿地中的砷少数溶解于水体中,大多数在湿地沉积物中累积并对底栖生物构成影响,同时沉积物中的砷污染物在物理、化学、生物等作用下会被重新释放进入水体而形成二次污染,从而影响整个湿地生态系统的平衡发展[5-7]。因此,研究湿地水体和沉积物中砷的分布情况,能够对砷在湿地中的迁移转化规律有更深入的了解。
草海位于贵州威宁县,属国家级自然保护区,对维护区域生态系统的平衡有重要作用。目前对于草海流域砷污染的研究多集中于周边土壤[8]、部分表层沉积物[9-10]等,但未考虑湿地水层的差异和沉积物剖面分布变化,特别是将水体和沉积物孔隙水结合讨论进而反映污染物释放趋势的研究未见报道。基于此,本文以沉积物-水体中砷为研究对象,分析草海附近河流及内部不同区域、不同水深、沉积物剖面及孔隙水中砷的变化特征,并利用一维孔隙水扩散模型(Fick定律)估算砷在沉积物-水界面的扩散通量,为今后研究草海流域砷污染水平及来源提供基础数据,同时对深入了解草海中砷的生物地球化学行为具有重要的指导意义。
1 材料与方法
1.1研究区域概况
草海国家级自然保护区位于贵州省西部威宁县城西南侧(地理坐标26°49′~26°53′N,104°12′~104° 18′E),流域面积96 km2,湖面面积大约25 km2,最大水深小于5 m,属于长江水系,是金沙江支流横江洛泽河的上源湿地(图1),共有四条入湖河流(H1、H3、H4和H5),出水口仅1条河流(H2)。年平均降雨量为950.9 mm,5—10月为雨季,其降雨量占全年的88%;12月至次年3月为旱季,降雨量仅占全年的5%[11],草海湿地生态系统属于完整的、典型的高原湿地生态系统[12],具有日照丰富、水质良好、透明度大、多为淤泥底质、各类水生植物布满湖区等特点。
1.2样品采集与分析
本研究于2014年9月进行样品采集,利用重力采样器共采集三组沉积物柱状剖面,其中1号剖面设在草海挺水植物生长区(1#),2号剖面设在湿地中心区(2#),3号剖面靠近出水口(3#),2#和3#属于沉水植物区(图1)。在每个剖面采样点均采集表层水、中层水和界面水。现场用水质参数仪Multi 3430测定所采剖面上覆水pH、水温(T)、溶解氧(DO)、氧化还原电位(Eh)、电导率(EC)等物理化学参数。
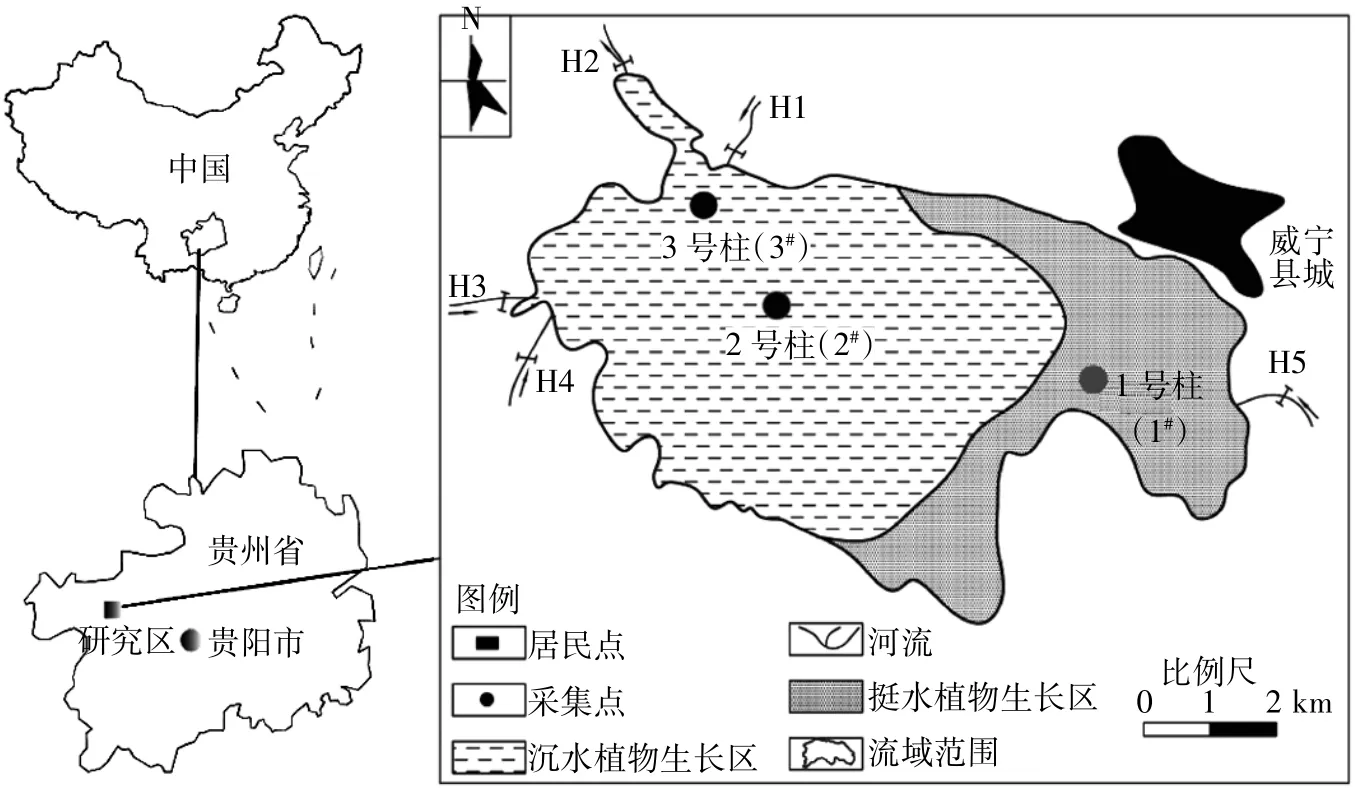
图1 草海样品采样布点图Figure 1 Sampling locations in Lake Caohai
所采剖面沉积物样品1~10 cm以1 cm为一个单位进行分样,10 cm以下均以1.5 cm为一个单位分样,于4℃下保存,24 h内将分割后样品以5000 r· min-1离心15 min,上清液过0.45 μm滤膜即为沉积物孔隙水。将离心后的沉积物样品经冷冻干燥后压散,剔除砾石、贝壳等动植物残体杂质,研磨后过0.149 μm筛备用。选用王水水浴消解[13],采用双道-原子荧光光度仪(AFS-9230,北京吉天)进行测定,测定前仪器需预热30 min以上。同时采用国家土壤标准物质(ESS-4)、平行样及空白样进行质量控制。结果显示,测定值与标准值的相对偏差均小于10%,符合测定要求。
所采集的上覆水、河水、雨水和孔隙水样品用ICP-MS(7500a,美国安捷伦公司)检测。上述分析测试工作在贵州大学资源与环境工程学院测试中心完成。
2 结果与讨论
2.1水体中砷含量及形态分布特征
草海不同区域沉积物剖面上覆水中砷浓度如表1所示。1#、2#、3#样点上覆水中砷的含量分别为2.99~3.45、1.79~2.21、2.16~2.34 μg·L-1,呈现挺水植物区>沉水植物区(2#和3#),出水口(3#)>湖中心区(2#)的特征。水体中大多数砷以无机的As(Ⅲ)和As(Ⅴ)形态存在,这两种形态砷的存在和转化与水体的pH值、氧化还原电位有很大关系[14-15]。由表2可知,1#处pH值(6.9~7)低于2#(9.2~9.4)和3#(9.6~9.7),1#处Eh 为-164.8~-179.3 mV,呈较强的还原性。2#和3#处Eh分别为-7~103.9、44.1~116.4 mV,呈弱氧化性。Cheng等[16]研究发现,在pH值4~9范围内,以H2AsO-4或HAsO2-4形态存在的As(Ⅴ)易于被带有正电荷的铁、锰和铝(氢)氧化物[17-18]甚至黏土矿物吸附[19];而以H3AsO3形态存在的As(Ⅲ)在典型的土壤和地下含水层中的吸附是很少的。1#上覆水体中的砷以H3AsO3形态存在,呈还原环境,随着水流方向到达沉水植物区(2#和3#),上覆水体呈氧化环境,As以HAsO2-4形态存在(图2)。HAsO2-4被胶体或铁、锰氧化物、氢氧化物吸附,从而导致沉水植物区上覆水体中砷的含量低于挺水植物区。
此外,在垂直分布上3个采样点的砷含量变化不大,上覆水中易变参数也呈现相似规律,可能因为草海湿地较浅、水流缓慢,导致上覆水体混合均匀[20]。一般来说河流和雨水是湿地重要的水源[21],其所携带的重金属对湿地生态系统有重要的影响[21],而本研究中草海流入的河流(H1:0.27 μg·L-1、H3:0.48 μg·L-1、H4:0.19 μg·L-1、H5:0.32 μg·L-1)和雨水(0.37 μg·L-1)砷浓度明显低于流出草海的河流(H2:1.59 μg·L-1),H2水体砷含量分别为流入草海河流和雨水的3.3~8.4倍和4.3倍,这个差异说明可能存在其他高浓度砷向上覆水体中释放。

表1 沉积物剖面上覆水中砷含量(μg·L-1)Table 1 Content of arsenic in overlying water of sediments(μg·L-1)
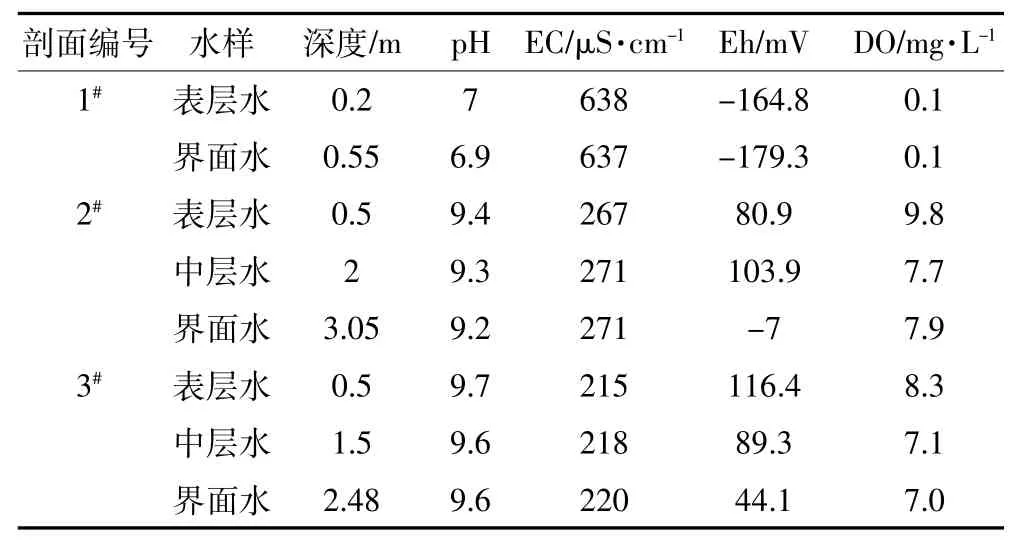
表2 沉积物剖面上覆水体易变参数Table 2 Parameters of overlying water of sediment
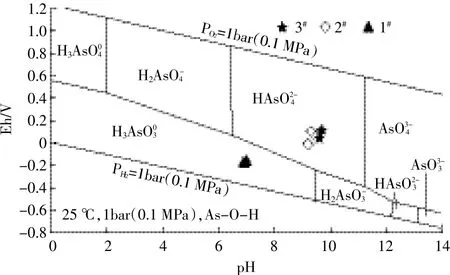
图2 草海上覆水中砷的Eh-pH相位图Figure 2 Eh-pH phase diagram for arsenic in overlying water of Lake Caohai
2.2沉积物剖面及孔隙水中砷分布
草海沉积物及其孔隙水中砷的垂直分布波动较大(图3、图4)。沉积物剖面砷总量浓度介于13.05~36.45 mg·kg-1,平均值22.47 mg·kg-1。1#沉积物砷含量为19.86~36.45 mg·kg-1,平均值27.84 mg·kg-1,高于贵州土壤砷背景值(20.0 mg·kg-1)[9];2#沉积物砷含量为13.05~32.32 mg·kg-1,平均值19.49 mg·kg-1;3#沉积物砷含量为16.3~30.57 mg·kg-1,平均值20.09 mg·kg-1。导致上述沉积物剖面呈现该分布特征的原因可能是由于1#靠近威宁县城,受人为活动影响较大,导致砷含量相对较高。随着湖水的流动作用,湖中心处砷含量相对降低,但是细小颗粒物会继续随水流动且其比表面积相对较大,能够吸附更多的砷,所以可能聚集在湖出水口处,进而沉降使得湖出水口处沉积物中砷含量比湖中心处偏高。1#剖面沉积物中砷含量在沉积物深度为10 cm以下含量较高,最底层有最大值;2#剖面沉积物中砷含量在沉积物深度为8 cm处有最大值,此后减小且随着深度的增加无明显变化;3#剖面沉积物中砷含量随深度的增加并无太大的变化,只是有小幅度的波动,在31 cm处有最大值。此外,湖中心处表层沉积物中砷含量比底层相对较高,即表现为砷趋向富集于表层沉积物中。原因可能是,在有机质的降解过程中导致吸附的砷被释放到孔隙水中,而表层有活性的有机质又将其吸附,使得表层沉积物中砷含量较高。
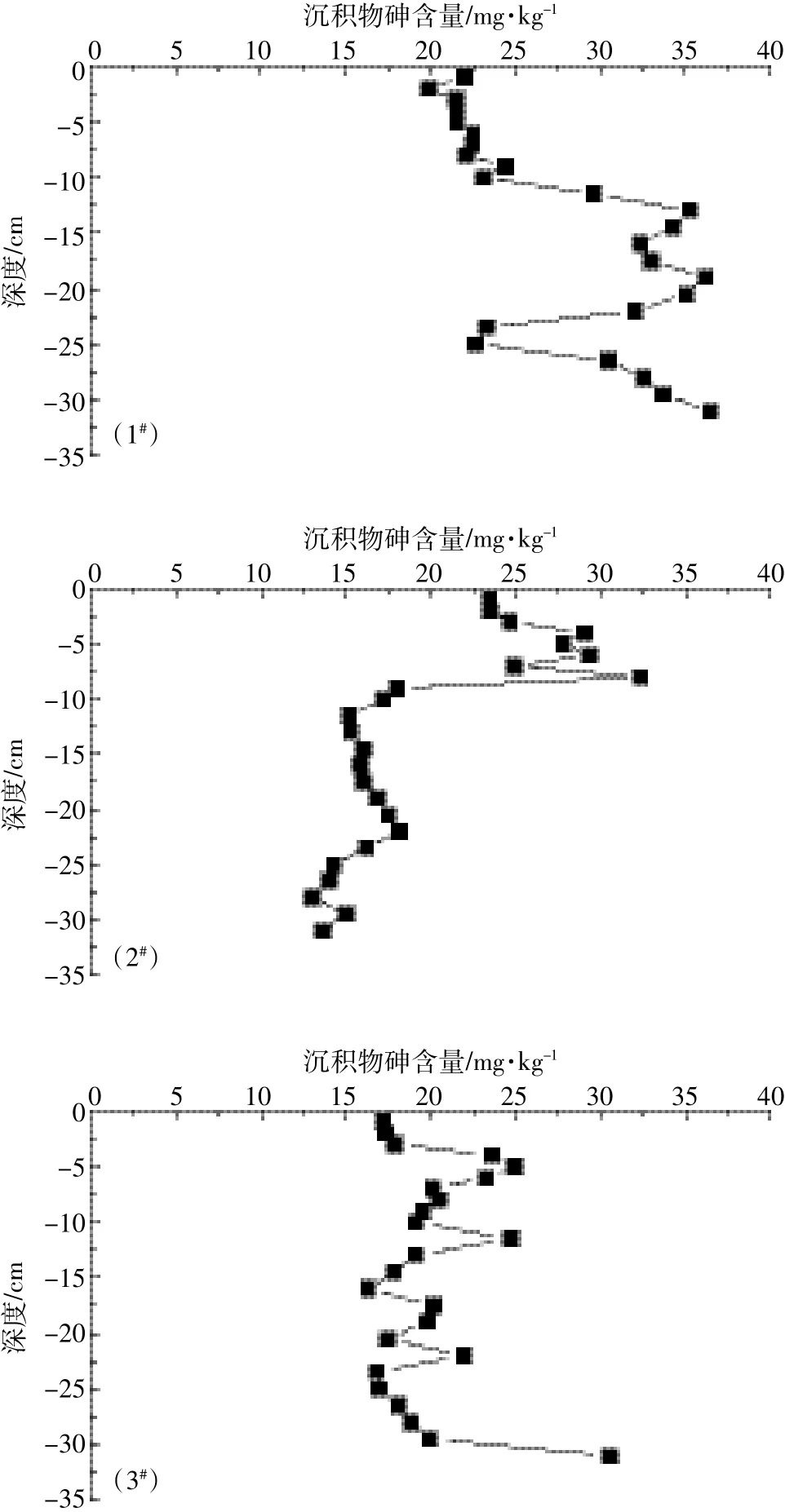
图3 沉积物剖面砷含量Figure 3 Arsenic content in sediment profile
孔隙水中砷(图4)浓度介于1.42~17.69 μg·L-1,平均值4.99 μg·L-1。1#孔隙水砷浓度为2.88~17.69 μg·L-1,平均值7.94 μg·L-1;2#孔隙水砷浓度为1.42~7.96 μg·L-1,平均值3.90 μg·L-1;3#孔隙水砷浓度为1.53~5.53 μg·L-1,平均值3.33 μg·L-1。且界面附近砷含量都明显低于孔隙水相应浓度,孔隙水中砷浓度自界面向下随深度增加呈现先升高后降低的趋势,但各采样点变化趋势稍有不同。挺水植物区孔隙水中砷含量在沉积物3 cm处出现峰值(17.69 μg·L-1),随后逐渐降低,直到9 cm处出现最低值(2.88 μg·L-1),最后趋于稳定;湖中心区孔隙水中砷含量先是逐渐升高,在沉积物5 cm处出现最高值(7.96 μg·L-1),随后又逐渐降低,在9 cm处出现最低值(1.42 μg·L-1)最终趋于稳定;3#孔隙水中的砷含量除了在4 cm处出现峰值(5.53 μg·L-1)外,从表层到底层无明显变化。该分布特征表明沉积物中普遍存在砷的沉积后再迁移现象,有机质降解引起界面附近氧化还原状况的变化,砷也因受此过程及矿物平衡的影响而波动[21-23]。孔隙水中砷的这种分布状况也表明,砷有可能按照浓度梯度经孔隙水从沉积物向上覆水扩散,进而影响上覆水的水质。
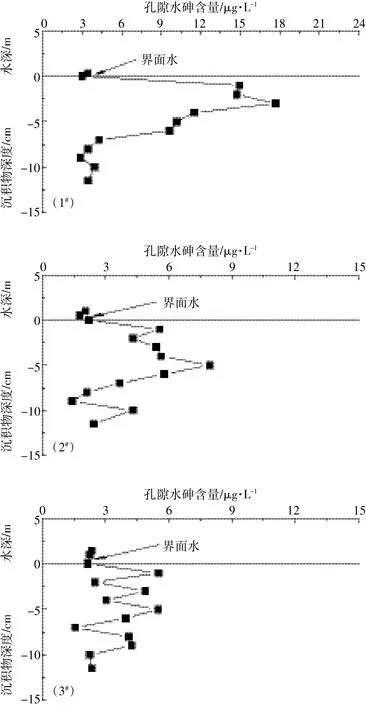
图4 沉积物剖面孔隙水砷含量Figure 4 Arsenic content in pore water of sediment profile
2.3孔隙水的环境效应
沉积物中的重金属以孔隙水为介质向上覆水体扩散影响上覆水体水质,重金属界面扩散通量可由Fick第一定律估算得到[24]:

式中:F为通过沉积物-水界面的扩散通量;φ为表层沉积物的孔隙度[25];Δc/Δx为表层沉积物间隙水-上覆水的浓度梯度;Ds为扩散系数(通常当φ≤0.7时,Ds= φDo;当φ≥0.7时,Ds=φ2Do,Do为离子在无限稀释溶液中的理想扩散系数[26])。
分别将上面的参数值代入公式,可算出由于扩散作用引起的界面处沉积物孔隙水中As的扩散通量(表3)。

表3 草海沉积物-水界面砷扩散通量Table 3 Fluxes of arsenic across sediment-water interface of Lake Caohai
由Fick定律估算得到的扩散通量,只考虑了污染物在界面水-沉积物界面之间的质量浓度梯度、沉积物孔隙度以及颗粒物对溶解态营养盐迁移扩散的影响,是一种理论通量[27]。在沉积物实际扩散通量中,沉积物-水界面的环境参数,如pH值、吸附作用、氧化还原条件、水力扰动等因素都会影响沉积物的扩散通量[20]。Fick定律计算得到的扩散通量要低于水库的实际扩散通量。但从表4中可以看出,各沉积物剖面扩散通量均为正值,1#、2#、3#在沉积物-水界面的扩散通量分别为73.84、18.99、11.45 μg·m-2·d-1,说明草海沉积物孔隙水中砷向上覆水中扩散,沉积物孔隙水中砷的释放可能是导致草海水体中砷浓度高于附近河流和雨水的重要因素。此外,挺水植物区释放通量明显高于沉水植物区,与挺水植物区靠近草海威宁县城,大量的人为含砷污染物(如农药、除草剂、杀虫剂等)进入草海,加之该区域呈还原环境,易使大量的砷从沉积物中释放出来。至于是否具有季节性的影响有待进一步研究。
3 结论
(1)草海水体、附近河流和雨水中砷浓度普遍偏低,草海水体中砷浓度明显高于附近河流和雨水。草海沉水植物区上覆水体pH值呈中性,属还原环境,而挺水植物区上覆水体pH值均呈碱性,属氧化环境,表明沉水植物区水体中的砷以As(Ⅲ)形态存在,而挺水植物区水体中的砷以As(Ⅴ)形式为主。
(2)草海沉积物及孔隙水中总砷含量垂直方向波动较大,但与上覆水有相似的规律,均表现为挺水植物区>沉水植物区,且挺水植物区可能受到周边人为活动的影响,导致砷的含量超过贵州土壤背景值。
(3)草海挺水植物区和沉水植物区在沉积物-水界面均表现为孔隙水向上覆水释放特征,揭示沉积物孔隙水扩散可能是草海水体中砷重要的输入源。
参考文献:
[1]Nickson R,McArthur J,Burgess W,et al.Arsenicpoisoningof Bangladesh groundwater[J]. Nature, 1998, 395:338.
[2]刘淑民,姚庆祯,刘月良,等.黄河口湿地表层沉积物中重金属的分布特征及其影响因素[J].中国环境科学, 2012, 32(9):1625-1631. LIU Shu-min, YAO Qing-zhen, LIU Yue-liang, et al. Distribution and influence factors of heavy metals in surface sediments of the Yellow River Estuary wetland[J]. China Environmental Science, 2012, 32(9):1625-1631.
[3]张连凯,杨慧,杨永亮,等.秦皇岛河口及附近水域沉积物砷分布特征及生态风险评价[J].环境科学与技术, 2013, 36(1):146-151. ZHANG Lian-kai, YANG Hui, YANG Yong-liang, et al. Distribution characteristics and ecological risk assessment of arsenic in surface sediments of Qinhuangdao Estuary and its adjacent waters[J]. Environmetal Science & Technology, 2013, 36(1):146-151.
[4]Matschullat J. Arsenic in the geosphere:A review[J]. Science of the Total Environment, 2000, 249(1-3):297-312.
[5]朱立峰,郑祥民,周立旻,等.崇明东滩湿地沉积物砷的形态特征[J].城市环境与城市生态, 2009, 22(5):27-33. ZHU Li-feng, ZHENG Xiang-min, ZHOU Li-min, et al. Arsenic morphological characteristics in sediments in Chongming Dongtan[J]. Urban Environment & Urban Ecology, 2009, 22(5):27-33.
[6]徐泽新,张敏.太湖流域湖荡湿地沉积物砷汞的空间分布及污染评价[J].长江流域资源与环境, 2013, 22(5):626-632. XU Ze-xin, ZHANG Min. Spatial distribution and pollution assessment of As and Hg in sediments from lakes in Lake Taihu watershed[J]. Resources and Environment in the Yangtze Basin, 2013, 22(5):626-632.
[7]Nikolaidis N P. Dobbs G M, Chen J, et al. Arsenic mobility in contami-nated lake sediments[J]. Environmental Pollution, 2004, 129(3):479-487.
[8]李一兵,彭熙,黄仁海,等.草海湿地保护区土壤重金属及其污染评价[J].贵州科学, 2012, 30(3):57-62. LI Yi- bing, PENG Xi, HUANG Ren-hai, et al. Caohai wetland nature reserve soil heavy metals content and pollution evaluation[J]. Guizhou Science, 2012, 30(3):57-62.
[9]张清海,林昌虎,谭红,等.草海典型高原湿地表层沉积物重金属的积累分布与污染评价[J].环境科学, 2013, 34(3):1055-1061. ZHANG Qing-hai, LIN Chang-hu, TAN Hong, et al. Accumulation, distribution and pollution assessment of heavy metals in surface sediment of Caohai plateau wetland, Guizhou Province[J]. Environmental Science, 2013, 34(3):1055-1061.
[10]林绍霞,张清海,郭媛,等.贵州草海沉积物重金属污染特征及潜在生态风险分析[J].农业环境科学学报, 2012, 31(11):2236-2241. LIN Shao-xia, ZHANG Qing-hai, GUO Yuan, et al. Pollution characteristics and potential ecological risk assessment of heavy metals in sediments of Caohai in Guizhou Province, China[J]. Journal of Agro-Environment Science, 2012, 31(11):2236-2241.
[11]任晓冬.自然保护与社区发展来自草海的经验[M].贵阳:贵州科技出版社, 2005:15-90. REN Xiao-dong. Nature conservation and community development experience from Caohai[M]. Guiyang:Guizhou Science and Technology Press, 2005:15-90.
[12]彭益书,付培,杨瑞东.草海湿地生态系统健康评价[J].地球与环境, 2014, 42(1):68-79. PENG Yi-shu, FU Pei, YANG Rui-dong. Assessment of wetland ecosystem health in the Caohai Lake of Guizhou Province[J]. Earth and Environment, 2014, 42(1):68-79.
[13]王成,张红艳,肖英,等.水浴消解-原子荧光光谱法测定土壤中砷[J].现代科学仪器, 2006(1):126-127. WANG Cheng, ZHANG Hong-yan, XIAO Ying, et al. Determination of As in soils by water bath-atomic fluorescence spectrometry[J]. Modern Scientific Instruments, 2006(1):126-127.
[14]Cherry J A, Shaikh A U, Tallman D E, et al. Arsenic species as an indicator of redox conditions in groundwater[J]. Journal of Hydrology, 1979, 43(1-4):373-392.
[15]Robertson F N. Arsenic in ground-water under oxidizing conditions, southwest United States[J]. Environment Geochemistry and Health, 1989, 11(3):171-185.
[16]Cheng H F, Hu Y A, Luo J, et al. Geochemical processes controlling fate and transport of arsenic in acid mine drainage(AMD)and natural systems[J]. Journal of Hazardous Materials, 2009, 165(1-3):11-26.
[17]Matis K A, Zouboulis A I, Zamboulis D, et al. Sorption of As(V)by goethite particles and study of their flocculation[J]. Water, Air & Soil Pollution, 1999, 111(1):297-316.
[18]Gupta S K, Chen K Y. Arsenic removal by adsorption[J]. Journal Water Pollution Control Federation, 1978, 50(3):493-506.
[19]Frost R R, Griffin R A. Effect of pH on adsorption of arsenic and selenium from landfill leachate by clay minerals[J]. Soil Science Society of America Journal, 1976, 41(1):53-57.
[20]钱晓莉,冯新斌.贵州草海沉积物-水界面无机汞和甲基汞的扩散通量[J].西南大学学报, 2011, 33(3):104-108. QIAN Xiao-li, FENG Xin-bin. A preliminary study of the diffuse flux of inorganic mercury and methylmercury at the sediment-water interface of Lake Caohai, Guizhou Province[J]. Journal of Southwest University, 2011, 33(3):104-108.
[21]何介南,康文星,袁正科.洞庭湖湿地污染物的来源分析[J].中国农学通报, 2009, 25(17):239-244. HE Jie-nan, KANG Wen-xing, YUAN Zheng-ke. Analysis of the pollutant source in the Dongting Lake[J]. Chinese Agricultural Science Bulletin, 2009, 25(17):239-244.
[22]Balistieril L S, Murry J W, Paul B. The biogeochemical cycling of trace metals in the water column of Lake Sammamish, Washington:Response to seasonally anoxic condition[J]. Limnol Oceanogr, 1992, 37(3):529-548.
[23]Shaw T J, Gieskes J M, Jahnke R A. Early diagenesis in differing depositional environments:The response of transition metals in pore water[J]. Geochim Cosmochim Acta, 1990, 54(5):1233-1246.
[24]宋金明.中国近海沉积物-海水界面化学[M].北京:海洋出版社, 1997:6-8. SONG Jin-ming. China offshore deposits-water interface chemistry[M]. Beijing:Ocean Press, 1997:6-8.
[25]万国江.环境质量地球化学原理[M].北京:中国环境科学出版社, 1988:1-216. WAN Guo-jiang. Environmental quality geochemical principle[M]. Beijing:China Environmental Science Press, 1988:1-216.
[26]Li Y H, Gregory S, Diffusion of ions in seawater and in deep-sea sediments[J]. Geochim Cosmochim Acta, 1974, 38(5):703-714.
[27]原盛广,张文婧,郑蓓.北京市沙河水库沉积物重金属分布特征及扩散通量估算[J].安全与环境学报, 2014, 14(2):244-249. YUAN Sheng-guang, ZHANG Wen-jing, ZHENG Bei. Heavy metal contaminant distribution features and the diffusion flux estimation in the sediments of Shahe Reservoir, Beijing[J]. Journal of Safety and Environment, 2014, 14(2):244-249.
腐植酸对水体中五价钒的吸附
刘梦1,2,王华静1,王鲲鹏2,杨金燕2*
(1.四川师范大学地理与资源科学学院,成都610101;2.四川大学建筑与环境学院,成都610065)
摘要:采用批次实验法,研究了腐植酸浓度、钒离子浓度、吸附时间、温度、溶液pH、离子强度、电解质等对腐植酸吸附水体中五价钒的影响。结果表明,钒溶液浓度为90.91 mg·L-1条件下,腐植酸的浓度为1.09 g·L-1时,腐植酸对钒的吸附量最大。随着钒溶液浓度的增加,吸附率逐渐降低并趋于0;而吸附量呈增加-缓慢增加-平衡的趋势;在腐植酸浓度为1.09 g·L-1条件下,钒溶液浓度为1 818.18 mg·L-1时,吸附量达到最大值,吸附等温线与Langmuir模型基本吻合。随着溶液pH、温度的增加,腐植酸对钒的吸附量逐渐减少,即在酸性、温度较低的条件下更有利于腐植酸对钒的吸附。随着溶液电解质浓度的增加,腐植酸对钒的吸附量逐渐降低。红外光谱和扫描电镜的结果显示,腐植酸对钒的吸附机制为钒在腐植酸的表面和内部形成稳定的络合物,这与腐植酸的O-H(或N-H)的氢键、C-O和C-H键的伸缩振动有关。因此,可以考虑用适量的腐植酸作吸附剂,去除水体中的钒,并调整环境条件增强吸附效果。
关键词:腐植酸;钒;吸附;影响因素
中图分类号:X52文献标志码:A文章编号:1672-2043(2016)05-0969-07doi:10.11654/jaes.2016. 05.022
刘梦,王华静,王鲲鹏,等.腐植酸对水体中五价钒的吸附[J].农业环境科学学报, 2016, 35(5):969-975.
LIU Meng, WANG Hua-jing, WANG Kun-peng, et al. Adsorption of pentavalent vanadium by humic acid in water[J]. Journal of Agro-Environment Science, 2016, 35(5): 969-975.
收稿日期:2015-11-19
基金项目:四川师范大学研究生优秀论文培育基金(校研字[2015]5号-42);国家自然科学基金项目(41101484);科技部欧盟国际科技合作项目(2011DFA101222)
作者简介:刘梦(1988—),女,硕士研究生,主要研究方向为水资源与水环境。E-mail:714823069@qq.com
*通信作者:杨金燕E-mail:yanyang@scu.edu.cn
Adsorption of pentavalent vanadium by humic acid in water
LIU Meng1,2, WANG Hua-jing1, WANG Kun-peng2, YANG Jin-yan2*
(1.College of Geography and Resources Science, Sichuan Normal University, Chengdu 610101, China:2. College of Architecture and Environment, Sichuan University, Chengdu 610065, China)
Abstract:Vanadium(V)is released naturally and anthropogenically to the environment and becomes an important pollutant. This study is conducted to examine adsorption characteristics of pentavalent V[V(Ⅴ)]as NaVO3in water by humic acid under a series of initial V concentrations, humic acid concentrations, adsorption time, solution pH, temperature, ionic strength, and electrolyte type and concentrations. Results showed that:(1)at 90.91 mg·L-1V(Ⅴ), the highest adsorption capacity of V was found at 1.09 g·L-1of humic acid concentration; (2)with increases of V(Ⅴ)initial concentrations in solution, the adsorption rate gradually decreased, whereas the adsorption amount increased and reached the maximum at 1 818.18 mg·L-1at 1.09 g·L-1of humic acid concentration. Adsorption isotherm of V by humic acid could be well described by Langmuir model;(3)increasing solution pH and temperature gradually reduced the adsorption amount of V by humic acid, indicating that low temperature and low pH favored V adsorption by humic acid;(4)increasing electrolyte concentrations suppressed the adsorption of V by humic acid;(5)infrared spectrum and scanning electron microscopy showed that V complex was formed on the surface and the inside of humic acid and that the stretching vibration of O-H or N-H, C-O and C-H might also played role in V adsorption. Therefore, appropriate amount of humic acid could be used to remove V in water under certain environmental conditions.
Keywords:humic acid:vanadium:adsorption:influencing factors
随着我国经济快速增长,环境污染呈现出种类多、数量大、波及范围广等特点。钒在自然界分布很广,常伴生在钛磁铁矿、风化堆积残留矿、含钒铁矿、含钒磷矿等矿床中[1]。钒是人与动物正常生长都需要的营养元素[2-3],在调节酶活、降低血糖、生物固氮等方面起着重要作用[4-5],但钒在生物体内含量过多,则会产生毒害作用。20世纪80年代末,钒被列为环境危险元素[6-7]。
未被钒污染的水体中钒含量为0.2~100 μg·L-1[8],而沉钒废水中的钒含量为100~400 mg·L-1[9],高于我国地表水环境质量标准中钒的限值。我国水体中钒的主要污染源为原油冶炼厂、燃油和燃煤工厂以及含钒矿物冶炼厂等在生产过程中产生的废水[10]。因此,研究去除污染水体中的钒很有必要。
腐植酸是自然界中的天然高分子聚合物,具有结合金属离子和有机分子的活性[11-12],能与重金属形成稳定的络合体[13-14],其结构含有大量硫羟基、酚羟基、羧基、醇羟基、氨基等活性基团,且彼此间以氢键结合成网络状,因此分子表面具有孔状结构,可提供良好的吸附表面,是良好的吸附载体。目前,国内有关腐植酸的研究主要有四个方面:腐植酸对重金属的吸附作用及重金属间的竞争、腐植酸与重金属之间的相互作用、腐植酸对重金属的络合/螯合作用、腐植酸对重金属的氧化-还原作用。也有学者以腐植酸或者富里酸作为吸附剂,研究其对重金属离子的解吸特征。但腐植酸对钒离子的吸附研究鲜见报道,吸附特征及机制也尚不明确。本文以腐植酸作为吸附剂,探讨其对水体中钒的吸附特性,为钒污染水体的修复提供理论依据和技术支持。
1 材料与方法
1.1主要试剂来源
腐植酸(HA)购于Sigma-Aldrich公司,主要元素组成见表1。钒标液由分析纯NaVO3配制。

表1 腐植酸主要元素含量Table 1 Elemental content of humic acid studied
1.2溶液中钒浓度的测定方法
溶液中钒的浓度采用磷酸-钨酸钠分光光度法测定,该方法的检测下限约为0.5 mg·L-1,上限为21.5 mg·L-1[15],样品加标回收率为98.33%~101.25%。
1.3反应物浓度与反应时间对腐植酸吸附钒的影响
1.3.1腐植酸浓度的影响实验
分别称取0、10、20、30、40、50、80 mg腐植酸于50 mL塑料离心管中,加入25 mL浓度为100 mg·L-1的钒溶液(以NaVO3的形式加入)和2.5 mL的0.005 mol·L-1的NaNO3[16-18]电解质溶液,使溶液中腐植酸的浓度为0.00、0.36、0.73、1.09、1.45、1.82、2.91 g·L-1,钒溶液浓度为90.91 mg·L-1,放入恒温振荡器中,在25℃下以200 r·min-1的速度振荡24 h,在5000 r·min-1下离心5 min,过滤,用紫外可见光分光光度计测定滤液中钒的浓度。每个处理3个重复。
1.3.2钒溶液浓度的影响实验
称取30mg腐植酸于50 mL塑料离心管中,分别加入25 mL浓度为10、30、50、100、200、300、500、1000、1500、2000、3000、4000、5000、7000、8000 mg·L-1的钒溶液,再加入0.005 mol·L-1NaNO3电解质溶液2.5 mL,使钒的最终浓度依次为9.09、27.27、45.46、90.91、181.82、272.73、454.55、909.09、1363.64、1818.18、2 727.27、3 636.36、4 545.46、6 363.64、7 272.73 mg·L-1,放入恒温振荡器中,在25℃下以200 r·min-1的速度振荡24 h,在5000 r·min-1下离心5 min,过滤,用紫外可见光分光光度计测定滤液中钒的浓度。每个处理重复3次。
1.3.3反应时间的影响实验
称取30 mg腐植酸于50 mL塑料离心管中,加入25 mL浓度为100 mg·L-1的钒溶液和2.5 mL的0.005 mol·L-1NaNO3电解质溶液,使钒溶液浓度为90.91 mg·L-1,在25℃恒温振荡器中以200 r·min-1的速度振荡,分别反应10、30、60、150、240、300、360、420、480、600、660、720、960、1200、1440 min取出,在5000 r·min-1下离心5 min,过滤,用紫外可见光分光光度计测定滤液中钒的浓度。每个处理重复3次。
1.4环境因素对腐植酸吸附钒的影响
1.4.1pH的影响实验
称取30 mg腐植酸于50 mL塑料离心管中,加入25 mL浓度为100 mg·L-1的钒溶液和0.005 mol·L-1的NaNO3电解质溶液2.5 mL,分别用0.1 mol·L-1HCl 和0.1 mol·L-1NaOH调节溶液pH为(2.00±0.05)、(3.00±0.05)、(4.00±0.05)、(5.00±0.05)、(6.00±0.05)、(7.00±0.05)、(8.00±0.05)、(9.00±0.05)、(10.00±0.05),放入25℃恒温振荡器中以200 r·min-1的速度振荡24 h,在5000 r·min-1下离心5 min,过滤,用紫外可见光分光光度计测定滤液中钒的浓度。每个处理重复3次。
1.4.2离子强度的影响实验
称取30 mg腐植酸于50 mL塑料离心管中,加入25 mL浓度为100 mg·L-1的钒溶液,依次加入0.005、0.010、0.050、0.100、0.500、1.000 mol·L-1NaNO3电解质溶液2.5 mL,放入25℃恒温振荡器中以200 r·min-1的速度振荡24 h,在5000 r·min-1下离心5 min,过滤,用紫外可见光分光光度计测定滤液中钒的浓度。每个处理重复3次。
1.4.3温度的影响实验
称取30 mg腐植酸于50 mL塑料离心管中,加入25 mL浓度为100 mg·L-1的钒溶液和0.005 mol·L-1的NaNO3电解质溶液2.5 mL,分别在4、25、40、60、80℃进行24 h吸附试验,在5000 r·min-1下离心5 min,过滤,用紫外可见光分光光度计测定滤液中钒的浓度。每个处理重复3次。
1.4.4电解质的影响实验
称取30 mg腐植酸于50 mL塑料离心管中,加入25 mL浓度为100 mg·L-1的钒溶液,分别加入2.5 mL浓度为0.005 mol·L-1的NaCl、Na2CO3、Na2SO4、NaNO3、NaNO3+NaCl、NaNO3+Na2CO3、NaNO3+Na2SO4电解质溶液,放入25℃恒温振荡器中以200 r·min-1的速度振荡24 h,在5000 r·min-1下离心5 min,过滤,用紫外可见光分光光度计测定滤液中钒的浓度。每个处理重复3次。
1.5扫描电镜与红外光谱分析方法
分别取适量的吸附前后的腐植酸粉末样品,粘在有导电双面胶的样品台,在真空镀膜机中喷金处理,再用日本电子公司JSM-7500F扫描电子显微镜观察腐植酸表面的微观形貌。
分别取少量吸附前后的腐植酸样品于玛瑙研钵中,加入高纯度溴化钾,充分研磨后用压力机压制成透明的片状,用美国Thermo Nicolet公司Nicolet6700傅里叶变换红外分光光度计测定红外光谱,扫描范围为400~4000 cm-1。
1.6统计分析
采用SPSS 16.0软件进行数据统计分析,用最小显著差数法(LSD法)在P=0.05水平下进行检验分析。
2 结果与分析
2.1反应物浓度与反应时间对腐植酸吸附钒的影响
2.1.1腐植酸浓度的影响
当腐植酸浓度≤1.09 g·L-1时,腐植酸对钒的吸附量和吸附率均呈上升趋势,吸附量由趋于0增加至47.58 mg·g-1,吸附率由趋于0增加至47.19%;当腐植酸浓度>1.09 g·L-1时,吸附量由47.58 mg·g-1减少至22.84 mg·g-1,吸附率继续呈上升趋势(图1)。这是由于腐植酸浓度的增加增大了腐植酸的表面积和有效活性位点;继续增加腐植酸浓度时,由于腐植酸质量增加,溶液中钒的质量浓度不断降低,同时过多的腐植酸聚合或者重叠,使得可利用的腐植酸表面积减少,有效活性位点减少,以致吸附量减少[19]。当钒溶液浓度为90.91 mg·L-1、腐植酸浓度为1.09 g·L-1时,腐植酸对钒的吸附量达到最大。因此,后续实验腐植酸的添加量确定为30 mg,即最终溶液中腐植酸浓度为1.09 g·L-1。
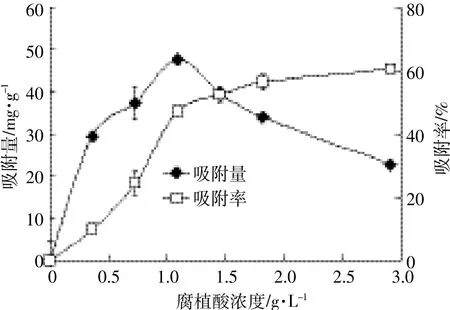
图1 腐植酸添加量对吸附钒的影响Figure 1 Effects of humic acid concentrations on V adsorption from solution
2.1.2钒离子初始浓度的影响
随着钒溶液浓度的增加,腐植酸对钒的吸附量逐渐增加,而吸附率呈下降趋势(图2)。当钒溶液浓度≤27.27 mg·L-1时,腐植酸对钒的吸附率接近100%;随着钒离子初始浓度的升高,腐植酸对钒的吸附率逐渐趋于0,吸附量呈缓慢增加趋势直至平衡。当钒溶液浓度≤454.55 mg·L-1时,吸附量增加较快;钒溶液浓度在454.55~1 818.18 mg·L-1时,吸附量呈缓慢增加趋势;当钒溶液浓度为1 818.18 mg·L-1时,吸附量达到最大值172.10 mg·g-1;当钒溶液浓度>1 818.18 mg·L-1时,腐植酸对钒的吸附量趋于平衡。这是因为在腐植酸的量一定的情况下,吸附剂的表面积和有效活性位点是固定的,随着钒溶液浓度的增加,腐植酸表面的吸附位点逐渐被占据或覆盖。因此,当钒溶液浓度持续增加时,吸附率逐渐降低并趋于0;吸附量呈增加-缓慢增加-平衡的趋势。
用Langmuir模型和Freundlich模型对等温吸附曲线进行拟合(表2)。Langmuir模型拟合结果相关性系数为0.998 9,最大吸附量为169.49 mg·g-1,与实际最大吸附量172.10 mg·g-1较为接近;而Freundlich模型的拟合结果略差,相关性系数为0.827 4,拟合最大吸附量为143.09 mg·g-1,与实际最大吸附量相差较大。Langmuir等温吸附模型是基于吸附作用发生在单分子层,吸附剂表面的吸附位点具有同一性[20],忽略被吸附分子间的横向作用的一种理论模型[21],能较好地表征腐植酸对水体中钒的吸附过程;而Freundlich等温吸附模型拟合效果略差,可能是因为Freundlich等温吸附模型是以实验观察数据为依据建立的经验模型[20],环境因素的选取对实验结果影响较大。

表2 腐植酸吸附钒的等温线拟合结果Table 2 Isotherm models and their parameters for V adsorption by humic acid

表3 腐植酸吸附钒的动力学拟合结果Table 3 Kinetic models and their parameters for V adsorption by humic acid
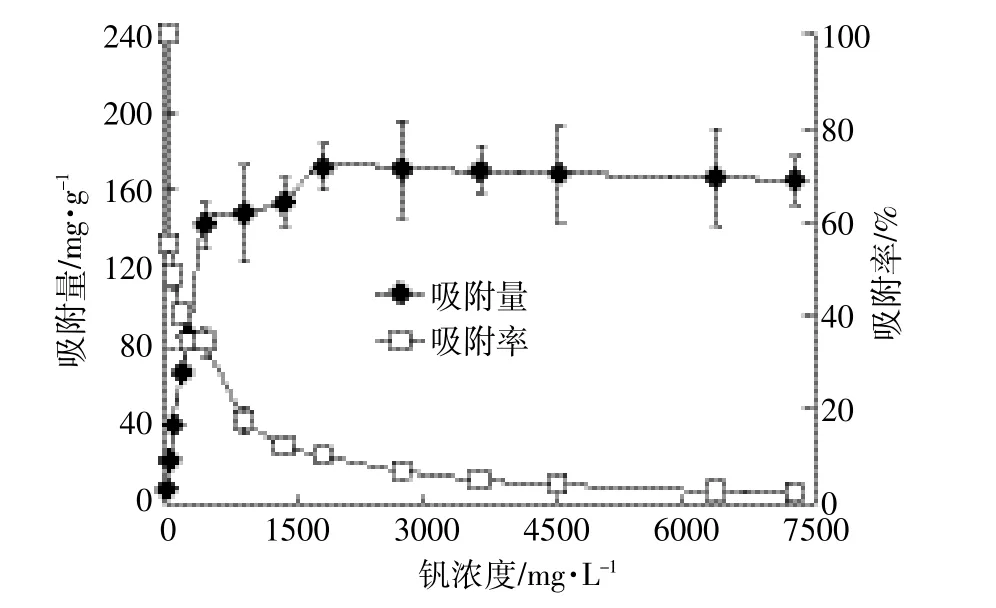
图2 钒离子初始浓度对腐植酸吸附钒的影响Figure 2 Effects of initial V(Ⅴ)concentrations on V adsorption by humic acid
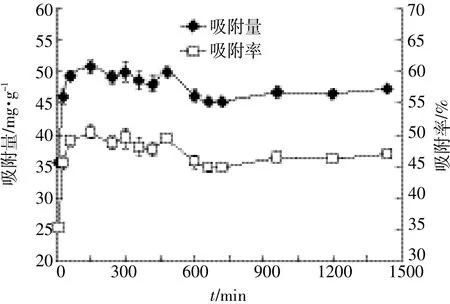
图3 吸附时间对腐植酸吸附钒的影响Figure 3 Effect of time on V adsorption by humic acid
2.1.3吸附时间的影响
在0~150 min内,腐植酸对钒离子的吸附量和吸附率随时间增加而迅速增加,此后吸附量与吸附率略有下降,而到660 min后逐渐趋于平衡(图3)。在吸附初始阶段,腐植酸与钒的反应可能发生在腐植酸分子表面,因此反应速率较快,而到吸附后期,吸附反应主要发生在腐植酸内部,因此减缓了吸附速率[16]。
用拟一级速率方程、拟二级速率方程和双常数动力学模型对吸附动力学数据进行拟合(表3),结果表明拟一级速率方程和双常数动力学模型不能较好地表征腐植酸对钒吸附的动力学过程;拟二级动力学模型能够较好地表征腐植酸对钒的吸附规律,拟合最大吸附量52.25 mg·g-1与150 min时实际值50.74 mg·g-1较为接近;动力学模型表明在整个吸附过程中表面吸附、液膜扩散等都在进行,起主要作用的是腐植酸与钒通过电子交换或电子共享引起的化学吸附,整个吸附过程呈现多级线性关系,表明整个吸附过程伴随着多个控制速率的步骤参与。
2.2环境因素对腐植酸吸附钒的影响
2.2.1pH值的影响
腐植酸不溶于酸,溶于碱,是一种聚电解质[17],pH值会影响腐植酸在溶液中的溶解度。溶液pH值在2~
7之间时,腐植酸对钒的吸附量无显著性差异(P>0.05),吸附量在50.03 mg·g
-1
以上;而当pH值在7~10时,吸附量由50.03 mg·g
-1
下降为4.76 mg·g
-1
,吸附量减少幅度高达90.49%(图4)。随着pH值的增大,由酸性环境逐渐过渡到碱性环境时,腐植酸对钒的吸附量和吸附率均呈下降趋势,即酸性和中性条件较利于腐植酸对钒的吸附,二者相比酸性环境更佳。这是因为,腐植酸不溶于酸,酸性环境有利于腐植酸与钒形成强螯合物,促进了腐植酸对钒的吸附;当反应在碱性环境下进行时,腐植酸溶于碱性溶液而发生离解
[22]
,使得固态的腐植酸量减少,从而减少了腐植酸的表面积和有效活性位点,不利于腐植酸对钒的吸附作用。因此欲提高腐植酸对钒的吸附效果,可以适当降低溶液的pH值。
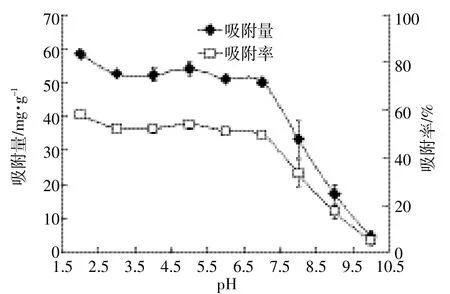
图4 pH对腐植酸吸附钒的影响Figure 4 Effect of pH on V adsorption by humic acid
2.2.2电解质的影响
加入电解质是为了减小由于溶液的离子失衡而对吸附效果造成的影响,不同电解质的存在对腐植酸吸附钒的能力有不同程度的影响(表4)。NaNO3和Na2SO4这两种电解质存在时,与不加电解质时腐植酸对钒离子的吸附相比没有显著性差异(P>0.05),其余五种电解质及电解质组合的存在,与不加电解质时腐植酸对钒的吸附存在显著性差异(P<0.05)。这可能是因为有些离子与钒离子结合,形成络合离子而出现沉淀,使得腐植酸不能较好地与钒离子结合,因此腐植酸对钒的吸附量出现差异。
2.2.3温度的影响
在温度≤25℃时,腐植酸对钒的吸附效果较好,且吸附量没有显著差异;而当温度≥40℃时,腐植酸对钒的吸附显著降低。从图5可以看出,60℃时吸附量由4℃的53.36 mg·g-1降为31.12 mg·g-1,减少了约41.68%。研究表明,温度高于25℃不利于腐植酸对钒的吸附,即常温和低温条件下的吸附效果较佳。原因可能是低温条件可以保持腐植酸的有效活性位点,随着温度的升高,腐植酸的溶解度增加,减少了固态腐植酸含量,腐植酸的表面吸附位点和有效活性位点减少[16],从而在一定程度上降低腐植酸对钒的吸附能力。因此,在利用腐植酸吸附水体中的钒时,可以选择在常温条件下进行。
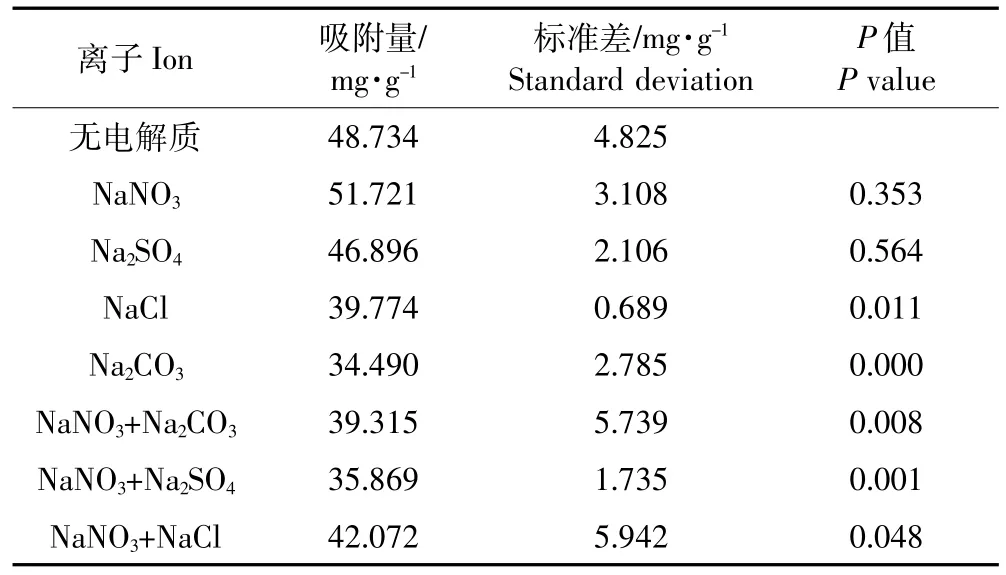
表4 不同电解质存在条件下腐植酸对钒的吸附Table 4 Adsorption of V by humic acid under different electrolytes
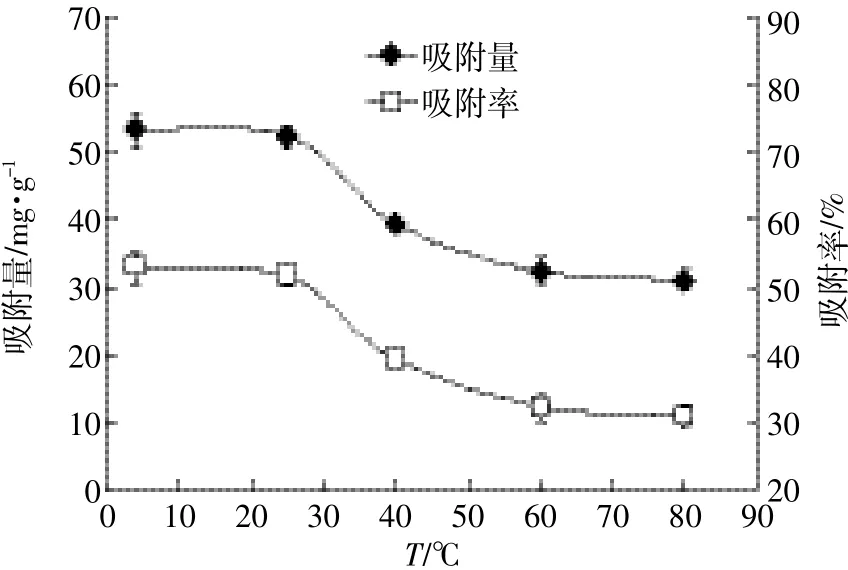
图5 温度对腐植酸吸附钒的影响Figure 5 Effect of temperature on V adsorption by humic acid
2.2.4离子强度的影响
在低离子强度条件下(0.005~0.1 mol·L-1),腐植酸对钒的吸附量随着NaNO3浓度的增加而快速下降,而随着离子强度的进一步增加,腐植酸对钒的吸附并没有显著变化(图6)。这是因为电解质NaNO3的浓度增加会抑制腐植酸分子官能团的离解,溶液中正负电荷增多,导致腐植酸分子间斥力减弱,由于电性的中和使得腐植酸分子卷曲或聚集凝集,从而减少腐植酸的表面积和有效活性位点[23],减少钒离子与腐植酸的结合位点,因此降低了腐植酸吸附钒的能力,使得腐植酸对钒的吸附量和吸附率均降低。
3扫描电镜与红外光谱特征
为表征吸附钒前后腐植酸结构和化学基团的变化特征,对其做了吸附前后的扫描电镜(SEM)分析和红外光谱(FTIR)分析。
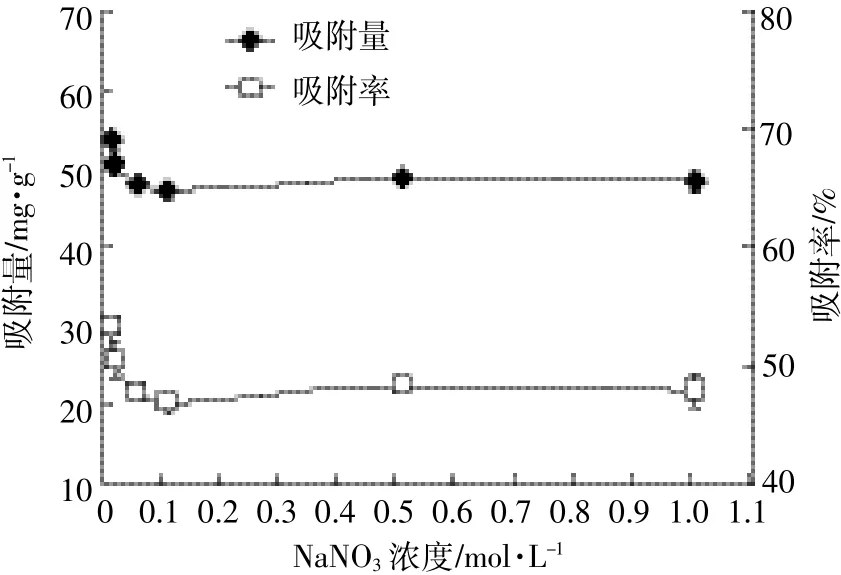
图6 离子强度对腐植酸吸附钒的影响Figure 6 Effect of ionic strength on V adsorption by humic acid
从扫描电镜图(图7)可以看出吸附前的腐植酸表面呈零碎的片状或颗粒状,并有松散小裂缝。腐植酸的碎片状表面结构有利于钒离子扩散到腐植酸的内部,与其形成稳定的络合物;吸附后的腐植酸表面变得均匀板结,几乎没有裂缝存在。这可能是由于腐植酸对钒的吸附不仅发生在表面,而且深入到腐植酸的内部,并与腐植酸结合形成稳定的络合物。也可能是实验过程中由于震荡等造成的腐植酸表面均匀板结。

图7 腐植酸吸附钒前后的扫描电镜图像Figure 7 SEM images of humic acid before and after V adsorption
从红外光谱谱图(图8)可以看出,吸附钒后的腐植酸主要官能团发生了相应的变化,3403 cm-1处的吸收峰移动至3407 cm-1附近,是由于O-H或N-H的氢键伸缩振动;1592 cm-1处的吸收峰移动至1596 cm-1附近和1382 cm-1处的吸收峰移动至1384 cm-1附近,是由于肪烃类-CH3、-CH2的伸缩振动;1031 cm-1处的吸收峰移动至1033 cm-1附近和912 cm-1处的吸收峰移动至914 cm-1附近,是由于多聚糖和类多聚糖结构的C-O键伸缩振动,也可能是存在硅酸盐杂质的Si-O键;796 cm-1处的吸收峰移动至798 cm-1附近,是由于C-H的伸缩振动;538 cm-1处吸收峰小幅移动至539 cm-1附近,是由于C-O-C的伸缩振动;468 cm-1处的吸收峰移动至470 cm-1附近,是由于腐植酸芳香环和-OH的存在。主要官能团的变化说明腐植酸上的羟基、甲基、碳氧键和硅氧键参与了腐植酸对水体中钒的吸附过程。
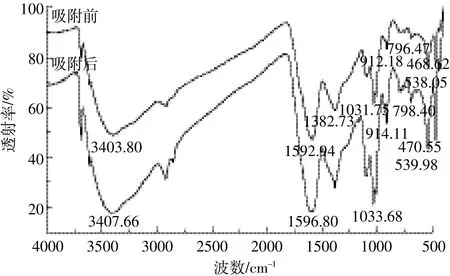
图8 腐植酸吸附钒前后的红外光谱谱图Figure 8 FTIR of humic acid before and after V adsorption
4 结论
(1)溶液钒浓度为90.91 mg·L-1时,随着腐植酸浓度的增加,其对水体中钒离子的吸附量逐渐增加;当腐植酸添加浓度为1.09 g·L-1时,腐植酸对钒离子的吸附量达到最大,继续增加腐植酸浓度,吸附量减少。腐植酸对钒离子的等温吸附曲线可以用Langmuir模型拟合,最大吸附量为169.49 mg·g-1。
(2)随着吸附时间的延长,腐植酸对钒的吸附量呈现迅速增加-缓慢增加-略有减少-吸附平衡的趋势。腐植酸对钒的吸附符合拟二级动力学模型。
(3)随着溶液pH、温度的增加,腐植酸对钒的吸附量均逐渐减少;溶液中电解质浓度增加,可能会与钒离子产生竞争吸附;加入不同的电解质时,会有不同的离子与钒结合形成螯合离子,或是与钒发生竞争吸附,吸附效果差异较大。
(4)红外光谱结果表明腐植酸上的羟基、甲基、碳氧键和硅氧键参与了腐植酸对水体中钒的吸附过程。
基于以上结论,去除水体中的钒污染,可以考虑用适量的腐植酸作吸附剂,在条件允许的情况下,可以适当降低溶液的pH值和温度。同时,应考虑腐植酸本身对水环境的影响。
参考文献:
[1]杨金燕,唐亚,李廷强,等.我国钒资源现状及土壤中钒的生物效应[J].土壤通报, 2010, 41(6):1511-1517. YANG Jin-yan, TANG Ya, LI Ting-qiang, et al. Soil biogeochemistryand resources situation of vanadium in China[J]. Chinese Journal of Soil Science, 2010, 41(6):1511-1517.
[2]滕彦国,矫旭东,王金生.攀枝花矿区土壤对钒的吸附特征研究[J].土壤学报, 2009, 46(2):356-360. TENG Yan-guo, JIAO Xu-dong, WANG Jin-sheng. Adsorption characteristics of vanadium on soils in Panzhihua mining area[J]. Acta Pedologica Sinica, 2009, 46(2):356-360.
[3]汪金舫,刘铮.钒在土壤中的含量分布和影响因素[J].土壤学报, 1994, 31(1):61-67. WANG Jin-fang, LIU Zheng. Vanadium distribution and its affecting factors in soil of China[J]. Acta Pedologica Sinica, 1994, 31(1):61-67.
[4]Cammack R. Nitrogen fixation:A role for vanadium at last[J]. Nature, 1986, 322:312.
[5]李青仁,王月梅,李晓波.钒的生物学功能及与疾病的关系[J].微量元素与健康研究, 2007, 24(2):65-66. LI Qing-ren, WANG Yue-mei, LI Xiao-bo. Vanadium biology function and disease relations[J]. Studies of Trace Elements and Health, 2007, 24 (2):65-66.
[6]Hindy K T, Abdel Shafy H I, Farag S A. The role of the cement industry in the contamination of air, water, soil and plant with vanadium in Cairo [J]. Environmental Pollution, 1990, 66:195-205.
[7]樊灏,杨金燕,边静虹,等. V(Ⅴ)与V(Ⅳ)在不同土壤中的吸附-解吸行为研究[J].环境科学与技术, 2014, 37(8):1-7. FAN Hao, YANG Jin-yan, BIAN Jing-hong, et al. Study on adsorptiondesorption of V(Ⅳ)and V(Ⅴ)in different soils[J]. Environmental Science & Technology, 2014, 37(8):1-7.
[8]吴涛,兰昌云.环境中的钒(V)及其对人体健康的影响[J].广东微量元素科学, 2004, 11(1):11-15. WU Tao, LAN Chang-yun. Vanadium in environment and its harm to human health[J]. Guangdong Trace Elements Science, 2004, 11(1):11-15.
[9]王英.沉钒废水处理技术的研究现状[J].铁合金, 2012, 43(6):41-45. WANG Ying. Current situation of the vanadium precipitating waste water treatment technology[J]. Ferro-Alloys, 2012, 43(6):41-45.
[10]邹宝方,何增耀.钒的环境化学[J].环境污染与防治, 1993, 15(1):26-31. ZOU Bao-fang, HE Zeng-yao. Environmental chemistry of vanadium [J]. Environment Pollution & Control, 1993, 15(1):26-31.
[11]Marang L, Eidner S, Kumke M U, et al. Spectroscopic characterization of the competitive binding of Eu(Ⅲ), Ca(Ⅱ), and Cu(Ⅱ)to a sedimentary originated humic acid[J]. Chemical Geology, 2009, 264(1-4):154-161.
[12]周岩梅,张琼,汤鸿霄.多环芳烃类有机物在腐植酸上的吸附行为研究[J].环境科学学报, 2010, 30(8):1564-1571. ZHOU Yan-mei, ZHANG Qiong, TANG Hong-xiao. Sorption behavior of polycyclic aromatic hydrocarbons onto humic acid particulates[J]. Acta Science Circumstantiae, 2010, 30(8):1564-1571.
[13]陈颖,袁旭音.河口湿地沉积物中腐植酸含量对外源重金属分布的影响研究[J].水土保持学报, 2008, 22(4):185-189. CHEN Ying, YUAN Xu-yin. Effects of humic acid on partitioning of extrinsic heavy metal for the estuarine wetland sediment[J]. Journal of Soil and Water Conservation, 2008, 22(4):185-189.
[14]Dong L H, Yang J S, Yuan H L, et al. Chemical characteristics and influences of two fractions of Chinese lignite humic acid on urease[J]. European Journal of Soil Biology, 2008, 44(2):166-171.
[15]周静,於利慧.磷钨钒杂多酸分光光度法测定钛精矿中五氧化二钒[J].冶金分析, 2014, 34(12):66-69. ZHOU Jing, YU Li-hui. Determination of vanadium pentoxide in titanium concentrate by phosphorus-tungsten-vanadium heteropoly acid spectrophotometry[J]. Metallurgical Analysis, 2014, 34(12):66-69.
[16]马明广,周敏,蒋煜峰.不溶性腐植酸对重金属离子的吸附研究[J].安全与环境学报, 2006, 6(3):68-71. MA Ming-guang, ZHOU Min, JIANG Yu-feng. Study on adsorption of heavy metal ions onto insolublized humic acid[J]. Journal of Safety and Environment, 2006, 6(3):68-71.
[17]孔德星.腐植酸在土壤中对Cu2+的吸附特性影响[J].广东化工, 2014, 41(17):41-42. KONG De-xing. Adsorption characteristic of Cu2+on loess soil affected by humic acid[J]. Guangdong Chemical Industry, 2014, 41(17):41-42.
[18]蒋煜峰,张媛,马明广,等.腐植酸对Cd在西部黄土上吸附特性影响的研究[J].农业环境科学学报, 2006, 25(5):1379-1382. JIANG Yu-feng, ZHANG Yuan, MA Ming-guang, et al. Adsorption characteristic of Cd on loess soil affected by humic acid[J]. Journal of Agro-Environment Science, 2006, 25(5):1379-1382.
[19]于春光.改性山桃壳吸附水中重金属的效能研究[D].哈尔滨:哈尔滨工业大学, 2013. YU Chun-guang. The study of adsorption efficiency of heavy metal from aqueous solution using Chinese walnut shell[D]. Harbin:Harbin Institute of Technology, 2013.
[20]蒋新宇,黄海伟,曹理想,等.毛木耳对Cd2+、Cu2+、Pb2+、Zn2+生物吸附的动力学和吸附平衡研究[J].环境科学学报, 2010, 30(7):1431-1438. JIANG Xin-yu, HUANG Hai-wei, CAO Li-xiang, et al. Kinetics and equilibrium of biosorption of Cd2+, Cu2+, Pb2+, Zn2+by mancrofungus (Auricularia polytricha)biomass[J]. Acta Scientiae Circumstantiae, 2010, 30(7):1431-1438.
[21]马宏飞,李薇,韩秋菊,等.茶叶渣对Ni(Ⅱ)的吸附动力学及等温吸附模型研究[J].科学技术与工程, 2013, 13(16):4761-4764. MA Hong-fei, LI Wei, HAN Qiu-ju, et al. Research on the adsorption kinetics and thermal adsorption model of Ni(Ⅱ)with tea dust[J]. Science Technology and Engineering, 2013, 13(16):4761-4764.
[22]王亚军,朱琨,王进喜,等.腐植酸对铬在砂质土壤中吸附行为的影响研究[J].安全与环境学报, 2007, 7(5):42-47. WANG Ya-jun, ZHU Kun, WANG Jin-xi, et al. Study on the humic acid adsorption of chromium in sandy soil[J]. Journal of Safety and Environment, 2007, 7(5):42-47.
[23]杨毅,王晓昌,金鹏康,等.水环境中腐植酸与镉离子结合作用的影响因素[J].环境工程学报, 2013, 7(12):4603-4606. YANG Yi, WANG Xiao-chang, JIN Peng-kang, et al. Influencing factors of binding of humic acid and cadmium ion in the water environment[J]. Chinese Journal of Environment Engineering, 2013, 7(12):4603-4606.
中图分类号:X820.3
文献标志码:A
文章编号:1672-2043(2016)05-0955-08
doi:10.11654/jaes.2016.05.020
收稿日期:2015-10-22
基金项目:国家水体污染控制与治理科技重大项目(2012ZX07101-001)
作者简介:罗明科(1989—),男,湖南邵阳人,硕士研究生。E-mail:luoke1125@126.com
*通信作者:余辉E-mail:yuhui@craes.org.cn
Vertical pollution characteristics of sediments from lakes in middle reaches of Yangtze River
LUO Ming-ke1,2, TIAN Xue-da1, YU Hui2*, YANG Chao3, NIU Yuan2, LIU Peng1,2, NIU Yong2
(1.College of Chemical Engineering, Xiangtan University, Xiangtan 411105, China;2.State Key Laboratory of Environmental Criteria and Risk Assessment, Chinese Research Academy of Environmental Sciences, Beijing 100012, China;3.Policy Research Center for Environment and Economy, Ministry of Environmental Protection, Beijing 100029, China)
Abstract:Sediment vertical pollution characteristics are important for understanding the history of lake pollution. Here sediments from Lake Donghu in Wuhan, Lake Haikou in Huangshi, and Lake Nanhu in Zhongxiang in the middle reaches of the Yangtze River were collected to reveal the variation patterns and the main pollution sources of pollutants. The vertical distributions of total organic carbon(TOC), total nitrogen(TN), and heavy metals(Zn, Cu, Ni, Cr, Pb)were examined. Results showed that:concentrations of TOC and TN increased rapidly from 10 to 30 cm depth of sediment, which was consistent with the environmental changes around the lakes. The maximum value of TOC concentrations appeared in Lake Haikou, while that of TN concentrations occurred in Lake Donghu. Zn, Cu and Pb were mainly influenced by human activities, while Cr was primarily derived from natural sources. The pollution of heavy metals decreased in order of Lake Donghu>Lake Haikou>Lake Nanhu. Correlation analysis and principal component analysis showed that pollution contributed by human activities was greater than that by natural sources in these three lakes. Nutrients and Pb were the common pollutants. Heavy metal pollution in the sediments of these three lakes was affected by multiple factors. These results would provide useful information for controlling lake pollution in this area.
Keywords:core sediment; TOC; TN; heavy metal; correlation analysis; principal component analysis

