洪湖湿地地质碳汇效应初步研究
刘 波, 何师意
((1.湖北省地质局 水文地质工程地质大队,湖北 荆州 434020; 2.中国地质科学院 岩溶地质研究所,广西 桂林 541004)
洪湖湿地地质碳汇效应初步研究
刘 波1, 何师意2
((1.湖北省地质局 水文地质工程地质大队,湖北 荆州 434020; 2.中国地质科学院 岩溶地质研究所,广西 桂林 541004)
湿地是陆地上巨大的有机碳库,具有调节气候功能,在全球增温和CO2浓度上升的背景下,对湿地地质碳汇的研究,会帮助人类更好地应对全球气候变化。本研究以洪湖湿地为研究对象,利用现场测定、室内样品分析及同位素方法,获得了主要碳汇指标强度及其变化,分析了洪湖湿地水体水化学特征、溶解无机碳及同位素组成特征、水体及沉积物有机碳特征,初步识别了湖泊碳库的碳来源。洪湖水体无机碳库达17 792 tC。测得洪湖水体溶解有机碳平均浓度为6 mg/L、总有机碳平均浓度为8.25 mg/L;估算洪湖水体溶解有机碳库和总有机碳库分别为4 080 tC和5 610 tC。水生植物总固碳量为32 656 tC/L。表层沉积物中有机碳量为69 350 tC/a,无机碳量为78 280 tC/a,总碳量为147 630 tC/a。洪湖每年地质碳汇中固定于大型水生植物中的碳可以达到14 534 tC/a。
湿地;地质碳汇;洪湖;有机碳;无机碳
大量的观测和研究表明,自工业革命以来,由于受人类活动的影响,CO2浓度正以前所未有的速度增加,导致温室效应增强并有可能引起全球性气候变暖。近年来,科学界针对工业革命以来人类活动不断增加,大气CO2浓度及全球气候变暖而建立了现代地球系统碳循环平衡模型,根据地球各碳库之间的源汇的估算,源值大于汇值,存在一个遗漏汇,即“未知汇”,该遗漏汇从1985年的1.7 PgC/yr,增加到2005年的2.5 PgC/yr。目前,对如此大的“遗漏汇”,多数人认为是估算的可靠性问题,没有考虑地质碳汇。
所谓地质碳汇,是指消耗空气中二氧化碳的各类地质作用。岩土中的碳,一般以有机或无机形式存在,地质系统中每时每刻都在发生着以碳为生成物或反应物的化学反应。近年来中国有关地质碳汇的研究越来越受到世界各国政府和学术界的关注。据蒋忠诚等中国地质碳汇潜力研究,生物作用参与下的地质碳汇过程主要是短时间尺度过程,能及时响应气候、降雨、植被的变化,而且碳汇量和潜力大,是“未知汇”的重要部分。因此,在全球增温和CO2浓度上升的背景下,对地质碳汇的研究,会帮助人类更好地应对全球气候变化。
湿地被称为“地球之肾”,与森林、海洋并列为全球三大生态系统类型,具有调节气候的功能。湿地是陆地上巨大的有机碳库,其碳储量变化对全球气候变化和碳循环起着重要作用。当前对于湿地植被、土壤碳储量的研究已经取得了不少的成果,但是对于湖泊湿地的地质碳汇的研究还较少。
洪湖湿地是长江中游地区重要湿地生态区域,在长江中下游浅水湖泊型湿地中具有代表意义。开展洪湖湿地地质碳汇效应研究,可以较精确地估算洪湖湿地地质碳汇量状况,评价洪湖湿地地质碳汇通量,为研究典型湖泊湿地地质碳汇效应在未来气候变化中的作用提供基础数据,为合理开发、利用、恢复和保护洪湖湿地提供理论基础。
1 研究区概况
研究区洪湖位于湖北省东南部(113°07′~114°05′E,29°39′~30°12′N)、江汉平原四湖水系的尾端,是湖北省最大、全国第七大天然淡水湖泊。洪湖是长江和汉水支流东荆河之间的大型浅水洼地壅塞湖,集水区面积383.75 km2,是一个以调蓄为主,兼具灌溉、渔业、航运、饮水等多种功能的湖泊[1]。洪湖所处的四湖地区是由燕山运动形成的断陷盆地,后受外营力作用形成深厚洪积沉积层,形成了一些河流洼地,有些洼地部分水流不畅,因而形成了洪湖。湖底平坦,地势由西北向东南倾斜,地面径流随地势高低从四湖总干渠进入洪湖,洪湖东南部有出水口闸通长江,与长江进行物质能量的交换。洪湖属于典型的北亚热带湿润季风气候,夏季炎热多雨,盛行东南风;冬季寒冷少雨,多为东北风,且冬夏长,春秋短。年降雨量平均在1 000~3 000 mm,且4—10月份总降水量约占全年降雨量的77%;年均蒸发量为1 353 mm。在洪湖湿地自然保护区分布有维管束植物472种21变种1变型种,浮游植物280种,植物资源丰富。其中浮游植物主要有绿藻门、硅藻门、蓝藻门等;高等水生植物中沉水植物分布面积占绝对优势(约占总面积的72.49%),挺水和漂浮植物分布面积较小[2]。
2 研究内容及方法
2.1 研究内容

2.2 研究方法
(1) 利用现场测定和室内样品分析,获得主要碳汇指标强度及其变化;
(2) 设置观测剖面,统测碳汇指标,分析其时空变化特征;
(3) 利用同位素方法,初步识别湖泊碳库的碳来源;
(4) 利用水化学方法,无机碳汇量(DIC)由下列公式计算得到:
式中:Q为流量(或水体体积);t为观测时间段(湖泊碳储量计算不是必须)]为现场测得的浓度;Kcs为观测时间段内的无机碳汇量。
(5) 湖水溶解有机碳总量利用水中DOC浓度和湖水体积进行估算;

图1 洪湖观测点布置示意图Fig.1 Schematic diagram of observation point layout in Honghu
(6) 底泥(表层)有机碳总量利用底泥(表层)有机碳含量和参考中国主要湖泊底泥沉积速率进行估算;
(7) 湖水表面释放的CO2速率采样自制静态箱现场测定。
3 结果及分析
3.1 水化学特征与分析
3.1.1 水化学特征
采样过程中洪湖水体水温(T)的变化范围为20.4~25.2 ℃,平均值为22.1 ℃;pH值变化范围为7.46~9.01,平均为8.54。电导率(Spc)的变化范围较大,为300~482 μS/cm,平均为381.11 μS/cm。总溶解性固体(TDS)同电导率变化范围较大,为162.74~270.13 mg/L,平均为212.52 mg/L,二者的变化可能与岩层出露的分布不均有关。溶解氧(DO)的变化范围较大,测得的最小值为7.77 mg/L,最大值未测出,超出仪器检测值(20 mg/L),平均为10.26 mg/L。


图2 洪湖水体水化学组成Piper图Fig.2 Piper trilinear nomograph of water chemistry in Honghu Lake
3.1.2 水化学特征分析




图3 洪湖湖水Gibbs图Fig.3 Gibbs figure of Honghu Lake
此外,已有很多关于洪湖水质的研究发现:洪湖水质主要受四湖(长湖、三湖、白露湖、洪湖)流域地区工农业废水、生活污水等外源污染和湖内围网养殖的影响,其中,围网养殖是水质最主要的制约因素[12-14]。这些人类活动也必然会对洪湖水体的水化学造成影响,已有研究表明,水体中Na+和Cl-浓度变化最容易受到人类活动的影响,特别是Cl-浓度易受工业污水排放的影响[15],所以,除了蒸发盐岩的溶解,洪湖水中较高的Na+和Cl-浓度还受控于流域污水的排放。

图4 洪湖湖水主要离子相关关系图Fig.4 Correlation of major ions in Honghu Lake
3.2 洪湖溶解无机碳及其同位素组成特征分析
3.2.1 溶解无机碳及其同位素组成特征
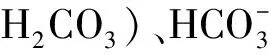
在本研究的观测期间,各采样点不同深度处DIC及δ13CDIC的分布情况如图5。从图中可以看出:在垂直方向上,大部分采样点的DIC自表层向底层逐渐增大,δ13CDIC自表层向底层有逐渐变轻的趋势,两者之间呈较弱的负相关关系,但除HH12点外其余采样点的DIC及δ13CDIC的这种垂向变化并不显著。在垂直方向上DIC浓度的最小值(0.9 mmol/L)和最大值(3 mmol/L)分别出现在HH12的底层和表层,与之相对应,HH12点底层(δ13CDIC=-7.79‰)和表层(δ13CDIC=-0.49‰)的δ13CDIC分别为最小值和最大值。在水平方向上,各点之间的DIC及δ13CDIC存在一定差异,若取消各采样点的分层差异,DIC浓度变化介于1.02~2.51 mmol/L,平均为1.94 mmol/L,δ13CDIC变化介于-5.33‰~-0.68‰之间,平均为-2.50‰。
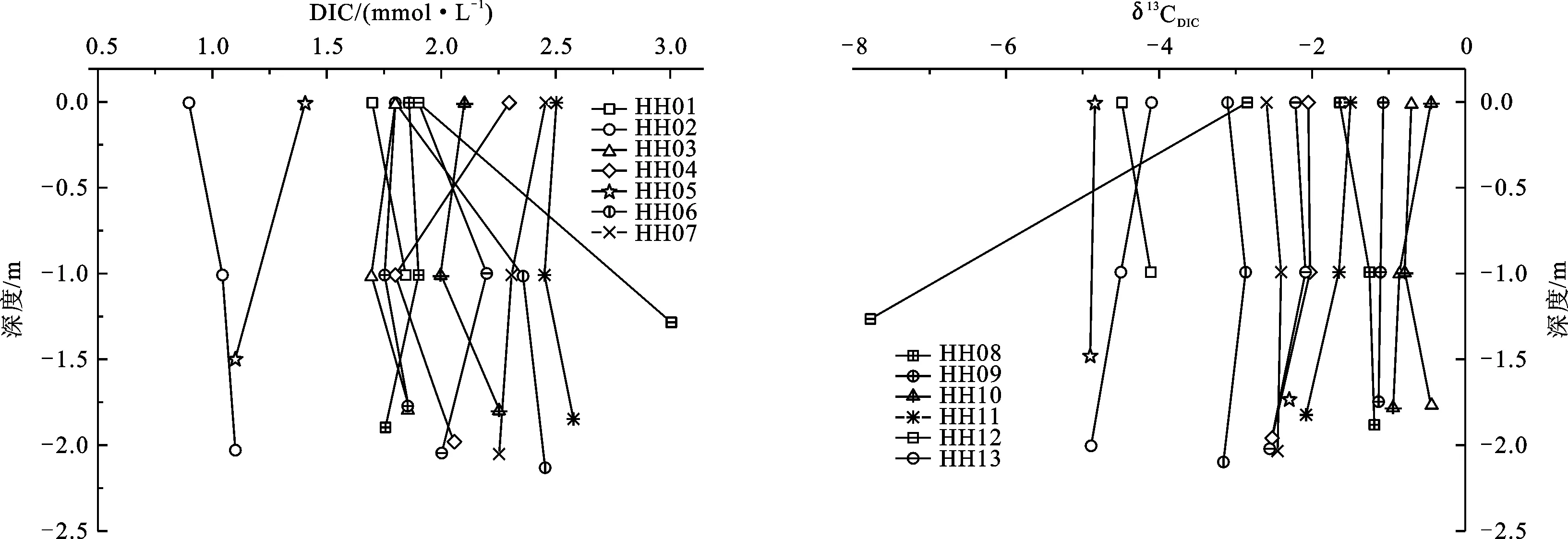
图5 洪湖水体DIC及δ13CDIC分布特征Fig.5 Distribution characteristics of DIC and δ13CDIC in Honghu Lake
3.2.2 溶解无机碳及其同位素组成特征分析
湖泊水体DIC及其同位素组成主要受入湖河流水体DIC及δ13CDIC、水—气界面CO2交换、有机质的氧化分解、碳酸盐物质的溶解与沉淀及水生植物生物作用等过程的影响[17-19]。并且近期相关研究发现,在一个相对封闭水体(水库或湖泊),流域碳酸盐岩风化、水生植物活动及有机质分解是影响水体DIC及δ13CDIC变化特征的主要因素。湖泊DIC经典模型认为,由于表层水生植物较强的光合作用吸收CO2,而底层通常发生有机质的降解及可溶盐的溶解,在垂向上DIC浓度将表现出表层浓度低、底层浓度较高的现象;而光合作用优先吸收12C,底层有机质降解产生的CO2又贫13C,因而δ13CDIC值则表现出表层偏正、底层偏负的特征[20]。如前文述及,本次采样洪湖水体的DIC及δ13CDIC在垂直方向的变化较小,并且相关性较弱。这可能与洪湖自身“湖浅面大”、人类活动对湖水的扰动有关。此外,本次采样时间为10月下旬,季节特征不明显,水体热分层不显著。如表1所示,表层与底层的温差介于0.3 ~2.1 ℃,平均为1.15 ℃,水深介于1.0~2.13 m,远小于同类研究水库的垂向温差及水深(平均为5.5 ℃,20~30 m)[17-18]。因而,整个水柱剖面上DIC及其碳同位素组成的差异性较小。

表1 洪湖水温分布图(T/℃)
在本次采样中,HH12点异于其它点DIC及其碳同位素组成,表现出显著的垂向变化及显著的负相关关系。这可能主要归功于HH12点周围浮水植物(主要为水葫芦)生长茂盛,水体表层水生植物光合作用强烈对DIC利用显著,水体下层光合作用受到抑制,对DIC利用减少,同时造成上层水体δ13CDIC偏重,下层水体δ13CDIC偏轻。与其他参数相比,溶解氧(DO)更能反映水生生态系统中新陈代谢的情况。HH12点表层溶解氧达到本次采样最高值(DO>20 mg/L),由于过于饱和,甚至形成了很多气泡,相反下层溶解氧(DO=7.77 mg/L)浓度大大下降。这主要得益于表层水体几乎被植物叶片覆盖,光合作用产氧量极高,而下层水体由于光照强度减弱,阻碍了一些水生植物进行光合作用,并且由上层向下层输入的有机物较多,由此加强的呼吸作用使得下层的溶解氧浓度大大下降,远低于湖水上层及湖区其他区域同深度的溶解氧值。
3.3 洪湖水体及沉积物有机碳特征分析
3.3.1 洪湖水体有机碳特征分析
湖泊水体溶解有机碳(DOC)的来源分内源和外源两种:内源是指藻类和水生生物释放的DOC,约占其初级生产力的12%~75%,其浓度通常与浮游生物量呈正相关;外源则主要来源于陆源植物和土壤有机质分解,由河流携带进入湖泊[21-23]。同时,人类活动排放的污水也会增加湖泊水体DOC的含量[23]。
如图6所示,洪湖水体溶解有机碳(DOC)和总有机碳(TOC)浓度的总体变化范围分别为5.29~7.70 mg/L(平均为6.00 mg/L)和5.97~17.07 mg/L(平均为8.25 mg/L)。HH12点由于表层与底层的水生植物及藻类分布的巨大差异性,以致DOC浓度的垂向差异较大,剩余其它点的DOC和TOC在垂直方向上几乎没有差异,没有表现出前人对分层期湖泊(Superior Lake、红枫湖、百花湖)水体DOC呈“上层高,下层低”的相同趋势[23-25]。这可能与前文所述采样时间处于秋季且湖浅没有形成热分层有直接关系。并且由于洪湖受人类活动的影响较大,其DOC浓度远高于Superior Lake(1.07~2.50 mg/L)、红枫湖(1.60~3.08 mg/L)和百花湖(1.97~3.26 mg/L)的DOC浓度。

图6 洪湖水体溶解有机碳(DOC)和总有机碳(TOC)浓度分布特征Fig.6 Distribution characteristics of dissolved organic carbon and total organic carbon in Honghu Lake
3.3.2 洪湖沉积物有机碳特征分析
(1) 洪湖沉积物有机碳来源分析。碳是湖泊沉积物的主要组分之一,由无机碳和有机碳两部分构成。有机碳主要来源于湖泊水生植物及流域侵蚀带来的陆源植物碎屑;无机碳则来源于湖泊自生碳酸盐和外源碳酸盐[26]。如图7所示,洪湖沉积物中有机碳含量(Corg)百分比为1.24%~5.47%,平均为3.66%;总碳含量(TC)百分比为2.92%~17.14%,平均为7.66%。
本次采样中,几乎各层所有点方解石饱和指数SIc(平均为0.32)、白云石饱和指数SId(平均为0.61)都接近或>0,表明水体对碳酸盐是平衡或过饱和的,进一步说明洪湖可形成自生碳酸盐;再则长江流域自上游至下游碳酸盐岩分布广泛,碳酸盐岩的风化溶解控制着水体的化学组分,所以,洪湖沉积物可能会受外源碳酸盐岩的影响。此外很多研究表明,沉积物有机质C/N原子比可有效指示有机质的来源[27]。当碳氮比(C/N)值在4~10之间时,有机质的来源以挺水植物、浮游植物和沉水植物为主的水生植物或各种藻类;当碳氮比(C/N)值处于10~20之间时,指示了水生沉水或浮游植物,或者与陆生植物的混合来源;而若有机质来源以挺水植物或陆生高等植物为主时,碳氮比(C/N)值>20[28-29]。本次采样中洪湖沉积物有机质C/N原子比介于9.11~12.24,平均为10.77,说明洪湖沉积物有机质主要源自水生植物,受陆源有机质的影响少。如上分析,假设洪湖水体有机质仅为大型水生植物(沉水植物或挺水植物)和浮游藻类两种物源的混合,则沉积物有机质中来自大型水生植物的比例计算可表述为:
Asample=Bsquat×Asquat+(1-Bsquat)×Aalga
式中:A为C/N;B为大型水生植物的贡献率;下标squat和alga分别表示大型水生植物和浮游藻类。取Asquat=16(取淡水水生植物的碳氮比C/N(12~20)的平均值)[29];Aalga=6(取淡水浮游藻类平均值)[30]。结果显示Bsquat=47.7%,即洪湖大型水生植物(沉水植物或挺水植物)和浮游藻类对沉积有机质的贡献相近。
(2) 洪湖表层沉积物有机碳分布特征分析。从图7-a还可以发现洪湖沉积物有机碳(Corg)在沿岸带含量明显较高,并且通过将采样点与图7-b对比发现有机碳(Corg)含量较高的HH01、HH02、HH03、HH08、HH09、HH10、HH11和HH13恰好都处于养殖区,而有机碳(Corg)含量较少的采样点分布在开阔水体或保护区。研究显示河水挟带的污染颗粒以及鱼类排泄物、残饵等有机物的沉积对湖泊表层沉积物的有机碳含量有明显增加作用[31-32],故洪湖表层沉积物含量表现出靠近河岸、养殖区范围较丰富的分布特征。HH12点表现出较低的有机碳(Corg)含量,可能是受表层浮水植物影响以致下层水生植物或藻类生物量极少,HH12点底层的溶解氧及DOC最低也佐证了这一可能性。

图7 洪湖沉积物有机碳及总碳分布特征和不同水环境功能区域分布图[33](据班璇等,2010修改)Fig.7 Distribution map of organic carbon & total carbon and functional region in different water environment
3.4 洪湖地质碳汇估算
3.4.1 洪湖碳储量估算
(2) 水体有机碳储量。本研究测得洪湖水体溶解有机碳(DOC)、总有机碳(TOC)浓度分别平均为6 mg/L和8.25 mg/L,那么可估算洪湖水体溶解有机碳库和总有机碳库分别为4 080 tC和5 610 tC。
(3) 水生植物固碳量。当前洪湖水生植物中沉水植物占绝对优势,分布面积约占总面积的72.49%,挺水植物菰群落和莲群落分布面积较小,其中沉水植物又以微齿眼子菜(黄丝草)、穗状狐尾藻、金鱼藻、苦草和黑藻为主。已有研究表明洪湖沉水植物平均固碳能力为62.73 gC/m2·a,菰的平均固碳能力为14.45 gC/m2·a[34],则洪湖沉水植物总固碳量为17 450 tC/a,菰的总固碳量为15 206 tC/a,则洪湖水生植物总固碳量为32 656 tC/a。
(4) 表层沉积物固碳量。已有研究表明洪湖在1954年—2002年间,沉积物平均沉积速率为0.155 cm/a[35]。并且根据太湖20世纪80年代末的沉积通量(0.6 g/cm2·a)与沉积速率(0.188 cm/a)[36],估算出太湖沉积物密度为3.19 g/cm3。那么可利用太湖沉积物密度来表征洪湖沉积物密度,最终求得洪湖沉积物通量为1.9×106t/a。本文测得洪湖沉积物有机碳和无机碳(总碳—有机碳)含量(%)分别平均为3.65和4.12,则可进一步估算出表层沉积物中有机碳量为69 350 tC/a,无机碳量为78 280 tC/a,总碳量为147 630 tC/a。
3.4.2 地质碳汇通量计算


式中:Q为流量(或水体体积);t为观测时间段(湖泊碳储量计算不是必须的)] 为现场测得的浓度;Kcs为观测时间段内的无机碳汇量。
通过计算,Kcs=8 896 tC,即无机碳储量中地质碳汇作用的贡献为8 896 tC。
(2) 水生植物生物固碳作用及其对地质碳汇稳定的贡献。美国地球化学专家Curl(2012)认为岩溶地质作用(碳酸盐风化)是一个碳迁移过程,而不是碳汇。这一观点源于把地质作用当作一种纯无机的过程[40],但随着人们认识到生物在岩溶地质作用中的广泛参与[6,37,41],即地质作用吸收大气CO2产生的DIC可以被水体中水生植物的光合作用所利用而形成有机碳,使地质碳汇以有机碳的形式稳定下来。

δT=δA(1-fB)+ δBfB


可见,通过碳酸盐岩风化以及水生植物的光合利用作用,可以将大气CO2转化为有机体中的C而固定下来,即洪湖每年地质碳汇中固定于大型水生植物中的碳可以达到14 534 tC/a。

表2 几种主要水生植物群落fB值及固定重碳酸根碳量
注:“”指无数据。

综上,洪湖水体、水生植物、表层沉积物的碳储量及地质作用对水体无机碳及水生植物固碳量的贡献如表3所示:

表3 洪湖碳储量分布特征
注:“”指无数据。

4 结论与建议
4.1 结论
(1) 洪湖湿地水体的水化学组成受流域碳酸盐岩、蒸发盐岩和硅酸盐岩的风化溶解的共同控制,碳的来源主要为碳酸盐岩和硅酸盐岩的风化作用形成,且碳酸盐岩的风化溶解占据主要地位,而硅酸盐岩的贡献相对较小。
(2) 洪湖湿地水体和表层底泥碳储量巨大。碳储量主要由水体中无机碳储量(DIC)、水体中有机碳(DOC)和表层沉积物固碳量(水生生物的作用)组成。
(3) 洪湖碳储量为:洪湖水体无机碳库达17 792 tC。测得洪湖水体溶解有机碳(DOC)、总有机碳(TOC)浓度分别平均为6 mg/L和8.25 mg/L,估算洪湖水体溶解有机碳库和总有机碳库分别为4 080 tC和5 610 tC。水生植物总固碳量为32 656 tC/a。表层沉积物中有机碳量为69 350 tC/a,无机碳量为78 280 tC/a,总碳量为147 630 tC/a。洪湖每年地质碳汇中固定于大型水生植物中的碳可达14 534 tC/a。
4.2 存在问题与建议
(1) 本研究仅就洪湖湿地的水体和表层底泥湖泊地质碳储量及碳汇指标空间分布特征进行了初步调查或估算工作[46]。对近湖岸陆地湿地区域未进行采样分析和调查,对湖泊深部底泥未进行采样分析和调查,对湖泊中水生植物未进行全面采样分析和调查。因此,估算的湖泊碳库数量是偏低的,若考虑上述方面,可能整个所研究的湖泊湿地系统的碳储量会有较大的增加。建议今后继续安排相关方面的调查和研究。
(2) 本研究仅进行了一次野外现场测试和采样,加上缺少湖泊径流量资料。因此,尽管湖泊湿地的碳储量及碳汇潜力巨大,但仍无法计算出这个储量在不同季节或年度的变化情况和准确评价其碳汇潜力,即无法计算地质净碳汇。建议今后继续开展不同季节碳汇指标动态变化方面的调查和研究,更准确估算地质净碳汇。
(3) 本研究设置的观测点和采样点未能较均匀地布置在整个湖泊水体范围内,观测点偏少,不能很好的代表整个湖泊范围的情况,在估算时,水体深度、水中DOC浓度、水中DIC浓度均为平均值,湖面水域面积计算也存在一定误差,这些对估算碳储量可能产生一些偏差。
(4) 利用同位素示踪技术,本研究对碳的来源进行了初步识别,但仅仅是半定量或定性地说明湖泊水体中碳的主要来源,还不能满足精确地区分碳的来源,在计算地质碳汇时需要扣除与地质作用或风化作用无关的碳来源的贡献。
[1] 蔡述明,王学雷,陈世俭.湖北省湿地自然保护区科学考察报告[R].武汉:中国科学院测量与地球物理研究所,2005.
[2] 闫伟伟.基于 GIS 的洪湖湿地水生植物分布结构的研究[D].武汉:华中师范大学,2013.
[3] Gibbs R J.Mechanisms Controlling Word Water Chemistry [J].Science,1970,170:1088-1090.
[4] Chen J S,Wang F Y,Xia X H,et al.Major element chemistry of the Changjiang(Yangtze River)[J].Chemical Geology,2002,187:231-255.
[5] 夏学齐,杨忠芳,王亚平,等.长江水系河水主要离子化学特征[J].地学前缘,2008,15(5):194-202.
[6] Xu H,Hou Z H,AN Z S,et al.Major ion chemistry of waters in Lake Qinghai catchments,NE Qinghai-Tibet plateau,China[J].Quaternary International,2010,212(1):35-43.
[7] 夏星辉.60—90年代长江水系河水水质(主要离子)变化研究[D].北京:北京大学,1998:1-10.
[8] 刘从强,蒋颖魁,陶发祥,等.西南喀斯特流域碳酸盐岩的硫酸侵蚀与碳循环[J].地球化学,2008,7(4):404-414.
[9] 陈静生,关文荣,夏星辉,等.长江中上游水质变化趋势与环境酸化关系初探[J].环境科学学报,1998,18(3):265-270.
[10] 陈静生,关文荣,夏星辉,等.长江干流近三十年来水质变化探析[J].环境化学,1998,17(1):8-13.
[11] 陈静生,王飞越,夏星辉.长江水质地球化学[J].地学前缘,2006,13(1):74-85.
[12] 杜耘,陈萍,Kieko SATO,等.洪湖水环境现状及主导因子分析[J].长江流域资源与环境,2005,14(4):481-485.
[13] 姜刘志,王学雷,厉恩华.生态恢复前后的洪湖水质变化特征及驱动因素[J].湿地科学,2012,10(2):188-193.
[14] 马燕,郑祥民.洪湖水体氮、磷营养元素变化规律及富营养化进程研究[J].广州环境科学,2005,20(2):5-7.
[15] Chetelat B,Liu C Q,Zhao Z Q,et al.Geochemistry of the dissolved load of the Changjiang Basin rivers: Anthropogenicimpacts and chemical weathering [J].Geochimica et Cosmochimica Acta,2008,72:4254-4277.
[16] 林清,王绍令.沉水植物稳定碳同位素组成及影响因素分析[J].生态学报,2001,21(5):806-809.
[17] 李干蓉,刘丛强,陈椽,等.猫跳河流域梯级水库夏—秋季节溶解无机碳(DIC)含量及其同位素组成的分布特征[J].环境科学,2009,30(10):2891-2897.
[18] 刘文,蒲俊兵,于奭,等.广西五里峡水库夏季溶解无机碳行为的初步研究[J].环境科学,2014,35(8):2959-2966.
[19] 莫雪,蒲俊兵,袁道先,等.亚热带典型岩溶区地表溪流溶解无机碳昼夜变化特征及其影响因素[J].第四纪研究,2014,34(4):873-880.
[20] Myrbo A,Shapley M D.Seasonal water-column dynamics of dissolved inorganic carbon stable isotopic compositions(delta13CDIC)in small hardwater lakes in Minnesota and Montana [J].Geochimica et Cosmochimica Acta,2006,70(11):2699-2714.
[21] McNichol A P,Aluwihare L I.The power of radiocarbon in biogeochemical studies of the marine carbon cycle:Insights from studies of dissolved and particulate organic carbon(DOC and POC)[J].Chemical reviews,2007,107(2):443-466.
[22] Raymond P A,Bauer J E.Use of14C and13C natural abundances for evaluating riverine,estuarine,and coastal DOC and POC sources and cycling: a review and synthesis[J].Organic Geochemistry,2001,32(4):469-485.
[23] 徐丹,陈敬安,杨海全,等.贵州百花湖分层期水体有机碳及其稳定碳同位素组成分布特征与控制因素[J].地球与环境,2014,42(5):597-603.
[24] Zigah P K,Minor E C,Werne J P.Radiocarbon and stable-isotope geochemistry of organic and inorganic carbon in Lake Superior[J].Global Biogeochemical Cycles,2012,26(1).
[25] 黎文,吴丰昌,傅平青,等.贵州红枫湖水体溶解有机质的剖面特征和季节变化[J].环境科学,2006,27(10):1979-1985.
[26] 陈敬安,万国江,汪福顺,等.湖泊现代沉积物碳环境记录研究[J].中国科学:D辑 地球科学,2002,32(1):73-80.
[27] Dean,W.E.The carbon cycle and biogeochemical dynamics in lake sediments[J].Journal of Paleolimnology,1999,21(4):375-393.
[28] Ishiwatari,R.,Uzaki,M.Diagenetic changes of lignin compounds in a more than 0.6million-year-old lacustrine sediment(Lake Biwa,Japan)[J].Geochim Cosmochim Acta,1987,51:321-328.
[29] Hedges,J.I.,Clark,W.A.,Quay,RD.et al.Compositions and fluxes of particulate organicmaterial in the Amazon River[J].Limnology and Oceanography,1986,31:717-738.
[30] 朱松泉,窦宏身.洪泽湖[M].合肥:中国科学技术大学出版社,1993.
[31] 陈芳,夏卓英,宋春雷,等.湖北省若干浅水湖泊沉积物有机质与富营养化的关系[J].水生生物学报,2007,31(4):467-471.
[32] 范成新.湖沉积物理化特征及磷释放模拟[J].湖泊科学,1995,7(4):341-350.
[33] 班璇,余成,魏珂,等.围网养殖对洪湖水质的影响研究[J].环境科学与技术,2010,33(9):125-129.
[34] 付硕章.洪湖湿地植物储碳、固碳能力及营养元素积累研究[D].武汉:湖北大学,2012.
[35] 姚书春,薛滨,李世杰,等.江中下游湖泊沉积速率的测定及环境意义——以洪湖、巢湖、太湖为例[J].长江流域资源与环境,2006,15(15):569-573.
[36] 姚书春,李世杰,刘吉峰,等.太湖THS孔现代沉积物137Cs、210Pb的分布及计年研究[J].海洋地质与第四纪地质,2006,26(2):79-83.
[37] 刘彦,张金流,何媛媛,等.单生卵囊藻对DIC的利用及其对CaCO3沉积影响的研究[J].地球化学,2010,39(2):191-196.
[38] 袁道先.碳循环与全球岩溶[J].第四纪研究,1993(1):1-6.
[39] 袁道先.地球系统的碳循环和资源环境效应[J].第四纪研究,2001,21(3):223-232.
[40] Berner R A,Lasaga A C,Garrels R M.The carbonate-silicate geochemical cycle and its effect on atmospheric carbon dioxide over the past 100 million years[J].Am.J.Sci,1983,283(7):641-683.

[42] 黄亮,吴莹,张经,等.长江中游若干湖泊水生植物体内C、N、P及δ13C分布[J].地球学报,2003,24(6):515-518.
[43] 吴沿友,邢德科,刘莹.植物利用碳酸氢根离子的特征分析[J].地球与环境,2011,39(2):273-277.
[44] 章程,谢运球,宁良丹,等.桂林会仙岩溶湿地典型水生植物δ13C特征与固碳量估算[J].中国岩溶,2013,32(3):247-252.
[45] 张强.岩溶地质碳汇的稳定性——以贵州草海地质碳汇为例[J].地球学报,2012,33(6):947-952.
[46] 刘波,袁琴,左丽敏,等.江汉平原湿地生态环境地质调查报告[R].荆州:湖北省地质局水文地质工程地质大队,2016.
(责任编辑:于继红)
Preliminary Study on Geological Carbon Sink Effect in Honghu Wetland
LIU Bo1, HE Shiyi2
(1.HubeiInstituteofHydrogeologyandEngineeringGeology,Jingzhou,Hubei434000; 2.InstituteofKarstGeology,ChineseAcademyofGeologicalSciences,Guilin,Jiangxi541004)
Wetland is a huge organic carbon pool on the land,with the function of regulating climate,in the background of global warming and increasing CO2concentration,the study of wetland geological carbon sink will help us to better cope with global climate change.The study on Honghu wetland as the research object,using the field test,indoor sample analysis and isotope method,the authors obtain the main indicators of carbon inensity and change,analyse hydrochemical characteristics in the water of Honghu wetland,characteristics of isotopic composition and dissolved organic carbon,characteristics of organic carbon of water and sediment preliminarily identify carbon sources of lake carbon pool.Dissolved inorganic carbon base in Honghu is up to 17 792 tC.The average concentration of dissolved organic carbon in Honghu is 6 mg/L,the average concentration of total organic carbon is 8.25 mg/L.Estimation of dissolved organic carbon and total organic carbon pools in Honghu Lakeare 40 80 tC and 5 610 tC,respectively.Total carbon accumulation of aquatic plants is 32 656 tC/a.The amount of organic carbon in the surface sediments is 69 350 tC/a,inorganic carbon is 78 280 tC/a,and the total amount is 147 630 tC/a.Carbon accumulation in the annual geological carbon sequestration in Honghu can reach 14 534 tC/a.
wetland; geological carbon sink; Honghu; organic carbon; inorganic carbon
2016-08-29;改回日期:2016-10-09
刘波(1979-),男,高级工程师,水文地质与工程地质专业,从事水工环地质调查与研究工作。E-mail:liubo790612@163.com
P941.78
A
1671-1211(2016)06-0862-10
10.16536/j.cnki.issn.1671-1211.2016.06.013
数字出版网址:http://www.cnki.net/kcms/detail/42.1736.X.20161026.0907.006.html 数字出版日期:2016-10-26 09:07

