HPLC法测定复方石斛颗粒中黄酮类化学成分的含量
徐小婷,徐应淑,杨 俊
(遵义医学院 药剂学教研室,贵州 遵义 563099)
技术与方法
HPLC法测定复方石斛颗粒中黄酮类化学成分的含量
徐小婷,徐应淑,杨俊
(遵义医学院 药剂学教研室,贵州 遵义563099)
[摘要]目的 建立高效液相色谱法测定复方石斛颗粒中槲皮素、山奈素和异鼠李素含量的方法。方法 高效液相色谱法测定黄酮类化学成分槲皮素、山奈素和异鼠李素含量,色谱柱为Agilent ZORBAX Extend-C18(150 mm×4.6 mm,5 μm),流动相为甲醇-0.4%磷酸水溶液,采用梯度洗脱,流速1.0 mL/min,检测波长360 nm,柱温为40 ℃;进样量为10 μL。结果 槲皮素、山奈素和异鼠李素的进样量分别在5~80、5~80、1.875~30 μg/mL,该范围内与各自峰面积呈良好的线性关系,线性回归方程分别为y=41.592x+34.684(R2=0.999 9)、y=40.24x+36.804(R2=0.999 9)和y=84.668x-44.102(R2=0.999 8);平均回收率分别为99.69%、100.26%和99.63%,RSD分别为1.59%、1.74%和2.08%(n=6)。结论 该方法分离良好、精密准确,可用于复方石斛颗粒的质量控制。
[关键词]复方石斛颗粒;槲皮素;山奈素;异鼠李素;HPLC
复方石斛颗粒是由银杏叶、山楂和金钗石斛等组成的复方制剂,研究表明其具有效调节大鼠血脂代谢水平,且能提高机体的抗氧化能力和改善肝组织脂肪变性,有补肝益肾、活血化瘀、化浊降脂的功效,适用于高脂血症、高粘血症和脂肪肝等病症[1],对血脂代谢紊乱具有辅助治疗作用。由于中药制剂的药材来源和提取方式不同等诸多方面的影响,都会对其效应和产品质量产生一定的影响[2],因而为复方石斛颗粒建立质量控制方法及将来的工业化大生产具有现实意义。已有文献[3-7]采用高效液相色谱法测定槲皮素、山奈素和异鼠李素的含量,但从环境保护、检测效率提高的角度考虑,尚有必要进一步优化色谱条件。本文建立了HPLC法检测复方制剂中黄酮类化学成分槲皮素、山奈素和异鼠李素含量的方法,为复方石斛颗粒的质量控制提供安全、可靠的试验依据。
1材料与方法
1.1仪器与试剂Agilent1260高效液相色谱仪(安捷伦科技有限公司);电子天平(梅特勒-托利多仪器上海有限公司);HH-S6型恒温水浴箱(郑州长城科工有限公司);SZ-93自动双重纯水蒸馏器(上海亚荣生化仪器厂);DL-820D型智能超声波清洗器(上海之信仪器有限公司)。 复方石斛颗粒(遵义医学院药学院自制,编号:20150717、20150718、20150719);槲皮素对照品(150302,纯度:99.73%)、山奈素对照品(140608,纯度:99.24%)、异鼠李素对照品(141119,纯度:98.57%)均购自成都普菲德生物技术有限公司;甲醇、乙腈(色谱纯)购自美国TEDIA天地试剂有限公司;水为双蒸水;其余试剂为分析纯。
1.2色谱条件与溶液配制
1.2.1色谱柱Agilent ZORBAX Extend-C18(150 mm×4.6 mm,5 μm);流动相A为甲醇,B为0.4%磷酸溶液;梯度洗脱,洗脱条件为0~12 min,20%~40% A;12~20 min,40%~43% A;20~27 min,43%~47% A;27~30 min,47%~65% A;流速1.0 mL/min,柱温40 ℃,进样量10 μL,检测波长360 nm。
1.2.2对照品溶液配制取经五氧化二磷减压干燥24 h的槲皮素、山奈素和异鼠李素对照品制成含槲皮素80 μg/mL、山奈素80 μg/mL、异鼠李素30 μg/mL对照品混合溶液。
1.2.3样品溶液制备精密称取复方颗粒粉末5.0 g,置索氏提取装置中,加石油醚(60~90 ℃)100 mL加热回流提取至提取液无色(约3 h),取出药渣挥干,置具塞锥形瓶中;向瓶中加入甲醇100 mL,称重,超声处理(功率250 W,频率45 kHz ) 40 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过;精密量取续滤液24 mL,并加25%盐酸溶液8 mL,称重,摇匀,置85 ℃水浴中加热回流90 min,迅速冷却至室温,再称定重量,用溶液(甲醇∶25%盐酸=3∶1)补足减失的重量,用微孔滤膜(0.45 μm)滤过,取续滤液,作为样品溶液。
1.2.4空白溶液另取按处方工艺配置的空白辅料适量,按同法配成空白溶液。
2结果
2.1方法学考察
2.1.1专属性考察取空白溶液、对照品溶液和样品溶液,按己建立的色谱条件,取10 μL进行HPLC分析,分别得色谱图(见图1)。槲皮素、山奈素和异鼠李素的保留时间分别为19.10、26.29和28.51 min。结果显示,槲皮素、山奈素、异鼠李素的峰位置无杂质峰出现,辅料不干扰检测样本的测定,峰型良好。结果表明,本方法具有较高的专属性。
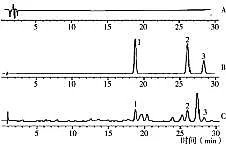
A:空白溶液;B:对照品溶液;C:样品溶液。1:槲皮素;2:山奈素;3:异鼠李素。图1 3种溶液的高效液相色谱图
2.1.2线性关系考察精密量取槲皮素(80 μg/mL)、山奈素(80 μg /mL)、异鼠李素(30 μg /mL)对照品混合溶液0.625、1.25、2.5、5.0、7.5 mL分别置于10 mL容量瓶中,用甲醇定容至刻度,摇匀,进样。按上述色谱条件测定,记录峰面积,以各对照品浓度(x)为横坐标坐标,峰面积(y)为纵坐标,得到槲皮素回归方程为y=41.592x+34.684,R2=0.999 9;山奈素回归方程为y=40.24x+36.804,R2=0.999 9;异鼠李素回归方程为y=84.668x-44.102,R2=0.999 8,分别在5~80、5~80、1.875~30 μg/mL范围内,峰面积与浓度之间呈良好的线性关系。
2.1.3精密度试验精密量取“1.2.2”项下槲皮素(40 μg /mL)、山奈素(40 μg /mL)、异鼠李素(15 μg /mL)的混合溶液10 μL,按“1.2.1”项下色谱条件连续进样6次,记录峰面积。测得槲皮素、山奈素和异鼠李素峰面积的RSD分别为0.41%、0.62%、0.45%,表明该仪器精密度较好。
2.1.4稳定性试验取样品溶液分别在配制0、2、4、6、12、24 h时进样,记录峰面积,测得槲皮素、山奈素和异鼠李素峰面积的RSD分别为0.41%、0.62%、0.45%,表明样品溶液在24 h内稳定。
2.1.5重复性试验取同一批号(编号:20150717)样品,平行测定6份。测得槲皮素、山奈素和异鼠李素的峰面积RSD分别为1.82%、2.39%、2.97%(n=6),表明该方法重现性较好。
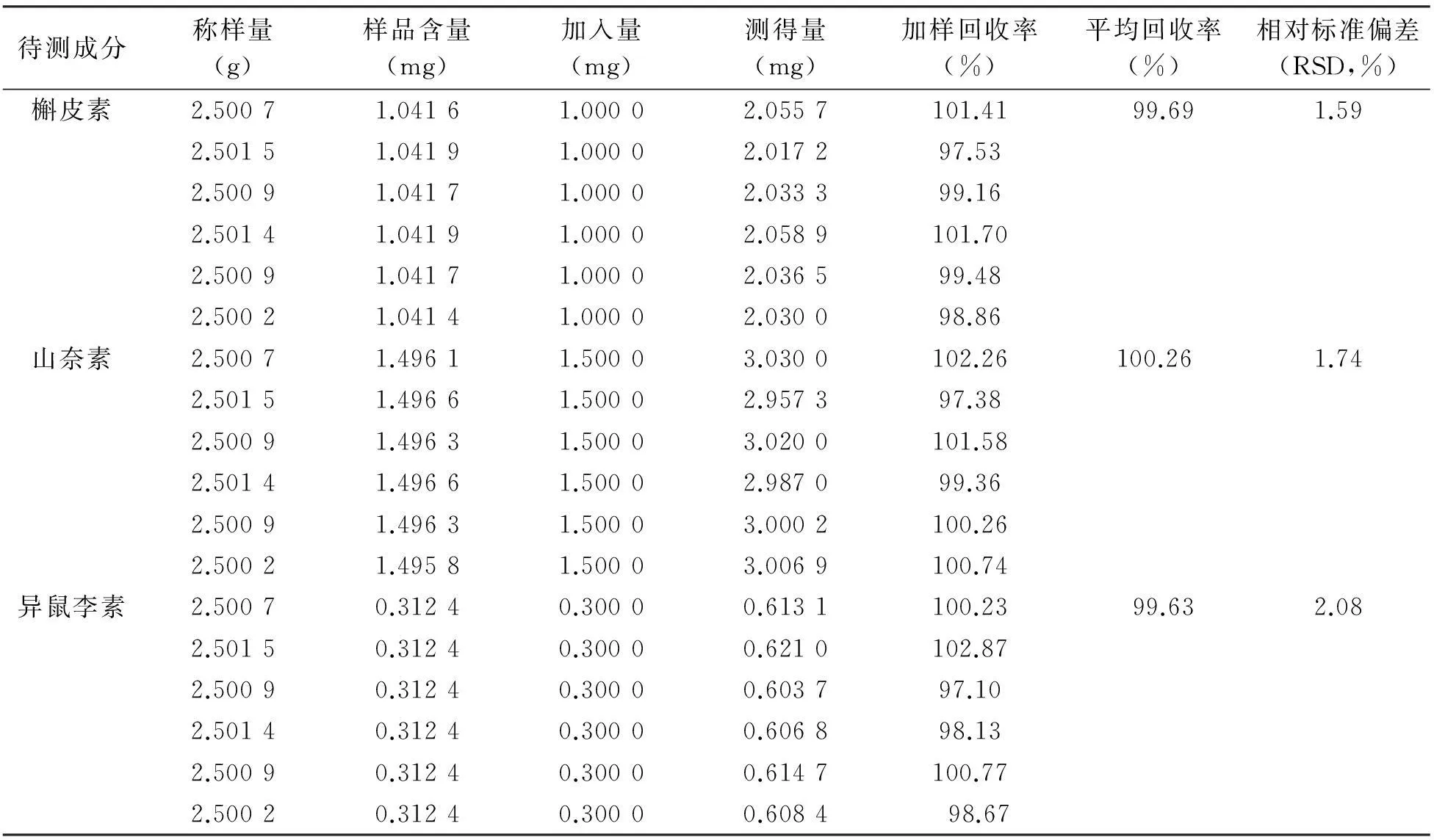
2.1.6回收率试验精密称取已测知含量的样品6份,每份约2.5 g,分别精密加入一定量的槲皮素、山奈素、异鼠李素对照品溶液,按“1.2.3”项下方法制备供试品溶液,再按“1.2.1”项下色谱条件进样测定,记录峰面积,并计算得加样回收率及其RSD值(见表1)。
表1复方石斛颗粒加样回收率试验结果
待测成分称样量(g)样品含量(mg)加入量(mg)测得量(mg)加样回收率(%)平均回收率(%)相对标准偏差(RSD,%)槲皮素2.50071.04161.00002.0557101.4199.691.592.50151.04191.00002.017297.532.50091.04171.00002.033399.162.50141.04191.00002.0589101.702.50091.04171.00002.036599.482.50021.04141.00002.030098.86山奈素2.50071.49611.50003.0300102.26100.261.742.50151.49661.50002.957397.382.50091.49631.50003.0200101.582.50141.49661.50002.987099.362.50091.49631.50003.0002100.262.50021.49581.50003.0069100.74异鼠李素2.50070.31240.30000.6131100.2399.632.082.50150.31240.30000.6210102.872.50090.31240.30000.603797.102.50140.31240.30000.606898.132.50090.31240.30000.6147100.772.50020.31240.30000.608498.67
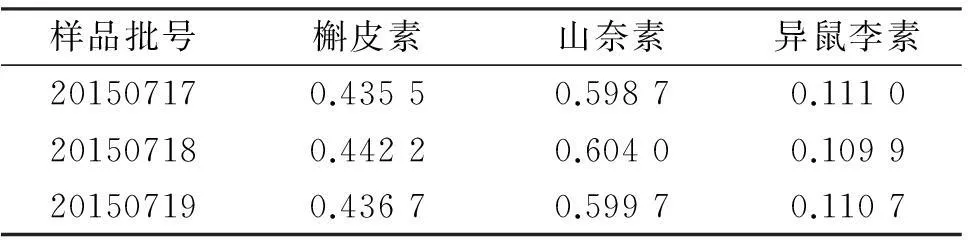
2.2样品含量测定取3个批号的复方石斛颗粒,研细,分别精密称定5 g,按样品制备方法制备,按“1.2.1”项下色谱条件测定,记录峰面积,计算得样品含量(见表2)。
表2复方石斛颗粒样品中槲皮素、山奈素和异鼠李素含量测定结果(mg/g)
样品批号槲皮素山奈素异鼠李素201507170.43550.59870.1110201507180.44220.60400.1099201507190.43670.59970.1107
3讨论
本文在脱脂方法与溶剂的选择中,参照2015版《中国药典》[8]中银杏叶测定槲皮素、山奈素和异鼠李素的测定方法,即索氏提取器回流提取法。此方法虽较张玲等[9]测定补血草中槲皮素、山奈素和异鼠李素所用超声法提取所用时间长,但超声提取后的溶剂将直接挥发掉,造成溶剂的浪费和环境的污染。但是药典索氏提取器回流提取法中,采用的三氯甲烷毒性大,故本文选用比三氯甲烷毒性小的石油醚(60~90 ℃),作为复方石斛颗粒的脱脂溶剂。
在植物体内的黄酮类化合物常与糖结合成苷类或碳糖基的形式存在,因而为了准确测定其苷元的含量,需对其进行水解去糖。参阅文献酸水解法[10-12],糖水解的关键因素有温度、盐酸含量、水解时间等。温度过高将降低黄酮类物质的含量,因此我们选取的温度为85 ℃。对于盐酸用量和水解时间我们进行了一系列实验研究进行比较,选取体积比为5∶1、4∶1、3∶1、2∶1的甲醇∶25%盐酸进行比较的实验结果显示,相同时间下当甲醇与25%盐酸体积比为3∶1时,槲皮素、山奈素和异鼠李素的峰面积和已到达最大;以水解时间为30、60、90、120、150 min,甲醇与25%盐酸体积比为3∶1,测定各条件下各成分峰面积之和的结果显示,在水解时间90 min时峰面积之和达到最大,随着时间的延长峰面积之和反而减少,故水解时间90 min最为适宜。
本文采用高效液相色谱法建立复方石斛颗粒中槲皮素、山奈素和异鼠李素的测定方法,结果表明该方法安全、可靠、可重复性强,为复方石斛颗粒的质量控制提供试验依据。该方法也可为其它中药复方制剂中槲皮素、山奈素和异鼠李素的检测提供参考。
[参考文献]
[1]徐小婷, 徐应淑, 高健美, 等. 复方石斛对高脂血症大鼠脂质代谢和肝脏的影响[J]. 中国药业, 2015, 24(21): 30-32.
[2] 兰雪, 唐富山, 陈曾妮, 等. HPLC法测定小柴胡汤剂中黄芩苷的含量[J]. 遵义医学院学报, 2015, 38(4): 435-438.
[3] 牟洋, 李顺兴, 陈丽惠, 等. 高效液相色谱法同时检测4种金线莲黄酮苷元及其在提取工艺评价中的应用[J]. 分析科学学报, 2013, 29(4): 465-468.
[4] 南海军, 陈阿丽, 王峰, 等. HPLC法测定银荞胶囊中4种黄酮类成分的含量[J]. 中国药房,2015, 26(18): 2573-2575.
[5] 徐飞, 陆兔林, 谢辉, 等. HPLC测定复方银杏颗粒中槲皮素、山奈素、异鼠李素及总黄酮醇苷含量[J]. 中成药, 2007, 29(11): 1617-1619.
[6] 李爱红, 陈伟健, 胡文军. 一测多评法测定银杏叶胶囊中总黄酮醇苷的含量[J]. 中国药房, 2012, 23(36):3446-3448.
[7] 梅赞, 杨杰, 范慧佳, 等. 4种柴胡地上部分黄酮类成分的含量测定[J]. 中国新药杂志, 2011, 20(10): 932-935.
[8] 国家药典委员会. 中华人民共和国药典[S]. 北京: 中国医药科技出版社, 2015: 316.
[9] 张玲, 李岩, 田文睿, 等. 河北环渤海地区补血草不同部位黄酮类化合物的研究[J]. 中国食品学报, 2014, 14(4): 57-63.
[10] 何丽梅, 郑德勇, 叶乃兴, 等. 白茶黄酮醇类物质的HPLC测定及水解工艺优化[J]. 福建农林大学学报:自然科学版, 2014, 43(6): 579-584.
[11] 李明娟, 刘磊, 傅春燕, 等. 高效液相色谱法分析车前草中的黄酮化合物[J]. 光谱实验室, 2013, 30(3): 1437-1443.
[12] 杜安全, 王先荣, 周正华, 等. 银杏叶总黄酮苷的HPLC法分析水解条件[J]. 安徽医药, 2001, 5(3): 164-165.
[收稿2016-01-13;修回2016-03-15]
(编辑:王福军)
Simultaneous determination of the flavonoids in Compound Dendrobium particles by HPLC
XuXiaoting,XuYingshu,YangJun
(Department of Pharmacy, Zunyi Medical University, Zunyi Guizhou 563099, China)
[Abstract]Objective To establish the HPLC method determination of quercetin, kaempferol and isorhamneyin in Compound Dendrobium particles. Methods HPLC method was adopted. The Agilent ZORBAX Extend - C18column (150 mm × 4.6 mm, 5 microns) was used with the mobile phase of methanol-0.4% phosphoric acid solution in the gradient elution at 1.0 ml/min. The detection wavelength was 360 nm. The column temperature was 40 ℃ and the volume was 10 μl. Results There was a between the amount of quercetin and peak area in the range of 5~80 μg/ml, kaempferol in the range of 5~80 μg/ml and isorhamneyin in the range of 1.875~30 μg/ml. The liner regression qequations were y=41.592x+34.684 (R2=0.999 9), y=40.24x+36.804 (R2=0.999 9) and y=84.668x-44.102 (R2=0.999 8), respectively. The average recoveries were 99.69% (RSD=1.59%), 100.26% (RSD=1.74%) and 99.63% (RSD=2.08%) with 6 sample in each group. Conclusion This method is well separated, precise and accurate, and could be used for the quality control of Compound Dendrobium particles.
[Key words]Compound Dendrobium particles; quercetin; kaempferol; isorhamneyin; HPLC
[中图法分类号]R284.1
[文献标志码]A
[文章编号]1000-2715(2016)02-0200-04
[通信作者]徐应淑,女,硕士,教授,研究方向:新药研究与开发,E-mail:527822816@qq.com。
[基金项目]贵州省中医药管理局资助项目(NO:QZYY2012-52);贵州省赤水市科技局资助项目(NO:赤中药科合[2013])。

