HPLC法测定60℃烘烤前后滇重楼药材四种皂苷的含量变化
杜春华 徐怡 李东娴 曹红云 秦波 游燕

摘要:目的分析测定经过60℃烘烤前后滇重楼中重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ的含量变化。方法采用HPLC法,色谱柱为WatersSunFire-C18(4.6 mm×150 mm,5μm),流动相为乙腈-水为流动相,梯度洗脱;进样量10 μL,柱温30℃,检测波长203 nm。结果8个不同产地的滇重楼药材,经过60℃烘烤前后滇重楼中重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ的总量变化有差异,其中四种皂苷总量及重楼皂苷Ⅰ含量明显降低。结论经过60℃烘烤后对滇重楼的品质有影响。
关键词:滇重楼;重楼皂苷;含量变化;高效液相色谱法
中图分类号:R284.1文献标志码:A文章编号:1007-2349(2016)05-0049-03
重楼首载于《滇南本草》,为重楼属植物,学名为[Paris polyphylla var.yunnanensis(Franch.)Hand.-Mazz.],现称滇重楼。在云南的别名为土三七、七叶一枝花、重楼、大重楼、重台、两把伞、独角莲(滇南本草),根茎入药,有消肿解毒,止血止痛,利小便之功能[1-2]。滇重楼是中成药,如云南白药、季德胜蛇药片、宫血宁胶囊、楼莲胶囊、热毒清胶囊等的主要原料之一[3]-4]。甾体皂苷是重楼的主要活性成分,并含有氨基酸、甾酮、蜕皮激素、黄酮苷等化合物,具有止血、抗菌、抗肿瘤、免疫调节、镇痛和镇静等作用。甾体皂苷:按苷元的不同主要有两类,一类为薯蓣皂苷元(diosgenin)的糖苷,另一类为偏诺皂苷元(pennogenin)的糖苷,重楼皂苷中属于薯蓣皂苷元的有重楼皂苷I、重楼皂苷Ⅱ、重楼皂苷Ⅵ,属于偏诺皂苷元的有重楼皂苷Ⅶ[3,5]。现采用HPLC测定经过60℃烘烤不同产地的滇重楼药材中重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ的含量变化,为评价其内在质量、临床药理研究及产地加工提供理论参考。
1实验部分
1.1仪器和试药
1.1.1仪器Waters e2695高效液相色谱仪系统(美国Waters)、AG285型电子天平(瑞士Mettler-Toledo 公司)、DHG-9031A型电热恒温干燥箱(上海精宏实验设备有限公司)。
1.1.2试剂重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ对照品(中国药品生物制品检定所,批号分别为:111590-200402,111591-201103,111592-201203,111593-200402);乙腈为色谱纯(德国默克公司),甲醇为分析纯,水为超纯水。
1.1.3药材采集8个不同产地滇重楼药材,均为栽培品种,产地分别为:大理九顶山、新平县嘎洒镇、云龙县白石镇、云龙县关坪乡、耿马县大兴乡、蒙自冷泉镇、马关县南捞乡、禄劝县撒营盘乡(见表1),经云南省药物所究所天然药物资源研究中心高级工程师戚育芳鉴定为为百合科植物云南重楼[P.polyphylla var.yunnanensis(Fr.)Hand.-Mazz.]的干燥根茎。
1.2方法与结果
1.2.1色谱条件及系统适用性色谱柱为(WatersSunFire-C18,4.6 mm×150 mm,5 μm);流动相:乙腈(A)-水(B),梯度洗脱(流动相A 0→40 min,30%→70%;40→50 min,60%→40%),流速:1.0 min·mL-1,进样量:10 μL,柱温30℃,检测波长203 nm。在此色谱条件下,理论板数按重楼皂苷Ⅰ峰计算不低于4000。
1.2.2标准品溶液的制备取重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ对照品适量,精密称定,加甲醇分别制成浓度为0.4110、0.3950、0.4300、0.4380 mg/mL的溶液,即得对照品混合溶液。
1.2.3样品的制备将清洗前后各8个不同产地的滇重楼药材,每一批号的样品先用铁锤敲小平均分为2份,一份直接用万能粉碎机打粉,过3号筛;另一份用自来水清洗3遍,装于铁丝网筛中滤干水分后放入电热恒温干燥箱中,60℃恒温干燥24 h,放冷后用万能粉碎机打粉,过三号筛备用,同时测定水分含量。取约0.5 g 重楼药材粉末(过三号筛),精密称定,置具塞锥形瓶中,精密加入乙醇25 mL,称定重量,加热回流30 min,放冷,再称定重量,用乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
1.2.4线性关系考察精密吸取对照品混合溶液2、5、10、15、20、25、30 μL分别进样,记录色谱图,测定峰面积。以进样量为横坐标,峰面积为纵坐标,进行线性回归。重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ的回归方程分别为:YⅠ=145362XⅠ+20908(r=0.9995);YⅡ=280662XⅡ-15056(r=0.9993);YⅥ=370123XⅥ+10054(r=0.9996);YⅦ=254145XⅦ+13908(r=0.9995)。线性范围分别为2.1222~12.1000、2.1014~13.7500、1.6455~14.5000、1.8805~12.6600 μg。
1.2.5仪器精密度试验精密吸取对照品混合溶液10μl,按“1.2.1”项下条件连续进样5次,各成分峰面积的RSD分别为0.98%、1.17%、1.02%、0.88%。表明该方法仪器精密度良好。
1.2.6重复性试验取同一产地的样品5 份,按“1.2.3”项方法制备供试品溶液,按“1.2.1”项条件,分别进样10 μL,测定重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ的含量。其含量的RSD分别为1.78、2.00、1.65、2.12%。表明方法重复性良好。
1.2.7稳定性试验取同一供试品溶液,分别于0、2、4、8、12、24 h进样10 μL,测定峰面积,计算各成分峰面积的RSD分别为1.98、2.36、2.07、2.14%。表明供试品溶液在24 h内稳定。
1.2.8回收率试验取已知含量的同一供试品6份,每份0.5 g,精密称定,分别添加对照品贮备液1 mL(重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ分别为0.1058 mg.m l-1、0.0625 mg.m l-1、0.0682 mg.m l-1、0.0578 mg.m l-1),按“1.2.3”项方法制备供试品溶液。按“1.2.1”项条件,分别精密进样10μl,测得重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ的平均回收率分别为97.55、96.06、98.08、98.20%;RSD分别为2.88、2.65、2.58、2.76%。表明该方法的准确度良好。
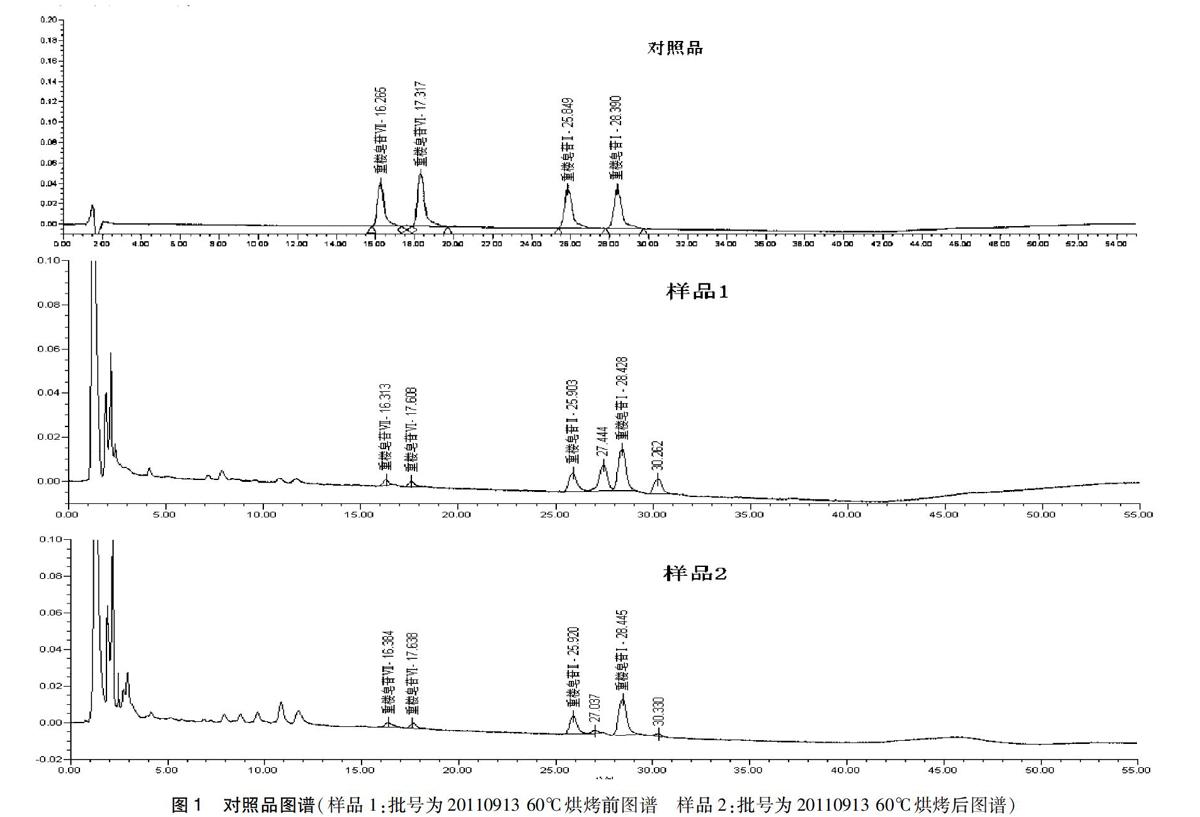
1.2.9样品的测定精密称取8个不同产地滇重楼药材粉末各2份,每份约0.5 g。按1.2.3项下方法制备供试品溶液,按1.2.1项条件进样,测得各色谱峰的峰面积。按外标一点法计算重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ的含量(见表1)。对照品及样品图谱(见图1)。结果表明,8个不同产地的滇重楼药材,经过60℃烘烤前后滇重楼中重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ的总量变化有差异,其中四种皂苷总量及重楼皂苷Ⅰ含量明显降低。重楼皂苷Ⅱ、重楼皂苷Ⅵ、重楼皂苷Ⅶ的变化无明显规律。
2讨论
滇重楼化学成分复杂,对滇重楼有效成分的药理研究表明其药理活性强,如:重楼皂苷Ⅰ、Ⅱ具有细胞毒活性、重楼皂苷Ⅰ~Ⅲ具有免疫调节活性,偏诺皂苷的止血活性强于薯蓣皂苷[6]。《中国药典》2015年版一部规定按干燥品计算,重楼皂苷Ⅰ(C44H70O16),重楼皂苷Ⅱ(C51H82O20),重楼皂苷Ⅵ(C39H62O13)和重楼皂苷(C51H82O21)的总量作为重楼含量测定的指标成分,且不得少于0.60%[7]。
实验结果表明,8个不同产地样品清洗后经过60℃烘烤后重楼皂苷Ⅰ、Ⅱ、Ⅵ、Ⅶ总量及重楼皂苷Ⅰ的含量有明显的降低,有效成分的药理活性是否也会相应的降低,还有待进一步的药理研究。在滇重楼干燥过程中,伴随着滇重楼内水分的散失,其生理活性和物理形态也发生着显著的变化,不同干燥方法对滇重楼的品质影响较大[8]。《中国药典》2015年版一部规定药材产地加工及炮制的干燥方法中低温干燥(一般不超过60℃)。滇重楼经过60℃烘烤24 h后,确实对其品质有影响。
近年来,随着国家对天然药物生产制剂和原料进行控制和管理,从天然药物的源头抓起,以保证药材质量的稳定,那么对滇重楼选取适宜的干燥方法和干燥温度还有待进一步摸索研究,从而保证其作为中成药的原料药的品质奠定基础,也为滇重楼产地采收加工提供理论依据。
参考文献:
[1]李恒.重搂属植物[M].北京:科学出版社,1998:35-36.
[2]中国科学院昆明植物研究所.云南植物志[M].第8卷.北京:科学出版社,1997.
[3]武珊珊,高文远,段宏泉等.重楼化学成分和药理作用研究进展[J].中草药,2004,35(3):344-347.
[4]邹亮,周浓,张海珠,等.HPLC测定不同产地滇重楼中的4种重楼皂苷[J].华西药学杂志,2009,24(5):521-523.
[5]王 羽,高文远,袁理春,等.滇重楼的化学成分研究[J].中草药,2007,38(1):17-20.
[6]黄贤校,高文远,满淑丽,等.重楼属药用植物皂苷类化学成分及其生源途径的研究进展[J].中草药,2009,40(3):483-489.
[7]国家药典委员会.中国药典[S].北京:中国医药科技出版社,2015:260.
[8]周浓,张华琦,丁博,等.不同干燥方法对滇重楼中薯蓣皂苷元含量的影响[J].时珍国医国药,2015,26(2):361-362.

