武汉市耐多药肺结核患者防治模式效果分析
周美兰 杜义祥 王坚杰 吴刚 陈梓 陈聪 王卫华
·论著·
武汉市耐多药肺结核患者防治模式效果分析
周美兰 杜义祥 王坚杰 吴刚 陈梓 陈聪 王卫华
目的 分析2006—2014年武汉市实施耐多药结核病(MDR-TB)患者防治模式的效果,为全球基金项目结束后制定我国MDR-TB防控措施提供参考和依据。 方法 2006年10月武汉市启动全球基金耐多药肺结核防治项目,实施的主要内容为MDR-TB疑似患者筛查、诊断;MDR-TB患者治疗、随访复查和全程管理。本研究收集2006年10月1日至2014年6月30日武汉市结核病防治所登记的中国全球基金耐多药肺结核项目基础资料、报表数据、病案信息,进行分析和总结。对登记管理的5524例涂阳肺结核患者进行痰培养,经菌种鉴定,结核分枝杆菌感染4870例;经过药物敏感性试验(简称“药敏试验”)检出MDR-TB患者593例。经专家组讨论,对359例MDR-TB患者以标准化与个体化方案相结合的方式进行治疗。分析MDR-TB患者治疗转归、药物不良反应情况;对初治涂阳和复治涂阳患者MDR-TB检出率的差异进行χ2检验,以P<0.05为差异有统计学意义。 结果 武汉市MDR-TB患者防治模式的实施过程中,MDR-TB检出率为12.2%(593/4870),其中初治涂阳和复治涂阳患者MDR-TB检出率分别为6.9%(188/2715)和18.8%(405/2155),复治涂阳患者MDR-TB检出率高于初治涂阳患者(χ2=158.26,P<0.05)。359例(60.5%)MDR-TB患者接受治疗,治愈率为73.3%(263/359),初治涂阳和复治涂阳患者治愈率分别为76.6%(95/124)和71.5%(168/235),复治涂阳患者中的复治失败者的治愈率最低(57.9%,22/38)。359例MDR-TB患者药物不良反应发生率为87.7%(315/359),耳鸣或听力下降、胃肠道反应和关节肿痛发生率分别为50.8%(160/315)、46.0%(145/315)和43.2%(136/315);环丝氨酸导致抑郁症状发生率为5.3%(6/113);因重度不良反应中断治疗率为3.6%(13/359)。 结论 武汉市实施的MDR-TB综合防治模式取得了一定的效果,患者治愈率维持在较高水平,对于制定我国MDR-TB防控措施具有一定的参考价值。
结核,抗多种药物性; 医师诊疗模式; 治疗结果; 武汉市
耐多药结核病(multidrug-resistant tuberculosis,MDR-TB)因疗程长、治疗费用高、疗效差等特点而成为结核病的重要传染源,为结核病防治带来沉重负担,是全球公共卫生领域的挑战之一。2015年WHO全球结核病报告显示:3.3%的初治肺结核患者和20%的复治肺结核患者罹患MDR-TB。据估计,2014年全球新发MDR-TB患者48万例,中国新发MDR-TB 患者5.4万例。全球MDR-TB治疗成功率仅为50%[1]。
2006年我国试点实施全球基金耐多药肺结核防治项目,武汉市是2个试点城市之一,于2006年10月启动并实施该项目。实施的主要内容为MDR-TB疑似患者筛查、诊断;MDR-TB患者治疗、随访复查和全程管理。笔者分析2006年10月1日至2014年6月30日武汉市MDR-TB防治模式主要做法,MDR-TB患者发现、治疗、治疗转归、药物不良反应及免费政策情况,为全球基金项目结束后,制定我国MDR-TB防控措施提供参考和依据。
资料和方法
一、实施MDR-TB防治模式的主要做法
武汉市实施MDR-TB防治模式的主要做法有:(1)持续政府承诺,落实经费保障,为MDR-TB患者提供全程免费治疗和管理;(2)进一步采取积极的质量保证措施,提高痰培养和药物敏感性试验(简称“药敏试验”)的质量,以加强检测发现MDR-TB患者的水平;(3)多学科专家组讨论确定治疗方案、不良反应处置,并进行治疗转归评价;(4)重视与保证高质量、持续的二线抗结核药物供应;(5)进一步建立健全的市-区-社区(乡镇)三级结核病防治体系,落实MDR-TB患者治疗管理;(6)实施患者支持和人文关怀策略,提高患者治疗依从性,保证完成疗程;(7)实时开展监测评价和效果评估。
二、MDR-TB患者发现和治疗管理
1. MDR-TB筛查:2006—2010年筛查对象以复治涂阳肺结核患者[包括复发、初治失败、复治失败、其他(返回和迁入)]为主,2011—2014年逐步扩大到新涂阳肺结核患者。筛查程序为区级结核病防治机构(简称“结防机构”)将筛查对象的痰标本送至武汉市结核病防治所,进行痰培养、菌种鉴定和药敏试验。采用酸性改良罗氏固体培养基进行分枝杆菌培养,以对硝基苯甲酸(PNB)和噻吩-2-羧酸肼(TCH)培养基作为鉴别培养基,区分结核分枝杆菌、牛分枝杆菌和非结核分枝杆菌;采用比例法[2],对6种抗结核药物INH、RFP、EMB、Sm、Km和Ofx进行药敏试验。
2. MDR-TB诊断:药敏试验结果提示至少对INH和RFP耐药,诊断为MDR-TB患者。所有患者均由武汉市结核病防治所确诊。2006年10月1日至2014年6月30日筛查涂阳肺结核患者5524例,经药敏试验检出MDR-TB患者593例。
3. MDR-TB治疗:具备以下条件者纳入治疗:(1)菌种鉴定为结核分枝杆菌,药敏试验结果证实至少同时耐INH和RFP者;(2)签署治疗知情同意书;(3)经专家组讨论同意。治疗方案经专家组讨论确定,以标准化和个体化治疗方案相结合。标准化治疗方案参照《中国全球基金结核病项目(一期)实施细则》[2]和《耐多药肺结核防治管理工作方案》[3];个体化治疗方案根据患者过去治疗用药史,参考药敏试验结果制定。治疗方式为住院隔离治疗(256例)和门诊督导治疗(103例)相结合,疗程为24个月。本研究纳入治疗者359例,其中男258例(占71.9%)、女101例(占28.1%)。
4. MDR-TB管理:市-区-社区(乡镇)三级结核病防治网无缝对接,落实MDR-TB患者治疗管理。住院期间由病区护士执行DOT;门诊治疗期间根据患者现住址分别在村医、社区卫生服务中心和武汉市结核病防治所耐多药门诊进行督导化疗。督导管理方式为医务人员督导患者服药(277例)和家庭督导员督导患者服药(82例)。
三、给予MDR-TB患者免费政策及人文关怀
1.免费政策:武汉市结核病防治所是MDR-TB防治定点医院,在全球基金项目和武汉市政府配套经费支持下,为武汉市户籍人口中的MDR-TB疑似患者提供免费筛查;为符合治疗条件的MDR-TB患者提供全疗程免费抗结核药物和不良反应辅助治疗药物、免费住院和随访复查、报销注射费和往返交通费(每例患者60元/月)、免费督导管理,MDR-TB患者全疗程零负担。免费政策为武汉市耐多药肺结核患者防治模式中的特有政策,由武汉市政府批准实施。
2.人文关怀:在MDR-TB患者治疗前和治疗中,实施有特色的健康教育,每次一对一进行健康宣传教育(简称“宣教”)不少于1 h,内容涵盖患者耐药情况、治疗方案与疗程、可能发生的不良反应和对策、随访复查频率及日常生活中注意事项等;定期举办同伴教育活动并提供心理疏导,解除患者忧虑和担心。针对每例患者家庭情况,动员家属共同参与,为患者提供情感支持。
四、相关定义
1.登记分类[4]:初治患者指从未使用过抗结核药物或使用抗结核药物不超过1个月或首次行标准化疗方案规律用药而未满疗程,并从未在结防机构登记过的肺结核患者。复治患者是因不合理或不规律使用抗结核药物治疗≥1个月的患者或初治失败和复发患者。
2.治疗和转归[3]:(1)治愈:患者完成疗程,在疗程的后12个月,至少最后5次痰结核分枝杆菌培养(间隔至少30 d)连续阴性;如出现1次痰结核分枝杆菌培养阳性,其后痰结核分枝杆菌培养(间隔至少30 d)最少连续3次阴性。(2)失败:在疗程的后12个月,最后5次痰培养中有2次或2次以上阳性;或最后的3次培养中有任何一次是阳性,判定为治疗失败(包括治疗后临床及影像学表现疗效不佳或因为不良反应而临床决定提前中止治疗)。(3)丢失:患者未经医生允许治疗中断连续2个月或2个月以上。(4)死亡:在治疗过程中患者由于各种原因导致死亡。(5)不能组成有效方案:根据患者过去抗结核用药史,参考药敏试验结果,不能构成含4种有效抗结核药物的MDR-TB治疗方案。(6)原规划方案治疗痰菌阴转:患者等待药敏试验结果期间,采用规划方案治疗2个月以上,诊断MDR-TB时,原规划方案治疗有效,复查痰菌阴转。
五、统计学分析
分析MDR-TB患者检出率、接受治疗率、不良反应发生率及治疗转归等指标,采用Excel表格录入数据,SPSS 19.0软件进行统计学分析;对初治涂阳和复治涂阳患者MDR-TB检出率的差异进行χ2检验,以P<0.05为差异有统计学意义。
结 果
一、MDR-TB检出率
2006年10月1日至2014年6月30日,对5524例涂阳肺结核患者痰标本进行结核分枝杆菌培养,其中培养阳性4977例(90.1%),培养阴性529例(9.6%),污染18例(0.3%)。经菌种鉴定,非结核分枝杆菌107例(2.1%),结核分枝杆菌 4870例。通过药敏试验,检出MDR-TB患者593例,检出率12.2%。其中初治涂阳和复治涂阳患者MDR-TB检出率分别为6.9%和18.8%,复治涂阳患者MDR-TB检出率高于初治涂阳患者,差异有统计学意义(χ2=158.26,P<0.05)。复治失败、初治失败、复发和其他患者MDR-TB检出率分别为36.7%、26.9%、17.3%和15.9%,以复治失败检出率最高。不同登记分类涂阳肺结核患者MDR-TB检出情况见表1。
二、MDR-TB患者治疗管理
1.落实治疗情况:593例MDR-TB患者中,落实治疗者359例(60.5%);未落实治疗者234例(39.5%)。未落实治疗的患者中,不能组成有效方案者74例(31.6%)、拒治者51例(21.8%)、失访者43例(18.4%)、死亡者28例(11.9%)、原规划方案治疗痰菌阴转者14例(6.0%)、外地打工者24例(10.3%)。不同年份MDR-TB患者发现及落实治疗情况见表2。
2.督导管理:256例(71.3%)住院治疗患者由病区护士执行DOT,平均住院29 d(11~93 d)。出院后及103例非住院患者,注射期由医护人员督导化疗,非注射期医护人员督导277例(77.2%),其中村医、社区卫生服务中心和武汉市结核病防治所耐多药门诊督导MDR-TB患者分别为46例、177例和54例,家庭成员督导82例。
3.不良反应发生情况:359例落实治疗的MDR-TB患者中,发生不良反应315例(87.7%)。其中耳鸣或听力下降不良反应发生率最高(50.8%),其次为胃肠道反应(46.0%)、关节肿痛(43.2%)。2012年6月1日开始使用环丝氨酸,累计113例MDR-TB患者服用环丝氨酸,发生抑郁症状者6例(5.3%)。不良反应发生的时间多为治疗后的2~6个月,因重度不良反应中断治疗的患者13例(3.6%)。不良反应发生情况见表3。

表1 不同登记分类涂阳肺结核患者MDR-TB检出情况
注a:含慢性患者,即经过多次不规则治疗后痰菌仍阳性的肺结核患者;b:其他指除复发和初治失败以外的复治涂阳患者,如返回、迁入等
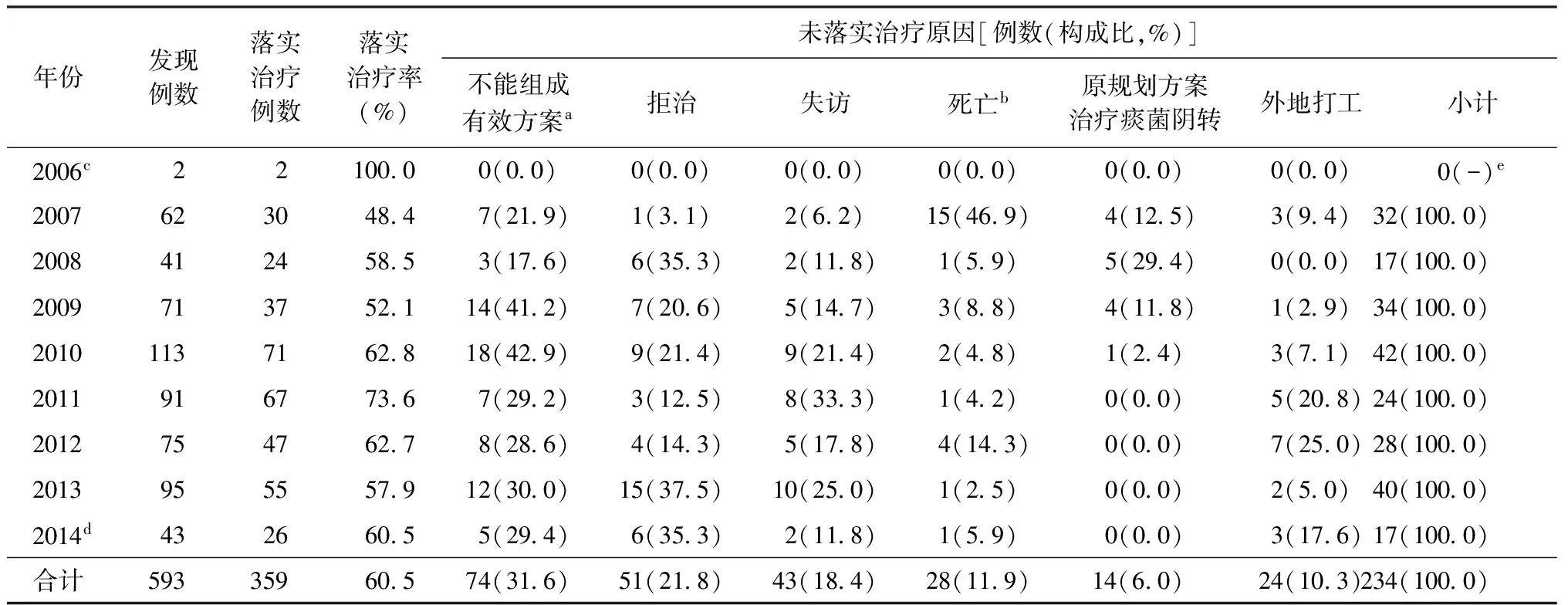
表2 不同年份MDR-TB患者发现及落实治疗情况
注a:不能组成有效方案指根据过去用药史和耐药种类不能组成含有4种有效药物的治疗方案;b:死亡指等待药敏结果期间患者因各种原因导致的死亡;c:2006年10月启动项目,12月开始进行患者耐药筛查;d:2014年统计1—6月的数据;e:小计总数为0,无构成比
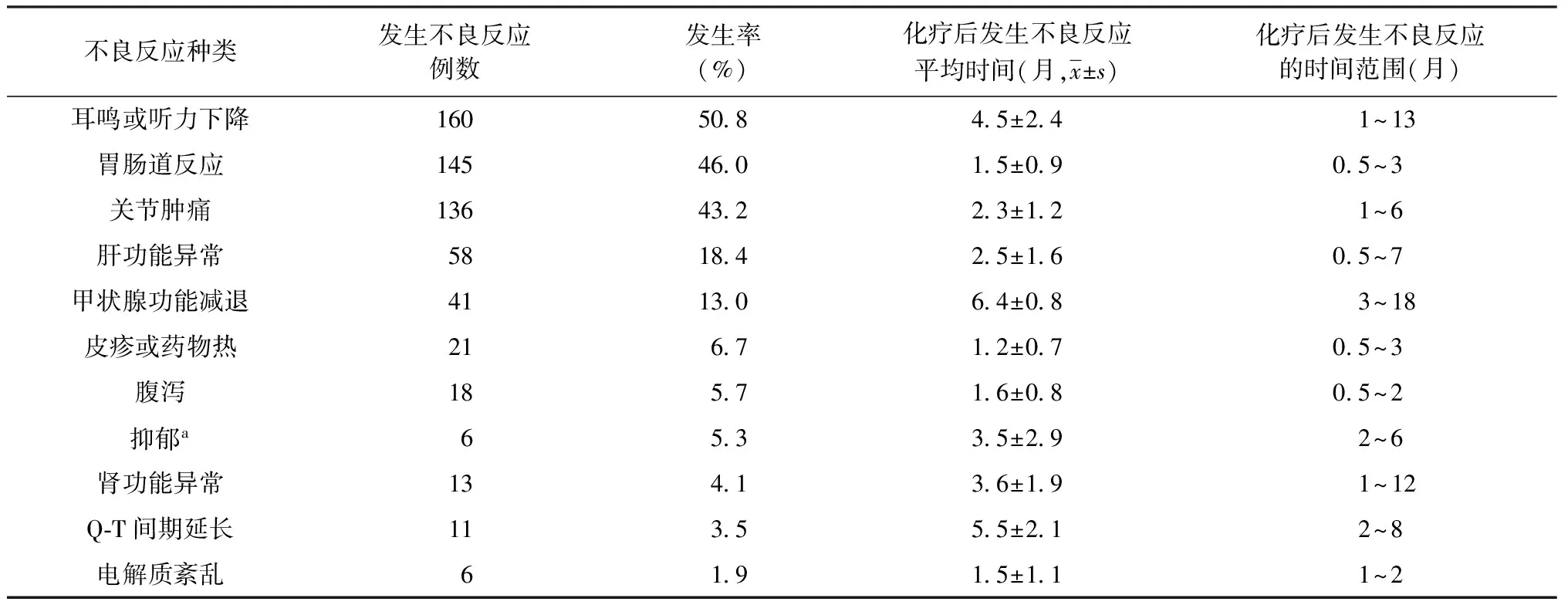
表3 315例MDR-TB患者化疗后不良反应发生情况
注a:113例MDR-TB患者服用环丝氨酸
注a:含慢性患者,即经过多次不规则治疗后痰菌仍阳性的肺结核患者;b:其他指除复发和初治失败以外的复治涂阳患者,如返回、迁入等
4.治疗转归情况:359例MDR-TB患者落实治疗,其中治愈263例(73.3%)、治疗中死亡4例(1.1%)、失败39例(10.9%)、丢失53例(14.8%)。初治涂阳患者治愈率76.6%、复治患者治愈率71.5%,复治患者中以复治失败者的治愈率最低(57.9%)。不同登记分类MDR-TB治疗转归结果见表4。
讨 论
目前关于我国MDR-TB防治的研究报道较少,已有的研究中探讨MDR-TB流行趋势、耐药机制、耐药影响因素的较多[5-7],对MDR-TB诊疗管理的研究多从临床角度探索不同技术及药物疗效之间的差异性,关于MDR-TB患者发现模式和规范性治疗管理模式的研究报道较少[8]。武汉市依托全球基金结核病项目,以地方政府提供专项经费作为补充,结合武汉市实际情况,对全球基金耐多药结核病项目的流程和环节进行了优化和完善,形成了“政府承诺,实施免费诊治;市-区-社区三级联动,落实MDR-TB患者发现、治疗和管理;专家组集体讨论确定治疗方案;开展有特色的健康教育和患者关怀”的MDR-TB防治模式。经过8年实施,取得良好成效,MDR-TB患者治愈率达到73.3%,接近WHO计划——2015年MDR-TB治疗成功率达到75%[9]的目标。武汉市MDR-TB防治模式取得成功的主要原因如下。
一、持续的政府承诺和免费政策是关键措施
政府承诺是项目实施的关键。2014年WHO全球结核病报告指出,有力的政府承诺是控制MDR-TB流行的5项重要措施之一[10]。本研究依托全球基金提供抗结核药品、MDR-TB患者住院、随访复查及交通补助等经费支持;同时地方政府支持新建生物安全二级(BSL-2)实验室、配备生物安全柜,修建符合医院感染控制要求的MDR-TB病区和门诊专用诊室;每年投入专项经费20~50万,补充项目经费不足。项目支持与地方政府专项经费相结合,保证了MDR-TB患者全疗程免费治疗和管理,人均免费金额4.2万元,患者“零负担”,增加了治疗依从性从而提高治愈率。
二、以涂阳肺结核为目标人群发现MDR-TB患者
本研究进行药敏试验的涂阳肺结核患者共4870例,发现MDR-TB患者593例,其中复治涂阳患者MDR-TB检出率为18.8%,复治失败患者检出率最高(36.7%),初治涂阳患者检出率6.9%。2006—2010年以复治涂阳肺结核患者为目标人群筛查MDR-TB,2011—2014年筛查对象扩大到新涂阳肺结核患者,结果显示,MDR-TB构成比发生改变,后4年检出的MDR-TB患者中,50%~60%来源于初治患者,与高谦和梅建[11]认为的“传播是造成我国结核病高耐药率的主要原因”的观点相吻合。因此,对于筛查MDR-TB的目标人群,可根据各地区经济条件确定,在资源有限时,优先对复治涂阳等高危人群进行药敏试验检测,能以有限的投入尽可能地发现MDR-TB患者;资源允许时建议对所有涂阳肺结核患者进行药敏试验,发现MDR-TB患者。
三、落实治疗管理,及时监测和早期处理不良反应
本研究359例(60.5%)纳入项目落实的治疗者,其中医务人员全程督导管理277例,占77.2%;家庭成员督导82例,占22.8%。因多种药物联合治疗,不良反应发生率高,本研究中,359例MDR-TB患者不良反应发生率为87.7%,与邝浩斌等[12]报道的86.5%相似。耳鸣或听力下降发生率为50.8%,耳毒性反应可能与氨基糖苷类累积用药时间有关。使用环丝氨酸的患者抑郁症状发生率为5.3%,低于国内相关报道[13-14],可能与本研究对患者治疗前评估,治疗过程中有精神病专家密切观察、及时处理相关不良反应有关,但仍需引起足够的重视和警惕。本研究96.4%为轻、中度不良反应,其中胃肠道反应(46.0%)、关节痛(43.2%)、肝功能异常(18.4%)、甲状腺功能减退(13.0%)等不良反应通过及时监测、早期对症处理或调整治疗方案可缓解。因重度不良反应临床中止治疗的发生率较低(3.6%)。及时监测、评估和处理不良反应非常重要,对患者进行健康教育,使其知晓可能发生的不良反应,一旦不适及时就诊。早期发现和及时处理不良反应,可以减少因不良反应导致的中断治疗,从而提高治愈率。
四、多措并举,取得高治愈率
文献资料显示:MDR-TB和(或)XDR-TB 治疗成功率为36%~79%[15-16],平均治疗成功率为50%[1]。本研究MDR-TB治愈率达到73.3%。取得高治愈率主要有以下4个方面的原因:(1)武汉市结核病防治所具备预防和临床医疗功能,可以实现患者的发现、治疗和管理一体化。(2)多学科专家组(临床专家、影像学专家、预防及心理咨询专家)讨论确定每例MDR-TB患者治疗方案、不良反应处置和疗效评价,保证了患者的规范治疗,减少丢失。(3)重视健康教育和人文关怀,提供情感支持,建立良好的医患关系,保证患者按时随访复查,提高患者治疗依从性。(4)高质量药品持续不断的供应是高治愈率的保证。
五、重视未接受治疗患者的随访管理
本研究39.5%的MDR-TB患者因死亡、不能组成有效方案、原规划方案治疗痰菌阴转、拒治、失访和外地打工而未能落实治疗管理,其中死亡和原规划方案治疗痰菌阴转两类患者(占17.9%,42/234)不会产生传播危害。对不能组成有效方案和拒绝治疗者,缺乏法律法规强制性隔离依据,本研究采取健康教育的方式,培训患者增强公共卫生意识,建议其居家隔离,减少社区传播。需要关注的重点对象是拒绝治疗、失访和外地打工三类患者(占50.4%,118/234),分析原因为:(1)本项目采取的传统固体方法进行痰培养和药敏试验,耗时较长,部分患者因搬迁、联系方式改变而失访;或因生活需要到外地打工,多次追踪不到位;(2)部分患者因年龄大、基础疾病多、行动不便或吸毒等拒绝治疗;(3)项目免费政策宣传力度不够,导致患者认识不足而未能主动治疗。2014年全球基金项目结束前已开始应用分子生物学方法与液体培养相结合的方法开展药敏试验,缩短了药敏试验的报告时间。
目前,对规划方案治疗痰菌阴转的患者是否更改治疗方案争论较多,专家意见不统一。主张更改治疗方案的专家认为INH和RFP药敏试验可靠性高,可以为临床更改治疗方案提供依据。之所以用原规划方案治疗痰菌阴转是由于强化期方案中除INH和RFP外,还含有PZA和EMB发挥作用;到继续期时停用PZA和EMB,只用INH和RFP,但因患者对INH和RFP耐药,可能导致治疗无效,因此主张根据药敏试验结果尽早更改治疗方案,避免无效治疗增加耐药,导致更严重的肺损伤和耐药结核分枝杆菌传播。主张规划方案治疗的专家认为:药敏试验为体外试验结果,可能与体内环境有差异,且MDR-TB长疗程易导致患者治疗依从性差而中断治疗。可以在规划方案治疗下动态观察,每3个月进行痰涂片和痰培养检测,一旦发现阳性,立即实施耐多药化疗方案进行治疗。
六、本研究存在的不足
本研究缺乏DOT执行情况对治疗结果的影响、不同治疗方案效果、感染控制效果及MDR-TB患者社会经济情况与治疗效果的关系等资料分析,有待今后进一步总结。
综上所述,武汉市MDR-TB防治模式在本地区具有可行性,实现了针对MDR-TB患者发现、治疗管理和效果评价大样本队列研究,建立了以地市级为中心的MDR-TB诊疗和管理模式,可为国家制定MDR-TB防控政策和技术措施提供参考和依据。但MDR-TB防控形式不容乐观,需要多部门参与,从医保政策、技术策略和经费投入等方面建立长效机制,减少MDR-TB产生和积极有效地治疗现有患者,为消除MDR-TB而努力。
[1] World Health Organization. Global tuberculosis report 2015. Geneva: World Health Organization, 2015.
[2] 中国全球基金结核病项目办公室.中国全球基金结核病项目(一期)实施细则(耐多药结核病防治领域).北京:中国全球基金结核病项目办公室,2010:31-39.
[3] 王宇.耐多药肺结核防治管理工作方案.北京:军事医学科学出版社,2012.
[4] 中华人民共和国卫生部疾病预防控制局,中华人民共和国卫生部医政局,中国疾病预防控制中心.中国结核病防治规划实施工作指南(2008年版). 北京:中国协和医科大学出版社,2009.
[5] 刘荣梅,王玉清,高孟秋,等.青海省耐多药肺结核病危险因素的病例对照研究.临床肺科杂志, 2015,20(4): 592-595.
[6] 陆伟,周扬,陈诚,等.江苏省社区人群结核杆菌耐药状况及影响因素研究.中华疾病控制杂志, 2013, 17(7): 560-563.
[7] 李莉,孙建胜,张海清,等.徐州市耐多药结核病流行病学特征及危险因素分析.江苏预防医学, 2015,26(4):60-61.
[8] 吴哲渊,张青,张祖荣,等.上海市耐多药肺结核防治管理模式效果评价.中国防痨杂志,2015,37(11):1118-1125.
[9] World Health Organization.The global plan to stop TB 2011—2015: transforming the fight towards elimination of tuberculosis. Geneva: World Health Organization, 2010.
[10] World Health Organization. Global tuberculosis report 2014. Geneva: World Health Organization, 2014.
[11] 高谦,梅建. 传播才是造成我国结核病高耐药率的主要原因. 中国防痨杂志,2015,37(11):1091-1096.
[12] 邝浩斌,谭守勇,谢育红,等.耐多药肺结核化学治疗不良反应及处理. 结核病与肺部健康杂志, 2015, 4(4): 219-222.
[13] 程武,谭守勇,李艳,等.环丝氨酸在治疗耐多药肺结核患者中的不良反应分析.结核病与肺部健康杂志, 2015, 4(4): 247-249.
[14] 宋艳华,郭少晨,高孟秋,等.环丝氨酸治疗耐多药结核病的血药浓度及不良反应监测. 中国防痨杂志,2014,36(5):399-401.
[15] Falzon D, Gandhi N, Migliori GB, et al. Resistance to fluoroquinolones and second-line injectable drugs: impact on multidrug-resistant TB outcomes. Eur Respir J, 2013, 42(1): 156-168.
[16] Orenstein EW, Basu S, Shah NS, et al. Treatment outcomes among patients with multidrug-resistant tuberculosis: syste-matic review and meta-analysis. Lancet Infect Dis, 2009, 9(3): 153-161.
(本文编辑:郭萌)
Effect analysis on control and prevention model of multidrug-resistant pulmonary tuberculosis in Wuhan city
ZHOUMei-lan,DUYi-xiang,WANGJian-jie,WUGang,CHENZi,CHENCong,WANGWei-hua.
WuhanInstituteforTuberculosisControl,WuhanPulmonaryHospital,Wuhan430030,China
WANGWei-hua,Email:drwang65@163.com
Objective To analyze the effect of implementation of the model for control and prevention of multi-drug resistant pulmonary tuberculosis (MDR-TB) in Wuhan city in 2006-2014, and to provide references for the development of MDR-TB control and prevention strategy after the Global Funds’ MDR-TB program in China. Methods In October 2006, Wuhan launched the Global Fund of MDR-TB program. The main content of the program included suspected MDR-TB cases screening and diagnosis; MDR-TB patients treatment, follow-up and mana-gement. Program baseline materials, report data; medical records of period between October 1th 2006 to June 30th 2014 were collected for analysis and evaluation, 5524 cases of sputum smear positive patients who had been registered in Wuhan, conducted sputum culture to identify strains, and 4870 cases of them were infectedM.Tuberculosis(MTB). With confirmation provided by a drug susceptibility test (DST), 593 cases of MDR-TB were detected. Through a consultation by a penal of experts, 359 of these confirmed MDR-TBs received treatment of standardized anti-MDR-TB chemo regimen supplemented with individualized drug choices. Treatment outcomes, adverse reactions and causes of non-treatment were analyzed. A comparison was drawn between MDR-TB detection rate of new smear positive TB cases and that of relapsed TB cases. Results The overall detection rate for MDR-TB is 12.2% (593/4870), of which, MDR-TB detection rates among new smear positive and relapsed TB cases are 6.9% (188/2715) and 18.8% (405/2155)respectively, MDR-TB detection rate of relapsed TB cases is higher than that of new smear positive TB cases (χ2=158.26,P<0.05). Among 359 MDR-TBs (60.5% of all MDR-TBs) who received treatment, cure rate is 73.3% (263/359), of which, cure rates for new smear positive and relapsed TB cases who turned out to be MDR-TB, are 76.6% (95/124) and 71.5% (168/235) respectively, MDR-TBs who registered under the classification of retreatment failure (chronical) has the lowest cure rate of 57.9% (22/38). Overall incidence of adverse reaction is 87.7% (315/359), incidences for tinnitus or hearing loss, gastronomical reactions and joint pain are 50.8% (160/315), 46.0% (145/315) and 43.2% (136/315) respectively. Incidence for cyclonserin induced depression is 5.3% (6/113). Only 3.6% (13/359) of those treated MDR-TB defaulted treatment due to severe adverse reactions. Conclusion Wuhan prevention and treatment model for MDR-TB has achieved some effectiveness. which has made possible for a large sample cohort analysis covering all aspects of MDR-TB management such as, case detection, treatment management and evaluation of efficacy, to establish a municipal center for MDR-TB treatment and management, which has reference value.
Tuberculosis, multidrug-resistant; Physicians practice patterns; Treatment outcome; Wuhan city
10.3969/j.issn.1000-6621.2016.11.006
中国全球基金结核病控制项目(CHN-S10-G14-T);武汉市卫生和计划生育委员会医疗卫生科研项目(WG15A04)
430030 武汉市结核病防治所 武汉市肺科医院
王卫华,Email:drwang65@163.com
2016-07-14)

