养真接骨胶囊微生物限度检查方法验证
杨劼 段肖翠 李涛 崔力剑 马华民 李三铁 焦宁
050051 石家庄市,河北医科大学第三医院(杨劼、崔力剑、马华民、焦宁);河北医科大学实验动物学部,河北省实验动物重点实验室(段肖翠);河北医科大学第二医院(李涛);河北医科大学药学院(李三铁)
·论著·
养真接骨胶囊微生物限度检查方法验证
杨劼段肖翠李涛崔力剑马华民李三铁焦宁
050051石家庄市,河北医科大学第三医院(杨劼、崔力剑、马华民、焦宁);河北医科大学实验动物学部,河北省实验动物重点实验室(段肖翠);河北医科大学第二医院(李涛);河北医科大学药学院(李三铁)
【摘要】目的建立养真接骨胶囊的微生物限度检查方法。方法采用平皿法(培养基稀释法)与常规法,以金黄色葡萄球菌,大肠埃希菌,枯草芽孢杆菌,白色念珠菌,黑曲霉菌和乙型副伤寒沙门菌为阳性对照菌,进行细菌数、霉菌和酵母菌数与控制菌验证。结果规定条件下培养,结果3个批次药品本底组菌落数均为0。3个批次药品五种阳性菌回收率均高于70%,证明无抑菌现象。3个批次药品试验组和菌液组在加入靛基质试液后液面出现玫瑰红色,而对照组和稀释组未出现。3个批次药品试验组和菌液组产酸产气,而对照组和稀释组未出现。3个批次药品试验组和菌液组有菌落,而对照组和阴性对照未出现。结论养真接骨胶囊样品可采用1∶10供试液,平皿法检查细菌数,常规法检查霉菌及酵母菌数和控制菌。
【关键词】养真接骨胶囊;微生物限度检测;方法学验证;培养基稀释法
中药合剂、口服液、片剂、胶囊剂、颗粒剂、注射剂等是目前发展起来的中成药新制型。具有易于服用、便于携带、储存、患者用药的依从性好等优点,然而,由于中药成分复杂,营养物质丰富,我细菌的生长繁殖提供了适宜的环境,增加了药物应用的不良反应发生率和患者就医风险。因此,如何有效的检测和控制细菌的种类和数量尤为重要。然而,建立的中药检测方法是否灵敏、准确、可行,仍需要验证方法的可适用性,那么中药质量标准分析方法验证的目的, 就是证明采用的方法是否适合于相应的检测要求。在建立中药质量标准时, 分析方法需经验证; 在处方、工艺等变更或改变原分析方法时, 也需对分析方法进行验证。而有些药物的检测方法现在看来专属性差,不能有效地验证真假伪劣,还需要制定更准确、更先进的检测方法[1]。中国药典规定的检查项目包括有细菌数、霉菌数、酵母菌数和控制菌的检查[1],同时参考相关文献[2-5],本文按照相关操作规范,对相应的微生物限度检查方法进行验证。
1材料与方法
1.1主要仪器高压蒸汽灭菌器、恒温电热培养箱,电热鼓风干燥箱、匀浆仪。
1.2主要试剂养真接骨胶囊,生产单位:河北医科大学第三医院;培养基主要有营养琼脂培养基、胆盐乳糖培养基、玫瑰红钠琼脂培养基、营养肉汤培养基、改良马丁培养基、改良马丁琼脂培养基、pH值7.0氯化钠-蛋白胨缓冲液、4-甲基伞形酮葡糖苷酸培养基、乳糖胆盐发酵培养基四硫磺酸钠亮绿培养基(TTB)、曙红亚甲蓝琼脂培养基(EMB)、胆盐硫乳琼脂培养基(DHL)。以上培养基均购买自北京三药并且通过了药典所规定的相关适用性试验;阳性对照菌主要有金黄色葡萄球菌[CMCC(B)26003]、大肠埃希菌[CMCC(B)44102]、枯草芽孢杆菌[CMCC(B)63501]、白色念珠菌[CMCC(F)98001]、黑曲霉菌[CMCC(F)98003]和乙型副伤寒沙门菌[CMCC(B)50094],以上菌种均购买自中国药品生物制品检定所,且传代次数未超过第五代。稀释剂为pH值7.0氯化钠-蛋白胨缓冲液。
1.3菌液制备于10 ml营养肉汤培养基中接种金黄色葡萄球菌、大肠埃希菌、枯草芽孢杆菌的斜面新鲜培养物,34℃条件下培养24 h;于10 ml改良马丁培养基中接种白色念珠菌的斜面新鲜培养物,25.0℃条件下培养48 h;取上述培养物 1 ml置9 ml 0.9%无菌氯化钠溶液无菌试管内,采用10倍递增稀释法使菌数为50~100 cfu/ml。于改良马丁琼脂斜面培养基中接种黑曲霉的斜面新鲜培养物,25℃条件下培养5 d,之后加入含0.05%(ml/ml)聚山梨酯-80的0.9%无菌氯化钠溶液5 ml,洗下霉菌孢子,吸出孢子悬液,取1 ml菌液加0.05%(ml/ml)聚山梨酯-80的0.9%无菌氯化钠溶液9 ml,采用10倍递增稀释法使菌数为50~100 cfu/ml。
1.4实验步骤
1.4.1平皿法供试液制备:取样品10 g加pH值7.0无菌氯化钠-蛋白胨缓冲液至100 ml,设定匀浆仪2 000 r/min,混匀1 min,作为1∶10供试液。
1.4.2细菌数:取上述1∶10供试液0.2 ml置1个无菌平皿中,平行制备2个皿,倒入45℃左右的营养琼脂培养基中混匀,作为供试品对照组,按平皿法测定细菌本底菌落数;取上述1∶10供试液0.2 ml与上述阳性对照菌悬液1 ml同置一无菌平皿中,每种阳性菌平行制备2个皿,倒入45℃左右的营养琼脂培养基中混匀,作为试验组,按平皿法测定菌落总数;分别取制备好的阳性对照菌悬液或孢子悬液1 ml,置1个无菌平皿中,每种阳性菌平行制备2个皿,倒入45℃左右的营养琼脂培养基中混匀,作为菌液组,按平皿法测定菌落数。
1.4.3霉菌和酵母菌数:常规法验证取上述1∶10供试液1 ml置1个无菌平皿中,平行制备2个皿,倒入45℃左右的营养琼脂培养基中混匀,作为供试品对照组,按平皿法测定细菌本底菌落数;取上述1∶10供试液1 ml与上述阳性对照菌悬液1 ml同置1个无菌平皿中,每种阳性菌平行制备2个皿,倒入45℃左右的营养琼脂培养基中混匀,作为试验组,按平皿法测定菌落总数;分别取制备好的阳性对照菌悬液或孢子悬液1 ml,置1个无菌平皿中,每种阳性菌平行制备2个皿,倒入45℃左右的营养琼脂培养基中混匀,作为菌液组,按平皿法测定菌落数。
1.4.4大肠埃希菌:常规法验证取100 ml胆盐乳糖培养基4份,2份分别加入1∶10供试液10 ml,其中1份加入上述大肠埃希菌的菌悬液(营养琼脂平板计数菌落数为85 cfu/ml)1 ml,其他2份分别加入上述大肠埃希菌的菌悬液1 ml和10 ml pH值7.0无菌氯化钠-蛋白胨缓冲液。置于34℃培养24 h,取培养物 0.2 ml,接种至含5 ml MUG培养基的试管内34℃培养,24 h在366 nm紫外灯下观察是否有蓝白色荧光后,加入靛基质试液,观察液面是否出现玫瑰红色。
1.4.5大肠菌群:常规法验证取10 ml胆盐乳糖发酵培养基管4份,2份分别加入1∶10供试液1 ml,其中1份加大肠埃希菌的菌悬液1 ml;第3份加上述大肠埃希菌的菌悬液(营养琼脂平板计数菌落数为85 cfu/ml)1 ml、第4份加稀释剂1 ml。于34℃培养24 h后,观察是否产酸产气。
1.4.6沙门菌:常规法验证取3份200 ml营养肉汤培养基,2份各加入10 g供试品,其中1份加入上述沙门菌菌悬液(营养琼脂平板计数菌落数为64 cfu/ml)1 ml,与第3份同置34℃培养24 h后,分别取上述培养物1 ml接种于10 ml四硫磺酸钠亮绿培养基中,同条件下培养24 h后分别划线于DHL和EMB平板上,继续培养过夜,观察菌落生长情况。
2结果
2.1按平皿法测定供试品对照组菌落数,霉菌和酵母菌数。规定条件下培养,结果3个批次药品本底组菌落数均为0。见表1。
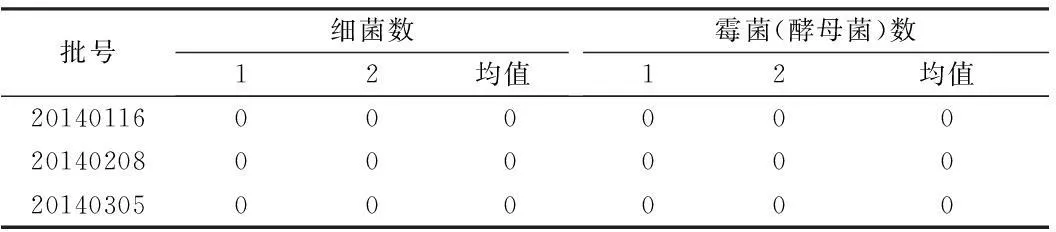
表1 供试品对照组计数结果 cfu
2.2按平皿法测定试验组、菌液组菌落数结果3个批次药品五种阳性菌回收率均高于70%,证明无抑菌现象,说明养真接骨胶囊样品可用平皿法进行微生物限度检查。见表2。

表2 五种阳性菌回收率计算结果
2.3常规法检测大肠埃希菌结果3个批次药品试验组和菌液组在加入靛基质试液后液面出现玫瑰红色,而对照组和稀释组未出现。说明养真接骨胶囊样品可用常规法进行微生物限度检查。见表3。
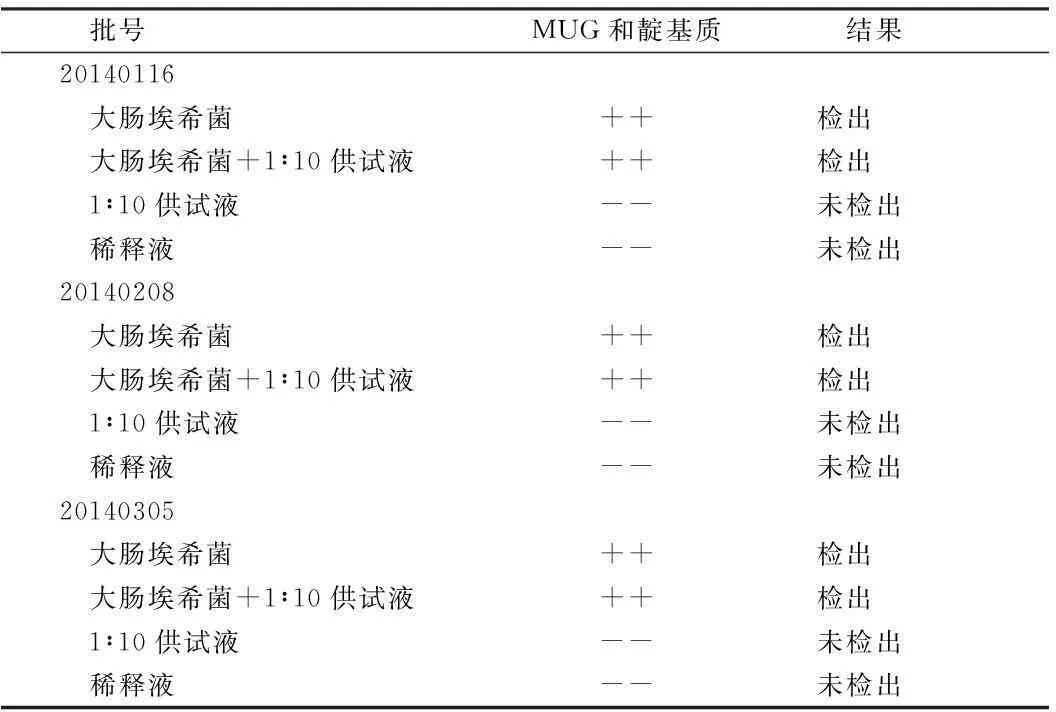
表3 大肠埃希菌的验证结果
2.4常规法检测大肠菌群结果3个批次药品试验组和菌液组产酸产气,而对照组和稀释组未出现。说明养真接骨胶囊样品可用常规法进行微生物限度检查。见表4。
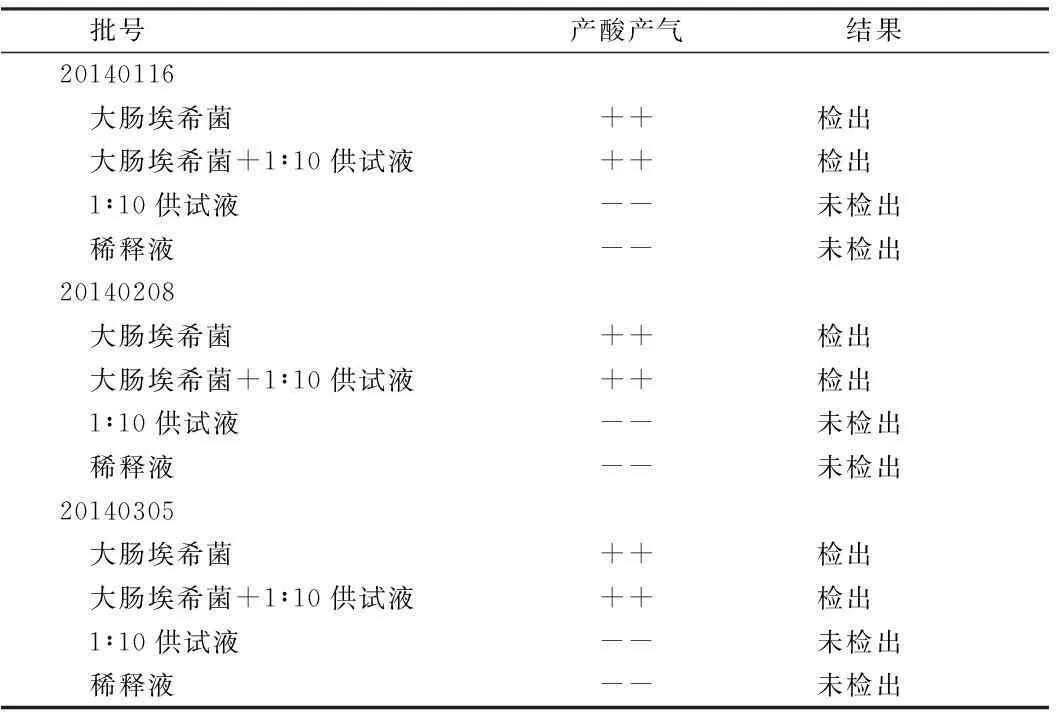
表4 大肠菌群的验证结果
2.5常规法检测沙门菌结果3个批次药品试验组和菌液组有菌落,而对照组和阴性对照未出现。说明养真接骨胶囊样品可用常规法进行微生物限度检查。见表5。
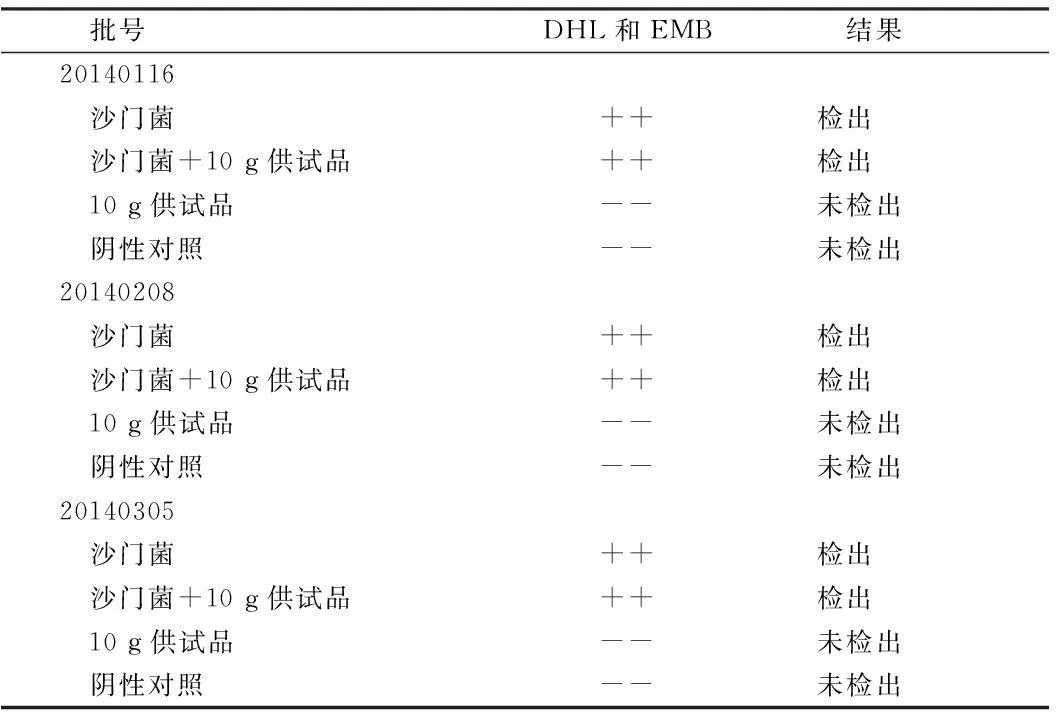
表5 沙门菌的验证结果
3讨论
中药是指在中医理论指导下应用的药物。中药传统剂型是汤剂,但因其体积较大、味苦,服用、携带不方便;易发霉、发酵、不能久贮;不宜大量制备,也不利于及时抢救危重患者等缺点,因此近年来,广大中医药研究者对汤剂进行了有效的剂型改革,例如中药合剂、口服液、片剂、胶囊剂、颗粒剂、注射剂等,都是尽量保留汤剂药效,并克服其缺点的基础上发展起来的中成药新制型。目前中药材的来源非常复杂,参差不齐,中药材科属不同、环境不同以及栽培、采收、加工炮制方式不同且品种繁多,造成中成药的质量难以控制,也给中成药的临床应用带来了一定的隐患;中成药生产工艺控制不当也是造成成药质量不佳的原因之一。中药制剂的生产过程对最终成品质量的影响至关重要,不恰当的制剂工艺或者不按照规程的操作,均会影响制剂的疗效以及有效成分的均一性。另一方面,研发阶段生产工艺制定不当。比如,有的生产工艺过于复杂,生产工艺参数不合理,生产厂家对生产工艺缺乏筛选优化方面的系统研究,难以保证制剂质量。
在药物制剂的质量检测中,微生物的检测是一个十分重要的方面,对于中药制剂,微生物的检测和控制尤为重要。由于大部分中成药的处方十分复杂,其药用成分的组成甚至不被研究者完全了解,要对其进行质量控制,防止劣药出现,加强品控,防止医疗事故的发生,我们必须对微生物限度的检测方法进行验证,这些方法包括常规检测法、培养基稀释法、薄膜过滤法等[6,7]。
养真接骨胶囊为我院自制的中药制剂,其处方为骨碎补120 g,续断60 g,自然铜120 g,黄瓜子400 g,乳香120 g,没药120 g,制川乌120 g,土鳖虫60 g,红花60 g,川芎120 g,具有较强的滋补肝肾,强筋壮骨,活血化瘀,消肿止痛的作用,能加速成骨、促进骨折愈合,用于治疗骨折等,在我院应用较为广泛。为保证药品质量,确保使用的有效性和安全性,需要对该药进行微生物限度检查。养真接骨胶囊成分为中成药,其成分复杂,某些成分可能含有一定的抑菌作用,按照《中国药典》(2010年版)要求,在建立药品的微生物限度检查方法时,需要对检查方法进行验证。
养真接骨胶囊是含有多种中药成分,其中任何成分含有抑菌性均可影响微生物限度检查的准确性,本实验所应用的菌株,在验证过程中,为防止供试液的抑菌活性对试验菌株的抑制作用,在操作过程中,一定要注意细节,以免对回收率产生影响,本实验通过稀释法,对供试品进行稀释,减少其对各类菌株的抑制作用,而在此实验中,我们采用了平皿法(培养基稀释法)与常规法对细菌数、霉菌和酵母菌数以及控制菌进行了验证[8]。
本实验采用平皿法对大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌、黑曲霉菌进行验证,上述菌株的回收率均大于70%,说明养真接骨胶囊对上述菌株无抑菌作用。养真接骨胶囊微生物限度检测的验证实验确认了该检测方法的正确性,确定了检测结果的有效性与数据的可靠性,确保了药品的质量。
近年来,随着中药现代化进程的加快,带动了对中药复方质量控制从初级研究层次向更深层次迈进。多学科的交叉融合,各种新技术、新方法的出现也为复方质量控制的研究发展带来了新的思路,中药复方制剂的质量控制将仍逐步向药效物质基础控制的模式转变([9-12])。目前国家药典及行业标准目前还不完善,而且国家药典收载的中药材和中药制剂品种很有限,许多中药材缺乏统一的国家标准。很多中成药指标成分检验标准过于单一,使企业容易忽视其它指标成分,造成各指标成分间的比例失调,影响中药制剂的临床疗效。对于中成药的质量控制,我们仍应加快质量标准体系的建设,制定完善的制剂工艺,严格规范中药生产的全过程,在此基础上,多种分析技术联用控制中药制剂的质量([13,14])。
参考文献
1董建平.关于中药材质量存在问题的思考.中国医药指南,2012,10:235-236.
2中华人民共和国药典委员会主编.中华人民共和国药典.2005版.北京:化学工业出版社,2005.424-442.
3刘元昆,张立贤.芪参清幽胶囊微生物限度检查方法验证.中国执业药师,2010,8:30-33.
4中国药品生物鉴定所.中国药品检验标准操作规范(2010年版).北京:中国医药科技出版社,2010.351-389.
5戚继红,蒋孜杰.通心络胶囊微生物限度检查方法验证.临床合理用药,2015,8:39-40.
6张美丽,杨晓东,邓媛,等.中成药微生物限度检查方法验证.河南中医,2014,37:532-534.
7黄英.14种中成药微生物限度检查方法研究.中国执业药师,2013,11:27-30.
8赵会兰.20种中成药微生物限度检查方法验证.中国执业药师,2014,12:21-24.
9苏松柏,张永萍,张丽丽,等.拉曼光谱在中药质量控制中的应用.中国实验方剂学杂质,2011,17:284-286.
10刘家水,梁欣健,张丹雁.近红外光谱技术在中药鉴定中的应用.广东药学院学报,2011,27:332-335.
11孙爱萍,张西如,谷菲菲.LC-MS/MS 方法测定中成药麻仁丸中添加伪品大黄的研究.中成药, 2011,33:357-359.
12周莹君,孙立亚,苏会霞,等.中药饮片质量控制分析.中国中医药现代远程教育,2011,9:98-99.
13潘炜,顾鑫荣,刘志璋,等.LC-MS/MS 法测定中成药制剂中23个非甾体抗炎药.药物分析杂质, 2012,32:261-266.
14王赵,陈佳,林彤,等.中药及其制剂辐射杀菌现状调研及监管意义.中国药学杂志,2015:314-316.
(收稿日期:2015-11-26)
【中图分类号】R 915.1
【文献标识码】A
【文章编号】1002-7386(2016)09-1363-04
通讯作者:焦宁,050051石家庄市,河北医科大学第三医院;
doi:10.3969/j.issn.1002-7386.2016.09.026
项目来源:河北省中药管理局中医药类科研计划(编号:2012011)
E-mail:jn8026@126.com

