体外循环实施无血浆预充策略对小儿心脏术后凝血及临床预后的影响
王 甜,刘晋萍,邹丽华,赵明霞,崔勇丽,冯正义,赵 举
体外循环实施无血浆预充策略对小儿心脏术后凝血及临床预后的影响
王 甜,刘晋萍,邹丽华,赵明霞,崔勇丽,冯正义,赵 举
[摘要]:目的 探索先天性心脏病患儿体外循环中无血浆预充策略对术后凝血功能和临床预后的影响,并分析术后胸液引流量的相关因素。方法 回顾性分析阜外医院自2012年1月至2013年4月在体外循环下行先天性心脏病矫治术的患儿资料1 164例,根据年龄及预充液类型分为婴儿血浆组(n=336)、婴儿佳乐施组(n=335)、幼儿血浆组(n=225)和幼儿佳乐施组(n=268)。通过血液学检查、止血药物用量、术后胸液引流量、体外循环及住院期间血制品用量等指标分别对婴儿和幼儿群体评估无血浆预充策略对术后凝血功能的影响,并统计分析不同预充策略组内患儿的住院死亡率及并发症发生率。通过多因素线性回归分析术后胸液引流量的相关因素。结果 婴儿佳乐施组、幼儿佳乐施组分别与婴儿血浆组、幼儿血浆组相比,死亡率无显著差异( P>0.05)。婴儿佳乐施组与婴儿血浆组相比,术后12 h及24 h胸液引流量显著增加( P<0.05),但在体外循环及住院期间的血制品使用量显著减少( P<0.05),肺部感染发生率显著下降( P<0.05)。幼儿佳乐施组在体外循环及住院期间的血制品使用量显著少于幼儿血浆组( P<0.05),术后并发症发生率无显著差异( P>0.05)。多因素线性回归分析显示预充液类型、年龄、转机时间与婴儿术后胸液引流量显著相关。结论 对于常规择期先天性心脏病矫治术患儿,根据临床指南合理应用人工胶体液替代新鲜冰冻血浆用于体外循环是安全可行的。
[关键词]:体外循环;小儿;先天性心脏病;凝血;人工胶体;新鲜冰冻血浆
Impact of priming strategy without fresh frozen plasma on postoperative coagulation and clinical prognosis in pediatric patients after cardiac surgery
Wang Tian,Liu Jin-ping,Zou Li-hua,Zhao Ming-xia,Cui Yong-Li,Feng Zheng-yi,Zhao Ju
Department of Cardiopulmonary Bypass,Fu Wai Hospital,CAMS and PUMC,National Center for Cardiovascular Diseases,Beijing 100037,China
Corresponding author:Liu Jin-ping,Email:jinpingfw@ hotmail.com
[Abstract]:Objective To explore the effect of priming strategy without fresh frozen plasma on postoperative coagulation and clinical prognosis in pediatric patients undergoing cardiac surgery and analyze the factors associated with postoperative chest tube drainage.Methods This is a retrospective study of 1,164 pediatric patients who underwent cardiac surgery with cardiopulmonary bypass(CPB) between January 2012 and April 2013.Patients were divided into four groups:the infants plasma group(n=336),the infants gelatin group(n=335),the children plasma group(n=225)and the children gelatin group(n=268).The hematologic data,pharmacological agents,postoperative chest tube drainage and transfusion requirements during CPB and hospitalization were collected to evaluate postoperative coagulation function.In-hospital mortality and incidence of morbidity were calculated and compared between groups of different priming strategies.Multiple linear regression analysis was used to explore factors associated with postoperative chest tube drainage.Results The incidence of mortality were comparable between the plasma and gelatin groups of infants and children( P>0.05).Significantly lower incidence of pulmonary infection and more chest tube drainage were demonstrated in the infants gelatin group( P<0.05).But requirement of transfusion waslower in the gelatin groups of infants and children( P<0.05).Multiple linear regression analysis indicated that the type of prime,age and the bypass time were associated with postoperative chest tube drainage in infants.Conclusion For general pediatric patients undergoing elective cardiac surgery,it is feasible to substitute FFP with gelatin in CPB prime.
[Key words]: Cardiopulmonary bypass;Pediatric;Congenital heart disease;Coagulation;Artificial colloids;Fresh frozen plasma在小儿先天性心脏病(先心病)手术中,传统体外循环系统内的预充液总量与小儿自身血容量比例过大,常引起血液过度稀释,导致胶体渗透压过低及术后水肿[1],还可引起凝血因子及纤维蛋白原浓度过低,导致术后凝血功能障碍[2-3]。因此,一直以来,国内外心脏中心广泛性使用新鲜冰冻血浆(fresh frozen plasma,FFP)作为小儿体外循环预充液的主要成分,以补充凝血因子及纤维蛋白原,保障患儿术后凝血功能[4]。然而近年来,血源紧张及血浆输注的相关并发症[5]等问题日益凸显,围体外循环期预防性输注FFP的临床获益也饱受质疑,这一系列因素促使临床医师积极寻找在先心病患儿体外循环领域安全有效的血浆代用品。因此,本研究拟采用大样本临床资料来回顾性分析佳乐施替代FFP用于先心病患儿体外循环预充的可行性,并通过多因素线性回归分析,探索预充液类型与术后胸液引流量的相关性。
1 资料与方法
1.1 一般资料 本研究收集了本院自2012年1月至2013年4月在体外循环下行先心病矫治术的1 164例患儿临床资料,根据年龄是否小于1岁及预充采用FFP或佳乐施分为婴儿血浆组(n=336)、婴儿佳乐施组(n=335)、幼儿血浆组(n=225)和幼儿佳乐施组(n=268)。资料排除标准为:采用除佳乐施外人工胶体液预充者,人工胶体液与FFP混合预充者,二次手术,急诊手术,术前凝血或肝肾功能障碍或数据资料不全者。
1.2 麻醉及体外循环方法 术中均采用气管内插管机械通气,采用以咪达唑仑、舒芬太尼、罗库溴铵为主静脉麻醉,或复合七氟烷吸入麻醉,常规行五导联心电图、脉搏血氧饱和度、桡动脉及中心静脉压力、鼻咽温、直肠温及尿量监测。主动脉插管前,给予400 IU/kg肝素抗凝,使得激活全血凝固时间(ACT)延长大于480 s,转机过程中多次测定并适时添加肝素以确保ACT大于480 s。停机后,给予4 mg/kg鱼精蛋白注射液以中和肝素作用。体外循环中统一使用Jostra HL20型体外循环机(德国MAQUET公司)、氧合器主要为Terumo CAPIOX RX05膜式氧合器(TerumoBaby-RX,Terumo Corporation,Tokyo,Japan)和Dideco 902膜式氧合器(D902 Lilliput 2,Dideco,Mirandola,Italy),采用阜外婴幼儿循环管道(中国天津塑料研究所,天津,中国)、一次性动脉微栓滤器(宁波费拉尔医疗用品有限公司,宁波,中国)和Jostra小儿超滤器(Maquet,Munich,Germany)。研究早期,常规采用浓缩红细胞100~150 ml及醋酸钠林格液(Baxter International,Inc.,Shanghai,China)50~100 ml及FFP 100~150 ml进行管路预充,实施无血浆预充策略后,采用4%琥珀酰明胶(Gelofusine;Braun Medical,Inc.,Suzhou,China)20~30 ml/kg替代FFP预充。转机过程中采用常规超滤,连续监测静脉血氧饱和度(SvO2)和红细胞比容(Hct),并根据胶体渗透压及血气分析评估患儿状况,个体化合理追加佳乐施。根据手术复杂程度及主动脉阻断时间控制温度,停机时复温到直肠温35.5°C以上,鼻咽温36.0°C以上。停机后,采用改良超滤技术。关胸时,剩余机血回输患儿体内。在鱼精蛋白完全中和肝素作用后,如果患儿异常出血不能被止血药物或纱布填塞纠正,则适量输注FFP或血小板(Plt)。ICU医生根据术后胸液引流量速度、血流动力学状况及实验室检查结果[Hct、Plt、纤维蛋白原、凝血酶原时间(PT)]等指导术后血制品的输注。
1.3 资料收集 查阅病历系统,记录患者一般资料,如年龄、术前体重、性别,采用RACHS-1(Risk Adjustment for Congenital Heart Surgery)评分系统评估先心病手术复杂程度,紫绀型根据术前诊断(法洛四联症、右室双出口、完全肺静脉异位引流、肺动脉闭锁、大动脉转位、三尖瓣闭锁等)并同时伴有血红蛋白(Hb)>150 g/L判断。同时,收集血液学指标(手术前后Hct、Plt及PT),术中资料(预充液成分、转机时间、升主动脉阻断时间、最低温度),止血药物用量(氨甲环酸、人纤维蛋白原、人凝血酶原复合物),术后胸液引流量(术后12 h及24 h胸液引流量),是否在住院期间死亡及存在术后并发症,记录体外循环及住院期间的红细胞(RBC)、FFP及Plt等血制品用量。
1.4 统计学处理 采用统计软件SPSS 19.0及SAS进行统计学处理,计数资料采用频率和率表示。计量资料采用Shapiro-Wilk检验评估其正态性,正态计量资料采用均数±标准差(±s)表示,非正态计量资料采用四分位数间距法表示。采用独立样本t检验或Mann-Whitney U检验比较两计量资料间差异,卡方检验用于两计数资料间率的比较。单变量线性回归分析影响术后胸液引流量的因素,其中P<0.05的变量纳入多变量线性回归分析。P<0.05认为差异有统计学意义。
2 结 果
2.1 一般资料和血液学指标 患儿一般资料和血液学指标数据如表1所示。在年龄、术前体重、性别、紫绀型比例及RACHS-1评分方面,婴儿血浆组和婴儿佳乐施组无显著性差异( P>0.05),幼儿血浆组和幼儿佳乐施组无显著性差异( P>0.05)。在术前Plt、术前Hct及PT、术后Plt方面,婴儿血浆组和婴儿佳乐施组比较差异无统计学意义( P>0.05),幼儿血浆组和幼儿佳乐施组比较差异无统计学意义( P>0.05)。婴儿佳乐施组的术后Hct(0.357±0.048)显著低于婴儿血浆组(0.365±0.050)( P<0.05)。
2.2 术中资料 患儿的术中资料如表2所示。婴儿佳乐施组的转机时间显著低于婴儿血浆组( P< 0.05),幼儿佳乐施组的转机时间和阻断时间均显著低于幼儿血浆组( P<0.05)。与婴儿血浆组相比,婴儿佳乐施组的预充RBC显著减少( P<0.01)。
2.3 术后凝血功能相关指标 术后凝血功能相关指标如表3所示。婴儿佳乐施组术后12 h及24 h胸液引流量均显著高于婴儿血浆组( P<0.05)。在体外循环及总住院期间的RBC和FFP用量方面,婴儿佳乐施组均显著少于婴儿血浆组( P<0.01),幼儿佳乐施组显著少于幼儿血浆组( P<0.01)。在总Plt用量及止血药物应用方面,婴儿血浆组和婴儿佳乐施组无显著性差异( P>0.05),幼儿血浆组和幼儿佳乐施组无显著性差异( P>0.05)。

表1 一般资料及血液学指标
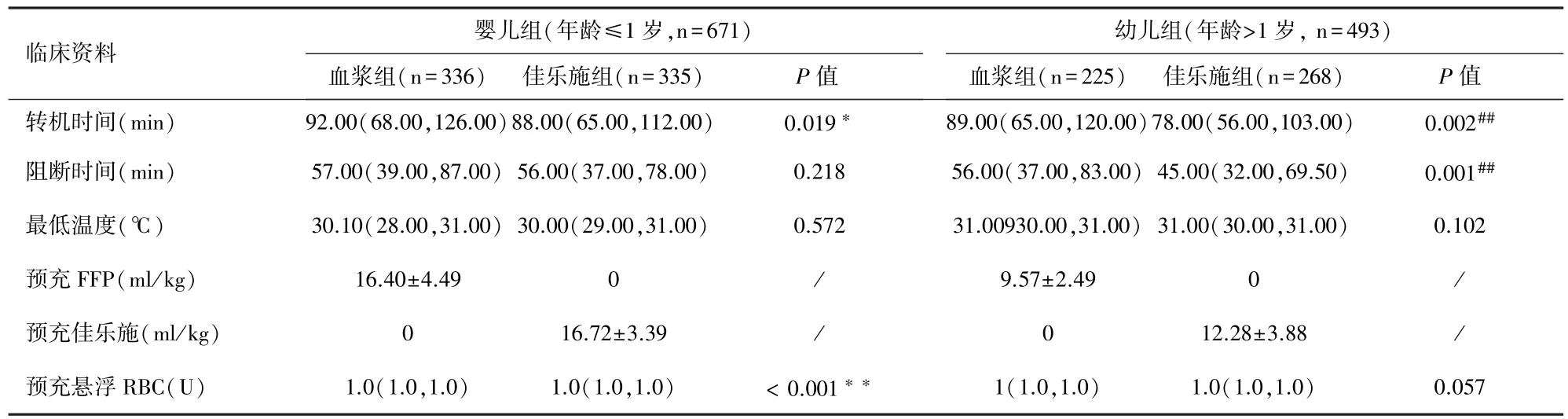
表2 术中资料
2.4 死亡率及并发症发生率 住院死亡率及并发症发生率如表3所示。在住院死亡率方面,婴儿佳乐施组3例(0.9%)与婴儿血浆组0例(0%)相比较无显著性差异( P>0.05),幼儿佳乐施组2例(0.9%)与幼儿血浆组0例(0%)相比较无显著性差异( P>0.05)。在术后腹膜透析和再次气管插管发生率方面,婴儿佳乐施组与婴儿血浆组相比较无显著性差异( P>0.05),幼儿佳乐施组与幼儿血浆组相比较无显著性差异( P>0.05)。婴儿佳乐施组的术后肺部感染率8例(2.4%)低于婴儿血浆组29例(8.6%)( P<0.01)。
2.5 回归分析 采用SAS软件分别对336例婴儿和225例幼儿的术后24 h胸液引流量进行单变量线性回归分析。对于幼儿,预充液类型(0=血浆,1=佳乐施)与术后24 h胸液引流量间的相关性无统计学意义(r=-0.15,P=0.67)。对于婴儿,预充液类型(0=血浆,1=佳乐施)与术后24 h胸液引流量显著正相关(r=1.71,P<0.001)。针对婴儿术后24 h胸液引流量,课题组进一步采用多因素线性回归分析。在排除多重共线性因素后,将单变量线性回归分析中P<0.05的独立变量:预充液类型(0=血浆,1=佳乐施)、年龄、转机时间、氨甲环酸、人纤维蛋白原和术后Plt采用进入法纳入多因素线性回归分析模型,分析结果如表4显示,婴儿术后24 h胸液引流量与预充液类型(0=血浆,1=佳乐施;β=1.940,P<0.001)和转机时间(min;β=0.024,P <0.001)显著正相关,与年龄(month;β=-0.257,P =0.002)显著负相关。
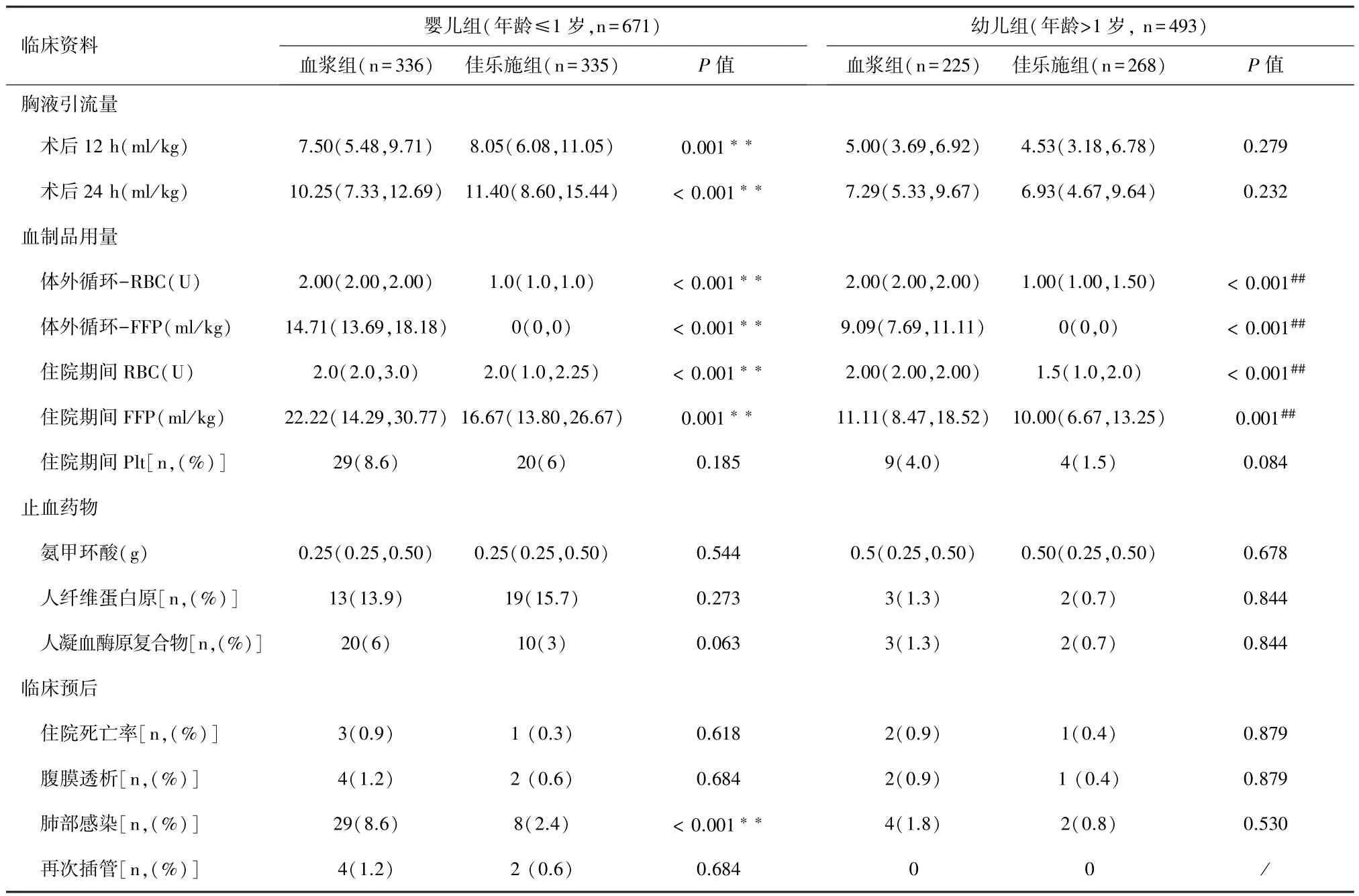
表3 术后凝血功能相关指标及不良事件
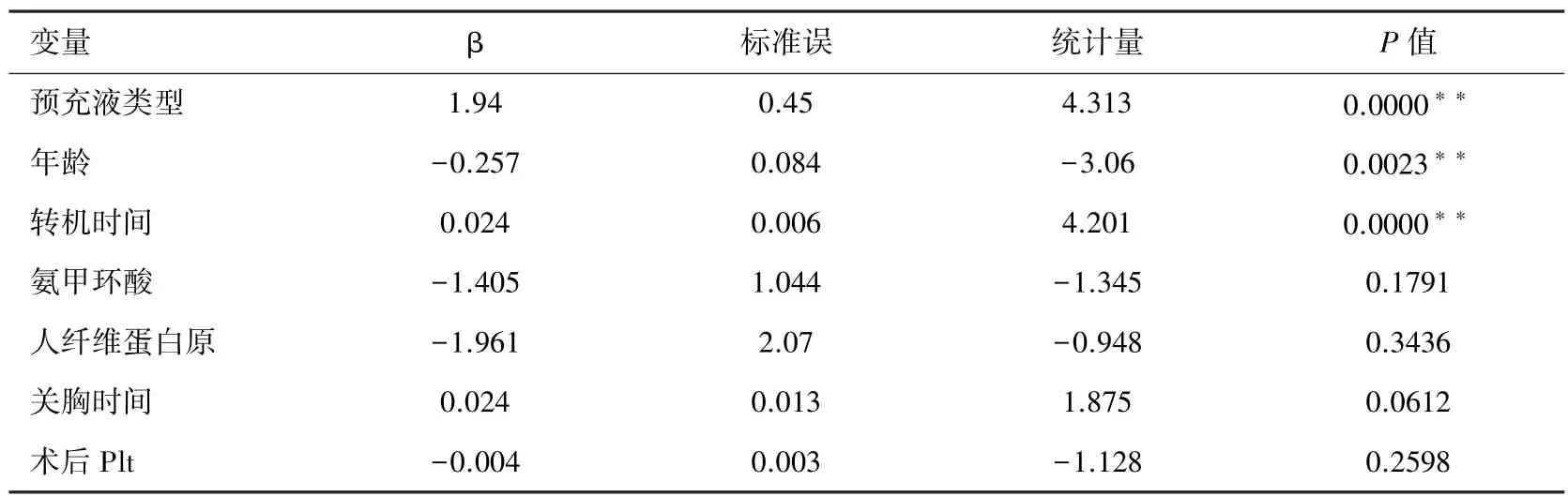
表4 婴儿术后24 h胸液引流量的多元线性回归结果
3 讨 论
在小儿体外循环中,人工胶体液能否替代FFP用于预充这一问题始终存在争议。本课题组回顾性分析阜外医院自2012年1月至2013年4月在体外循环下行先心病矫治术的患儿资料,基于不同年龄阶段患儿的发育特点不同,将婴儿与幼儿区分,比较采用FFP和佳乐施预充后的相关临床指标,以全面科学地评价人工胶体液替代FFP用于小儿体外循环预充的可行性。
在小儿先心病矫治术中,凝血功能障碍和血小板功能不全十分常见,停机后更易引起术后出血量增多等不良后果[6-7]。因此,国内外心脏中心广泛采用FFP用于小儿体外循环预充,以提供足够的纤维蛋白原[4],保障术后凝血功能。近年来,一系列随机对照研究及系统性综述并未证实患儿预防性输注FFP具有确切的临床获益,其在先心病患儿体外循环中的应用也饱受质疑[4,8-9]。在本课题组前期完成的前瞻性临床试验中,将80例6个月至3岁先心病患儿随机纳入两种不同预充方案组,应用血栓弹力图分别监测术前、转中与停机后的凝血功能,结果表明,与佳乐施预充组相比,血浆预充组在停机后或术后纤维蛋白原含量(FLEV)及由纤维蛋白原产生的振幅(MAf)数值显著升高,即纤维蛋白原浓度显著较高,但两组的术后胸液引流量和血制品用量并无统计学差异,再次证实预防性输注FFP并未产生确切的临床获益[10]。
本次回顾性研究中,幼儿佳乐施组与幼儿血浆组相比,在体外循环及总住院期间的血制品用量显著降低,在胸液引流量、总Plt用量及止血药物应用方面无显著性差异。先心病患儿围术期血制品用量较大,主要包括术中血制品输注及术后因止血不确切或凝血功能障碍引起的血制品输注。本研究中,采用新型预充策略后围术期血制品总用量显著减少,主要有以下两方面原因。一方面,体外循环期间血制品用量占据总用量的很大比重,新型预充策略导致体外循环血制品用量显著减少,进而使总用量减少。另一方面,新型人工胶体预充策略并未对术后凝血功能产生显著不利影响:尽管婴儿佳乐施组与婴儿血浆组相比较,术后胸液引流量增加,术后Hct显著降低,但其水平仍在小儿术后可接受范围内,因此并未导致输注血制品或使用止血药物等临床治疗措施。在血制品用量庞大的先心病手术领域,体外循环预充策略的改进是节约用血策略的重要环节[11]。本研究证实了人工胶体液替代血浆用于小儿体外循环这一策略有利于减少血制品用量。
在针对术后胸液引流量的回归分析中,幼儿术后24 h胸液引流量与预充液类型无显著相关性,但婴儿术后24 h胸液引流量与预充液类型显著正相关,这可能与小于1岁的婴儿凝血功能发育不完善和对人工胶体输注的影响敏感性强有关。以往研究报道,佳乐施可能会损害Plt功能,降低von Willebrand和VIII:c因子浓度[12],可能对凝血功能存在抑制作用。此外,多因素线性回归分析表明婴儿术后24 h胸液引流量与转机时间显著正相关,与年龄显著负相关。因此,对于特殊因素高危患儿,如低龄、转机时间长、术前已有凝血功能障碍等,建议谨慎应用人工胶体液,同时重视对于术后胸液引流量的监测,应及时进行实验室凝血功能检查,或采用更为快速高效的血栓弹力图检测[13],合理使用止血药物或输注FFP。
本次研究表明,采用佳乐施替代FFP用于小儿体外循环后,对死亡率和术后并发症发生率并未产生不利后果。这些结果与本课题组两项前瞻性研究结果一致[10,14]。佳乐施本身相对分子质量较低(18 ~27 kDa),可快速经肾小球过滤以及被蛋白酶水解,不易在体内蓄积,在目前临床应用的多种人工胶体液中,佳乐施对重要脏器的不利影响相对较小[15]。在Lancet杂志中,一项针对776例早产儿输注佳乐施或FFP的多中心对照研究结果显示,血浆输注组两年内死亡率(21.0%)和佳乐施输注组两年内死亡率(24.9%)无显著差异,证明预防性输注FFP并未显著改善早产儿存活率[16]。在Intensive Care Medicine杂志中一项最新meta分析同样证实,在液体急救复苏中,佳乐施替代传统白蛋白是安全的,即使在大剂量应用佳乐施的亚组中(累计剂量≥30 ml/kg),总体死亡率和并发症发生率也未显著增加[17]。本研究进一步证实对于接受常规择期先心病矫治术的一般患儿,采用佳乐施替代FFP用于体外循环预充后,对住院死亡率和术后并发症的发生率并未造成显著不利影响。尽管如此,在小儿先心病手术中,应严格参照临床指南,合理适量使用人工胶体液,防止过量输注的不良后果,同时密切关注术后重要脏器功能,及时发现并处理相关并发症。
本研究存在三方面局限性。首先,研究并非随机对照试验,影响最终结果的混杂因素仍可能存在。其次,由于本科室研究期间使用其它胶体的数据较少,研究并未评估其它胶体用于小儿体外循环的可行性。第三,所有数据取自医院数据库,用于分析的指标有限,例如,对于复杂先心病矫治术中患儿,体外循环医师在实际管理中均及时监测胶体渗透压,从而指导人工胶体液的合理应用,但对于简单先心病矫治术中的患儿,体外循环医师常常根据临床经验管理人工胶体液的应用,因此导致了本次病历资料中胶体渗透压的数据不足,限制了评估小儿体外循环中佳乐施替代FFP的全面性。
4 结 论
在小儿体外循环中,预防性输注血浆并未产生显著的临床获益。对于常规择期先心病矫治术患儿,根据临床指南合理应用人工胶体液替代FFP用于体外循环预充是安全可行的。但对于某些高危患儿,建议谨慎应用人工胶体液,密切监测术后临床指标,保障患儿安全。
参考文献:
[1]Seghaye MC,Grabitz RG,Duchateau J,et al.Inflammatory reaction and capillary leak syndrome related to cardiopulmonary bypass in neonates undergoing cardiac operations[J].J Thorac Cardiovasc Surg,1996,112(3):687-697.
[2]Hornykewycz S,Odegard KC,Castro RA,et al.Hemostatic consequences of a non-fresh or reconstituted whole blood small volume cardiopulmonary bypass prime in neonates and infants[J].Paediatr Anaesth,2009,19(9):854-861.
[3]Tanaka KA,Taketomi T,Szlam F,et al.Improved clot formation by combined administration of activated factor VII(NovoSeven) and fibrinogen(Haemocomplettan P)[J].Anesth Analg,2008,106(3):732-738.
[4]McCall MM,Blackwell MM,Smyre JT,et al.Fresh frozen plasma in the pediatric pump prime:a prospective,randomized trial[J].Ann Thorac Surg,2004,77(3):983-987.
[5]Pandey S,Vyas GN.Adverse effects of plasma transfusion[J].Transfusion,2012,52 Suppl 1:65S-79S.
[6]Eaton MP,Iannoli EM.Coagulation considerations for infants and children undergoing cardiopulmonary bypass[J].Pediatric Anesthesia,2011,21(1):31-42.
[7]Williams GD,Bratton SL,Riley EC,et al.Coagulation tests during cardiopulmonary bypass correlate with blood loss in children undergoing cardiac surgery[J].J Cardiothorac Vasc Anesth,1999,13(4):398-404.
[8]Lee JW,Yoo YC,Park HK,et al.Fresh frozen plasma in pump priming for congenital heart surgery:evaluation of effects on postoperative coagulation profiles using a fibrinogen assay and rotational thromboelastometry[J].Yonsei Med J,2013,54(3):752-762.
[9]Yang L,Stanworth S,Hopewell S,et al.Is fresh-frozen plasma clinically effective?An update of a systematic review of randomized controlled trials[J].Transfusion,2012,52(8):1673-1686.
[10]Miao X,Liu J,Zhao M,et al.Evidence-based use of FFP:the influence of a priming strategy without FFP during CPB on postoperative coagulation and recovery in pediatric patients[J].Perfusion,2015,30(2):140-147.
[11]Van der Linden P,Dumoulin M,Van Lerberghe C,et al.Efficacy and safety of 6%hydroxyethyl starch 130/0.4(Voluven) for perioperative volume replacement in children undergoing cardiac surgery:a propensity-matched analysis[J].Crit Care,2015,19:87.
[12]Levi M,Jonge Ed.Jonge.Clinical relevance of the effects of plasma expanders on coagulation[J].Semin Thromb Hemost,2007,33(8):810-815.
[13]Girdauskas E,Kempfert J,Kuntze T,et al.Thromboelastometrically guided transfusion protocol during aortic surgery with circulatory arrest:A prospective,randomized trial[J].J Thorac Cardiovasc Surg,2010,140(5):1117-1124.
[14]Miao X,Liu J,Zhao M,et al.The influence of cardiopulmonary bypass priming without FFP on postoperative coagulation and recovery in pediatric patients with cyanotic congenital heart disease[J].Eur J Pediatr,2014,173(11):1437-1443.
[15]Bailey AG,McNaull PP,Jooste E,et al.Perioperative crystalloid and colloid fluid management in children:where are we and how did we get here[J]?Anesth Analg,2010,110(2):375-390.
[16]No authors listed.Randomised trial of prophylactic early fresh-frozen plasma or gelatin or glucose in preterm babies:outcome at 2 years.Northern Neonatal Nursing Initiative Trial Group[J].Lancet,1996,348(9022):229-232.
[17]Thomas-Rueddel DO,Vlasakov V,Reinhart K,et al.Safety of gelatin for volume resuscitation--a systematic review and meta-analysis[J].Intensive Care Medicine,2012,38(7):1134-1142.
(修订日期:2015-12-08)
(收稿日期:2015-12-03)
通讯作者:刘晋萍,Email:jinpingfw@ Hotmail.com
基金项目:北京市科技计划首都临床特色应用研究(Z131107002213172)
DOI:10.13498/j.cnki.chin.j.ecc.2016.01.02
作者单位:100037北京,中国医学科学院,北京协和医学院,国家心血管病中心,阜外医院体外循环科

