影响促红细胞生成素治疗老年低危骨髓增生异常综合征疗效持续时间的因素
毛淑丹 吕 芳 金捷萍
(辽宁医学院附属一院血液科,辽宁 锦州 121001)
影响促红细胞生成素治疗老年低危骨髓增生异常综合征疗效持续时间的因素
毛淑丹吕芳金捷萍
(辽宁医学院附属一院血液科,辽宁锦州121001)
〔摘要〕目的探讨促红细胞生成素(EPO)治疗老年低危骨髓增生异常综合征(MDS)患者疗效持续时间的影响因素。方法回顾性分析64例老年低危MDS患者应用EPO治疗,皮下注射,50 000 U/w,12 w评估疗效,继续巩固维持治疗,随访时间8~75个月。评定低危MDS患者血清EPO水平、输血依赖、骨髓原始细胞数、开始治疗的时间等因素与疗效持续时间的关系。结果单因素分析治疗前非难治性贫血伴有原始细胞过多(RAEB)-1亚型、血清EPO水平低、非输血依赖、开始治疗时间<6个月与疗效持续时间相关。多因素分析EPO水平低、非输血依赖、开始治疗时间<6个月是影响疗效持续时间的主要因素。结论对于老年低危MDS患者的EPO早期治疗、血清低EPO水平及非输血依赖者疗效持续时间长,且副作用小。
〔关键词〕促红细胞生成素;骨髓增生异常综合征;低危; 疗效持续时间
骨髓增生异常综合征(MDS)是起源于造血干细胞的一组异质性髓系恶性克隆性疾病。主要发生于老年人群,表现为无效造血、难治性血细胞减少、造血衰竭,高风险向急性髓系白血病(AML)转化。尽管MDS目前尚缺乏有效的标准治疗方案,原则是刺激残存正常造血干/祖细胞的造血功能,减少或脱离血制品输注,改善生活质量〔1,2〕。促红细胞生成素(EPO)作为治疗方法之一已达成对低危MDS治疗的中国专家共识。本文分析老年低危MDS患者经EPO治疗后疗效持续时间相关因素。
1对象与方法
1.1研究对象2007年1月至2013年2月就诊于辽宁医学院附属第一医院血液科的老年低危MDS患者64例,男38例,女26例,年龄60~86(平均68)岁。均行骨髓细胞形态、骨髓活检、染色体检查后诊断分型,可评估的为63例,1例因副作用终止治疗,未纳入评估体系,其中难治性贫血(RA)11例,难治性贫血伴有环状铁粒幼细胞(RAS)6例,难治性血细胞减少伴有多系发育异常(RCMD)25例(其中伴环铁增多9例),难治性贫血伴有原始细胞过多-1(RAEB-1)21例。 按国际预后积分系统(IPSS)评分≤1.0分的低危组和中危-1组,低危组29例,中危-1组34例。诊断分型标准参照MDS诊断与治疗专家共识〔3〕及《血液病诊断及疗效标准》〔4〕。
1.2方法
1.2.1治疗治疗前所有患者均有贫血(男性血红蛋白<90 g/L,女性<80 g/L)。应用EPO皮下注射10 000 U/d,5次/w。12 w后评估疗效。原剂量巩固治疗8 w,以后每2 w减量10 000 U,最后20 000 U/w维持,观察反应持续时间及药物不良反应。
1.2.2观察指标性别、年龄、IPSS评分、MDS分型、治疗前EPO水平(<100 U/L、100≤EPO<500 U/L和≥500 U/L)、是否输血依赖、诊断到开始治疗的时间(< 6个月和≥6个月),EPO治疗疗效持续时间。
1.2.3疗效标准根据MDS诊断与治疗专家共识,评估红系反应。有效:血红蛋白升高≥15 g/L;如治疗前需红细胞输注者,红细胞输注减少,与治疗前比较,每8 w输注量至少减少4个单位。疾病进展或复发:血红蛋白下降≥15 g/L或依赖输血。持续测定对EPO的反应时间至疾病进展或复发。
1.2.4随访截止日期为2013年2月1日,随访时间8~75个月,中位随访时间35个月,随访资料来源于门诊、住院及电话追踪随访。
1.3统计学方法采用SPSS17.0统计软件行Pearsonχ2检验。单因素分析采用Log-rank统计方法。多因素分析采用COX回归分析。
2结果
2.1有效率64例老年低危MDS患者,1例因副作用终止治疗,其余63例经 EPO治疗后的总体反应率为52%(33/63)。治疗前不同血清EPO水平(<100 U/L,100~500 U/L,≥500 U/L)疗效分别为67%(20/30),38%(8/21),17%(2/12)(P=0.007);MDS类型RA、RAS、RCMD、RCMD-RS、RAEB-1有效率分别为55%(6/11),67%(4/6),50%(8/16),67%(6/9),43%(9/21)。伴有环状铁粒幼红细胞组(RAS和RCMD-RS)有效率67%(10/15)与其他三种类型之间有效率有明显差异(P=0.048);诊断后<6个月与≥6个月治疗的有效率分别为67%(20/30),36%(12/33)(P=0.023);非输血依赖与输血依赖有效率分别为65%(31/48),33%(5/15)(P=0.041)。EPO疗效与年龄、性别、IPSS分组(低危组、中危-1组)红系反应率无统计学差异(P>0.05)。
2.2持续反应时间平均随访28个月,平均持续反应时间23.6个月(0~73个月)。治疗前低血清EPO水平(<100 U/L,100~500 U/L,≥500 U/L)平均持续疗效时间分别为26.8,17.1,11.4个月;MDS类型RA、RAS、RCMD、RCMD-RS、RAEB-1平均持续疗效时间分别为26.2,27.8,23.0,24.1,14.6个月。诊断后<6个月与≥6个月治疗的持续有效时间分别为26.3,15.2个月。单因素分析在6个月内开始治疗时间(P=0.010)、非输血依赖(P=0.049)、低EPO水平(P=0.017)、骨髓原始细胞正常(即非RAEB-1型,P=0.047)有统计学意义(图1)。而年龄、性别、IPSS评分、WHO分型(非RAEB-1各亚型间)及伴环状铁粒幼红细胞的MDS与其他亚型间对疗效持续时间无影响。多因素分析显示,早期治疗、低EPO水平和非输血依赖EPO治疗反应持续时间显著增长。见表1。
2.3副作用64例在EPO治疗过程中仅5例出现血压增高,1例出现骨痛,经对症处理后3例好转,1例终止治疗。其余患者未见明显副作用发生。
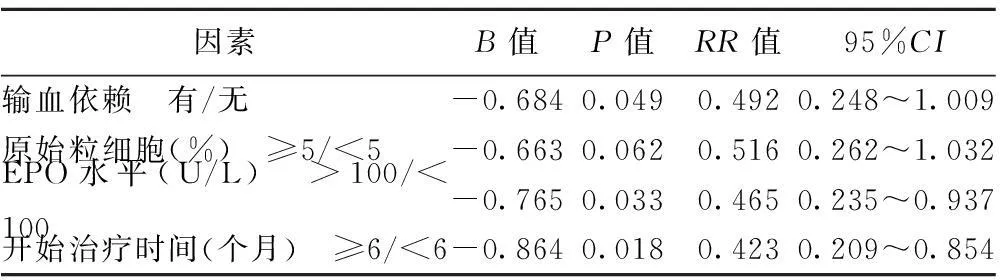
表1 COX回归分析疗效持续时间

图1 持续疗效时间的影响因素单因素分析
3讨论
MDS是一种老年性血液系统疾病,是以髓系细胞分化和成熟异常、骨髓衰竭为特征的髓系肿瘤。贫血在MDS普遍存在,目前研究认为,低危MDS贫血主要是红系祖细胞的凋亡,EPO可以可逆转白细胞介素(IL)-1、肿瘤坏死因子(TNF)等炎性因子对红系的抑制,促进红系增殖并促使红系祖细胞分化成熟〔5,6〕。老年MDS患者随年龄增加,各脏器功能逐渐衰减,同时多半有其他器官疾病,对贫血耐受能力减低,患者生活质量降低及心功能不全的发生概率增加。MDS治疗的主要是解决骨髓衰竭和并发症、急性髓细胞白血病转化。低危MDS病程相对缓慢,向髓系白血病转化概率明显低于高危MDS,因此,改善血细胞减少的程度提高生活质量和脱离输血依赖减少并发症是低危MDS患者治疗的首要目标。有资料显示EPO治疗较低危MDS可改善骨髓红系造血,提升血红蛋白水平,改善总体生存率,且不增加白血病转化率〔7~9〕。因此EPO越来越多的用于较低风险MDS贫血的治疗中。本研究显示红系的反应率与治疗前低血清EPO水平、非输血依赖明显相关,与文献〔10〕报道结果相似。在低危MDS亚型中,伴有环形铁粒幼红细胞增高的显示较高的疗效。EPO治疗在诊断后6个月内开始可提高老年低危MDS的血红蛋白水平,减少因贫血导致的并发症的发生,可在明显延缓贫血并发症的发生,改善MDS的预后。
EPO 的早期介入可延缓低危MDS疾病进程,延长其红细胞输注依赖时间〔11〕。本研究结果显示骨髓原始细胞水平、是否非输血依赖、治疗时机及血清EPO水平是影响EPO治疗疗效持续时间的主要因素。
EPO的生物学效应是通过骨髓红系组细胞表面特意受体介导来完成的。赵婷等〔12〕研究结果表明低危MDS患者红系祖细胞EPO受体表达正常,而血清EPO水平却明显不足。本研究结果证实EPO在低危MDS可以刺激正常的红系祖细胞增殖、分化,尤其在早期正常红系祖细胞减少前是非常重要的。应用EPO治疗老年低危MDS可以提升血红蛋白水平,并且在低血清EPO水平、较早治疗的患者获得较长的反应持续时间,延缓输血依赖的发生,改善患者的生活质量。
MDS老年多见,且以预后较差RCMD、RAEB-1和RAEB-2三种亚型居多〔13〕。且老年MDS患者并发其他系统疾病较多,治疗方法有限,本组老年低危MDS患者应用EPO治疗取得较好疗效,降低因贫血所致的心血管事件发生风险,且副作用不明显。即使在EPO水平增高的患者也收到一定疗效,因此对于以贫血为主的老年MDS患者,即使EPO水平大于500 U/L,但无其他合适治疗选择,仍可试用EPO治疗。
4参考文献
1Hellstrom-Lindberg E,Birgegard G,Garlsson M,etal.A combination of granulo-cyte colony-stimulatingfactor and erythropoietin may synergisticallyimprove the anaemia in patients with myelodysplasticsyndromes 〔J〕.Leuk Lymphoma,1993;11(3-4):221-8.
2Hellstrom-Lindberg E,Ahlgren T,Beguin Y,etal.Treatment of anemia in mye-lodysplastic syndromes with granulocyte colony-stimulating factor plus erythropoietin:results form a randomized phase Ⅱ study and long-term follwup of 71 patients〔J〕.Blood,1998;92(1):68-75.
3中华医学会血液学分会.骨髓增生异常综合征诊断与治疗专家共识〔J〕.中华血液学杂志,2012;33(4):347-52.
4张之南,沈悌.血液病诊断及疗效标准〔M〕.第3版.北京:科学出版社,2007:157-63.
5Jonckeere S,Dierieck J,Vanhouteghem H.Erythrocyte indices in the assessment of iron status in dialysis-dependent patients with end-stsge renal disease on continuous erythropoietin activator versus epoetin beta therapy〔J〕.Haematology,2010;124:27-33.
6Komblan SM,Mccue D,Singh N.Recurrent expression signatures of cytokines and chemokines are present and are independently prognostic in acute myelogenous leukemia and mylodysplasia〔J〕.Blood,2010;38(3):188-91.
7Jädersten M,Montgomery SM,Dybedal I,etal.Longterm outcome of treatment of anemia in MDS with erythropoietin and G-CSF〔J〕.Blood,2005;106(3):830-11.
8Jädersten M,Malcovati L,Dybedal I,etal.Erythropietin and granulocyte-coiny stimunlating factor treatment associated with improved surival in myelody-splastic syndrome〔J〕.J Clin Oncol,2008;26(21):3607-13.
9Musto P,Lanza F,Balleari E,etal.Darbepoetin alpha for the treatment of anaemia in low-intermediate risk myelodyspastic syndromes〔J〕.Br J Haematol,2005;128(2):204-9.
10Terpos E,Mougiou A,Kouraklis A,etal.Prolonged adminstration of erythropietin increases erythroid respoine rate in myelodysplastic syndromes:a Ⅱ trial in 281 patients〔J〕.Br J Haematol,2002;118:174-80.
11Sophie P,Charikleia K,Rosa S,etal.Early introduction of ESA in low risk MDS patients may delay the need for RBC transfusion:a retrospective analysis on 112 patients〔J〕.Leukemia Res,2010;34:1430-6.
12赵婷,宋强,李丽珍,等.骨髓增生异常综合征患者EPO水平的测定及受体的表达〔J〕.山东大学学报(医学版),2011;49(1):67-70.
13隗佳,陈燕.老年骨髓增生异常综合征的临床特点和预后分析〔J〕.中国老年学杂志,2009;29(1):91-4.
〔2014-09-25修回〕
(编辑安冉冉/曹梦园)
〔中图分类号〕R556.9
〔文献标识码〕A
〔文章编号〕1005-9202(2016)07-1700-03;
doi:10.3969/j.issn.1005-9202.2016.07.075
通讯作者:金捷萍(1962-),女, 教授,硕士生导师, 主要从事血液系统肿瘤诊治研究。
第一作者:毛淑丹(1978-),女,主治医师,硕士,主要从事血液系统肿瘤诊治研究。

