燃料对燃烧法制备Ni-Al2O3催化剂结构及浆态床甲烷化催化性能的影响
吉可明, 孟凡会, 高 源, 李 忠
(太原理工大学, 煤科学与技术教育部和山西省重点实验室, 太原 030024)
燃料对燃烧法制备Ni-Al2O3催化剂结构及浆态床甲烷化催化性能的影响
吉可明, 孟凡会, 高源, 李忠
(太原理工大学, 煤科学与技术教育部和山西省重点实验室, 太原 030024)
摘要分别采用浸渍燃烧法和共燃烧法制备了一系列Ni-Al2O3催化剂, 并对催化剂进行了表征, 研究了燃料种类对不同方法制备的催化剂结构及浆态床CO甲烷化性能的影响. 结果表明, 以尿素、甘氨酸和乙二醇为燃料时, 采用浸渍燃烧法制备的Ni-Al2O3催化剂织构性质均与载体相近, 各催化剂金属Ni分散度和Ni晶粒相差不大, 甲烷化性能接近, 在260 ℃反应温度下CO转化率在80.1%~83.5%之间. 而共燃烧法制备的Ni-Al2O3催化剂受燃烧过程影响明显, 以甘氨酸和乙二醇为燃料时制得的催化剂比表面积较小, 金属Ni分散度低且Ni晶粒较大, 因而甲烷化活性较低; 以尿素为燃料制备的催化剂比表面积大且Ni晶粒较小, CO转化率和CH4选择性分别达到84.7%和91.1%.
关键词浆态床甲烷化; Ni-Al2O3催化剂; 浸渍燃烧法; 共燃烧法; 燃料
天然气的主要成分为CH4, 其热值高, 使用清洁, 近年来需求增长迅速[1]. 通过煤气化和甲烷化过程可以合成天然气, 甲烷化反应放热大, 催化剂床层易局部过热导致催化剂烧结[2]. 工业甲烷化工艺均在固定床反应器中进行, 需要通过多级反应器串联和尾气循环的方式控制床层温度, 工艺流程复杂且能耗高. 浆态床反应器将催化剂悬浮于惰性液相介质中, 可及时移除反应热, 避免催化剂烧结失活. 近年来, 在浆态床中进行甲烷化反应的研究[3~7]逐渐增多. 浆态床甲烷化反应温度一般在350 ℃以下[7,8], 而针对固定床甲烷化工艺开发的商业Ni基催化剂在低温浆态床甲烷化反应中催化活性较差[9,10]; 采用浸渍法制备的Ni/Al2O3催化剂甲烷化性能在280 ℃时CO转化率和CH4选择性仅为82.5%和87.4%[10]. 开发具有更高低温活性和稳定性的Ni基催化剂是浆态床甲烷化工艺的关键.
燃烧法是在制备无机材料时需加入一定量的有机物, 借助有机物燃烧时放出大量的热来制备材料, 该法具有制备周期短、操作简便、产品颗粒小且组成均匀等优点[11~15]. 燃烧法的特点是用氧化还原反应制备无机材料, 反应温度较高, 释放的热量和气体量较大, 通过改性燃烧法可获得性能更好的氧化物材料. 对于由活性组分和载体组成的负载型催化剂, 可采用浸渍燃烧法和共燃烧法制备. 其中浸渍燃烧法可以采用商品氧化物载体, 制得的催化剂具有稳定的织构性质和较高的催化性能. Shi等[16]采用浸渍燃烧法制备的Co/SiO2催化剂的Co3O4粒径(10 nm)明显小于浸渍法制备的Co3O4粒径(32 nm), 因而前者催化剂的费托合成反应活性是后者的3倍. Yan等[17]采用共燃烧法制备的Co/CeO2催化剂具有中孔结构且比表面积和Co分散度较高, 且Co与载体相互作用较强, 因而在CO优先氧化反应中CO转化率可达100%. Colussi等[18]制备了Pd-CeO2催化剂, 其动力学研究表明, 采用共燃烧法制备的催化剂活性高于浸渍法制备的催化剂, 这主要是由于前者制备的催化剂存在较多的Pd活性中心和纳米Pd颗粒, 因而具有更高的催化活性.
Ni基催化剂目前仍是研究甲烷化反应的优选催化剂[1,2,19]. 在前期研究中发现, 以尿素为燃料, 采用共燃烧法[20]制备的Ni-Al2O3催化剂的催化性能优于以ZrO2, La2O3和CeO2为载体的Ni基催化剂活性. 本文以尿素、甘氨酸和乙二醇为燃料, 分别采用浸渍燃烧法和共燃烧法制备Ni-Al2O3催化剂, 并研究催化剂的浆态床CO甲烷化性能, 探讨燃料种类对2种制备方法的Ni基催化剂的织构性质、金属Ni分散度、Ni物种与载体的相互作用等的影响, 阐明催化剂结构与甲烷化活性之间的匹配关系.
1实验部分
1.1试剂
硝酸镍(纯度>98%, 国药集团化学试剂有限公司); 硝酸铝(纯度>99%, 天津市光复精细化工研究所); 尿素、甘氨酸和乙二醇(纯度>99%, 天津市风船化学试剂科技有限公司);γ-Al2O3载体(比表面积191 m2/g, 山东铝业).
1.2催化剂的制备
1.2.1浸渍燃烧法制备催化剂将6.2 g硝酸镍溶解于5 mL去离子水中, 加入适量的燃料, 如尿素(U)、甘氨酸(G)或乙二醇(E), 并完全溶解. 加入5 gγ-Al2O3载体连续搅拌, 在室温下浸渍24 h. 将悬浊液倒入坩锅中并置于300 ℃的马弗炉中加热, 一段时间后悬浊液自行点燃, 燃烧结束后将产物冷却至室温, 收集得到NiO-Al2O3催化剂. 按照燃料的不同分别记为NiAl-IU, NiAl-IG和NiAl-IE. 催化剂中金属Ni质量分数为25%. 燃料与硝酸盐用量根据燃烧反应的化学计量比[21]进行计算.
1.2.2共燃烧法制备催化剂称取6.2 g硝酸镍和36.8 g硝酸铝并加入少量去离子水搅拌溶解, 加入一定量的燃料并搅拌. 将溶液倒入坩锅中并放入300 ℃的马弗炉中加热, 一段时间后自行点燃, 燃烧结束后将产物冷却至室温, 收集得到NiO-Al2O3催化剂, 按照燃料不同分别记为NiAl-CU, NiAl-CG或NiAl-CE. 催化剂中金属Ni质量分数为25%, 其中燃料用量计算方法与浸渍燃烧法相同.
1.3催化剂的反应性能评价
将催化剂在固定床中于550 ℃常压下还原4 h, 采用V(H2)∶V(N2)=1∶4还原气体, 流速125 mL/min. 将还原后的2 g催化剂和120 mL液体石蜡加入到250 mL高压反应釜中, 在反应温度260 ℃, 反应压力1.0 MPa, 原料气V(H2)∶V(CO)=3∶1, 空速3000 mL·g-1·h-1, 反应釜搅拌速率750 r/min条件下进行活性评价. 反应釜排出的气体经过2 ℃的冷凝液冷却, 使反应中生成的水冷凝成液体, 不凝性气体通过气液分离后进入自动取样阀取样分析. 气体分析采用三阀四柱气相色谱(Aglient 7890A)在线分析, 以He气为载气, 采用毛细管HP-AL/S柱(30 m×530 μm×15 μm)和氢火焰离子检测器(FID)分析C1~4烃类产物; 以He气为载气, 采用填充柱PORAPAK Q为预分离柱, 毛细管柱HP-PLOT/Q(30 m×530 μm×40 μm)、HP-MOLESIEVE(30 m×530 μm×25 μm)和热导池检测器(TCD)分析CO, CO2和N2等气体. 采用外标法计算气体中各组分的含量.
1.4催化剂的表征
氮气吸附采用3H-2000PS2型静态容量法比表面积及孔径分析仪进行, 样品在30 Pa, 130 ℃脱气1 h. 在液氮温度吸附氮气, 用BET公式计算比表面积.
X射线衍射(XRD)采用DX-2007型X射线衍射仪, CuKα射线(λ=0.15418 nm), 石墨单色器, 管电压和管电流分别为40 kV和30 mA, 扫描范围10°~85°.
透射电镜(TEM)采用JEM-2100F型场发射透射电子显微镜, 加速电压200 kV, 将样品分散在乙醇中超声10 min后, 将悬浮液滴在铜网上制样.
程序升温还原H2-TPR采用AutochemⅡ2920型全自动程序升温化学吸附仪进行分析. 将约20 mg样品置于U型石英反应管中, 通入Ar气, 流速为50 mL/min, 以10 ℃/min速率升温至350 ℃, 恒温吹扫40 min, 降温至100 ℃, 切换V(H2)∶V(Ar)=1∶9混合气体, 流速50 mL/min, 待基线稳定后, 以10 ℃/min升温至800 ℃, H2的消耗量用TCD检测.
H2化学吸附采用AutochemⅡ2920型全自动程序升温化学吸附仪测定. 将约500 mg样品置于U型石英反应管中, 通入V(H2)∶V(Ar)=1∶9气氛, 流速50 mL/min, 以10 ℃/min的升温速率升温至550 ℃, 恒温还原4 h, 降温至120 ℃, Ar气氛吹扫1 h, 降温至50 ℃, 基线平稳后, 每3 min进行一次V(H2)∶V(Ar)=1∶9 气氛的脉冲吸附, 进行15次脉冲, 吸附信号用TCD检测. 根据H2吸附量分别计算得到催化剂金属Ni的分散度和表面积.
2结果与讨论
2.1催化剂燃烧过程分析
图1(A)~(C)为浸渍燃烧法制备催化剂的燃烧过程. 图1(A)是以尿素为燃料浸渍制备NiAl-IU催化剂, 可以看出, 悬浊液蒸干后火焰由四周向中间平缓连续地蔓延, 燃烧过程持续20 s, 产物为多孔固体; 图1(B)是以甘氨酸为燃料制备NiAl-IG催化剂, 燃烧过程中出现阴燃, 且燃烧不充分, 持续时间为14 s; 图1(C)是以乙二醇为燃料制备NiAl-IE催化剂, 该过程中出现明亮的火焰, 火焰由样品的一侧逐渐蔓延, 燃烧后形成疏松的固体. 图1(D)~(F)为共燃烧法制备催化剂的燃烧过程. 图1(D)是以尿素为燃料制备的NiAl-CU催化剂, 可以看出, 前驱体出现了明显的起泡现象, 随后出现烟雾及明亮的火焰, 燃烧持续23 s; 以甘氨酸为燃料时[图1(E)], 前驱体起泡后出现阴燃, 释放出棕黄色气体, 样品泡沫膨胀并凝固, 在9 s时形成蓬松的固体产物; 以乙二醇为燃料时[图1(F)], 前驱体泡沫引燃后火焰迅速蔓延, 5 s内即燃尽, 形成不规则的固体产物.

Fig.1 Images of catalysts prepared by different fuels and methods(A) NiAl-IU; (B) NiAl-IG; (C) NiAl-IE; (D) NiAl-CU; (E) NiAl-CG; (F) NiAl-CE.
2.2催化剂的织构性质
对燃烧法制备的催化剂进行N2吸附-脱附表征, 测得的吸附-脱附等温线如图2所示. 对于浸渍燃烧法制备的Ni基催化剂, 按照IUPAC分类方法, 其吸附-脱附等温线为Ⅳ型等温线, 表明催化剂具有中孔结构[22]. 采用共燃烧法制备的Ni基催化剂具有不同类型的吸附-脱附曲线, 其中NiAl-CU和NiAl-CE催化剂具有Ⅰ型等温线, 属于微孔结构[22], 而NiAl-CG催化剂具有Ⅳ型等温线, 属于中孔结构.
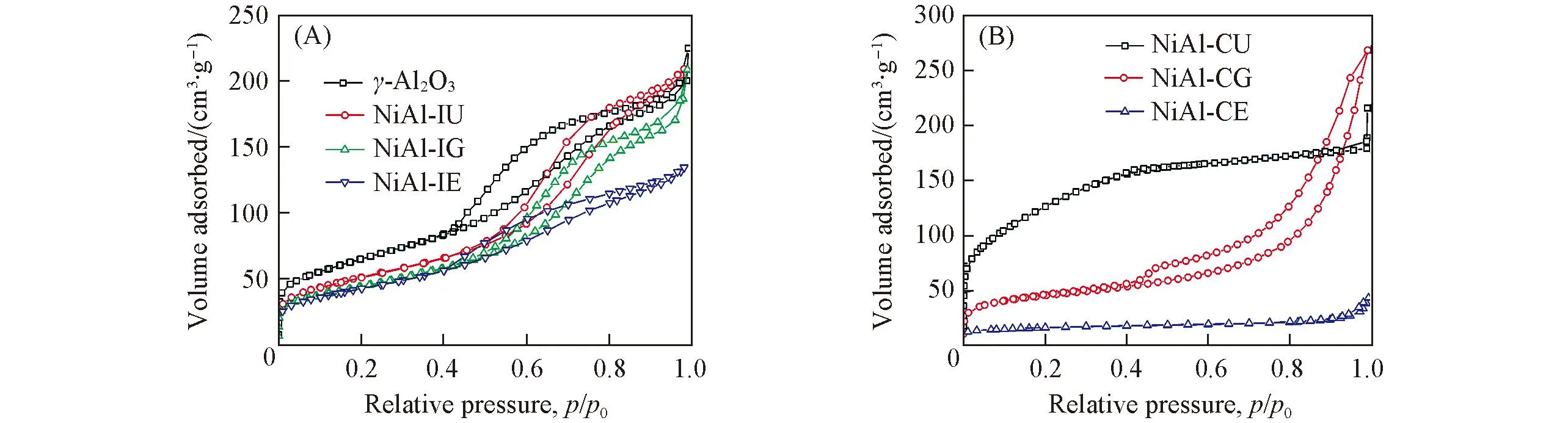
Fig.2 N2 adsorption-desorption isotherms of Al2O3 support and the catalysts
载体和催化剂的织构性质列于表1. 由表1可见, NiAl-IU催化剂的比表面积、总孔容和平均孔径分别为162 m2/g, 0.30 cm3/g和5.5 nm, 均小于γ-Al2O3载体, 表明浸渍燃烧过程中负载的Ni物种堵塞了载体孔道[23]; NiAl-IG和NiAl-IE催化剂的比表面积和孔容与NiAl-IU催化剂相近, 表明浸渍燃烧法制备的催化剂具有与载体类似的织构性质, 这是由于催化剂的载体在浸渍燃烧前为固体, 燃烧过程对载体的织构性质影响不大. 从表1中还可以看出, 共燃烧法制备的催化剂织构性质具有明显差别. 其中, NiAl-CU催化剂比表面积最大, 为468 m2/g, 平均孔径为2.4 nm; NiAl-CG催化剂比表面积为158 m2/g, 平均孔径为10.1 nm; NiAl-CE催化剂比表面积最小, 仅为51 m2/g, 表明不同燃料显著影响了催化剂的织构性质.

Table 1 Textural properties of Al2O3 support and the catalysts
2.3催化剂的微观结构和形貌
催化剂还原前的XRD谱图如图3(A)所示. 可以看出, 浸渍燃烧法制备的催化剂还原前均出现了明显的NiO(PDF No. 47-1049)特征衍射峰, 且各NiO衍射峰强度相差不大, 表明以不同燃料采用浸渍燃烧制备的催化剂的NiO晶粒相近, 同时各催化剂还保持了载体γ-Al2O3(PDF No. 10-0425)的特征衍射峰. 以尿素为燃料采用共燃烧法制备的NiAl-CU催化剂还原前出现了γ-Al2O3的特征衍射峰, 而以甘氨酸和乙二醇为燃料制备的催化剂未出现明显的特征衍射峰, 可见催化剂中未形成γ-Al2O3或NiO结晶[24,25].
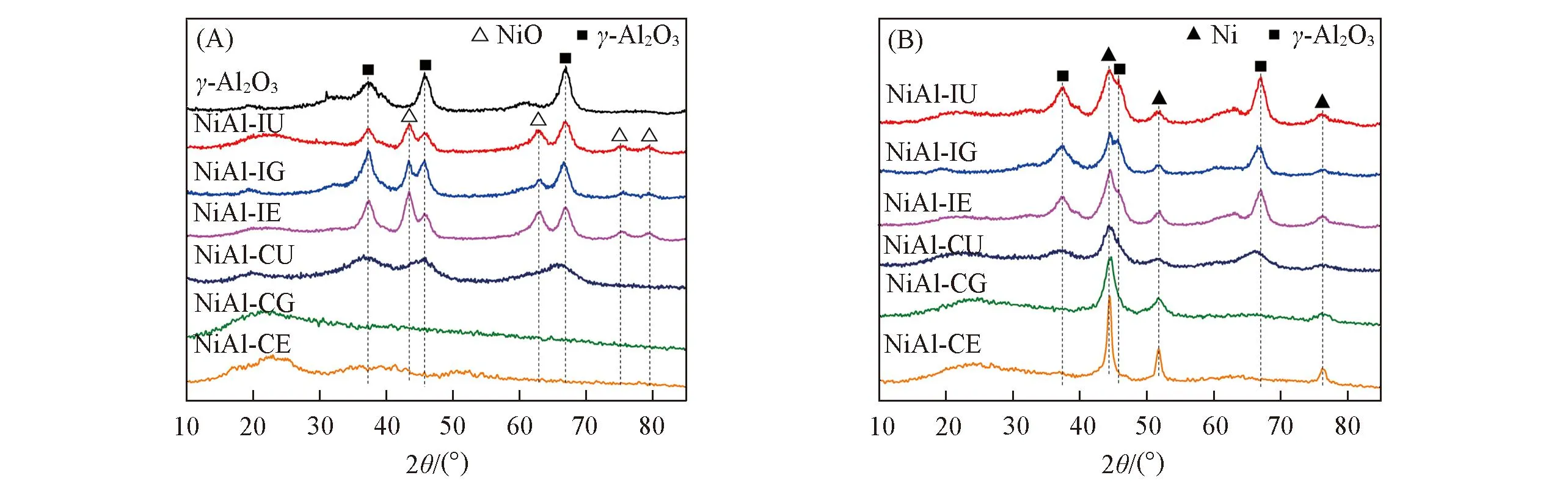
Fig.3 XRD patterns of catalysts prepared by impregnation combustion and co-combustion before(A) and after(B) reduction
催化剂还原后的XRD谱图如图3(B)所示. 可以看出, 浸渍燃烧法制备的催化剂还原后在2θ=44.5°, 51.8°, 76.4°处出现了金属Ni(PDF No. 04-0850)的特征衍射峰, 采用谢乐公式对2θ=51.8°处Ni晶粒尺寸的计算结果表明, Ni晶粒尺寸为6.9~7.3 nm(表2). 共燃烧法制备的催化剂还原后的金属Ni衍射峰强度差别较大, 计算表明, NiAl-CU催化剂Ni晶粒最小, 仅为6.3 nm; 而NiAl-CG和NiAl-CE催化剂的Ni晶粒较大, 分别为7.6和12.5 nm, 这可能是由于催化剂在还原过程中的Ni物种迁移聚集所致.

Table 2 XRD and H2 chemisorption analytic results for the catalysts
催化剂的TEM表征如图4所示. 其中黑色部分为Ni物种, 浅色部分为氧化铝载体. 可以看出, 浸渍燃烧法制备的催化剂还原前的颗粒分布较均匀; 还原后催化剂中的金属Ni颗粒粒径相近, 约5~10 nm. 共燃烧法制备的NiAl-CU催化剂还原前为块状形貌, NiO颗粒分散均匀, 粒径为3~5 nm, 还原后形貌变化不大; NiAl-CG催化剂还原前为不规则形貌, 还原后出现Ni颗粒, 粒径为7~12 nm; NiAl-CE催化剂还原前为均质团块堆积的形貌, 还原后出现较大的金属Ni颗粒, 粒径达10~25 nm.

Fig.4 TEM images of NiAl-IU(A, A′), NiAl-IG(B, B′), NiAl-IE(C, C′), NiAl-CU(D, D′), NiAl-CG(E, E′) and NiAl-CE(F, F′) catalysts before(A—F) and after(A′—F′) reduction
2.4 催化剂的H2还原和H2吸附性质

Fig.5 H2-TPR curves of catalysts
催化剂的H2-TPR表征结果见图5. 250 ℃以下的低温还原峰对应于催化剂中Ni2O3的还原[26~28]; 250 ℃以上的还原峰属于NiO的还原, 并可进一步分为α,β和γ还原峰[29]. 低温峰可归属于自由态α-NiO的还原, 该物相与载体无相互作用或相互作用较弱; 中温还原峰可归属于β-NiO的还原, 该物相与载体相互作用较强, 并可以进一步划分为β1(300 ~500 ℃)和β2(400~550 ℃)还原峰[29]; 高温还原峰γ对应类镍铝尖晶石的还原[29,30].
表3为催化剂H2-TPR谱图的高斯分峰拟合分析. 从图5和表3可以看出, 浸渍燃烧法制备的NiAl-IU催化剂具有Ni2O3还原峰, 其相对峰面积达到11%, 该物相是硝酸镍分解形成NiO过程的中间产物[31]; 催化剂中α-NiO还原峰相对峰面积较小, 仅为5%, 而β1-NiO和β2-NiO相对峰面积较大, 分别为36%和37%,γ-NiO还原峰面积为11%. 浸渍燃烧法制备的NiAl-IG和NiAl-IE催化剂中Ni2O3还原峰面积较小, 而NiO物相还原峰面积和还原温度与NiAl-IU催化剂相近, 可见浸渍燃烧法制备的催化剂NiO物相与载体相互作用差别不大. 共燃烧法制备的催化剂未出现Ni2O3还原峰. NiAl-CU催化剂中α-NiO还原峰温度为280 ℃, 相对峰面积为27%,β1-NiO,β2-NiO和γ-NiO的还原峰相对峰面积分别为35%, 31%和7%; NiAl-CG催化剂中α-NiO还原峰最大, 其相对峰面积为39%, 还原温度达到373 ℃; NiAl-CE催化剂中α-NiO相对峰面积达到83%, 还原峰温度达到345 ℃. NiAl-CG和NiAl-CE催化剂中α-NiO还原温度和峰面积相对较高, 表明催化剂中自由态NiO较多, 在Ni物种在还原过程中易迁移聚集形成较大的Ni颗粒[29,32].

Table 3 Gaussian fitting analysis of H2-TPR profiles of the Ni-based catalysts

Fig.6 Catalytic stability of Ni-Al2O3 catalysts for slurry CO methanation Reaction conditions: 260 ℃, 1.0 MPa, V(H2)∶V(CO)=3∶1, space velocity: 3000 mL·g-1·h-1.
对催化剂进行H2化学吸附表征, 并据此计算出催化剂的金属表面积和金属分散度, 结果列于表2. 浸渍燃烧法制备的各催化剂的金属Ni分散度和金属表面积差别不大, 分别为6.9%~7.7%和9.2~10.3 m2/g. 共燃烧法制备的NiAl-CU催化剂金属Ni分散度最大, 为7.9%, 金属表面积达到10.5m2/g; NiAl-CG和NiAl-CE催化剂金属Ni分散度较低, 分别为6.2%和3.5%, 金属表面积分别为8.3和4.8 m2/g.
2.5催化剂的甲烷化反应性能
Ni-Al2O3催化剂的浆态床CO甲烷化性能评价结果见图6. 由图6可见, 各催化剂反应10 h后其CO转化率达到稳定, 反应40 h内未出现明显的失活. 各催化剂反应10 h后的甲烷化平均活性数据列于表4. 由表4可见, 在260 ℃反应温度下, 采用不同燃料浸渍燃烧法制备的催化剂CO转化率相近, 在80.1%~83.5%之间, 而且产物的选择性也相差不大. 因此, 燃料对浸渍燃烧法制备的催化剂的性能影响不大. 表征结果也表明, 浸渍燃烧法所制备催化剂的结构受燃烧过程影响较小, 催化剂织构性质、金属Ni分散度和Ni晶粒尺寸相近, 催化剂的结构主要取决于载体的结构. 但是共燃烧法制备的催化剂活性差别较大, CO转化率为43.1%~84.7%, CH4选择性为81.6%~91.1%, C2~C4产物选择性为4.4%~7.1%, CO2选择性为4.5%~11.3%, 其中NiAl-CU催化剂CO转化率最高, 为84.7%, 而NiAl-CG和NiAl-CE催化剂的CO转化率较低, 分别为63.2%和43.1%. 在共燃烧法制备催化剂时, 不同燃料的燃烧过程表现不同, 显著影响了催化剂的织构性质、金属Ni分散度和Ni晶粒尺寸, 进而影响了催化剂的活性.

Table 4 Catalytic performance of Ni-Al2O3 catalysts for slurry CO methanation*
* Average value of catalytic performance for reaction between 10 h and 40 h.
3结论
以γ-Al2O3为载体, 通过浸渍燃烧法制备的Ni-Al2O3催化剂的织构性质与γ-Al2O3载体相似, 采用尿素、甘氨酸或乙二醇为燃料时制得的催化剂比表面积、金属Ni分散度、Ni晶粒尺寸及甲烷化活性和稳定性相近, 在260 ℃反应条件下, CO转化率在80.1%~83.5%之间. 共燃烧法制备的Ni-Al2O3催化剂的结构受燃烧过程影响较大, 采用甘氨酸和乙二醇为燃料时, 所制备催化剂的比表面积小, 金属Ni分散度低、Ni晶粒尺寸大, CO转化率分别为63.2%和43.1%; 以尿素为燃料时, 燃烧过程平缓连续, 其催化剂比表面积大, 金属Ni分散度高、Ni晶粒尺寸小, CO转化率达到84.7%.
参考文献
[1]Gao J., Liu Q., Gu F., Liu B., Zhong Z., Su F.,RSCAdv., 2015, 5(29), 22759—22776
[2]Kopyscinski J., Schildhauer T. J., Biollaz S. M. A.,Fuel, 2010, 89(8), 1763—1783
[3]Cui X. X., Meng F. H., He Z., Li Z., Zheng H. Y.,Chin.J.Inorg.Chem., 2013, 30(2), 277—283(崔晓曦, 孟凡会, 何忠, 李忠, 郑华艳. 无机化学学报, 2013, 30(2), 277—283)
[4]Meng F., Li Z., Liu J., Cui X., Zheng H.,J.Nat.Gas.Sci.Eng., 2015, 23, 250—258
[5]Meng F., Li Z., Ji F., Li M.,Int.J.HydrogenEnerg., 2015, 40(29), 8833—8843
[6]Meng F. H., Chang H. R., Li Z.,CIESCJ., 2014, 65(8), 2997—3003(孟凡会, 常慧蓉, 李忠, 化工学报, 2014, 65(8), 2997—3003)
[7]Zhang J., Bai Y., Zhang Q., Wang X., Zhang T., Tan Y., Han Y.,Fuel, 2014, 132(15), 211—218
[8]Götz M., Ortloff F., Reimert R., Basha O., Morsi B. I., Kolb T.,Energ.Fuel, 2013, 27(8), 4705—4716
[9]Meng F. H., Liu J., Li Z., Zhong P. Z., Zheng H. Y.,J.FuelChem.Technol., 2014, 42(2), 231—237(孟凡会, 刘军, 李忠, 钟朋展, 郑华艳. 燃料化学学报, 2014, 42(2), 231—237)
[10]Meng F., Zhong P., Li Z., Cui X., Zheng H.,J.Chem., 2014, 2014, 1—7
[11]Piumetti M., Fino D., Russo N.,Appl.Catal.B:Environ., 2015, 163, 277—287
[12]Cao Z., Qin M., Jia B., Gu Y., Chen P., Volinsky A. A., Qu X.,Ceram.Int., 2015, 41(2), 2806—2812
[13]Ghose R., Hwang H. T., Varma A.,Appl.Catal.A:Gen., 2014, 472, 39—46
[14]Groven L. J., Pfeil T. L., Pourpoint T. L.,Int.J.HydrogenEnerg., 2013, 38(15), 6377—6380
[15]González-Cortés S. L., Imbert F. E.,Appl.Catal.A:Gen., 2013, 452, 117—131
[16]Shi L., Jin Y., Xing C., Zeng C., Kawabata T., Imai K., Matsuda K., Tan Y., Tsubaki N.,Appl.Catal.A:Gen., 2012, 435/436, 217—224
[17]Yan C. F., Chen H., Hu R. R., Huang S., Luo W., Guo C., Li M., Li W.,Int.J.HydrogenEnerg., 2014, 39(32), 18695—18701
[18]Colussi S., Gayen A., Llorca J., de Leitenburg C., Dolcetti G., Trovarelli A.,Ind.Eng.Chem.Res., 2012, 51(22), 7510—7517
[19]Liu Q., Ren J., Qin Z. F., Miao M. Q., Li Z.,Chem.J.ChineseUniversities, 2013, 34(9), 2171—2177(刘泉, 任军, 秦志峰, 苗茂谦, 李忠. 高等学校化学学报, 2013, 34(9), 2171—2177)
[20]Ji K. M., Meng F. H., Gao Y., Li Z.,Chin.J.Inorg.Chem., 2015, 31(2), 267—274(吉可明, 孟凡会, 高源, 李忠. 无机化学学报, 2015, 31(2), 267—274)
[21]Jung C. H., Jalota S., Bhaduri S. B.,Mater.Lett., 2005, 59(19/20), 2426—2432
[22]Sing K. S. W., Everett D. H., Haul R. A. W., Moscou L., Pierotti R. A., Rouquerol J., Siemieniewska T.,PureAppl.Chem., 1985, 57(4), 603—619
[23]Aziz M. A. A., Jalil A. A., Triwahyono S., Mukti R. R., Taufiq-Yap Y. H., Sazegar M. R.,Appl.Catal.B:Environ., 2014, 147, 359—368
[24]Han S. J., Bang Y., Yoo J., Seo J. G., Song I. K.,Int.J.HydrogenEnerg., 2013, 38(20), 8285—8292
[25]Li G., Hu L., Hill J. M.,Appl.Catal.A:Gen., 2006, 301(1), 16—24
[26]Xu Y., Yang J., Demura M., Hirano T., Matsushita Y., Tanaka M., Katsuya Y.,Int.J.HydrogenEnerg., 2014, 39(25), 13156—13163
[27]Bai X., Wang S., Sun T., Wang S.,React.Kinet.Mech.Catal., 2014, 112(2), 437—451
[28]Hardiman K. M., Hsu C. H., Ying T. T., Adesina A. A.,J.Mol.Catal.AChem., 2005, 239(1/2), 41—48
[29]Zhang J., Xu H., Jin X., Ge Q., Li W.,Appl.Catal.A:Gen., 2005, 290(1/2), 87—96
[30]Zhang Y. H., Xiong G. X., Sheng S. S., Liu S. L., Yang W. S.,ActaPhys-Chim.Sin., 1999, 15(8), 735—741(张玉红, 熊国兴, 盛世善, 刘盛林, 杨维慎. 物理化学学报, 1999, 15(8), 735—741)
[31]Kumar A., Wolf E. E., Mukasyan A. S.,AIChEJ., 2011, 57(8), 2207—2214
[32]Thyssen V. V., Maia T. A., Assaf E. M.,Fuel, 2013, 105, 358—363
Effect of Fuel on Structure and Catalytic Performance for
Slurry Methanation over Ni-Al2O3Catalysts
Prepared by Combustion Method†
JI Keming, MENG Fanhui, GAO Yuan, LI Zhong*
(KeyLaboratoryofCoalScienceandTechnology,MinistryofEducationandShanxiProvince,
TaiyuanUniversityofTechnology,Taiyuan030024,China)
AbstractA series of Ni-Al2O3catalysts was prepared by impregnation combustion method and co-combustion method, and the catalysts were characterized by N2adsorption-desorption, XRD, TEM, H2-TPR and H2chemisorption. The effect of fuel type on structure and catalytic methanation performance over Ni-Al2O3catalysts in a slurry-bed reactor was studied. The results show that Ni-Al2O3catalysts, prepared by impregnation combustion method using urea, glycine or ethylene glycol as fuel, exhibited similar textural properties, metallic Ni dispersion and Ni crystallite size as those of the support, and the CO conversion was between 80.1% and 83.5% at 260 ℃. However, the Ni-Al2O3catalysts, prepared by co-combustion method, were significantly affected by the combustion process. The specific surface area of the catalysts prepared using glycine and ethylene glycol as fuel was small, and the metallic Ni dispersion was low and Ni crystallite size was large, which resulted in the low CO conversion. The Ni-Al2O3catalyst using urea as fuel exhibited the large specific surface area and metallic Ni dispersion and small Ni crystallite size, and the CO conversion and CH4selectivity reached 84.7% and 91.1%, respectively.
KeywordsSlurry-bed methanation; Ni-Al2O3catalyst; Impregnation combustion method; Co-combustion method; Fuel
(Ed.: V, Z)
† Supported by the Youth Foundation of Shanxi Province, China(No.2013021007-4), the China Postdoctoral Science Foundation(No.2013M541210) and the National Basic Research Program of China(No.2012CB723105).
doi:10.7503/cjcu20150369
基金项目:山西省青年基金(批准号: 2013021007-4)、中国博士后科学基金(批准号: 2013M541210)和国家“九七三”计划项目(批准号: 2012CB723105)资助.
收稿日期:2015-05-14.网络出版日期: 2015-11-17.
中图分类号O643.3; O614
文献标志码A
联系人简介: 李忠, 男, 博士, 教授, 主要从事碳一化学方面的研究. E-mail: lizhong@tyut.edu.cn

