阿帕替尼联合化疗治疗晚期胃癌的临床研究
朱华云, 孙小峰, 周 青, 陈凌翔, 陈 嘉, 吴平平
临床与基础研究
阿帕替尼联合化疗治疗晚期胃癌的临床研究
朱华云, 孙小峰, 周 青, 陈凌翔, 陈 嘉, 吴平平
目的 研究阿帕替尼联合化疗治疗晚期胃癌的临床疗效和不良反应。方法 2014年7月至2016年7月,选择既往化疗失败、疾病进展或复发转移入住江苏省肿瘤医院的晚期胃癌患者,分别采用阿帕替尼加以紫杉类、伊立替康类和氟尿嘧啶类药物为基础的化疗方案,另选择同期未接收阿帕替尼的化疗患者作为对照组,评价阿帕替尼联合化疗的治疗效果,并对不良反应结果进行分析。结果 共入组71例,均可以评价疗效。其中39例仅接受化疗(对照组),32例为阿帕替尼加化疗(实验组)。对照组的客观缓解率为15.4%,疾病控制率56.4%;实验组的客观缓解率为50.0%,疾病控制率84.4%。治疗过程中可见蛋白尿、高血压、白细胞减少、贫血等不良反应,但多为0~Ⅱ度。结论 阿帕替尼联合化疗能够提高晚期胃癌的治疗效果,且不良反应可控。
晚期胃癌; 阿帕替尼; 联合化疗
化疗是治疗晚期胃癌的主要手段,基于5-氟尿嘧啶(5-FU)、紫杉醇(PTX)、伊立替康(CPT-11)等抗肿瘤药物的单药、多药联合治疗方法已经广泛应用于胃癌的临床治疗[1-3]。但由于化疗药物的毒副作用、肿瘤细胞的耐药性等因素,化疗的结果仍不尽如意。一系列针对HER-2、EGFR和VEGFR等分子靶点的抗肿瘤药物的问世,为肿瘤的治疗带来了希望。研究表明,小分子靶向药物联合化疗治疗晚期胃癌显示出独特的优势[4-6]。近年来,针对血管生成信号通路的小分子酪氨酸激酶抑制剂(TKI)得到了临床研究人员的广泛关注,阿帕替尼(Apatinib,APA)便是第一个对晚期胃癌安全有效的小分子TKI[7-8]。本研究选取既往化疗失败、疾病进展或者复发转移的晚期胃癌患者,将阿帕替尼分别与以紫杉(PTX)类、伊立替康(CPT-11)类和氟尿嘧啶(FU)类药物为基础化疗方案合用,观察其治疗效果,并对不良反应进行分析如下。
1 资料与方法
1.1 一般资料 入选患者均为2014年7月到2016年7月在江苏省肿瘤医院肿瘤内科住院治疗患者。纳入标准为(1)经病理学、细胞学或影像学确诊为胃癌;(2)既往化疗失败、疾病进展或者复发转移;(3)ECOG评分0~2分;(4)预计生存期>3个月;(5)有至少1个可用影像学方法测量的靶病灶;(6)无相关化疗禁忌证。根据入院顺序、化疗方案等因素分为对照组和实验组。
1.2 治疗方案 对照组以紫杉类(PTX类)或伊立替康类(CPT-11类)或氟尿嘧啶类为基础化疗方案(FU类)化疗。实验组在以上化疗基础上同时接受口服阿帕替尼(商品名:艾坦,购自江苏恒瑞医药股份有限公司)治疗,剂量为500 mg/d。
1.3 疗效与毒副反应评定 采用实体瘤疗效评定标准(RECIST)评价临床疗效,分为CR(完全缓解)、PR(部分缓解)、SD(病情稳定)和PD(疾病进展)。客观缓解率ORR=(CR+PR)/n×100%,疾病控制率DCR=(CR+PR+SD)/n×100%。不良反应按世界卫生组织(WHO)抗肿瘤药物不良反应评分标准进行评价,分为0~Ⅳ度。
1.4 统计学方法 使用SPSS 21统计软件进行统
计学分析,计数资料使用卡方检验方法(Fisher精确检验),以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般情况比较 共入选符合条件患者71例,其中对照组39例,实验组32例,两组患者的年龄、性别比及所用化疗方案见表1。经卡方检验,两组的性别、年龄和基础化疗方案等因素不具有统计学差异(P>0.05),具有可比性。
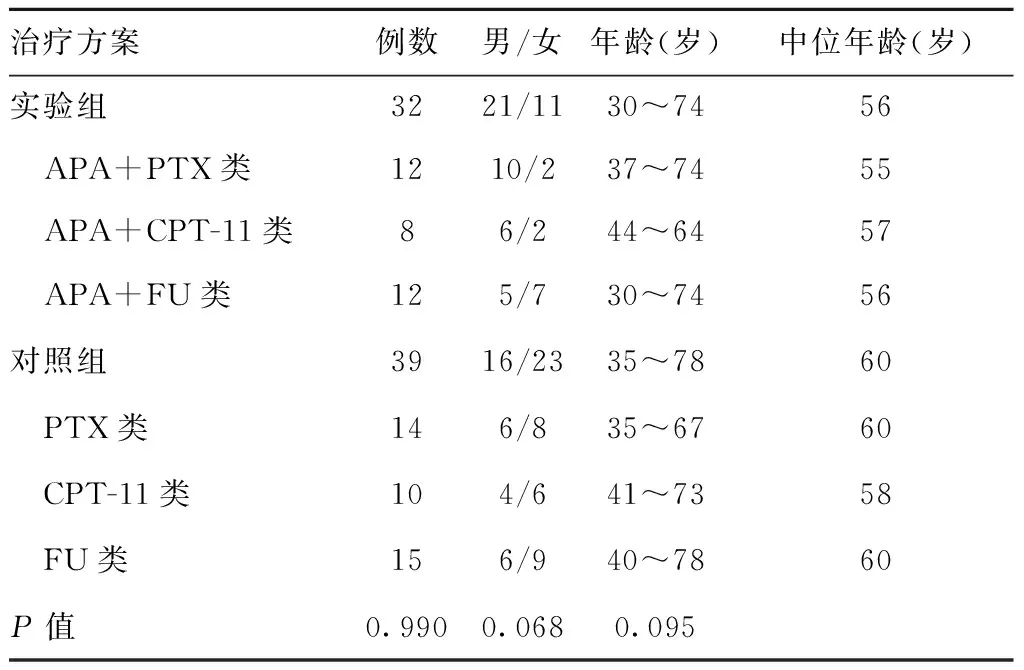
表1 71例患者的分组及一般情况
2.2 两组治疗效果比较 所有治疗患者均可以评价疗效,对照组中CR 0例,PR 6例,SD 16例,PD 17例,客观缓解率为15.38%,疾病控制率56.41%;实验组中CR 0例,PR 16例,SD 11例,PD 5例,客观缓解率为50.00%,疾病控制率84.38%(表2)。
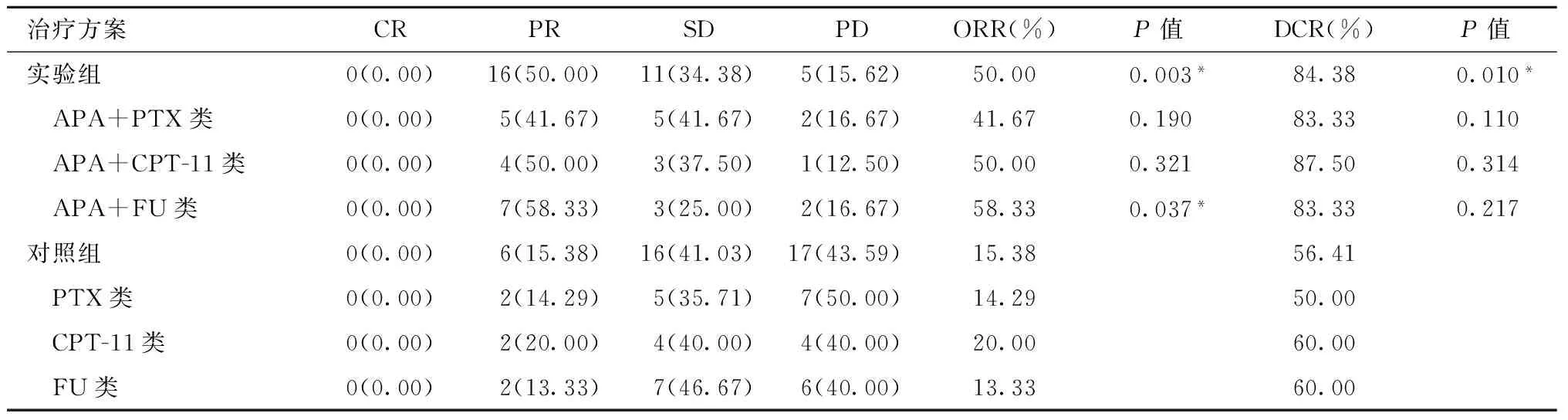
表2 两组治疗效果比较[例(%)]
注:*表示分别与对照组总ORR、DCR和分组ORR相比,P<0.05。
2.3 不良反应情况 本研究中患者常见的不良反应有蛋白尿、高血压、手足皮肤反应、白细胞减少、贫血、恶心呕吐、口腔溃疡等。可见的不良反应多为0~Ⅱ度,少数发生Ⅲ~Ⅳ度不良反应(表3),经相应处理后不良反应平稳可控,患者耐受性较好。
3 讨论
肿瘤在发生、发展以及转移的过程中都离不开新生血管的形成,因此抑制新生血管的生成是肿瘤治疗的关键[9]。阿帕替尼是最新批准用于治疗晚期胃癌的小分子TKI,能够与血管内皮生长因子VEGFR-2等配体结合,抑制肿瘤新生血管的形成[7-8]。临床研究表明,阿帕替尼对晚期胃癌具有较好的抑制作用,如国内王博等[10]分析60例治疗失败晚期胃癌患者,服用阿帕替尼后的疾病控制率达到41.67%。分子靶向药物联合化疗方案也被广泛用于临床。井小会[11]报道阿帕替尼联合替吉奥治疗老年晚期胃癌比替吉奥单药治疗的效果更为理想 。
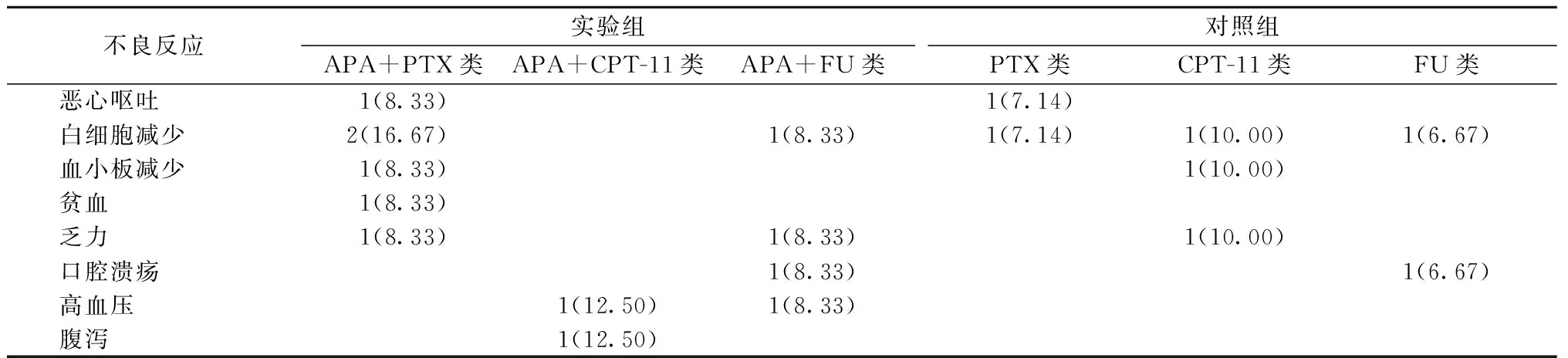
表3 两组患者严重不良反应(Ⅲ~Ⅳ级)发生率[例(%)]
我们在研究阿帕替尼联合化疗治疗晚期胃癌的过程中没有死亡病例出现,患者的疗效均可以评价,结果显示阿帕替尼联合化疗方案的效果优于仅用化疗药物的方案。对照组FU类化疗方案的客观缓解率和疾病控制率分别为13.33%和56.41%,而实验组APA+FU类的客观缓解率和疾病控制率分别为50.00%和84.38%,经Fisher精确检验,两组客观缓解率的差异有统计学意义(P<0.05),但疾病控制率的差异未见统计学意义(P>0.05)。由于样本量不足,其他小组间的比较也未见明显差异,但对照组和实验组的客观缓解率和疾病控制率之间的差异非常显著(P<0.01),阿帕替尼联合化疗方案能够提高晚期胃癌的疗效。
毒副作用是化疗过程中不可避免的话题,需要我们采取适当的措施,将其控制在可控范围内。在阿帕替尼联合化疗治疗晚期胃癌的过程中,不良反应主要是Ⅰ~Ⅱ度,Ⅲ~Ⅳ度少见。实验组共有5例Ⅰ~Ⅱ度蛋白尿,停药后会自行消失,无需用药治疗。高血压发生率为45.07%,但仅APA+CPT-11类组和APA+FU类组出现2例Ⅲ~Ⅳ度高血压,经降压处理后血压平稳。部分患者出现口腔溃疡等症状,溃疡区域予以伤口愈合促进(活性银离子抗菌液配合常规口腔护理)处理,能够明显改善患者的舒适度[12]。尽管如此,在阿帕替尼联合化疗治疗晚期胃癌的过程中仍需要密切关注不良反应,尤其是有肝肾功能不全、高血压等病史的患者。
综上所述,本研究结果表明,阿帕替尼联合化疗方案能够提高晚期胃癌的疗效,且不良反应可控。后续我们将扩大样本容量,延长治疗周期,进一步评估阿帕替尼联合化疗方案的远期疗效结果。
[1] IACOVELLI R, PIETRANTONIO F, MAGGI C, et al. Combination or single-agent chemotherapy as adjuvant treatment of gastric cancer: A systematic review and meta-analysis of published trials[J]. Crit Rev Oncol Hematol, 2016, 98: 24-28.
[2] LORDICK F, LORENZEN S, YAMADA Y, et al. Optimal chemotherapy for advanced gastric cancer: is there a global consensus?[J].Gastric Cancer, 2014, 17(2): 213-225.
[3] KANG B W, KWON O K, CHUNG H Y, et al. Taxanes in the treatment of advanced gastric cancer[J]. Molecules, 2016, 21(5): 651-651.
[4] LI K, LI J. Current Molecular Targeted Therapy in Advanced Gastric Cancer: A Comprehensive Review of Therapeutic Mechanism, Clinical Trials, and Practical Application[J]. Gastroenterol Res Pract, 2016, 2016. doi: 10.1155/2016/4105615.
[5] 寸英丽, 裴波. 靶向治疗联合化疗治疗晚期胃癌[J].中国肿瘤外科杂志, 2014, 6(4): 205-207.
[6] WILKE H, MURO K, VAN CUTSEM E, et al. Ramucirumab plus paclitaxel versus placebo plus paclitaxel in patients with previously treated advanced gastric or gastro-oesophageal junction adenocarcinoma (RAINBOW): a double-blind, randomised phase 3 trial[J]. Lancet Oncol, 2014, 15(11): 1224-1235.
[7] GENG R, LI J. Apatinib for the treatment of gastric cancer[J]. Expert Opin Pharmacother, 2015, 16(1): 117-122.
[8] ROVIELLO G, RAVELLI A,POLOM K,et al. Apatinib: A novel receptor tyrosine kinase inhibitor for the treatment of gastric cancer[J]. Cancer Lett, 2016, 372(2): 187-191.
[9] WANG Z, DABROSIN C, YIN X, et al. Broad targeting of angiogenesis for cancer prevention and therapy[C].Semin Cancer Biol, 2015, 35 Suppl: S224-S243.
[10] 王博, 宋丽杰, 牛鹏云, 等. 阿帕替尼治疗晚期胃癌的临床疗效及预后[J]. 世界华人消化杂志, 2016, 24(5): 759-764.
[11] 井小会. 阿帕替尼联合替吉奥一线治疗老年晚期胃癌[J].中国实用医刊, 2016,(10): 37-39.
[12] 刘慧敏. 两种不同口腔护理方法对化疗所致口腔溃疡的疗效观察[J]. 中国肿瘤外科杂志, 2015, 7(6): 397-398.
Clinical study of Apatinib combined chemotherapy in the treatment of advanced gastric cancer
ZHUHuayun,SUNXiaofeng,ZHOUQing,CHENLingxiang,CHENJia,WUPingping.
(DepartmentofOncology,JiangsuCancerHospital,Nanjing210009,China)
s:WUPingping,E-mail:wupingping210009@126.com
Objective To investigate the clinical efficacy and side-effect of Apatinib combined with chemotherapeutic agents in the treatment of advanced gastric cancer. Methods Patients with advanced gastric cancer adopted a Apatinib and Taxel, Irinotecan or Fluorouracil-based combination chemotherapy regimen. Concurrent patients who did not receive Apatinib were chosen as control group. The therapeutic efficacy and side-effect of Apatinib were evaluated. Results 71 patients were able to evaluate the clinical efficacy. The objective response rate (ORR) and the disease control rate (DCR) for patients receiving chemotherapy only (control group) were 15.4% and 56.4%. ORR and DCR for those receiving Apatinib combined chemotherapy were 50.0% and 84.4%, respectively. Side-effects were proteinuria, hypertension, anemia and others. Most of them were ranked as class 0~Ⅱ. Conclusions Apatinib combined chemotherapy can improve the treatment of advanced gastric cancer with tolerable side-effects.
Advanced gastric cancer; Apatinia; Combination chemotherapy
江苏省干部保健科研项目(BJ15029); 江苏省中医药局科技项目(YB2015170)
210009 江苏 南京,江苏省肿瘤医院 肿瘤内科
朱华云,女,主治医师,研究方向:消化道肿瘤化疗及靶向治疗,E-mail:304311140@qq.com
吴平平,女,副主任医师,研究方向:消化道肿瘤化疗及靶向治疗,E-mail:wupingping210009@126.com
10.3969/j.issn.1674-4136.2016.06.013
1674-4136(2016)06-0394-03
2016-09-28][本文编辑:李筱蕾]
——评《卵巢恶性肿瘤诊疗手册》

