改良Poppen入路切除镰幕交界区脑膜瘤
王汉东, 胡志刚
手术视频
改良Poppen入路切除镰幕交界区脑膜瘤
王汉东, 胡志刚

主刀医师介绍:王汉东,南京军区南京总医院神经外科主任,中国人民解放军神经外科研究所所长,医学博士,主任医师,教授,博士生导师,博士后指导老师。现任中国医师协会神经外科医师分会常委;中华医学会神经外科分会委员;全军神经外科专业委员会常委;江苏省医学会神经外科分会名誉主任委员;南京军区神经外科专业委员会主任委员;南京医学会神经外科分会名誉主任委员;《临床神经学杂志》及《医院研究生学报》副主编,《中华神经外科杂志》、《中华外科杂志》、《中华实验外科杂志》等十余种医学期刊的编委。
镰幕交界区脑膜瘤; Poppen入路; 托氏分流; 手术视频
1 病例资料
女,63岁。因“头痛1月余”入院。查体神经系统未见明显阳性体征。术前MRI显示镰幕交界区脑膜瘤,大小约37 mm×33 mm×32 mm,伴梗阻性脑积水(图1)。入院后行头颅CTV检查显示双侧大脑内静脉远端及大脑大静脉均未显影(图2)。
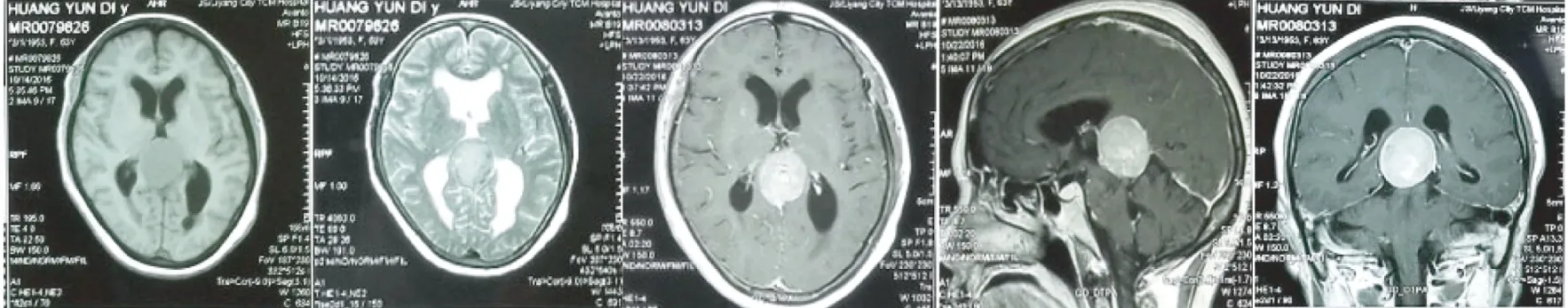
图1 术前MRI显示镰幕交界区脑膜瘤,T1像呈等信号,T2像呈高信号,增强扫描强化均匀、明显。

图2 术前CTV显示双侧大脑内静脉位于肿瘤下方; 双侧大脑内静脉后部及大脑大静脉均未显影。
2 病情分析及手术策略
患者为老年女性,镰幕交界区脑膜瘤伴梗阻性脑积水,可选择改良Poppen入路行肿瘤切除+托氏分流术,以一期切除肿瘤并确切解决脑积水问题。因CTV显示双侧大脑内静脉远端闭塞,可在术中离断大脑内静脉以彻底切除肿瘤。
3 Poppen入路行肿瘤切除+托氏分流术技巧及要点
因肿瘤位置深在,且伴有梗阻性脑积水,应避免强行牵拉脑组织以防引起脑组织挫伤。我们在打开颅骨后,见硬脑膜张力极高,立即切开少许硬脑膜并穿刺侧脑室枕角;充分释放脑脊液,脑组织张力下降后再完全打开硬脑膜,牵开枕叶,显露镰幕交界区。而后平行于直窦切开小脑幕,暴露肿瘤。首先行瘤内减压,获得充分操作空间后沿肿瘤边界显露深部结构,并将肿瘤连同基底全切除。手术要点见图3~图13。
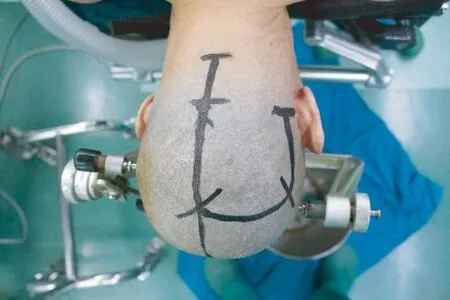
图3 患者取俯卧位,三点头钉固定头部。左侧枕部 马蹄形切口,内侧切口沿中线下延至枕骨大孔水平,小型手术 托盘置于患者头部右侧,便于术者在患者头顶和左侧变换位置。

图4 因硬脑膜张力极高,故切开少许硬膜, 在顶叶后部中线旁开3 cm处穿刺左侧侧脑室枕角, 进入脑室后拔除针芯,充分、缓慢释放脑脊液。

图5 脑脊液充分释放后,脑组织张力明显下降后, 打开硬脑膜,逐步牵开枕叶,暴露小脑幕缘。
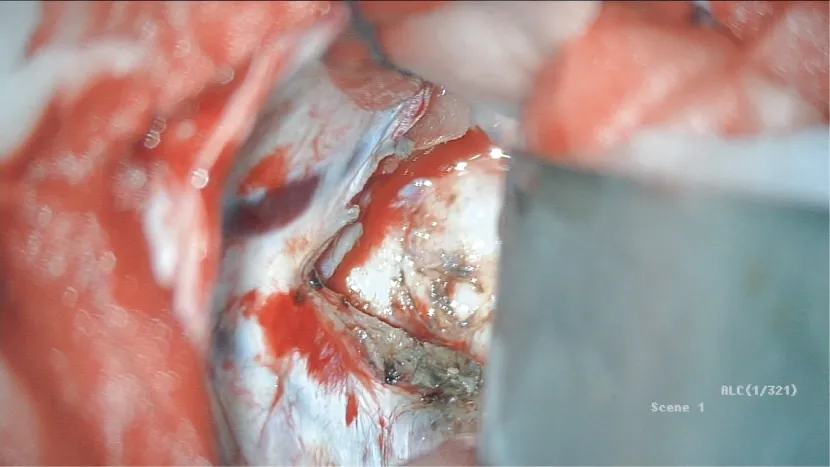
图6 平行于直窦在其旁1 cm处切开小脑幕,边切开 边止血,位于小脑幕下方的肿瘤可充分显露。

图7 在肿瘤内部以双极电凝、显微剪刀分块 切除肿瘤,内减压尽量充分,仅留薄层 瘤壁,以便牵拉瘤壁,显露深部结构。
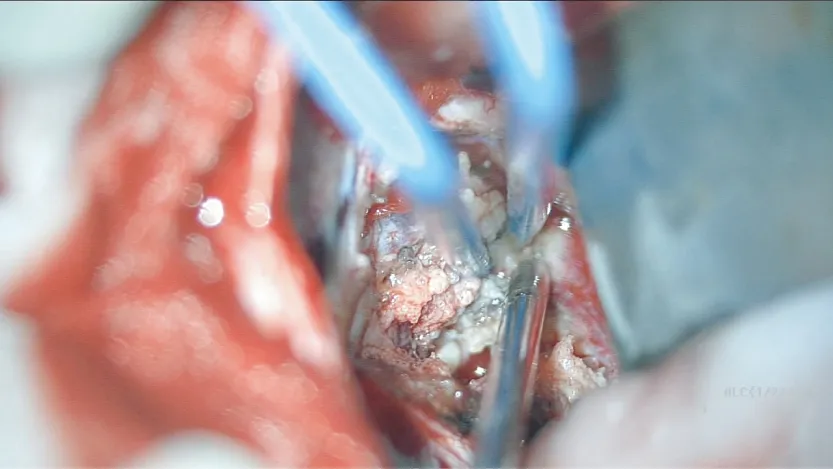
图8 轻轻牵拉残余薄层瘤壁,沿瘤壁分离肿瘤和 周围结构的粘连,并将肿瘤分块切除。

图9 显露、切除瘤壁过程中,可见肿瘤基底广泛,涉及 镰幕交界区大脑镰、小脑幕。沿肿瘤基底离断大脑镰, 电凝切断下矢状窦,并向后离断小脑幕上的基底, 直窦的近端已基本闭塞,予以切断。
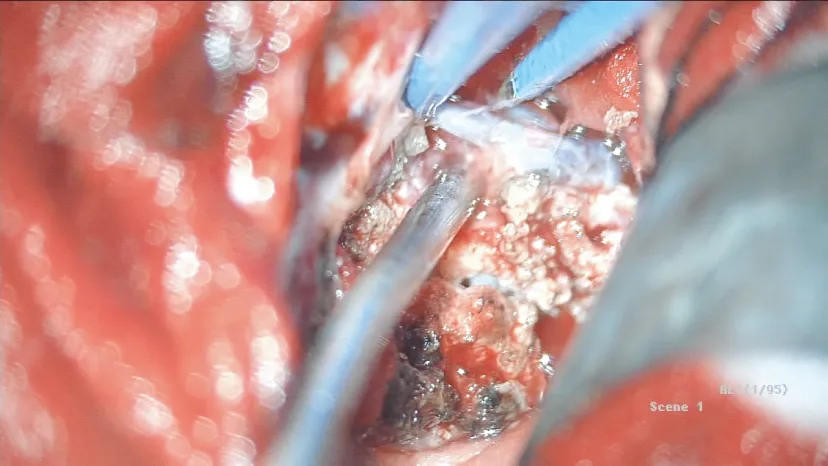
图10 再于肿瘤的后下方,电凝、离断已被肿瘤侵犯并 已闭塞的大脑内静脉远端。

图11 同侧肿瘤切除后,对侧肿瘤较易暴露、切除。
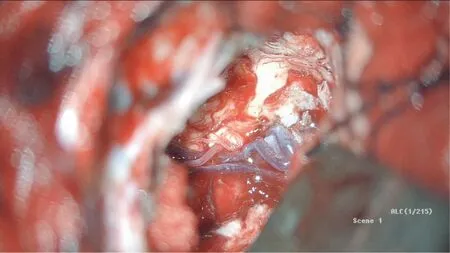
图12 肿瘤连同大脑镰、小脑幕基底一并被完全切除。
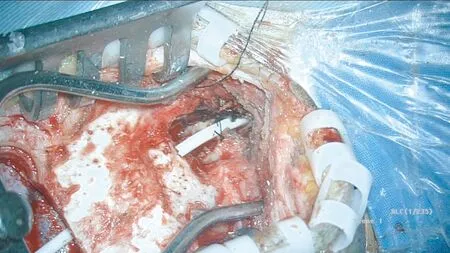
图13 分离显露枕大孔区,高速磨钻磨除枕大孔后缘 及小块鳞部骨质,将分流管自枕部术区从枕骨下 送至枕骨大孔区,置入枕大池并缝扎固定。
4 手术视频
扫描二维码观看。

5 术后处理和随访
术后第一天常规行头颅CT检查(图14),明确颅内有无出血、水肿等并发症,行腰椎穿刺释放脑脊液,以形成压力梯度差,促进分流管内脑脊液流动。术后病理:脑膜瘤,纤维型,WHO Ⅰ级。患者术后恢复良好,MRI复查显示肿瘤切除完全,脑积水消失(图15),无任何神经功能障碍,顺利恢复出院。
6 讨论
镰幕交界区脑膜瘤罕见,发生于小脑幕、大脑镰硬膜皱褶处,在大脑大静脉汇入直窦的前方生长,或沿镰幕交界长轴生长。此处,大脑镰终止于小脑幕,形成了大脑镰左右两侧、小脑幕下方三个分割空间,增加了镰幕交界区脑膜瘤的显露困难。大多数患者会有头痛(伴或不伴恶心、呕吐)及视觉症状,有时也会出现小便失禁、个性改变、步态不稳、头晕、轻度认知变化等症状。其中,部分症状可能由梗阻性脑积水引起。体检最常见的体征为视乳头水肿。
镰幕交界区脑膜瘤有几种不同的手术入路,包括幕下小脑上入路、坐位双侧顶枕开颅、窦上下联合入路等[1-2]。Poppen入路,即枕部经小脑幕入路,由Poppen首先描述。这一入路切除镰幕交界区脑膜瘤具有如下优点:(1)手术路径短;(2)无需切除脑组织,利用脑组织自然间隙,显露好,操作空间大。传统的Poppen入路为右侧枕部开颅。我们对这一入路进行了改良,一是将枕部切口和开颅改到左侧,这样做的好处有:(1)术者为右利手时操作更方便;(2)左侧横窦常无右侧发达,万一损伤不致引起严重后果;(3)便于术者在患者头顶和左侧变换位置。二是将切口沿中线下延至枕大孔区,同期进行侧脑室-枕大池分流术(即托氏分流)。分流管从硬膜外通过,更为平复,并不易滑动[3]。

图14 术后CT显示肿瘤切除完全,术区无明显出血、水肿,分流管在脑室端和枕大池端均显示在位,脑室恢复正常大小。
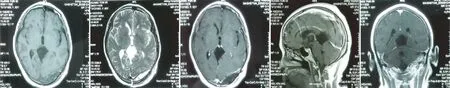
图15 术后MRI显示肿瘤切除完全,脑积水消失。
镰幕交界区脑膜瘤的手术还涉及大脑内静脉、大脑大静脉、直窦、窦汇等深静脉系统的保护问题。深静脉系统由于静脉壁薄弱,被肿瘤推挤后位置多变,因而容易损伤。深静脉急性损伤后,可能会影响丘脑、脑干等重要结构的静脉回流,导致静脉性脑梗死,产生严重的神经功能障碍,如偏瘫、昏迷,甚至死亡,因此术前所有患者均应进行脑血管检查以评估深静脉是否通畅。如果深静脉已完全闭塞而侧支循环良好,可连同肿瘤一并切除;如果深静脉受侵犯但未闭塞,要么切除并重建,要么次全切除后严密随访。在罕见的直窦通畅的大肿瘤病例中,可考虑行次全切除,以保证静脉通畅;必要时,可以待肿瘤继续生长、深静脉闭塞后再行手术治疗。我们曾在2005年报道了11例镰幕交界区脑膜瘤的手术结果,其中有8例切断了大脑大静脉,术后仅1例出现浅昏迷,两天后清醒,后痊愈出院;其余患者均未出现明显的神经功能障碍[4]。
镰幕交界区脑膜瘤常合并梗阻性脑积水,肿瘤即使全切,术后导水管也不一定能恢复通畅,需要进一步手术干预。因此,建议在切除镰幕交界区脑膜瘤同时一期进行托氏分流术。我们总结托氏分流术处理脑积水的优点是:(1)将脑脊液自侧脑室引流至枕大池,模拟了脑脊液的自然循环过程;(2)可以采用同一体位、通过一次手术解决肿瘤切除和缓解脑积水两个问题,避免术后患者因急性脑积水导致病情急剧加重,费用及风险都较二次手术大大减少;(3)分流管经枕角穿刺送入侧脑室额角,额角内脑脊液接近正常脑脊液,且不易被脉络丛组织包裹、堵塞,不易因术中出血堵塞分流管;(4)脑积水缓解率高于其他术式[5]。
[1] GOTO T, OHATA K, MORINO M,et al. Falcotentorial meningioma:surgical outcome in 14 patients[J]. J Neurosurg, 2006, 104(1):47-53.
[2] BASSIOUNI H, ASGARI S, KONIG H J, et al. Meningiomas of the falcotentorial junction: selection of the surgical approach according to the tumor type[J]. Surg Neuro, 2008, 69(4):339-349.
[3] 王汉东. 神经外科手术彩色图解[M]. 南京: 江苏科技出版社, 2013, 73-79.
[4] 王汉东, 史继新, 杭春华,等. 小脑幕脑膜瘤的手术治疗[J]. 中华神经外科杂志, 2005, 21(1): 39-41.
[5] 张治元, 王汉东, 史继新,等. 松果体区肿瘤导致脑积水的处理[J]. 中华神经外科杂志, 2011, 27(10): 1013-1015.
210002 江苏 南京,南京军区南京总医院 神经外科
王汉东,男,主任医师、博导,研究方向:颅内肿瘤、颅内创伤的基础与临床,E-mail:njhdwang@163.com
10.3969/j.issn.1674-4136.2016.06.001
1674-4136(2016)06-0349-04
2016-12-12][本文编辑:李筱蕾]

