磷钨酸二氧化钛光催化降解酸性大红3R催化效能研究*
王 信 岳 琳 马啸宙 万 琼 周 雯 伍高燕贺 涛 魏东洋 许振成 桑燕鸿#
(1.西安科技大学建筑与土木工程学院,陕西 西安710054;2.环境保护部华南环境科学研究所,广东 广州510535;3.河北科技大学环境科学与工程学院,河北 石家庄 050018)
印染废水作为工业废水排放大户,每天排放量为3×106~4×106m3[1],具有水量大、有机污染物含量高、色度深等特点[2-4],因其含有多种偶氮染料,属典型难处理工业废水,其中如何高效经济脱色成为国内外学者长久持续关注的问题。传统上印染废水脱色处理主要集中在物理吸附方面[5-9],如使用活性煤或活性炭进行吸附脱色;新型脱色技术诸如Fentons试剂氧化法、臭氧、电化学降解和絮凝沉淀法等国内外均深入进行了大量研究[10-11],相关结论及优缺点均有报道,因此研究并开发新型廉价实用的偶氮染料脱色技术具有重要的现实意义。
光催化氧化技术自1976年CAREY等[12]利用二氧化钛(TiO2)在紫外光下催化降解多氯联苯以来,因其在有机染料上的脱色优势成为研究热点[13-15]。李克斌等[16]研究发现,磷钨酸(PW12)对AR3R具有明显的还原脱色性能。刘淑芝等[17]进一步研究了PW12负载SiO2用于催化脱硫性能实验,催化剂经过多次回收利用,仍保持较高的活性。刘士荣等[18]研究报道了利用溶胶-凝胶法制备PW12修饰的TiO2催化剂薄膜,在对氯苯酚催化降解过程中两者表现为明显协同促进作用。然而将PW12掺杂TiO2纳米粉末光催化剂(PW12/TiO2)应用于催化降解偶氮染料酸性大红3R却鲜有报道,笔者利用PW12/TiO2,在自制反应器下催化降解偶氮染料酸性大红3R,研究了其催化降解优势性能及最优催化条件,并进行紫外光谱及光催化效能分析[19-20]。
1 材料和方法
1.1 实验材料
实验模拟印染废水采用配置的偶氮染料酸性大红3R(C20H11N2O10S3·3Na)溶液。实验药品:PW12(H3PW12O40·xH2O);无水乙醇;钛酸丁酯(Ti(OC4H9)4);冰醋酸;三乙醇胺;异丙醇;超纯水为实验室自制。以上药品均为分析纯。
实验仪器:UV-1800紫外—可见分光光度计;飞利浦TUV型石英紫外灯管(6W 2个);PHS-3C型精密酸度计;CLJ-2000型磁力搅拌机(2个);YZB/京0401-2008型离心机;FA2204B型电子天平;XL-1-4KW型马弗炉;S-3700N型扫描电子显微镜(SEM,日本日立仪器公司)、D/max-ⅢA型X射线衍射仪(XRD,日本理学仪器公司)。
1.2 PW12/TiO2的制备
采用溶胶-凝胶法[21-22]制备PW12/TiO2。制备方法如下:室温下,量取20 mL钛酸丁酯缓慢滴加到50 mL无水乙醇中,在60~120 r/min缓慢搅拌下加入3 mL冰醋酸和2 mL三乙醇胺,形成淡黄色透明溶液A,静置;室温量取30 mL无水乙醇、5 mL蒸馏水和2 mL冰醋酸,在80~100 r/min缓慢搅拌下混匀,分别加入不同质量PW12继续搅拌至完全溶解,形成溶液B;在60~120 r/min搅拌下将溶液B以一定的速率滴加到溶液A中,继续搅拌1 h,得到均匀透明溶胶,静置2 h得到凝胶,将凝胶在100 ℃水浴锅内干燥4 h,得到黄色晶体,研磨后放入马弗炉中500 ℃煅烧2 h,冷却后所得黄色粉末即为不同质量TiO2掺杂下的PW12/TiO2。
1.3 实验设计
模拟印染废水在紫外灯照射下进行光催化降解实验。实验采用250 mL培养皿作为反应器,放置于磁力搅拌器上并配以大小均匀磁力转子,盖上锡箔纸伴随紫外光照射进行实验;每次实验均添加100 mL模拟印染废水,每次取样10 mL,每15 min取样1次,在507 nm处测定吸光度,在相同实验条件下,控制4个单因素,即酸性大红3R溶液浓度、pH、PW12/TiO2投加量和异丙醇投加量,进行光催化降解实验,催化降解90 min,获得PW12/TiO2的最优催化条件,并在200~600 nm波长下做PW12/TiO2催化降解酸性大红3R的全波长扫描。其脱色率计算公式如下:
(1)
式中:c0为酸性大红3R初始质量浓度,mg/L;c1为实验结束后酸性大红3R质量浓度,mg/L;η为脱色率,%。
2 结果与分析
2.1 PW12/TiO2的表征
为便于催化剂样品分析和探究催化反应效能,对PW12/TiO2做了SEM扫描与XRD表征。由图1可看出,光催化剂PW12/TiO2表面光泽一致,能观察到明显的立面体结构,但是晶型并不整齐,这有利于扩大TiO2晶粒的比表面积[23]78-79,增加固液接触面,从而促进光催化降解反应[24-25]。

图1 PW12/TiO2的SEM图Fig.1 SEM image of PW12/TiO2
由图2可知,经过500 ℃煅烧后,溶胶-凝胶法制备的PW12/TiO2的衍射角(2θ)分别为25.30°、37.80°、48.10°、62.75°、68.84°,分别属于锐钛矿型的(101)、(004)、(200)、(204)、(116)晶面衍射峰,54.08°出现的衍射峰是(105)和(211)晶面衍射峰的综合体现,图谱中并没有发现明显的金红石相TiO2衍射峰,表明PW12掺杂TiO2经过煅烧以后,已基本转为锐钛矿型结构[26],由于PW12已经均匀掺杂在TiO2中,并且W原子部分取代TiO2中Ti原子进入其骨架中,导致图2中并没有出现明显的PW12特征峰,这与盛雪[27]、张霞等[28]的研究结果类似。

图2 PW12/TiO2的XRD谱图Fig.2 XRD pattern of PW12/TiO2
2.2 PW12与PW12/TiO2催化活性比较
室温、常压、不调pH条件下,在100 mL质量浓度为100 mg/L的酸性大红3R溶液中,通过投加0.09 g不同种类催化剂,比较PW12与不同TiO2掺杂量下的PW12/TiO2催化性能。由图3可知,酸性大红3R的脱色率随着TiO2掺杂量的增大先升高后降低,当PW12与TiO2质量比为0.35时,催化效率低于两者单独催化。当PW12与TiO2质量比为0.46时,催化效果明显优于两者单独催化,催化降解30 min,酸性大红3R脱色率可达91.0%,而在PW12与TiO2单独催化时脱色率仅分别为55.0%、43.0%;反应进行到45 min时,PW12/TiO2催化下脱色率达到95.0%:说明PW12经过TiO2掺杂以后,两者产生了协同促进作用,这与李云霞等[23]80和魏君等[29]的研究相符合。其原因可能是PW12掺杂TiO2后,PW12延长了TiO2表面的光生电子与空穴的复合时间,从而提高了催化剂的催化性能。确定PW12/TiO2中PW12与TiO2质量比0.46为最佳。

图3 PW12与不同TiO2掺杂量PW12/TiO2的催化性能比较Fig.3 The comparison of catalytic activities between PW12 and PW12/TiO2 under the different PW12 loaded
2.3 PW12/TiO2催化研究
2.3.1 PW12/TiO2投加量
室温、常压、不调节pH条件下,在100 mL质量浓度为100 mg/L酸性大红3R溶液中,PW12/TiO2中的PW12与TiO2质量比为0.46,考察了PW12/TiO2投加量与脱色率的关系,控制PW12/TiO2投加量在0.10~0.25 g/L。由图4可知, 随着PW12/TiO2投加量的增加,酸性大红3R溶液脱色率先上升后下降,这说明酸性大红3R溶液脱色的主要原因并不是单纯的物理吸附作用,结合前期实验,脱色是在紫外光下的催化反应的结果。当PW12/TiO2投加量为0.20 g/L时,脱色率达到最大,反应进行90 min,脱色率为96.6%,其原因是PW12/TiO2具有一个最佳催化浓度,在紫外光强度一定的情况下,染料分子的电子向催化剂转移,染料显示脱色,当催化剂用量较少时,被转移的电子跟染料分子又重新聚合显色,随着投加量的逐步增加,催化效果增强,但同时被催化剂吸附的也更多[30]。结合经济角度考虑,催化剂投加量在0.20 g/L时较为合理。
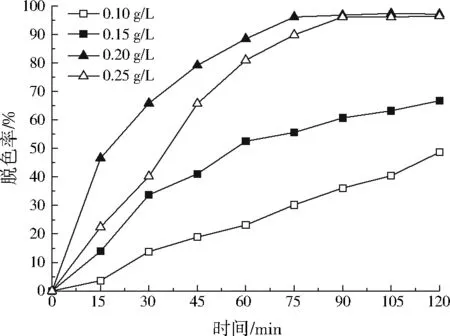
图4 PW12/TiO2投加量与脱色率的关系Fig.4 Relation of PW12/TiO2 additive amount and decolorizing rate
2.3.2 溶液pH
在相同的实验条件下,比较研究了PW12/TiO2和PW12单独催化下pH对脱色率的影响,两种催化剂用量均为0.20 g/L。从图5(a)可知,在酸性大红3R溶液质量浓度100 mg /L, pH在1~6变化时,随着pH的增大,溶液脱色率先上升后下降,当pH=3时,反应进行90 min时,脱色率高达96.5%,这与夏金红[31]的研究结果一致。而由图5(b)可知,在PW12单独催化时,最适pH为2。根据实验结果,两种催化剂最适pH不同,但均在溶液偏酸性时,催化效果最好。光催化过程是分散在溶液里面的催化剂吸附转移染料电子的过程,PW12/TiO2对pH的变化相对敏感:当pH=2时,PW12的分散性要好于溶胶-凝胶法制备的PW12/TiO2,更能吸收利用紫外光;但当pH=3时,PW12/TiO2催化效果优于PW12单独催化。其原因是pH改变了PW12/TiO2颗粒表面的带电情况,进而改变了其在溶液中的分布情况。根据王晓林[32]和熊克思[33]的研究结果,TiO2属于两性金属氧化物,pH与TiO2在溶液中的等电位点有关联,TiO2在水中的等电位点通常为pH=6.25。当溶液中pH高于等电位点时,TiO2表面带有负电荷;当pH小于等电位点时,TiO2表面带正电荷;当pH与等电位点相等时,TiO2表面呈中性。当TiO2表面带有正电荷时,有利于光生电子向表面迁移,从而抑制电子-空穴对(e-/h+)的复合,促进光催化氧化反应速率的提高[34-35]。 确定PW12/TiO2的最适pH为3。
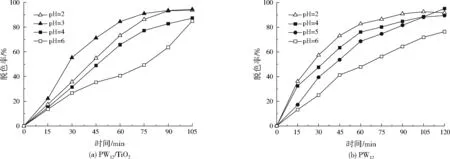
图5 酸性大红3R溶液pH与脱色率的关系Fig.5 Relation of acid scarlet 3R solution pH and decolorizing rate
2.3.3 溶液浓度
从图6可看出,当PW12与TiO2质量比为0.46,PW12/TiO2投加量为0.20 g/L, pH=3,酸性大红3R的脱色率随其浓度的升高先升高后降低。当酸性大红3R质量浓度为100 mg/L时,脱色效果最好,反应进行90 min,脱色率可达97.0%。出现该现象原因是当酸性大红3R溶液浓度较低时,紫外光透射率高,有机染料分子更多地直接接触PW12/TiO2表面,紫外光利用率较高;当溶液浓度继续升高时,PW12与TiO2表现为明显的协同作用,促进酸性大红3R溶液快速脱色;但是当酸性大红3R溶液质量浓度大于100 mg/L时,在一定反应时间内(105 min以内),脱色率表现为逐渐降低。
2.3.4 异丙醇投加量
从图7(a)可看出,在PW12/TiO2催化下,酸性大红3R溶液脱色率随异丙醇投加量的升高总体呈先降低后升高趋势,当异丙醇投加量为0.20 mol/L时,脱色率达到最大,反应进行90 min时,脱色率为87.0%。由图7(b)可看出,异丙醇表现出对PW12催化过程的明显抑制作用,这与魏红等[36]研究得出异丙醇作为电子供体在一定条件下促进酸性大红3R的降解不同,出现此现象的原因可能是异丙醇作为一种电子供体的同时,又是羟基自由基(·OH)的清除剂,并且在TiO2存在的情况下,降低了电子供体位点,突出表现出来的则是异丙醇的存在会大量消耗·OH,从而延缓酸性大红3R溶液的脱色,实验表明在PW12/TiO2催化降解过程中不应该添加电子供体异丙醇。
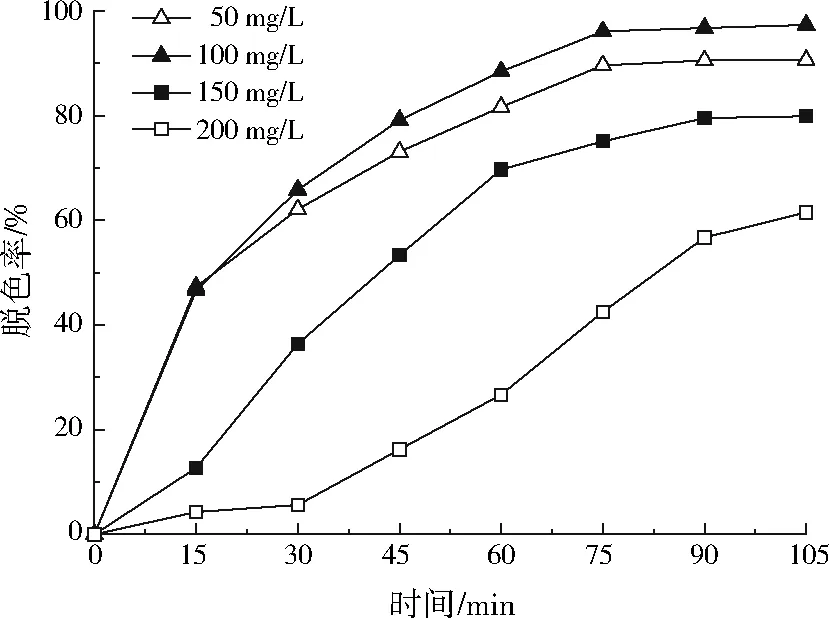
图6 酸性大红3R质量浓度与脱色率的关系Fig.6 Relation of acid scarlet 3R solution concentration and decolorizing rate
2.4 PW12/TiO2效能分析
2.4.1 PW12/TiO2催化动力学
光催化降解有机污染物的反应主要是在液固界面进行,因此PW12/TiO2催化降解偶氮染料的动力学规律可以用修正过的Langmuir-Hinshelwood模型对实验数据进行拟合。该修正公式可表达为:
(2)
式中:t为时间,min;ct为t时刻酸性大红3R质量浓度,mg/L;k为反应速率常数,min-1。
根据图8,由PW12/TiO2催化过程中数据拟合表明,光催化降解反应表现为一级反应。ln(c0/ct)与t成直线关系。
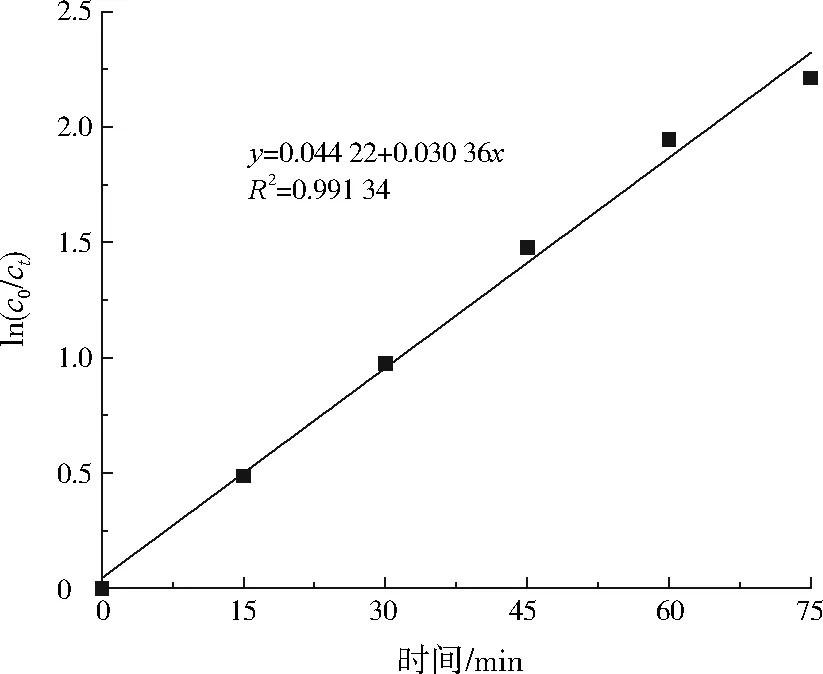
图8 PW12/TiO2催化反应数据拟合Fig.8 Date fitting of PW12/TiO2 catalytic reaction
2.4.2 PW12/TiO2紫外光谱分析
以PW12/TiO2作为光催化剂,在最优催化条件下,即:PW12与TiO2质量比为0.46,PW12/TiO2投加量为0.20 mg/L,酸性大红3R质量浓度为100 mg/L,pH=3,无异丙醇参与下进行反应,每15 min取样一次,在波长为200~600 nm下进行全波长扫描,光催化降解90 min,结果如图9所示。
偶氮染料的脱色降解主要由偶氮双键(—N=N—)的断开和萘的开环引起。催化初始时,酸性大红3R溶液的特征峰出现在507 nm处,即主要为偶氮双键特征吸收峰,随着催化时间的延长,偶氮双键特征峰值逐渐减小,并且吸收峰值逐渐蓝移,说明—N=N—发生断裂,表现为溶液脱色;在蓝移过程中,200~300 nm波长处峰值增大,说明萘开环生成一系列苯系物,表现为偶氮染料逐渐被降解。

图9 不同催化时间下PW12/TiO2催化降解过程的全波长扫描Fig.9 Full wave scanning of PW12/TiO2 catalytic degradation process under different catalytic time
2.4.3 PW12/TiO2效能机制
根据李云霞等[37]和刘秀华[38]的研究,用PW12做P的前躯体,成功将P负载到TiO2的晶体结构中:一方面掺杂后的TiO2粒子具有很大的比表面积,其禁带宽度比纯TiO2明显增大;另一方面,P能够抑制TiO2晶粒的生长并且W原子部分取代TiO2中的Ti原子,从而进入TiO2骨架结构中,这有助于改善Ti—O四面体结构,提高催化效率。柯强[39]研究发现,在受到紫外光照射后,PW12/TiO2能够吸收外界辐射的光能,在高能导带产生光生电子,而在价带则会相应生成e-/h+,可以引发以下反应 :①使催化剂表面的溶解氧、水分子等与e-/h+发生作用,同时生成· OH;②·OH无选择性,与有机污染物通过氢基加合、取代、电子转移等过程,最终生成无毒无害的小分子无机物质。
3 结 论
(1) 通过实验得出,TiO2在掺杂PW12得到PW12/TiO2后,PW12与TiO2表现为协同促进作用;常温下PW12/TiO2最优催化条件:PW12与TiO2质量比为0.46,PW12/TiO2投加量为0.20 g/L,pH=3,酸性大红3R质量浓度为100 mg/L,无异丙醇参与。在此条件下催化降解90 min,酸性大红3R脱色率达到97.0%。
(2) PW12/TiO2作为催化剂,加入电子供体异丙醇,相比PW12单独催化没有表现出明显的抑制作用,但仍低于不投加异丙醇时的催化效果,说明PW12负载TiO2以后,与单纯PW12催化相比,PW12/TiO2催化剂对异丙醇的浓度范围有一定适应性,但仍表现为抑制作用,其催化效果要低于不投加异丙醇。
(3) PW12/TiO2催化降解酸性大红3R的反应属于一级反应;通过紫外光谱分析得知,光催化降解偶氮染料脱色的主要原因是—N=N—断开;吸收峰蓝移,表明萘环断开生成了一系列苯系物,使染料逐渐脱色降解。
[1] 王大鹏.出水回流对强化循环高效厌氧反应器(SCAR)处理印染废水的影响研究[D].上海:东华大学,2015.
[2] 史会剑,朱大伟,胡欣欣,等.印染废水处理技术研究进展探析[J].环境科学与管理,2015,40(2):74-76,80.
[3] 黄丽,陈文艳,万玉山,等.制革废水和印染废水的综合毒性评估及鉴别[J].环境科学,2015,36(7):2604-2609.
[4] SHI Lingdong,BAI Sheying. Degradation of dye wastewater by catalytic wet oxidation at room temperature and atmospheric pressure[J].Chinese Journal of Environmental Engineering,2011,5(6):1325-1329.
[5] 郭丽,王纯莉,王宝臣.活化煤处理印染废水初探[J].环境工程,1993,11(4):7-8.
[6] 胡娟.活性炭吸附对印染废水深度处理的研究[J].环境污染与防治,2009,31(8):46-49,54.
[7] 沈浙萍,梅荣武,韦彦斐.磁生化法处理印染废水的工程实践[J].中国给水排水,2014,30(20):72-76.
[8] 曾杭成,张国亮,孟琴,等.超滤/反渗透双膜技术深度处理印染废水[J].环境工程学报,2008,2(8):1021-1025.
[9] 刘伟京,许明,吴海锁,等.厌氧—好氧—混凝工艺处理印染废水中试研究[J].环境科学研究,2009,22(4):478-483.
[10] ROBINSON T,MCMULLAN G,MARCHANT R,et al. Remediation of dyes in textile effluent:a critical review on current treatment technologies with a proposed alternative[J].Bioresource Technology,2001,77(3):247-255.
[12] CAREY J H,LAWRENCE J,TOSINE H M. Photodechlorination of PCBs in the presence of titanium dioxide in aqueous suspensions[J].Bulletin of Environmental Contamination & Toxicology,1976,16(6):697-701.
[13] LEE J H,KANG M,SUK JIN C,et al. The preparation of TiO2nanometer photocatalyst film by a hydrothermal method and its sterilization performance forGiardialamblia[J].Water Research,2004,38(3):713-719.
[14] KWON C H,KIM J H,JUNG I S,et al. Preparation and characterization of TiO2-SiO2nano-composite thin films[J].Ceramics International,2003,29(3):851-856.
[15] 徐高田,校华,曾旭,等.纳米TiO2光催化—SBR工艺处理印染废水的研究[J].环境科学学报,2007,27(9):1444-1450.
[16] 李克斌,赵峰,魏红,等.磷钨酸均相光催化还原降解水中偶氮染料酸性大红3R[J].高等学校化学学报,2011, 32(8):1812-1818.
[17] 刘淑芝,袁云.二氧化硅载过氧磷钨酸季铵盐催化剂的制备及脱硫性能研究[J].能源化工,2015,36(3):32-35.
[18] 刘士荣,毛明富,倪忠斌,等.磷钨酸修饰的纳米TiO2薄膜的制备及光催化性能[J].功能材料,2010,41(2):346-349.
[19] 汪言满.半导体光催化氧化法处理印染废水的研究[D].广州:广东工业大学,2002.
[20] ATTIA A,KADHIM S H,HUSSEIN F H. Photocatalytic degradation of textile dyeing wastewater using titanium dioxide and zinc oxide[J].Journal of Chemistry,2008,5(2):219-223.
[21] TASBIHI M,STANGAR U L,CERNIGOJ U,et al. Low-temperature synthesis and characterization of anatase TiO2powders from inorganic precursors[J].Photochemical & Photobiological Sciences Official,2009,8(5):719-725.
[22] CAMPOSECO R,CASTILLO S,MUGICA V,et al. Novel V2O5/NTiO2-Al2O3nanostructured catalysts for enhanced catalytic activity in NO reduction by NH3[J].Catalysis Communications,2013,45(5):54-58.
[23] 李云霞,李东妮,朱承驻,等.复合催化剂磷钨酸/TiO2光催化降解苯[J].环境科学与技术,2014(增刊2).
[24] 李珊珊.纳米光催化薄膜的制备及其在印染废水中的应用[D].西安:西安理工大学,2005.
[25] CAO S Y,CHEN C S,NING X T,et al. Preparation and photocatalytic property of graphene/TiO2composite powder[J].Integrated Ferroelectrics,2013,145(1):40-45.
[26] 盛雪,余足玲,刘士荣,等.溶胶凝胶法制备磷钨酸掺杂TiO2薄膜及其光催化性能[J].环境工程学报,2008,2(8):1026-1030.
[27] 盛雪.杂多酸掺杂TiO2薄膜的制备及光催化研究[D].无锡:江南大学,2008.
[28] 张霞,赵岩,张彩碚,等.混晶结构纳米TiO2粉的光催化活性[J].材料研究学报,2006,20(5):454-458.
[29] 魏君,李志奎.多酸/二氧化钛复合光催化剂的制备及光催化苯胺的研究[J].分子科学学报,2012,28(1):84-88.
[30] 刘梅,施翔宇,赵景联.二氧化钛固载杂多酸光催化耦合降解酸性品红染料的研究[J].水工业市场,2011(9):68-71.
[31] 夏金红.二氧化钛粉体光催化降解印染废水的研究[J].应用化工,2005,34(8):497-499.
[32] 王晓林.二氧化钛光催化材料离子掺杂行为及机理研究[D].南宁:广西大学,2005.
[33] 熊克思.掺磷纳米二氧化钛光催化氧化降解印染废水的研究[D].青岛:青岛大学,2008.
[34] 李玲.光催化氧化处理印染废水新进展[J].三峡生态与环境,2008,1(2):34-36.
[35] KATO K,TSUZUKI A,TAODA H. Crystal structure of TiO2thin coatings prepared by the alkoxide solution via the Dip-Coating technique affecting the photocatalytic decomposition of aqueous acetic acid[J].Journal of Materials Science,1993,29(22):5911-5915.
[36] 魏红,李克斌,李娟,等.直接大红4BE的磷钨酸均相光催化还原脱色[J].环境科学,2013,34(6):2271-2276.
[37] 李云霞,李东妮,朱承驻,等.磷钨酸/TiO2催化剂的制备与光催化性能[J].科学技术与工程,2014,14(34):307-311.
[38] 刘秀华.金属离子掺杂二氧化钛光催化剂的改性研究[D].北京:中国工程物理研究院,2007.
[39] 柯强.负载型TiO2可见光催化降解染料污染物的研究[D].杭州:浙江大学,2003.

