石榴皮多酚中安石榴苷的大鼠在体胃吸收动力学研究
田 莉,谢 莉, 张慧慧, 畅 静, 高晓黎
(1新疆医科大学中医学院;2新疆名医名方与特色方剂学重点实验室;3新疆医科大学药学院, 乌鲁木齐 830011)
石榴皮多酚中安石榴苷的大鼠在体胃吸收动力学研究
田莉1,2,谢莉1, 张慧慧1, 畅静1, 高晓黎3
(1新疆医科大学中医学院;2新疆名医名方与特色方剂学重点实验室;3新疆医科大学药学院, 乌鲁木齐830011)
摘要:目的研究石榴皮多酚中安石榴苷的大鼠在体胃吸收动力学特性。方法采用大鼠在体原位胃灌注模型,分别考察石榴皮多酚中安石榴苷的在体胃吸收情况,采用HPLC法测定胃灌注液中药量的变化,并计算胃内药物吸收率。结果石榴皮多酚精制物低浓度(190.55 μg/mL)、高浓度(527.40 μg/mL)及安石榴苷低浓度(80.03 μg/mL)、高浓度(221.50 μg/mL)在体胃每小时平均吸收率分别为(11.68±5.15)%、(11.82±2.41)%、(11.80±1.24)%、(13.02±4.22)%(n=3)。结论安石榴苷在胃部吸收较差,石榴皮多酚精制物中的其他成分对安石榴苷的胃吸收无影响。
关键词:安石榴苷; HPLC; 在体胃灌注模型
石榴皮为石榴(Punica granatum L.)的干燥果皮[1],安石榴苷是石榴皮中的一种特异性多酚成分,约占石榴皮总多酚含量的65.75%,作为一种可水解的单宁物质,其体内外均具有很强的抗氧化活性,具有抑制肿瘤及抗动脉粥样硬化等作用[2]。目前,对石榴皮多酚及其主要成分安石榴苷的研究报道主要为提取工艺的优化、含量测定及药效研究[3-4],对其口服给药后在胃肠道的吸收特性尚未见报道。本实验采用大鼠在体原胃灌注模型来研究安石榴苷单体和石榴皮多酚精制物中安石榴苷在胃内的吸收特性,采用HPLC法测定胃灌注液中药物含量的变化,为口服制剂的剂型设计和提高临床生物利用度提供依据。
1仪器与材料
1.1实验仪器Agilent1220型高效液相色谱仪(安捷伦公司), DKZ型系列恒温振荡浴槽(上海恒科学仪器有限公司),XS105型电子天平(德国,梅特勒-托利多仪器有限公司),TDL-40B型高速冷冻离心机(上海安亭科学仪器厂), PHSJ-3F pH计(上海仪电科学仪器股份有限公司)。
1.2试药石榴皮多酚精制物(新疆医科大学药学院制备),经HPLC测定,安石榴苷的含量为42%,安石榴苷对照品(成都曼思特生物科技有限公司;生产批号:MUST-13010903;HPLC≥98%),甲醇(美国Fisher Scientific;色谱纯),屈臣氏蒸馏水(广州屈臣氏食品饮料有限公司北京饮料分公司),其余试剂均为分析纯。
1.3实验动物健康雌性SD大鼠,体质量(200±10)g,由新疆医科大学实验动物中心提供,动物合格证号:SCXK(新)2011-0004。
2方法与结果
2.1溶液的配制
2.1.1人工胃液的配制按《中国药典》[5]方法配制,不加胃蛋白酶。
2.1.2安石榴苷对照品储备液精密称取安石榴苷对照品适量,用甲醇溶解稀释成230 μg/mL的储备液,-4℃冷藏备用。
2.1.3安石榴苷胃灌注液的配制称取安石榴苷对照品适量,用人工胃液稀释定容至100 mL,配制成浓度分别为低(80.03 μg/mL )、高(221.50 μg/mL)浓度的安石榴苷胃灌流液。
2.1.4石榴皮多酚精制物胃灌注液的配制精密称取石榴皮多酚精制物原料药适量,用人工胃液稀释定容至100 mL,配制成浓度分别为低(190.55 μg/mL)、高(527.40 μg/mL)浓度的石榴皮多酚精制物胃灌流液。
2.2色谱条件YMC-Triart C18色谱柱(4.6 mm×250 mm,5 μm),流动相:甲醇-0.1%磷酸梯度洗脱;梯度洗脱程序:0~10 min,0.1%磷酸95%→85%;10~20 min,0.1%磷酸85%→70%;20~30 min,0.1%磷酸70%→55%;柱温30℃;检测波长370 nm;流速1 mL∕min;进样量10 μL。
2.3方法学考察
2.3.1专属性考察取空白胃灌注液、安石榴苷对照品液、安石榴苷胃灌注液样品、石榴皮多酚精制物胃灌注液样品分别进样10 μL,按“2.2” 项下色谱条件测定,安石榴苷对照品与石榴皮多酚精制物胃灌注液样品特征峰保留时间一致,理论塔板数按安石榴苷的α-苷和β-苷计算均不低于2 000,分离度R>1.5,拖尾因子范围为0.95~1.05,见图1。

A:空白胃灌注液
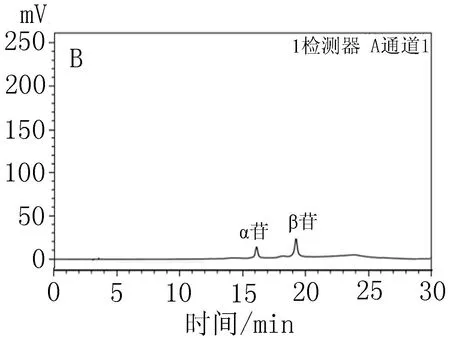
B:安石榴苷对照品液

C:安石榴苷胃吸收样品

D:石榴皮多酚制物胃吸收样品
图1安石榴苷的HPLC图
2.3.2线性范围考察精密吸取安石榴苷对照品储备液各0.5、1.0、2.0、4.0、6.0、8.0、10.0、14.0 μL,按“2.2” 项下色谱条件进样,记录峰面积。以峰面积(A)对安石榴苷含量(X,μg)进行回归,得回归方程A=7 274 485X+752 700(r2=0.999 1),结果安石榴苷在0.115~3.220 μg范围内线性关系良好。
2.3.3精密度和回收率试验取不同体积安石榴苷对照品储备液,置于10 mL棕色容量瓶中,用胃灌注液稀释定容至刻度,得高(230.0 0μg/mL)、中(115.00 μg/mL)、低(57.50μg/mL)浓度的安石榴苷胃灌注液,进样测定,以测定浓度与加入浓度之比计算方法回收率,以1 d内5次测定结果计算日内精密度,以1 w内3 d测定结果计算日间精密度。结果高、中、低浓度的安石榴苷胃灌注液日内精密度RSD分别为4.47%、4.51%、4.53%;日间精密度RSD分别为5.07%、5.05%、5.03%,表明仪器精密度良好。方法回收率RSD分别为9.56%、6.01%、7.76%,表明方法准确。
2.3.4稳定性试验以 “2.3.3” 项下方法配制高、中、低浓度的安石榴苷胃灌注液,置于(25±0.5)℃、(37±0.5)℃恒温水浴锅中避光保温4 h,分别于0、1、2、3、4 h取样测定,考察安石榴苷在胃灌注液中的稳定性。高、中、低浓度安石榴苷胃灌注液在室温25℃、37℃的平均RSD值分别为2.48%、2.96%、1.54%和3.27%、3.45%、5.32%,结果表明安石榴苷在空白胃灌流液中, 25℃、37℃条件下放置4 h保持稳定。
2.4胃壁对安石榴苷的物理吸附、摄取、代谢的考察取大鼠的胃,剖开,翻转胃壁,用生理盐水反复冲洗多次,置于浓度为115.00 μg/mL的供试液中,于(37±0.5)℃恒温孵育3 h后,测定供试液中安石榴苷的含量,结果孵育液中安石榴苷的剩余百分率平均为(96.85±0.02)%,表明胃壁对安石榴苷无明显吸附、摄取或代谢。
2.5安石榴苷的在体大鼠原位胃灌注实验[6]SD大鼠实验前禁食不禁水12 h,10%水合氯醛腹腔注射,麻醉后固定。沿腹中线剪开腹腔,将胃完全暴露,分别在贲门、幽门处切一小口,用人工胃液反复冲洗至无胃液残渣流出,结扎贲门。用注射器吸取含药胃灌注液2 mL从幽门处注入胃内,反复抽取多次至混合均匀,结扎幽门。将胃放回腹腔,保持体温37℃左右。2 h后将胃取出,将胃内容物转移至50 mL烧杯中,用人工胃液少量多次冲洗,将冲洗液一并转移至50 mL容量瓶中,人工胃液定容至刻度,得终浓度Ct的胃灌注液样品,计算药物在胃中2 h的吸收率P (%):
P (%) = (C0×V0-Ct×Vt)/ C0×V0
式中C0:灌注液药物初始浓度(μg/mL);V0:灌注液初始体积(mL);Ct:t时刻灌注液中药物浓度(μg/mL);Vt:t时刻灌注液的体积(mL)。
2.6安石榴苷在胃的每小时平均吸收百分率分别计算安石榴苷和石榴皮多酚精制物的高、低剂量组在大鼠胃的每小时平均吸收百分率,并比较组间差异。结果显示,安石榴苷和石榴皮多酚精制物在胃的每小时平均吸收百分率差异无统计学意义(P> 0.05),同时,高、低剂量在胃的每小时平均吸收百分率差异无统计学意义(P>0.05),见表1。

表1 安石榴苷在胃的每小时平均吸收百分率(±s, n=3)
3讨论
研究药物在胃肠道吸收转运特性可为其口服剂型的设计和提高生物利用度提供依据。安石榴苷分为安石榴苷A和B(α和β异构体),是含有配糖基的鞣花酸多聚体,水溶性好,分子量为1 084.72,不易透过生物膜,有必要研究其胃肠道吸收特性。本实验采用大鼠单向灌流模型研究安石榴苷的在体胃吸收特性,考察安石榴苷对胃壁的物理吸附、摄取、代谢的影响。结果表明,大鼠胃壁对安石榴苷并无明显的吸附、摄取或代谢。安石榴苷和石榴皮多酚精制物中安石榴苷在胃的每小时平均吸收百分率差异无统计学意义(P>0.05),均约为11%,表明安石榴苷的胃吸收差,且石榴皮多酚精制物中的其他成分对安石榴苷的胃吸收无影响。对高、低2个剂量组的每小时平均吸收百分率进行了随机区组方差分析,结果显示在同一浓度,安石榴苷单体和石榴皮多酚精制物中安石榴苷的胃吸收百分率差异无统计学意义(P>0.05),即在此剂量范围内,浓度对吸收百分率没有显著影响,表明其吸收可能为主动转运。
参考文献:
[1]热依木古丽·阿布都拉,来海中,马依努尔·拜克力,等.石榴皮化学成分及生物活性研究进展[J].新疆医科大学学报,2013,36(6):737-740.
[2]张杰,崔艳娜,刘绣华.等.安石榴苷的研究进展[J].化学研究,2014,25(6): 551-562.
[3]周众,焦谊,连政,等. 石榴皮提取物对糖尿病大鼠血糖和血脂的影响[J].新疆医科大学学报,2013,36(6):723-728.
[4]周湘龙,高晓黎,丁楠,等.新疆喀什酸石榴皮总多酚有效部位的纯化工艺优选[J].中国实验方剂学杂志,2013,19(23):54-58.
[5]国家药典委员会.中国药典2010年版[S].二部.北京:中国医药科技出版社,2010:附录XA.
[6]颜晓燕,曾维凤,李敏,等.白花丹醌大鼠在体胃肠吸收动力学初步研究[J].时珍国医国药,2012,23(3):622-624.
(本文编辑施洋)
In situ stomach absorption kinetics punicalagin of pomegranate peel polyphenols in rats
TIAN Li1,2,XIE Li1,ZHANG Huihui1,CHANG Jing1,GAO Xiaoli3
(1CollegeofTCM,XinjiangMedicalUniversity;2XinjiangKeyLaboratoryofFamousPrescription
andScienceofFormula;3CollegeofPharmacy,XinjiangMedicalUniversity,Urumqi830011)
Abstract:ObjectiveTo study the stomach absorption kinetics of punicalagin in pomegranate peel polyphenols in rats. MethodsThe absorption of punicalagin in the rat stomach was investigated using an in situ single-pass perfusion stomach model. The drug concentration was measured by HPLC method. The absorption rates of punicalagin were calculated in the stomach. ResultsThe absorption rates of pomegranate peel polyphenols′ purification at concentrations 190.55 μg/mL, 527.40 μg/mL and punicalagin at concentrations 80.03 μg/mL, 221.50 μg/mL were (11.68±5.15)%, (11.82±2.41)%, (11.80±1.24)%, (13.02±4.22)%, respectively. ConclusionThe absorption of punicalagin is poor in stomach. The other compositions in the purification of pomegranate peel polyphenol have little influence on the stomach absorption of punicalagin.
Keywords:punicalagin; HPLC; in situ single-pass perfusion stomach model
[收稿日期:2015-10-23]
doi:10.3969/j.issn.1009-5551.2016.02.003
中图分类号:R965
文献标识码:A
文章编号:1009-5551(2016)02-0139-03
作者简介:田莉,博士,教授,硕士生导师,研究方向:中药民族药新制剂研究与开发,E-mail:tianli109@126.com。
基金项目:国家自然科学基金(81260668);新疆医科大学“ 天山英才工程” 专项(Y0382002)

