两个含2-(1H-苯并咪唑基)-4-溴苯酚的钴(Π)、锌(Π)配合物的合成、晶体结构及表征
范 艳,瞿志荣
(杭州师范大学有机硅化学及材料技术教育部重点实验室,浙江 杭州311121)
两个含2-(1H-苯并咪唑基)-4-溴苯酚的钴(Π)、锌(Π)配合物的合成、晶体结构及表征
范艳,瞿志荣
(杭州师范大学有机硅化学及材料技术教育部重点实验室,浙江 杭州311121)
摘要:以乙酸钴、2-(1H-苯并咪唑基)-4-溴苯酚为原料通过水热法自组装成新型的配合物[Co(C13H8BrN2O)2]·2(CH3OH) 1;乙酸锌和2-(1H-苯并咪唑基)-4-溴苯酚通过自然挥发法自组装成新型的配合物[Zn(C13H8BrN2O)2]·DMF·3H2O 2.X射线单晶衍射结果表明配合物 1 和 2 都属于三斜晶系,Pī空间群,具有相似的晶胞参数,属于同构体.配合物 1 通过氢键的作用形成一维链状结构,配合物 2 通过氢键的作用形成二维层状结构.两者的荧光及热稳定表征结果表明,配合物 2 比配合物 1 的荧光强度高.
关键词:2-(1H-苯并咪唑基)-4-溴苯酚;配合物;晶体结构;荧光
苯并咪唑类配合物一直是过渡金属配合物研究的前沿领域之一[1-2].由于苯并咪唑类配体具有π-π堆积作用, 因此其金属配合物基元之间可以通过氢键及π-π堆积作用自组装成许多有单核或双核的结构新颖的超分子化合物[3-5].苯并咪唑类金属配合物是一种含有两个氮原子的苯并杂环配合物,具有多种生理活性,可模拟天然超氧化物歧化酶、酸性磷酸酯酶的活性部位[6].此外苯并咪唑结构单元是一类存在于多种药物中的重要结构基元,苯并咪唑的衍生物及其配合物是许多新型药物的有效成分,具有消炎、镇痛作用,并且对细菌、真菌、病毒及肿瘤细胞等表现出良好的抑制效果[7-9]. 苯并咪唑衍生物还可用作铜铝等金属防腐剂、光敏剂、无银照相、表面活性剂、荧光增白剂及光敏染料等[10-12].因此选择合适的配体以及金属离子有助于构筑新型的多功能配位化合物.2-(1H-苯并咪唑基)-4-溴苯酚含两个N原子和一个O原子,具有多个配位点,可以通过氢键、π-π堆积及C—H…π等非共价作用力自组装成多种具有单核或双核的新颖多功能配合物.
本文用乙酸钴、2-(1H-苯并咪唑基)-4-溴苯酚通过水热法合成了配合物 [Co(C13H8BrN2O)2]·2(CH3OH) 1;用乙酸锌、2-(1H-苯并咪唑基)-4-溴苯酚,通过自然挥发法合成了[Zn(C13H8BrN2O)2]·DMF·3H2O 2.X射线单晶衍射结果表明,配合物 1 属于三斜晶系,Pī空间群,是以Co原子为中心构筑的四配位的新型配合物;配合物 2 也属于三斜晶系,Pī空间群,具有相似的结构.并对两者的荧光及热稳定性进行了表征,配合物 1 与配合物 2 相比较,后者的荧光强度大.
1实验部分
1.1 试剂和仪器
所用试剂均为市售分析纯,未进一步提纯.2-(1H-苯并咪唑基)-4-溴苯酚参照文献[13]合成.荧光发射光谱采用Hitachi公司的F-2500荧光光谱仪,热重分析使用NETZSCH公司的TG209C热重分析仪,氮气氛围,氮气流量20 mL/min,升温速率10 ℃/min,温度从室温升至800 ℃.
1.2 配合物的合成
1.2.1配合物[Co(C13H8BrN2O)2]·2(CH3OH) 1 的合成
称取0.049 8 g的Co(CH3COO)2·4H2O(0.2 mmol),0.057 8 g的2-(1H-苯并咪唑基)-4-溴苯酚(0.2 mmol)溶于10 mL甲醇.混合物倒入25 mL聚四氟乙烯内衬的反应釜中,150 ℃反应保持3 d,关闭烘箱,在釜底收集到0.045 g的红色晶体(产率为64.3%).在显微镜下挑选出合适的晶体进行X-Ray晶体结构的测定.
1.2.2配合物[Zn(C13H8BrN2O)2]·DMF·3H2O 2 的合成
称取0.087 8 g的Zn(CH3COO)2·2H2O(0.4 mmol),0.115 6 g的2-(1H-苯并咪唑基)-4-溴苯酚(0.4 mmol)溶于6 mL DMF和4 mL水.混合物在回流条件下搅拌6 h,溶液变澄清,过滤,滤液静置于室温条件下缓慢挥发析出透明的晶体,收集到0.091 g的晶体(产率为59.4%).在显微镜下挑选出合适的晶体进行X-Ray晶体结构的测定.
1.3 晶体结构的测定
使用Bruker Smart Apex Π DUO X射线单晶衍射仪,在293 K条件下,挑选合适尺寸的晶体,用辐射MoKα射线(λ=0.071 073 nm),在设定的2θ范围内收集衍射数据,全部数据通过SADABS[14]程序进行经验吸收校正.晶体结构用SHELXS-97软件由直接法解出,精修采用 SHELXL-97.所有非氢原子的坐标及各向异性温度因子用全矩阵最小二乘法进行修正.除水上的氢原子外,其余氢原子均为理论加氢,通过差值Fourier合成得到.主要的晶体数据列于表1,主要的键长和键角数据列于表2~4.

表1 配合物1和2的主要晶体学参数
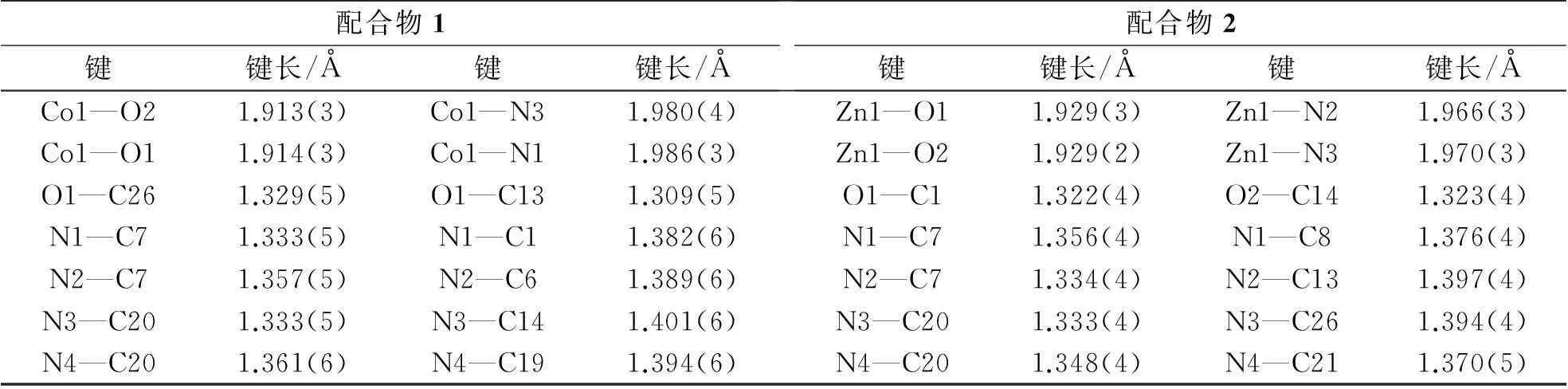
表2 配合物1和2的主要键长

表3 配合物1和2的主要键角
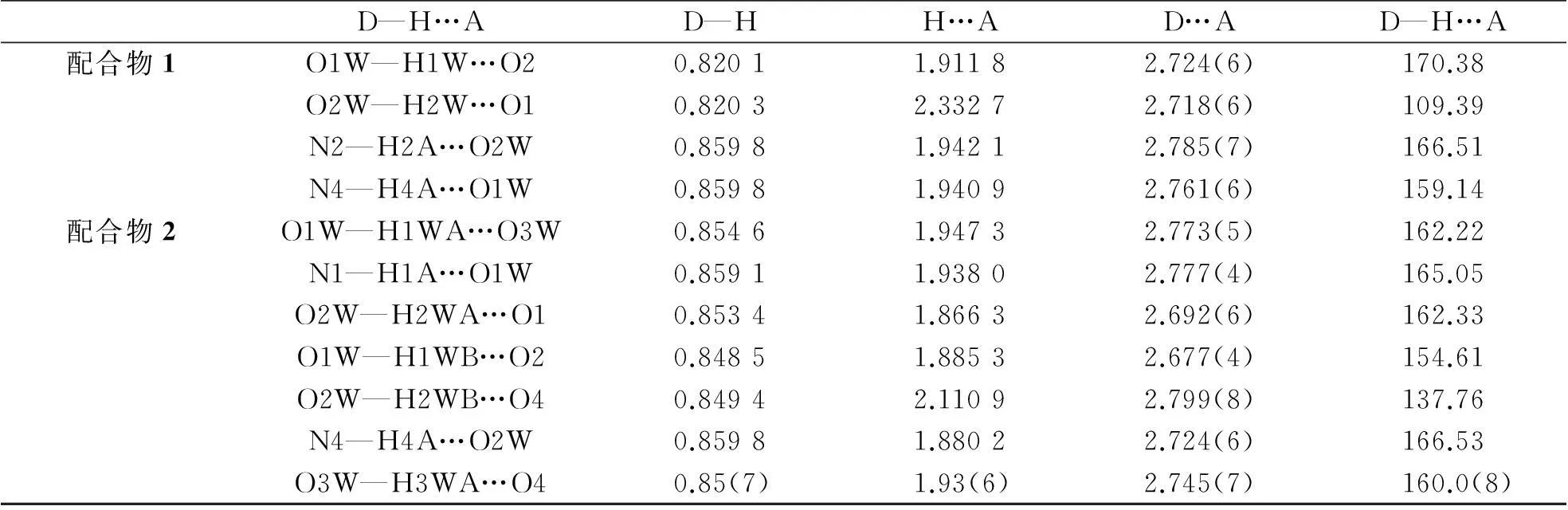
表4 配合物1和2主要的氢键键长和键角
对称操作码:配合物 1,i)-x,1-y,-z; ii)1-x,1-y,1-z.配合物 2, i)x,-1+y,z; ii)1-x,-y,-z; iii)1+x,y,z; iv)1-x,-y,1-z; v)1-x,1-y,1-z.
2结果与讨论
2.1 晶体结构
2.1.1配合物 1 的晶体结构
配合物 1 由一个Co2+、两个2-(1H-苯并咪唑基)-4-溴苯酚阴离子配体和两个游离的甲醇分子组成(图1).中心Co2+采取4配位数的配位模式,4个配位原子是分别来自两个2-(1H-苯并咪唑基)-4-溴苯酚阴离子配体中咪唑环的两个N原子和苯酚环的两个O原子,形成四面体的几何构型.苯并咪唑环和苯酚环的二面角为8.1°,几乎在同一个平面上,而两配体之间的二面角为82.9°.两个配体所在的面接近垂直,O1—Co1—N3的键角为92.33(14)°,O2—Co1—N1的键角为92.86(14)°,其主要的键长键角见表2、3.

图1 配合物1的晶体结构图Fig. 1 Molecular structure of complex 1
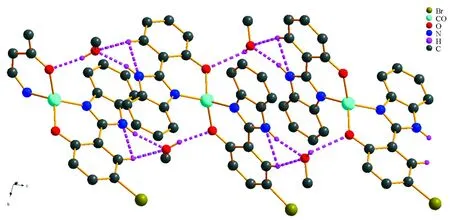
图2 配合物1的一维链状结构Fig. 2 1D chain structure of complex 1
配合物 1 中存在两种典型的分子间氢键:甲醇中的氧原子与配体中的氧原子之间O1W—H1W…O2键长为1.911 8 Å,O2W—H2W…O1为2.332 7 Å,键角分别为170.38°和109.39°;配体中的氮原子跟甲醇中的氧原子之间N2—H2A…O2W键长为1.942 1 Å,N4—H4A…O1W为1.940 9 Å,键角分别为166.51°和159.14°(对称操作码:i)-x,1-y,-z; ii)1-x,1-y,1-z).这几种氢键的存在使得分子之间形成一维的链状结构(图2).分子间还存在C—H…O,C—H…N这两种氢键,加固了一维链状的稳定性.
2.1.2配合物 2 的晶体结构
配合物 2 由一个Zn2+、两个2-(1H-苯并咪唑基)-4-溴苯酚阴离子配体、一个游离的DMF分子和3个游离的水分子组成(图3).中心Zn2+采取4配位数的配位模式,4个配位原子是分别来自两个2-(1H-苯并咪唑基)-4-溴苯酚阴离子配体中咪唑环的两个N原子和苯酚环的两个O原子,形成四面体的几何构型.配合物 2 中存在4种氢键:游离水的氧原子与氧原子之间O1W—H1WA…O3W键长为1.947 3 Å,键角为162.22°(对称操作码:x,-1+y,z);配体中的氮原子与游离水的氧原子之间N1—H1A…O1W键长为1.938 0 Å,N4—H4A…O2W为1.880 2 Å,键角分别为165.05°和166.53°(对称操作码:i)1-x,-y,-z; ii)1-x,1-y,1-z);游离水的氧原子与配体中的氧原子之间O2W—H2WA…O1键长为1.866 3 Å,O1W—H1WB…O2为1.885 3 Å,键角分别为162.33°和154.61°;游离水的氧原子与DMF中的氧原子之间O2W—H2WB…O4键长为2.110 9 Å,O3W—H3WA…O4为1.93(6) Å,键角分别为137.76°和160.0(8)°.通过这些氢键的作用,分子之间构成二维的层状结构(图4).另外,分子间还存在一种弱的非典型氢键C—H…N, C—H…O,这种氢键的存在加固了配合物的稳定性.

图3 配合物2的晶体结构图Fig. 3 Molecular structure of complex 2
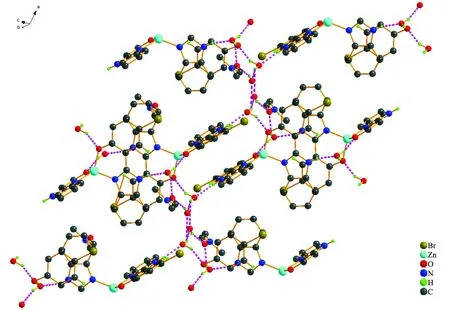
图4 配合物2的二维层状结构Fig. 4 2D layer structure of complex 2
2.2 配合物的热稳定性研究
配合物 1 和 2 从室温到800 ℃范围内的热重曲线见图5.配合物 1在84.3~102.9 ℃,质量损失约2.15%,可能是由于空气中的水分进入配合物中导致的.在178~201.4 ℃,质量损失约10.25%,这与失去两个甲醇分子相应的理论值9.15%吻合.随着温度的升高,配合物发生剧烈分解.配合物 2 在94.5~182.5 ℃,质量损失为6.72%,这与失去3个游离水分子的理论值6.90%吻合.当温度升高到248.8~360.8 ℃时,溶剂分子DMF发生分解,质量损失为8.25%,与理论值9.52%大致吻合.随着温度的升高,配体开始发生分解.可见,配合物 1 和 2 的热稳定性都不是很好,主要是因为配合物中都存在游离的溶剂分子,一般溶剂分子发生分解的温度都比较低.
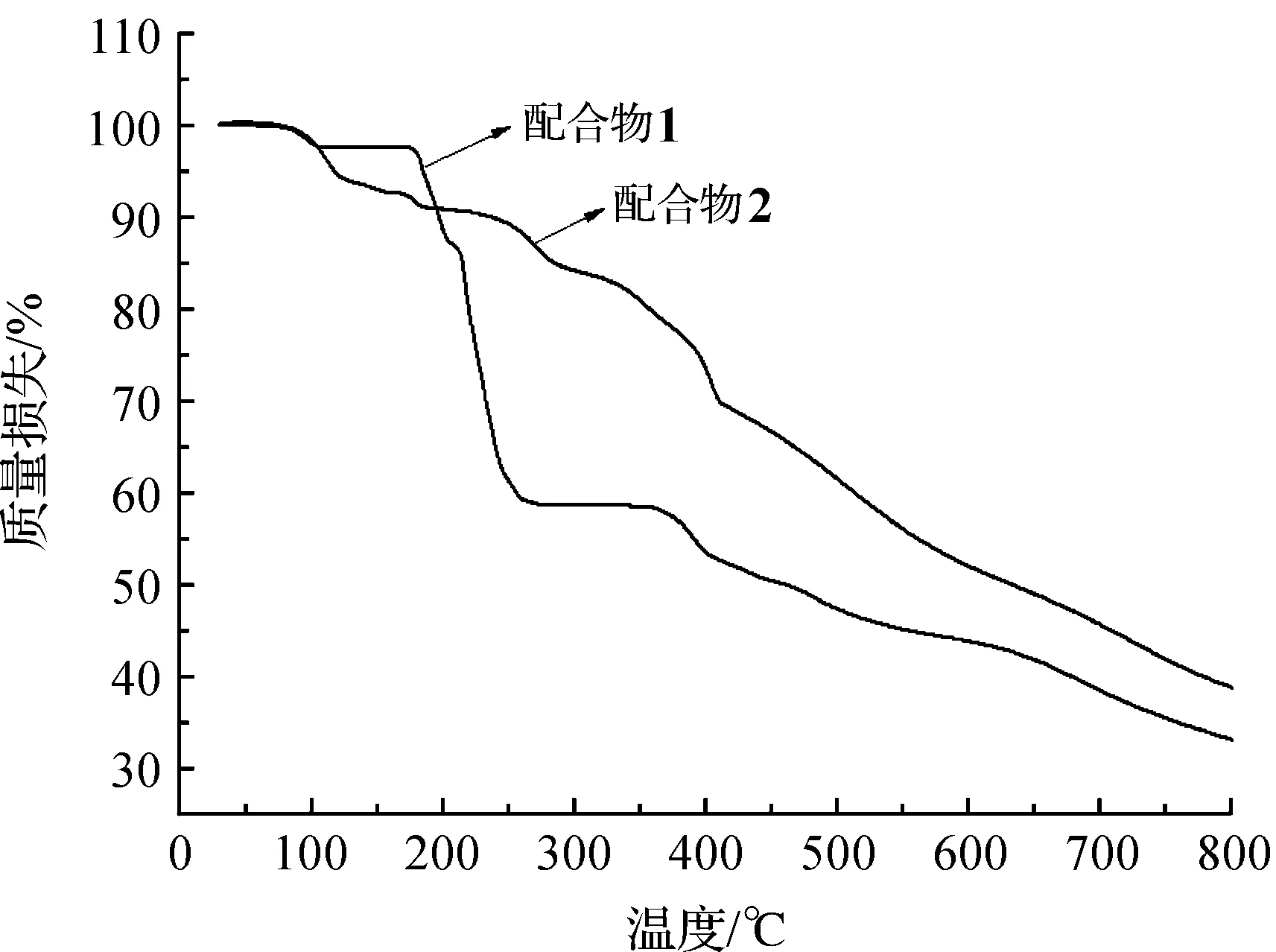
图5 配合物1和2的热重图Fig. 5 Thermogravimetric analysis diagram ofcomplexes 1 and 2

图6 配合物1,2和配体在DMSO溶液中的荧光光谱Fig. 6 Flourescence of complexes 1, 2 and theligand in DMSO solution
2.3 配合物的荧光光谱
配合物 1, 2 和配体在DMSO溶液中1×10-5mol/L的荧光光谱如图6所示,分别在最大激发波长下λ=340,367和342 nm,可能是由于配体分子的π-π*跃迁导致的.配合物 1 的发射峰位于472 nm,配合物 2 的发射峰位于427 nm,与配体的发射峰471 nm相比较,配合物 2 发生蓝移现象,荧光相对减弱,配合物 1 也是荧光淬灭.导致这种现象的原因主要是配合物中有结晶甲醇和结晶水,结晶溶剂有不同作用,在有些化合物中能增强荧光,但大部分情况下是减弱荧光.
为此,本研究测试了配体和配合物的荧光量子产率.9,10-二苯基蒽紫外吸收光谱的3个吸收峰在340,360,370 nm左右,跟本文的配合物相接近,吸收峰的峰型相似,因此选择以9,10-二苯基蒽作为参比,根据公式Φsample=Φstd[Isample/Istd][Astd/Asample][nsample/nstd]2计算配合物的荧光量子产率.9,10-二苯基蒽的Φstd=0.36,DMSO溶液的折射率nsample=1.479,环己烷溶液的折射率nstd=1.426 2,标准参比液在340 nm时吸光度A=0.090,积分面积I=159 679.074,360 nm时A=0.092,I=164 217.358.配合物 1 选择340 nm激发,A=0.055,I=4 329.775,所得Φsample=0.017 2;配合物 2 选择360 nm激发,A=0.085,I=7 725.459,所得Φsample=0.019 7;配体选择340 nm激发,A=0.057,I=15 987.891,所得Φsample=0.061 2.可见,本研究测得的荧光量子产率不高,但配合物 2 的荧光强度相对较大.
3结论
本文用乙酸盐与配体分别通过水热法和自然挥发法合成了两种配合物.配合物 1 通过分子间氢键自组装成了新颖的一维链状的金属配合物;配合物 2 通过分子间氢键自组装成了新颖的二维层状的金属配合物.采用单晶衍射确定了两者结构,并对其热稳定性及荧光性质进行表征,结果表明配合物 2 的荧光强度相对较大,可以作为潜在的荧光材料应用于光电材料领域.
参考文献:
[1] PUJAR M A, BHARAMGOUDER T D, SATHYANARAYANA D N. Cobalt(II), nickel(II) and copper(II) complexes of bidentate binezimidazoles[J]. Transition Met Chem,1998,13(6):423-425.
[2] MATTHEWS C J, CLEGG W, HEATH S L, et al. Coordination of Zn(II), Cd(II), Hg(II), and Ag(I) by bis(benzimidazole) ligands[J]. Inorg Chem,1998,37(2):199-207.
[3] 陈春龙,苏成勇,康北笙.含2-苯并咪唑类配体及其在过渡金属配合物中的配位形式的研究现状[J].中山大学学报(自然科学版),2002,41(5):40-44.
[4] YANG X P, SU C Y, KANG B, et al. Studies on lanthanide complexes of the tripodal ligand bis(2-benzimidazolylmethyl)(2-pyridylmethyl)amine. Crystal structures and luminescence properties[J]. J Chem Soc Dalton Trans,2000,19(7):3253-3260.
[5] SU C Y, YANG X P, KANG B S, et al.Th-symmetric nanoporous network built of hexameric metallamacrocycles with disparate cavities for guest inclusion[J]. Angew Chem Int Ed,2001,40(9):1725-1728.
[6] 胡锦霞.取代苯并咪唑的合成[D].南京:南京理工大学,2005.
[7] BALLET S, SALVADORI S, TRAPELLA C, et al. New 2,6’-dimethyl-L-tyrosine (Dmt)opioid peptidomimetics based on the Aba-Gly scaffold.Development of unique/μ-opioid receptor ligands[J].J Med Chem,2006,49(13):3990-3993.
[8] GUVEN O O, ERDOGAN T, GOKER H, et al. Synthesis and antimierobial activity of some novel phenyl and benzimidazole substituted benzyl ethers[J].Bioorg Med Chem Lett,2007,17(8):2233-2236.
[9] BRUNO R D, NJAR V C O. Targeting cytochrome P450 enzymes:a new approach in ant-cancer drug development[J].Bioorg Med Chem,2007,15(15):5047-5060.
[10] MATTHEWS C J, CLEGG W, ELSEGOOD M R J, et al. Synthesis and crystal structures of some bis-benzjmidazoles, benzothiazoles and benzoxazoles by an alternative route: their complexation with copper(Ⅱ) salts[J]. J Chem Soc Dalton Trans,1996,8(10):1531-1538.
[11] ALBADA G V, LAKIN M T, VELAMAN N, et al. Synthesis, characterization, spectroscopy, and magnetism of dinuclear azido- and alkoxo-bridged copper(II) complexes of bis(2-benzimidazolyl)alkanes. X-ray structures of [Cu2(tbz)2(CH3O)2](ClO4)2(CH3OH)2, [Cu2(tbz)2(NO3)(CH3O)2](NO3)(CH3OH)2, and [Cu(tbz)(N3)2]2(CH3OH)2(tbz = bis(2-benzimidazolyl)propane)[J].Inorg Chem,1995,34(19):4910-4917.
[12] RABAN M, CHANG H, CRAINE L, et al. Stereochemistry in trivalent nitrogen compounds. 42. N-(arylthio)benzimidazoles. Torsional barriers and 1,3 rearrangement[J].J Org Chem,1985,50(13):2205-2210.
[13] ESPARZA-RUIZ A, PENA-HUESO A, NOTH H, et al. Boron coordination compounds derived from 2-phenyl-benzimidazole and 2-phenyl-benzotriazole bidentate ligands[J]. J Org Chem,2009,694(9/10):3814-3822.
[14] SCHELDRICKCK G M. Sadabs[M]. Göttingen: University of Göttingen,1996.

第15卷第1期2016年1月杭州师范大学学报(自然科学版)JournalofHangzhouNormalUniversity(NaturalScienceEdition)Vol.15No.1Jan.2016
Synthesis, Crystal Structure and Properties of Co(Ⅱ), Zn(Ⅱ) Complexes
with 2-(1H-benzimidazol-2-yl)-4-bromophenolato
FAN Yan, QU Zhirong
(Key Laboratory of Organosilicon Chemistry and Material Technology of Ministry of Education, Hangzhou Normal University,
Hangzhou 311121, China)
Abstract:The complex1 [Co(C13H8BrN2O)2]·2(CH3OH) were self-assembled with Co(CH3COO)2·4H2O and the 2-(1H-benzimidazol-2-yl)-4-bromophenolato as raw material by a hydrothermal method and the same ligands with Zn(CH3COO)2·2H2O by natural evaporation method self-assemble into complex2 [Zn(C13H8BrN2O)2]·DMF·3H2O. And the crystal structure of the complexes was characterized by X-ray crystal diffraction. The results show that the complexes 1 and 2 crystallize in triclinic, space groupPī. Complex 1 assembles into a 1D chain structure by the intermolecular hydrogen bonding interactions and the complex 2 assembles into a 2D layer structure. The fluorescent property and thermal stability are also studied, the results show that complex 2 with stronger fluorescence intensity than complex 1.
Key words:2-(1H-benzimidazol-2-yl)-4-bromophenolato; complex; crystal structure; fluorescent
文章编号:1674-232X(2016)01-0001-06
中图分类号:O614.81+32;O614.24+1
文献标志码:A
doi:10.3969/j.issn.1674-232X.2016.01.001
通信作者:瞿志荣(1971—),女,教授,博士,主要从事功能配合物研究.E-mail:quzr@hznu.edu.cn
收稿日期:2015-06-11

