姜黄素炎症靶向自微乳的制备及质量评价*
刘乐环,茅玉炜,黎翊君,戴俊东,黄瑞雪,余家齐,王渐鸿
(北京中医药大学中药学院 北京 100102)
姜黄素炎症靶向自微乳的制备及质量评价*
刘乐环,茅玉炜,黎翊君,戴俊东**,黄瑞雪,余家齐,王渐鸿
(北京中医药大学中药学院 北京 100102)
目的:制备负电荷的姜黄素炎症靶向自微乳给药系统(NC-CUR-SMEDDS),并对其进行质量评价。方法:在前期姜黄素自微乳(CUR-SMEDDS)的研究基础上,以乳剂的粒径、Zeta电位、包封率和载药量为评价指标,通过单因素试验筛选电荷调节剂的最佳用量,制备NC-CUR-SMEDDS。通过观察微乳外观和微观形态并测定其粒径、Zeta电位、包封率及载药量对其进行质量评价。结果:当加入处方量4%的丁二酸二辛酯磺酸钠时,所形成的微乳Zeta电位可以达到-43.43±0.29 mV,外观澄清、透明,粒径分布均匀,平均粒径为14.08±0.082 nm,姜黄素载药量为26.48 mg·g-1,包封率为94.12%。结论:NC-CUR-SMEDDS包封率高,带负电,粒径分布均匀,符合结肠炎症靶向要求。
姜黄素 负电荷 炎症靶向 自微乳给药系统 质量评价
溃疡性结肠炎(Ulcerative Colitis,UC)是一种病因不明的肠道非特异性炎症,易复发,患者生存质量差,可能导致严重并发症,甚至存在癌变可能,目前尚无有效的根治措施[1,2]。当前,临床治疗UC的药物普遍存在靶向性差的问题,导致炎症部位药物浓度偏低,治疗效果不佳;糖皮质激素类药物给药后经吸收入血药量偏高,全身毒副作用较大[3]。所以,如何将药物特异性靶向作用于结肠炎症部位,实现UC的炎症靶向治疗,已成为国内外的研究热点。
分子生物学的研究表明,结肠炎症部位的转铁蛋白(Transferrin,TF)[4]、杀菌/通透性增强蛋白(Bactericidal/permeability-increasing Protein,BPI)[5]、嗜酸细胞阳离子蛋白(Eosinophilcationic Proteins,ECP)[6]等阳离子蛋白表达异常增高,因此使得结肠炎症部位带正电荷。根据此特点制备的炎症靶向水凝胶[7]、荷负电脂质体[8]等,均表现出良好的炎症靶向性。
本课题组前期制备的姜黄素-胡椒碱复方自微乳(CUR-PIP-SMEDDS)[9],可以显著提高姜黄素的溶解度、稳定性和对急性溃疡性结肠炎的治疗作用。本研究拟在前期试验的基础上,通过加入可使自微乳带负电的辅料,制备姜黄素炎症靶向自微乳(Negatively Charged Curcumin Self-microemulsifying Drug Delivery System,NC-CUR-SMEDDS)。利用自微乳乳化后表面负电荷与结肠炎症部位的静电吸附作用和纳米粒子的高度分散作用使药物靶向作用于结肠炎症部位[10],为炎症性肠病的治疗药物,特别是全身毒副作用较大的糖皮质激素和免疫抑制剂等药物的制剂研发提供新思路、新方法。
1 材料
1.1 仪器
SPD-20A型高效液相色谱仪(日本岛津公司);Purospher STAR LP C18色谱柱(4.6 mm×250 mm,5 μm,德国默克公司);BSA223S-CW型电子天平(德国赛多利斯科学仪器有限公司);NANO-ZS型动态光散射粒径仪(英国马尔文公司);Sigma 1-6P小型台式低速离心机(德国赛多利斯科学仪器有限公司); JEM-1230型透射电子显微镜(日本 JEOL 公司);RT10 Power IKA®-WERKE多点加热磁力搅拌器(上海大迈仪器有限公司)。
1.2 试剂
CUR对照品(纯度≥98%,上海诗丹德生物技术有限公司,批号:1784);CUR原料药(纯度=95%,上海源叶生物科技有限公司,批号:R03D6S6966);丁二酸二辛酯磺酸钠(纯度=96%,上海麦克林生化科技有限公司,批号:C10050237);聚氧乙烯氢化蓖麻油(Cremophor RH40,北京凤礼精求商贸有限责任公司,批号:87712168E0);二乙二醇单乙基醚(Transcutol HP,法国Gattefossé公司,批号:143339);丙二醇单辛酸酯(Capryol 90,法国Gattefossé公司,批号:141329);乙腈、甲醇(色谱纯,美国Fisher 公司);水为纯化水,其他试剂均为分析纯。
2 方法与结果
2.1 处方优化与制备
2.1.1 色谱条件
采用Purospher STAR LP C18色谱柱(4.6 mm ×250 mm,5 μm);以乙腈-4%冰醋酸溶液(55:45)为流动相;流速1 mL·min-1;检测波长428 nm;柱温30 ℃,进样量5 μL。理论塔板数按姜黄素峰计算应不低于4 000[11]。
2.1.2 药物的包封率与载药量
按文献方法[11],精密称取NC-CUR-SMEDDS 0.050 g(W0),加甲醇超声溶解,依法检测药物含量(W1)。另取NC-CUR-SMEDDS 0.1 g,精密称定,加37℃的纯化水溶解,依法检测药物含量(W2)。主要计算公式如下:

2.1.3 电荷调节剂用量筛选
自微乳乳化后表面的电性直接影响制剂的靶向性,根据预实验结果,选择调节电荷能力较强的丁二酸二辛酯磺酸钠作为电荷调节剂,按处方量[9](Cremophor RH40: Transcutol HP : Capryol 90=6:3:1)的2%、4%、6%、8%和10%加入,置于50 mL烧杯中,70℃,100 r·min-1磁力搅拌10 min,制备空白SMEDDS。取空白SMEDDS 1.0 g,加入过量CUR原料药,磁力搅拌混匀后超声助溶30 min,室温放置12 h,使药物达到溶解平衡,即得NC-CURSMEDDS。以粒径、Zeta电位、载药量和包封率作为评价指标,采用单因素实验筛选丁二酸二辛酯磺酸钠的加入量,实验结果见表1。
实验结果表明,随辅料加入量的增加,其电位的绝对值呈逐渐升高趋势,但其载药量和包封率呈下降趋势。综合考虑,选择4%作为丁二酸二辛酯磺酸钠的最佳加入量。

表1 丁二酸二辛酯磺酸钠 单因素实验筛选结果(n=3)
2.1.4 处方药物加入量的确定
取含4%的丁二酸二辛酯磺酸钠的空白自微乳1.0 g,分别加入CUR 60.0、50.0、40.0、30.0、20.0 mg,搅拌混合均匀,超声助溶。然后,分别用37℃纯化水稀释100倍,在15 min内60.0 mg和50.0 mg组均有药物析出,说明载药量过大,体系不稳定。因此,选择40.0 mg、30.0 mg和20.0 mg组分别测定0 h和放置8 h后的粒径、载药量和包封率,实验结果见表2。
由表2和图1的结果可知,40 mg组放置8 h后,有明显的药物析出,取上清液测定粒径,粒径明显增大,包封率和载药量也明显下降,说明8 h内稳定性较差;30 mg组在8 h内有少许药物析出,粒径基本保持在14 nm左右,包封率和载药量8 h内降低较少,基本保持稳定;20 mg组在8 h内无药物析出,粒径、包封率和载药量均未发生变化,稳定性最好,但载药量较低,仅为17.84 mg 左右。综合考虑,选择处方药物加入量为30 mg。
2.1.5 NC-CUR-SMEDDS的制备
取Cremophor RH40 6.0 g,Transcutol HP 3.0 g,Capryol 90 1.0 g,丁二酸二辛酯磺酸钠0.4 g,置于50 mL烧杯中,70℃,100 r·min-1磁力搅拌10 min,得空白SMEDDS;称取空白SMEDDS 1.0 g,加入CUR原料药30.0 mg,37℃,50 r·min-1磁力搅拌15 min使之完全溶解,得NC-CUR-SMEDDS。
2.2 NC-CUR-SMEDDS的质量评价
2.2.1 外观
NC-CUR-SMEDDS在4℃时为黏稠、不透明的深红色液体;25℃时为澄清、流动性相对较好、透明的深红色溶液。分别用纯化水、PBS缓冲液稀释100倍后,所得微乳为澄清、流动性好、透明的橙黄色溶液。
2.2.2 微观形态
取NC-CUR-SMEDDS适量,37℃纯化水稀释500倍后用2%磷钨酸染色,透射电镜下观察,结果见图2。NC-CUR-SMEDDS经纯化水稀释后呈圆球型,形态规则,大小较均匀,乳滴之间无粘连,粒径大小在10-50 nm。
2.2.3 粒径分布与Zeta电位
取自微乳适量,37℃纯化水稀释50倍,制备Zeta电位测定用微乳溶液;PBS缓冲液稀释100倍,制备粒径测定用微乳溶液。采用马尔文动态光散射粒径仪分别检测空白乳、CUR-SMEDDS和NCCUR-SMEDDS的Zeta电位和平均粒径,结果见表3。
2.3.4 药物的包封率与载药量
NC-CUR-SMEDDS中CUR的包封率和载药量测定方法同2.1.2。实验结果得CUR的包封率为94.12%,载药量为26.48 mg·g-1。

表2 NC-CUR-SMEDDS加药量的确定(n=3)

图1 0 h和8 h不同加药量自微乳纯化水稀释100倍的微乳外观形态

图2 NC-CUR-SMEDDS乳化后透射电镜图(×80 000倍)
3 讨论
结肠黏蛋白是柱状上皮细胞和杯状细胞分泌的糖蛋白,主要功能是保护肠壁黏膜细胞和润滑肠腔。聚糖中大量的神经氨酸与硫酸残基上带有负电荷,使得结肠组织表面带负电。文献报道[12],在自微乳处方中加入1%油胺,制备得到羟基喜树碱正电荷自微乳,与负电荷自微乳相比能显著提高药物的口服吸收。作者推测其原因主要与正电荷自微乳在体内乳化形成的正电荷微乳乳滴与带负电荷的小肠上皮细胞膜之间产生的静电吸附作用有关。
有研究表明,在UC的活动期,黏蛋白的硫酸化程度降低[13]。同时,在炎症部位,一些阳离子蛋白[4-6]表达异常增高,使得结肠组织表面的电性由带负电变为带正电。根据结肠表面带正电的特点,JubehT[8]等制备了不同Zeta电位(-28 mV,-66 mV)的负电荷脂质体,通过UC大鼠体外粘附试验表明负电荷脂质体在炎症组织部位的吸附强度是正电荷和电中性脂质体的2倍。在正常组织部位,正电荷和电中性脂质体的吸附强度是负电荷脂质体的3倍。其黏附程度与脂质体所带电荷多少直接相关。Zhang S[7]等分别采用DSS和T-bet-/-Rag2-/-(TRUC)制备BALB/c小鼠UC模型,通过小动物在体荧光检测技术进行体外(In vitro),间接体内(ex vivo)和体内(in vivo)黏附实验,证实负电水凝胶(Zeta电位在-40 mV左右)在UC动物模型结肠炎症部位体现出良好的炎症靶向作用,与正常动物对照组相比有显著性差异(P<0.000 1,P=0.012 0,P=0.044 0)。Tirosh B[4]等利用炎症部位转铁蛋白表达增高使结肠组织带正电的原理,制备了负电荷脂质体(Zeta电位为-35 mV),亦达到了较好的炎症靶向效果。综合考虑上述研究成果,本研究将Zeta电位小于-30 mV作为辅料筛选的指标。
通过检索文献,本实验选择了具有乳化作用的牛磺脱氧胆酸钠、牛磺胆酸钠、脱氧胆酸钠、油酸、油酸钠、抗坏血酸棕榈酸酯和丁二酸二辛酯磺酸钠作为自微乳的电荷调节剂。在不改变油相,助表面活性剂,表面活性剂的前提下,加入不同用量的辅料,测定Zeta电位,比较不同辅料之间使自微乳带负电的能力大小。试验结果表明牛磺脱氧胆酸钠、牛磺胆酸钠和油酸钠在空白自微乳中溶解性较差,在最大溶解度范围内,Zeta电位难以达到-30 mV以下;油酸和抗坏血酸棕榈酸酯调节电荷的能力较弱;脱氧胆酸钠和丁二酸二辛酯磺酸钠溶解度相对较好,在加入相同量的脱氧胆酸钠和丁二酸二辛酯磺酸钠时,丁二酸二辛酯磺酸钠调节电荷的能力较强,加入2%时电位即可小于-30 mV,可以达到炎症靶向需要的电位要求,因此选择丁二酸二辛酯磺酸钠作为最佳电荷调节剂。
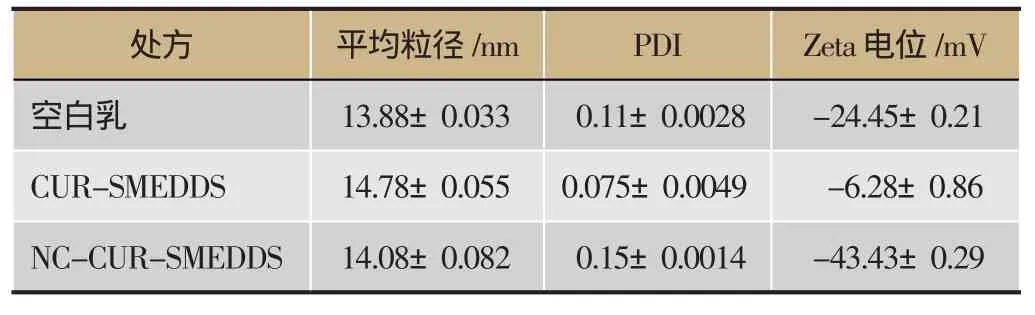
表3 NC-CUR-SMEDDS处方粒径和Zeta电位(n=3)
Zeta电位是表征离子表面电荷情况的一个重要指标,Zeta 电位大于60 mV(或小于-60 mV)时,荷电粒子相当稳定;Zeta电位在30-60 mV时(或在-30--60 mV),荷电粒子比较稳定;在Zeta电位小于30 mV(或大于-30 mV)时,荷电粒子不稳定,容易聚集[14]。本研究制备的自微乳Zeta电位为-43.43 mV,性质稳定。
与前述文献中具有炎症靶向作用的荷负电脂质体和水凝胶相比,本研究制备的负电荷自微乳制备工艺简单、性质稳定,更易于工业化生产。可直接填充于软胶囊,或经由微粉硅胶等固体吸附剂吸附后制备固体制剂[15]。然后根据结肠组织的生理结构特点进一步制备pH依赖型、时间依赖型、压力控制型、酶依赖型、pH-时间依赖型、pH-酶依赖型以及pH-时间-酶依赖型等口服结肠定位给药制剂(Oral Colon-targeted Drug Delivery System,OCDDS)[16],避免药物在体内上消化道的损失,从而实现制剂的结肠靶向作用。到达结肠后,本研究制备的自微乳可自发形成粒径小于20 nm O/W型微乳,通过静电吸附作用实现结肠炎症部位的靶向给药,显著提高难溶性药物的溶解性、稳定性和临床治疗效果。
本研究主要是解决自微乳到达结肠部位后在炎症部位的靶向性问题。后续工作将进一步研究结肠靶向制剂及自微乳中表面活性剂长期使用可能造成的胃肠道黏膜刺激、黏膜渗透性改变和对全身的慢性毒性等问题[17]。
1 Ordás I, EckmannL,Talamini M, et al. Ulcerative colitis. Lancet, 2012, 380: 1606-1619.
2 Bezzio C, Furfaro F, de Franchis R, et al. Ulcerative colitis: current pharmacotherapy and future directions. Expert Opin Pharmacother, 2014, 15(12):1659-1670.
3 Buchman A L. Side effects of corticosteroid therapy. J Clin Gastroenterol, 2001,33(4): 289-294.
4 Tirosh B, Khatib N, Barenholz Y, et al. Transferrin as a luminal target for negatively charged liposomes in the inflamed colonic mucosa. Mol Pharm, 2009, 6(4): 1083-1091.
5 Yoo J W, Irvine D J, Discher D E, et al. Mitragotri, Bio-inspired, bioengineered and bio-mimetic drug delivery carriers. Nat Rev DrugDiscov, 2011, 10(7): 521-535.
6 Lautenschlager C, Schmidt C, Lehr C M, et al. PEG-functionalized microparticles selectively target inflamed mucosa in inflammatory bowel disease. Eur J Pharm Biopharm, 2013,85(3 Pt A):578-586.
7 Zhang S, Ermann J, Succi M D, et al. An inflammation-targeting hydrogel for local drug delivery in inflammatory bowel disease. Sci Transl Med, 2015,7(300): 300ra128.
8 Jubeh T T, Barenholz Y, Rubinstein A. Differential adhesion of normal and inflamed rat colonic mucosa by charged liposomes. Pharm Res,2004,21(3):447-453.
9 Li Q P, Zhai W W, Jiang Q L, et al. Curcumin-piperine mixtures in self-microemulsifying drug delivery system for ulcerative colitis therapy. Int J Pharm, 2015, 490 (1-2):22-31.
10 Lamprecht A, Yamamoto H, Takeuchi H, et al. Nanoparticles enhance therapeutic efficiency by selectively increased local drug dose in experimental colitis in rats. J Pharmacol Exp Ther, 2005, 315(1):196-202.
11 李秋萍,戴俊东,翟文文,等. 单纯形网格法优化设计姜黄素-胡椒碱复方自微乳制剂处方. 中国中药杂志,2014,39(20):3936-3944.
12 郑晓清,张钧寿. 羟基喜树碱自微乳的制备及大鼠体内药动学. 中国药科大学学报,2008,39(2):132-135.
13 朱雄伟. 粘蛋白硫酸化与溃疡性结肠炎. 国外医学·消化系疾病分册,2003,2(1):18-21.
14 刘辉,汤韧,何晓霞,等. 脂质体处方和制备方法对阿昔洛韦棕榈酸酯脂质体稳定性的影响. 药学学报, 2002, 37(7):563-566.
15 赵佳丽,温许,张晶,等. 口服固体自微乳化给药系统的研究进展.药学实践杂志,2014,32(4):257-260.
16 Patel M M. Cutting-edge technologies in colon-targeted drug delivery systems. Expert Opin Drug Deliv, 2011, 8(10):1247-1258.
17 刘明星,王义明,罗国安. 自微乳药物传递系统的研究进展. 药学进展,2006,30(9):397-403.
Preparation and Quality Evaluation of Negatively Charged Self-Microemulsifying Drug Delivery System of Curcumin
Liu Lehuan, Mao Yuwei, Li Yijun, Dai Jundong, Huang Ruixue, Yu Jiaqi, Wang Jianhong
(School of Chinese MateriaMedica, Beijing University of Chinese Medicine, Beijing 100102, China)
The aim of the study was to prepare and evaluate the quality of negatively charged selfmicroemulsifying drug delivery system of curcumin (NC-CUR-SMEDDS). Based on the CUR-SMEDDS, the optimum amount of excipients was confirmed by the single-factor design experiment taking mean particle size, Zeta potential, drug entrapment efficiency and the drug loadings of curcumin as the evaluation indices for the preparation of NC-CUR-SMEDDS. The quality of NC-CUR-SMEDDS was evaluated by observing its appearance status, transmission electron microscope micrographs and determining particle diameter, Zeta electric potential, drug entrapment efficiency and drug loading. As a result, it was found that the Zeta potential reached -43.43±0.29 mV when 4% docusate sodium was added. The appearance of NC-CUR-SMEDDS remained clarified and transparent, and the microemulsion droplets appeared spherical without aggregation with uniform particle size distribution. The mean particle size was 14.08±0.082 nm, the drug loading of curcumin was 26.48 mg·g-1and the drug entrapment efficiency was 94.12%. It was concluded that NC-CUR-SMEDDS with high entrapment efficiency and uniform particle size distribution met the requirement of inflammatory target binding in the colon.
Curcumin, negatively charged, inflammatory target binding, self-microemulsifying drug delivery system, quality evaluation
10.11842/wst.2016.12.022
R943
A
(责任编辑:马雅静,责任译审:朱黎婷)
2016-11-01
修回日期:2016-12-11
* 北京中医药大学自主选题项目(2016-JYB-XS072):姜黄素炎症靶向自微乳治疗溃疡性结肠炎研究,负责人:刘乐环。
** 通讯作者:戴俊东,副教授,硕士生导师,主要研究方向:分子药剂学与新型给药系统研究。

