碳羟磷灰石的制备及对Pb(Ⅱ)的吸附性能
刘 芳,郑艳萍
(兰州城市学院化学与环境科学学院,甘肃 兰州 730070)
碳羟磷灰石的制备及对Pb(Ⅱ)的吸附性能
刘 芳,郑艳萍
(兰州城市学院化学与环境科学学院,甘肃 兰州 730070)
以磷酸和废弃的鸡蛋壳为原料,以尿素和氢氧化钙为添加剂,在50℃下热处理制备合成碳羟磷灰石。通过单因素试验研究碳羟磷灰石对水中铅离子的吸附性能。结果表明,碳羟磷灰石吸附铅的最佳工艺条件为:铅的初始浓度为80mg·L-1,碳羟磷灰石的用量为1.0g·L-1,温度30℃,pH值3.5,搅拌时间110min。在这种条件下,铅离子的去除率为98.01%。碳羟磷灰石对铅的吸附更符合Langmuir吸附模型。
碳羟磷灰石;吸附;铅;去除率
铅是一种广泛存在的不可降解的环境污染物,可通过食物链、土壤、水和空气进入人体,对人体的细胞产生危害[1]。去除铅离子的方法很多,大体可归纳为沉淀法、离子交换法、液膜法、电渗析法和吸附法等[2-3]。其中吸附法是利用多孔性的固体物质,使水中的一种或多种物质被吸附在固体表面从而使其去除的方法[4]。
本实验以废弃的蛋壳为原料合成新型吸附剂碳羟磷灰石(CHAP),并研究碳羟磷灰石对铅的吸附性能。该法吸附工艺操作简便有效,成本低,不会产生二次污染,实现了“以废治废”,是一种环境友好的绿色方案。
1 实验部分
1.1 主要试剂与仪器
氢氧化钾、氢氧化钠、氢氧化钙、氯化铵、硝酸、硝酸铅、尿素(均为AR)。
DF-101型集热式磁力加热搅拌器,DZF-6020型真空干燥箱,PH211型精密酸度计,TAS-990原子吸收分光光度计。
1.2 碳羟磷灰石的制备
将废弃的鸡蛋壳经过自来水洗涤,在5%的NaOH溶液中煮沸,脱去内膜,用蒸馏水洗涤至中性,烘干。将经过预处理的鸡蛋壳磨成粉末,过0.42mm筛,加入到H3PO4溶液中并控制pH值在2~3,在40℃反应3h。过滤去除不溶物,再添加一定量的尿素和Ca(OH)2,用KOH溶液调节pH值在9~10,在50℃条件下处理24h,最后用1%的NH4Cl溶液洗涤至中性,在60℃下干燥,冷却粉碎后得到碳羟磷灰石粉末。
1.3 吸附实验
取一定浓度的含铅模拟废水于烧瓶中,调节不同的pH,加入一定量的CHAP,一定温度下搅拌一段时间后离心分离,取一定量的上层清液,采用原子吸收分光光度计测定Pb(Ⅱ)的平衡浓度,并计算去除率和吸附容量。计算公式见式(1)、式(2)。

式中:Y为去除率;Qe为吸附容量;Co为初始浓度;Ce为吸附平衡时浓度;V为含铅溶液的体积;m为碳羟磷灰石的质量。
2 结果与讨论
2.1 碳羟磷灰石的红外光谱表征
图1是碳羟磷灰石的的红外光谱图。由图1可以看出,3422.2cm-1处为强的羟基特征吸收峰,567.3cm-1、604.4cm-1、960.8cm-1和1051.4 cm-1都是PO4
3-的振动吸收峰[5],1407.6cm-1以及1612.3cm-1处为碳酸根的吸收峰,是碳羟磷灰石含CO32-的重要标志。这些与文献[6]报道的碳羟磷灰石红外光谱图特征峰基本一致,因此,可初步断定所制产品为碳羟磷灰石。
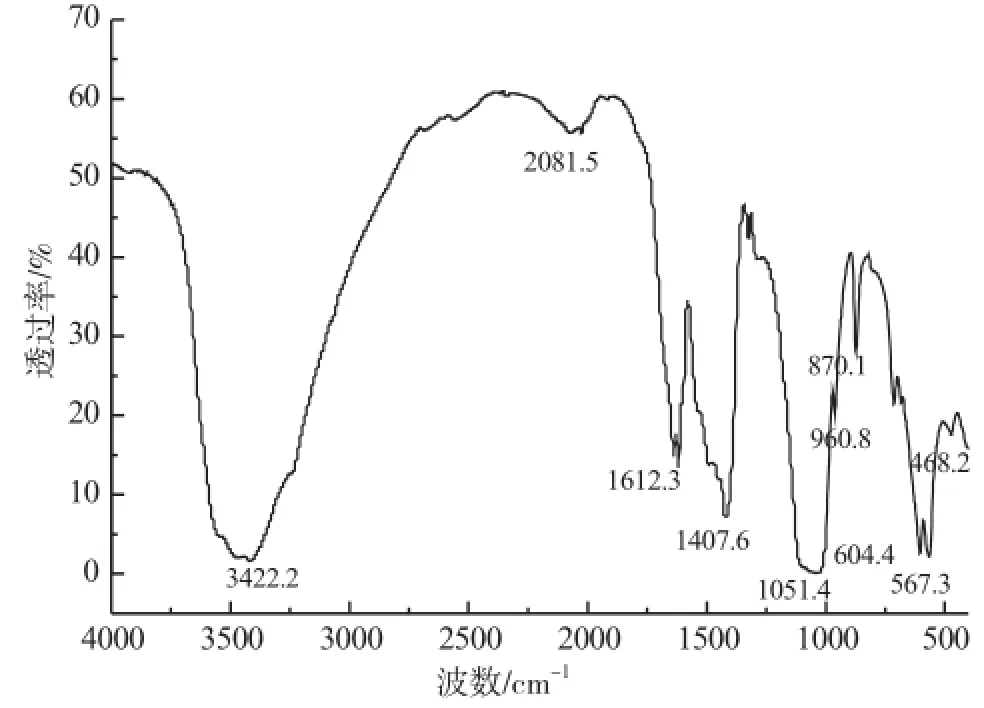
图1 碳羟磷灰石的的红外光谱图
2.2 Pb(Ⅱ)初始浓度对吸附作用的影响
取初始浓度分别为80mg·L-1、160mg·L-1、240mg·L-1、320mg·L-1、400mg·L-1、480mg·L-1的含铅溶液,分别加入1.0g·L-1的碳羟磷灰石,调节pH为3.5,温度控制为30℃,搅拌30min后离心,取上清液测定Pb(Ⅱ)的浓度,并计算去除率。实验结果见图2。

图2 Pb(Ⅱ)初始浓度对吸附作用的影响
从图2可以看出,随着Pb(Ⅱ)初始浓度的增加,去除率呈现下降的趋势,初始浓度为80mg·L-1的去除率最好,去除率为97.30%。其原因是:Pb(Ⅱ)的初始浓度增加,即溶液中Pb(Ⅱ)的总量增加,当吸附达到平衡后,CHAP的量没有增加,当达到吸附平衡后,CHAP没有能力再吸附过多的Pb(Ⅱ),去除率随着Pb(Ⅱ)的初始浓度增加而下降。
2.3 碳羟磷灰石加入量对吸附作用的影响
取5份浓度为80mg·L-1的Pb(Ⅱ)溶液各200mL,置于5个250mL烧杯中,分别加入0.2g·L-1、0.4g·L-1、0.6g·L-1、0.8g·L-1、1.0g·L-1的碳羟磷灰石吸附剂,溶液pH调到3.5,温度控制为30℃,搅拌30min后离心,取上清液测定Pb(Ⅱ)的浓度,并计算去除率。实验结果见图3。

图3 CHAP用量对吸附作用的影响
从图3可以看出,随着碳羟磷灰石加入量增加,去除率逐渐增加。当碳羟磷灰石的加入量为0.2~0.8g·L-1时,去除率增加趋势较大,而大于0.8g·L-1时,去除率增加平缓。原因是当碳羟磷灰石的量达到1.0g·L-1时,基本可以达到去除Pb(Ⅱ)的目的,残余的Pb(Ⅱ)浓度太低,与碳羟磷灰石接触的机会大大减少,故去除率增加不大。
2.4 吸附温度对吸附作用的影响
取5份浓度为80mg·L-1的含Pb(Ⅱ)溶液各200mL,置于5个250mL烧杯中,分别加入1.0g·L-1碳羟磷灰石吸附剂,调节pH值均为3.5,分别控制温度为 20、30、40、50、60℃,搅拌30min后离心,取上清液测定Pb(Ⅱ)浓度,并计算去除率。实验结果如图4所示。
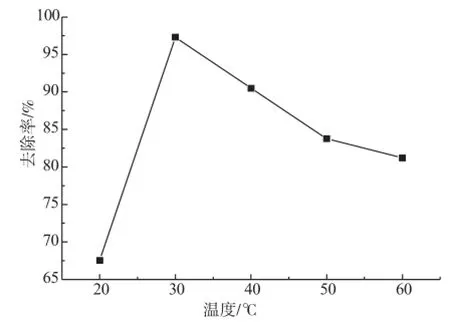
图4 温度对吸附作用的影响
从图4可以看出,温度对碳羟磷灰石的吸附效果有明显影响。随着温度增加,铅离子的去除率是先增大后减小,在30℃时,去除率达到最高。这是因为温度越低,Pb(Ⅱ)及碳羟磷灰石活性下降,导致去除率较低;吸附和脱附是一个动态过程,温度过高发生解吸作用,使得被吸附的Pb(Ⅱ)被解吸,去除率降低。所以温度过高或过低都不利于碳羟磷灰石对Pb(Ⅱ)的吸附。
2.5 溶液pH对吸附作用的影响
取5份浓度为80mg·L-1的含Pb(Ⅱ)溶液各200mL,置于5个250mL烧杯中,分别调节pH值为1.5、2.75、3.5、4.0、5.5,各加入1.0g·L-1碳羟磷灰石吸附剂,温度控制为30℃,搅拌30min后离心,取上清液测定Pb(Ⅱ)的浓度,并计算去除率。实验结果如图5所示。
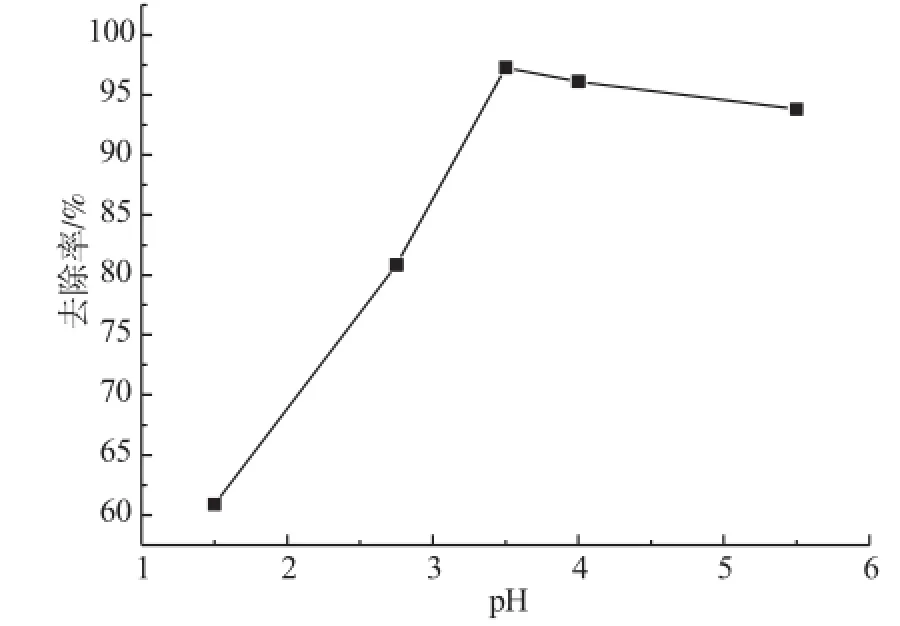
图5 溶液pH对吸附作用的影响
从图5可以看出,pH<3.5时,去除率随pH值增加而增大,pH>3.5时,去除率有所降低。这是因为在较低pH值条件下,溶液中大量存在的H+与Pb2+对活性吸附位点产生竞争吸附,并且少量碳羟磷灰石产生溶解,从而使得去除率不高;随pH值增大,Pb2+的竞争吸附作用占主导地位,促使碳羟磷灰石对 Pb2+的吸附量增大,继续增加pH,增加了铅离子的水解可能性,部分Pb2+转变成沉淀,影响Pb2+的交换及表面络合,降低了碳羟磷灰石对铅的吸附能力[7]。因此,本吸附实验 pH 值选3.5。
2.6 搅拌时间对吸附作用的影响
取5份Pb(Ⅱ)浓度为80mg·L-1的溶液各200mL,分别置于5个250mL烧杯中,各加入1.0g·L-1碳羟磷灰石吸附剂,调节pH值均为3.5,温度控制为30℃,分别搅拌30、70、110、150、190min,离心后,取上清液测定Pb(Ⅱ)的浓度,并计算去除率。实验结果如图6所示。
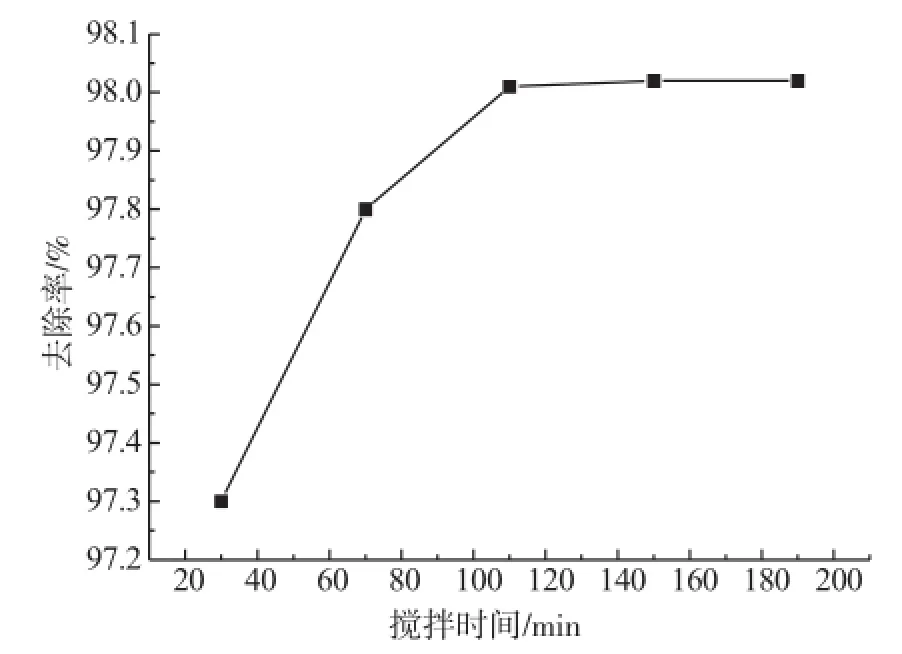
图6 搅拌时间对吸附作用的影响
从图6可以看出,随着吸附时间的延长,去除率逐渐增大再趋于平衡,当吸附110min时,去除率为98.01%。这是因为吸附开始时Pb(Ⅱ)浓度高,Pb(Ⅱ)向碳羟磷灰石表面及其内部的扩散速率较快,表现为去除率增加明显;随着吸附的进行,溶液中Pb(Ⅱ)浓度降低,扩散速率降低,同时由于碳羟磷灰石的有效吸附位减少,造成去除率增加缓慢[8]。由实验结果还可看出,随着时间的增加仍具有较高的去除率,没有出现解析现象,说明Pb(Ⅱ)与碳羟磷灰石的吸附位点形成较强化学键,一旦吸附就不容易解吸。
2.7 吸附等温线
目前常用的吸附等温曲线方程为Langmuir和Freundlich方程。Langmuir线性方程可表示如下:
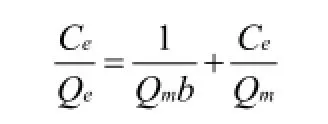
其中:Qm为吸附剂饱和吸附量,mg·g-1;b为吸附常数,L·mg-1。Qm和b可分别由Ce对Ce/Qe作直线方程的斜率)和截距)求出。
Freundlich线性方程可表示如下:
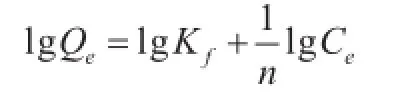
其中:Kf和为经验常数,n和Kf由lgCe对lgQe作直线方程的斜率)和截距(lgKf)求出。
用Langmuir等温式和Freundlich等温式描述CHAP对Pb(Ⅱ)的吸附行为。常温下作吸附实验,并对数据进行回归,结果见表1。

表1 Langmuir和Freundlich方程的吸附模型参数
由表1可知,Langmuir和Freundlich吸附模型均可较好地模拟此吸附实验。根据Langmuir吸附等温式,其模拟结果的相关系数R2=0.9958,说明碳羟磷灰石对Pb(Ⅱ)的吸附符合Langmuir吸附等温式,碳羟磷灰石对Pb(Ⅱ)的吸附符合单分子吸附形式。Freundlich经验分式中1/n为0.36059,说明碳羟磷灰石对Pb(Ⅱ)有较强的吸附能力,从确定系数R2=0.9655可以看出,碳羟磷灰石对Pb(Ⅱ)的吸附更符合Langmuir吸附模型。
3 结论
1)以废弃的鸡蛋壳为原料制备碳羟磷灰石产品。对产品进行红外光谱表征,分析确定该产品为碳羟磷灰石。实验表明,碳羟磷灰石对Pb(Ⅱ)有较好的吸附效果,达到了以废制废的目的,具有较高的开发利用价值。碳羟磷灰石可以作为一种新型的吸附剂对含重金属离子废水处理,治理一些环境污染问题。
2)通过单因素试验,分别探讨Pb(Ⅱ)初始浓度、CHAP用量、温度、pH和搅拌时间对去除效果的影响。由实验结果得到最佳吸附条件为:Pb(Ⅱ)初始浓度为80mg∙L-1,CHAP用量为1.0g∙L-1,温度为30℃,pH值为3.5,搅拌时间110min。在这种条件下,吸附效果较佳,Pb(Ⅱ)的去除率可达98.01%。
3)由实验结果可知,碳羟磷灰石对Pb(Ⅱ)的吸附更符合Langmuir吸附模型。
[1] 刘玉莹.环境铅污染的来源及对儿童的危害[J].职业与健康,2003,19(6):8-9.
[2] 孙文钊.含铅废水处理的分析与实验研究[J].北方环境,2012,24(1):107-108.
[3] 郑少平.碳羟磷灰石的制备及其吸附镍离子的动力学研究[J].工业用水与废水,2008,39(1):81-83.
[4] 陈伟,夏良树,胡思思.乳状液膜技术分离回收金属离子的研究进展[J].化学工程,2013, 41(3):10-15.
[5] 金科,李振兴,吴玟静,林洪.蛤蜊壳羟基磷灰石的制备及对Pb2+的吸附性能[J].食品科学,2013,34 (13):39-44.
[6] 唐文清,曾光明,曾荣英,冯泳兰.碳羟基磷灰石对废水中Zn2+的吸附性能及机理研究[J].金属矿山,2007(3):73-76.
[7] 唐文清,冯泳兰,李小明.掺硅碳羟基磷灰石的制备及其对 Pb2+的吸附性能[J].中国环境科学,2013,33(6):1017-1024.
[8] 张双圣,刘喜坤,刘倩,刘汉湖,于向辉,谢晗.纳米羟基磷灰石的制备及其对Pb2+的吸附性能[J].化工环保,2012,32(2):123-128.
Preparation of Carbonate Hydroxyapatite and its Adsorption Capacity for Pb(Ⅱ)
LIU Fang, ZHENG Yan-ping
(College of Chemistry and Environmental Science, Lanzhou City University, Lanzhou 730070, China)
Carbonate hydroxyapatite (CHAP) was synthesized through thermal treatment at 50℃ with phosphoric acid and wasted egg shells as the raw materials and urea and calcium hydroxide as the additives. CHAP’s property to absorb lead ion in water was researched by single factor experiment. The results showed that the optimum conditions for CHAP to absorb lead were: initial concentration of lead ions was 80mg/L, dosage of CHAP was 1.0g/L at 30℃, pH was 3.5 and the stirring time was 110min. Under these conditions, removal rate of lead ion was 98.01%. CHAP’s absorption of lead was more in line with the Langmuir absorption model.
cabonate hydroxyapatite; adsorption; lead; removal ratio
X 781
A
1671-9905(2016)05-0053-04
刘芳(1987-),女,硕士,主要从事功能材料的研究。电话:13893427219,E-mail: liufangq@163.com
2016-03-18

