可溶性微生物产物对偶氮染料废水脱色及产电性能的影响
朱 超, 解井坤, 王 媛, 易维洁
(1.陕西科技大学 资源与环境学院, 陕西 西安 710021; 2.贵州大学 农学院, 贵州 贵阳 550025)
可溶性微生物产物对偶氮染料废水脱色及产电性能的影响
朱超1, 解井坤1, 王媛1, 易维洁2
(1.陕西科技大学 资源与环境学院, 陕西 西安710021; 2.贵州大学 农学院, 贵州 贵阳550025)
摘要:可溶性微生物产物(Soluble Microbial Product,SMP)是活性污泥污水处理体系中的微生物的重要代谢产物,是污泥絮体形成以及保证体系稳定运行的关键因素之一.本文对CASS和A2O工艺产生的脱水污泥进行了好氧和厌氧培养,提取了SMP和胞外聚合物(Extracellular Polymeric Substances,EPS),表征并探究了两者对含偶氮染料废水的微生物燃料电池产电性能的影响,以及对脱色效率的改善情况.红外分析表明,不同工艺和培养方法得到的SMP和EPS的成分构成相似度很高;PACl沉降试验表明,SMP中的大分子物质含量普遍低于EPS.SMP和EPS均可提升微生物燃料电池的电压,最高可达130 mV,且两者均可提高偶氮染料的脱色率,最高可达93%.这些研究表明SMP和EPS有作为染料废水产电资源化助剂的价值.
关键词:可溶性微生物产物; 胞外聚合物; 偶氮染料; 微生物燃料电池
0引言
可溶性微生物产物(Soluble Microbial Products,SMP),是指微生物在降解底物、合成细胞生物质过程中产生的有机大分子,如溶解性的胞外酶、多糖等[1].有时,其也以胞外聚合物(Extracellular Polymeric Substances,EPS)的形式存在.EPS是一些不同类型高分子物质[2]的聚合体,是一类附着于细胞表面的不溶性有机物,主要来源于微生物的新陈代谢和细胞自溶,由多糖、蛋白质、核酸和腐殖酸等组成[3].SMP通常溶解于出水中,从而降低了出水水质,使出水难以达到排放标准[4].此外,SMP自身的毒性以及膜生物反应器中对膜的污染亦引起了人们越来越广泛的关注[5].
由于SMP本身是多种有机质的复合体,又包含氧化还原载体,故可作为电子载体,有成为微生物燃料电池燃料的潜力.微生物燃料电池(Microbial Fuel Cells,MFC)是一种利用微生物作为催化剂氧化有机和无机物质产生电流的装置[6].阳极附近的微生物氧化代谢基质产生的电子被转移至阳极并通过连有负载的外电路流至阴极,继而伴随产生相反的电流[7].其中,产生的电子可通过电子中介体、电子穿梭体或细胞膜的直接接触转移至阳极,有的微生物还具有转移电子的纳米导线结构,当然也有可能存在目前不为人知的电子转移机制[8].将微生物燃料电池代谢SMP这一思路用于基于活性污泥的污水处理系统,可在减缓系统中SMP污染的同时产生电能,并可偶联电解或产氢其它后续单元[9].
目前,关于SMP和EPS对微生物燃料电池(MFC)性能影响的研究仍然很有限.从SMP和EPS的组分构成角度来看,两者都有成为微生物燃料电池(MFC)燃料的潜力.SMP和EPS中众多氧化还原脱氢酶系能够促进微生物燃料电池(MFC)处理复杂的有机质[10].更重要的是,微生物燃料电池(MFC)中的电子转移机制之一是微生物依靠内源分泌的可溶性氧化还原介体作为电子载体来进行电子转移,但是其对MFC处理含偶氮染料废水体系产电能力的贡献度尚不清楚[11].
本研究对不同污水处理工艺中的脱水污泥进行了好氧和厌氧培养,提取了SMP和EPS,进行了表征,并进一步用于处理偶氮染料废水的单室微生物燃料电池的产电研究.通过监测其电压变化,探究了SMP和EPS对含偶氮染料废水的微生物燃料电池产电性能的影响.同时,还探究了SMP和EPS对偶氮染料脱色效率的改善情况,并阐明了可能机制.这对于利用MFC进行偶氮染料废水资源化技术的推广发展具有十分重要的意义.
1材料和方法
1.1材料和设备
试验用活性污泥样品均取自于污泥脱水车间.样品1取自陕西咸阳市某污水处理厂.该污水处理厂使用CASS工艺,运行效果良好,其进出水指标如表1所示;样品2取自陕西西安市第五污水处理厂.该污水处理厂使用A2O工艺,运行工艺良好,其进出水指标如表2所示.
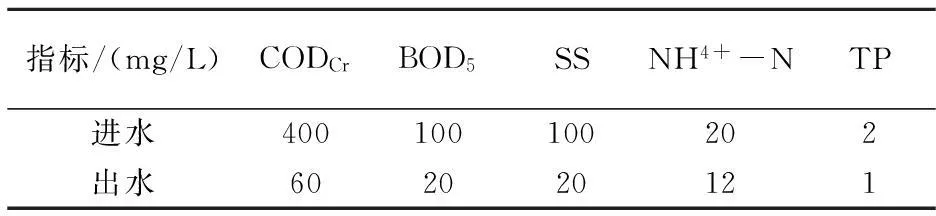
表1 CASS工艺水质指标
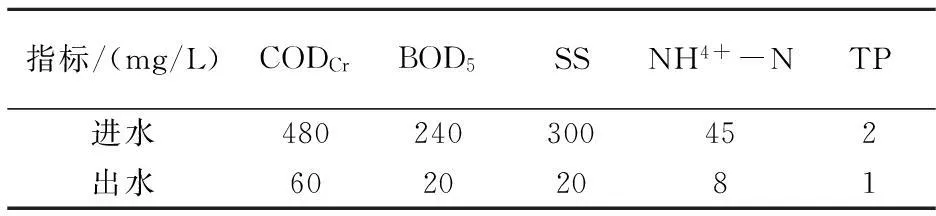
表2 A2O工艺水质指标
本研究所使用的MFC为单室无膜MFC,设备的搭建如图1所示.磁力搅拌器上放置一个100 mL的烧杯,用铜线将表面摩擦处理后的石墨棒与石墨片固定分别作为阴极和阳极.阴阳两极出线分别和万用表(上海优利德电子有限公司)、外接可变电阻箱(上海东茂电子科技有限公司),以及连接电脑的电流数据采集卡(National Instrument Corporation)串接.MFC运行条件为室温,无刻意避光处理.
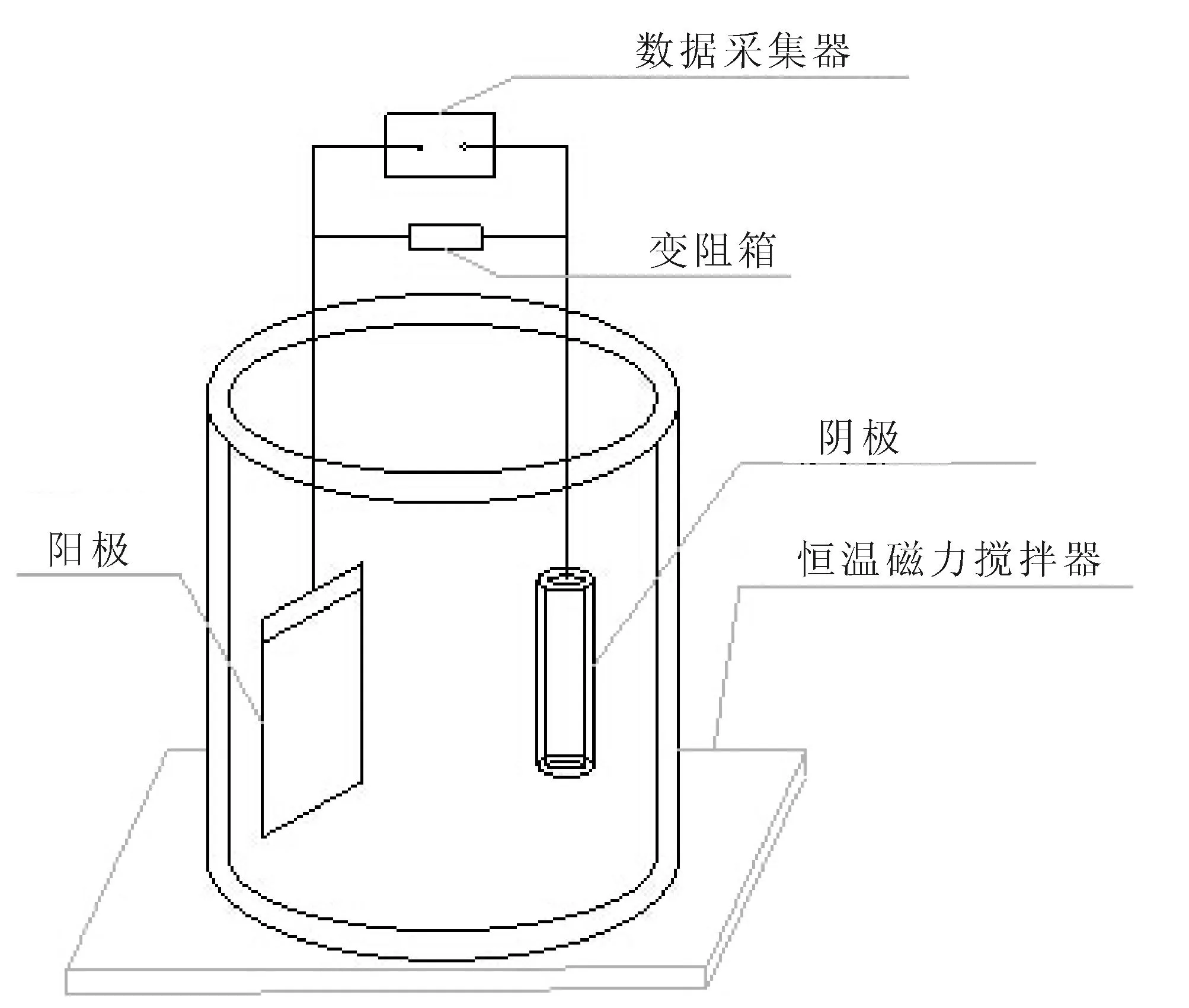
图1 MFC实验装置
1.2试验方法
1.2.1SMP和EPS的培养富集
所采集不同工艺的原始污泥一部分采用连续曝气进行好氧培养.实验装置采用2个5.0 L的平底塑料烧杯.反应器中分别加入150 g污泥和1 500 mL蒸馏水,在运行过程中保持溶解氧大于2 mg,温度保持在25 ℃,通过补加蒸馏水补偿水分蒸发损耗.
原始污泥的另一部分进行厌氧培养.使用4个500 mL的玻璃培养瓶,分别装入25 g污泥和250 mL蒸馏水,将培养瓶放入恒温箱中,保持在35 ℃,避光培养.培养时间为2个月,结束时所得污泥即为富集了EPS和SMP的消化污泥.
1.2.2SMP和EPS的分离
SMP和EPS的提取方法较多,没有建立标准方法[12,13].本实验所用方法建立在已有报道基础上[14,15],具体是:将章节1.2.1中所得污泥消化液在7 330 rpm(相对离心力)下离心10分钟,分离上清液,加入2倍体积的丙酮, 于4 ℃下放置24 h进行沉淀,所收集到的沉淀物即为SMP.
将上述离心分离后的沉淀物悬浮于0.85%(w/w)的NaCl溶液中,容器中放置多个玻璃珠,在20 kHz、330 W的条件下超声(上海乔跃电子有限公司生产的超声仪)处理2分钟,之后在120 rpm下振荡10分钟,最后再次超声处理2分钟,所得裂解液以10 460 rpm离心10分钟,再向所得上清液加入2倍体积的丙酮,于4 ℃放置24 h后沉淀EPS.
上述所得样品按照“分离物-(培养方式-工艺)”格式分别命名为EPS(好氧CASS)、EPS(好氧A2O)、EPS(厌氧CASS)、EPS(厌氧A2O)、SMP(好氧CASS)、SMP(好氧A2O)、SMP(厌氧CASS)和SMP(厌氧A2O)等.
1.2.3SMP和EPS的基本性质测定
对所得到的EPS和SMP,进行傅立叶红外光谱(德国Bruker公司生产的光谱仪)分析[16]以及电导(上海三信仪表厂生产的笔式电导率仪)和pH(上海精科公司生产的pH计)的测定.同时,对所得EPS和SMP溶液进行聚合氯化铝(PACL)沉降试验.通过进行PACL沉降试验,可以将水样中的胶体颗粒和大分子物质沉降下来,并可以比较SMP和EPS中的大分子物质量.
具体方法为:配置含11%Al2O3的1 000 mg/L的PACL溶液.将不同处理得到的SMP和EPS水溶液在200 rpm下离心1 min,然后将PACL缓慢地注入到磁力搅拌下的溶液中,再将混合溶液以50 rpm离心8.5 min,使用浊度计(上海昕瑞仪器仪表有限公司生产)测定离心后的溶液浊度.进行PACL沉降试验时,PACL的加入量分别为0.5 mg、1.0 mg、1.5 mg等.
1.2.4SMP和EPS对MFC产电性能的影响
首先,配制1 L浓度为 100 mg/L的金橙I溶液和1 L 浓度为4 g/L的葡萄糖溶液,将稳定启动后的微生物燃料电池MFC中的原溶液移除,随即加入60 mL金橙Ⅰ溶液和20 mL葡萄糖溶液,并测定此时的电压值.
在电压稳定时(25 mV左右),向其中加入4 mL的SMP或EPS,并测量随后的电压变化,记录电压峰值和持续时间;当电压再次下降到25 mV时,再加入另一种SMP或EPS溶液,如此交替,直到试验完所有的SMP和EPS样液,共有8个循环.
1.2.5SMP和EPS对MFC偶氮染料脱色性能的影响
为了考察SMP和EPS对偶氮染料金橙I的脱色率的影响,分别将3 mL不同处理得到的SMP或EPS溶液及0.5 mL接种液(分离株的对数生长期菌液)、6.5 mL金橙I溶液加到空白试管,避光室温培养,0小时和48小时后测量其吸光度,然后计算脱色率.
在研究偶氮染料脱色降解的过程中,采用分光光度法作为主要的分析手段.当染料内发生键的断裂,使其分子内离域的π键变化,从而影响其颜色时,染料的最大吸收峰处的数值会明显下降[17].因此,可以通过不同染料的最大吸收峰处吸光度的变化来表征染料的降解.将含有染料以及菌体的培养基离心(8 000 rpm,10 min),取上层清液,以未加染料的培养基作为参照,来测量染料最大吸收波长处的吸光度.
2结果与讨论
2.1SMP和EPS的基本性质
图2为从不同工艺活性污泥及富集方式得到的SMP和EPS溶液的pH值比较情况.从图2可以看出,所得SMP和EPS溶液均为中性偏碱性;图3为不同处理SMP和EPS样液的电导值比较情况.从图3可知,EPS的电导值明显高于SMP.厌氧CASS中的EPS电导值最高为49.9 ms,而SMP样液的最高电导值却只有不到10 ms.
一般来说,溶液电导率和温度、掺杂程度及各向异性有关[18].在相同的测量温度下,推测EPS中的掺杂程度高一些,其中的可移动的离子浓度高,离子所带的电荷数多,所以测得的电导率高.已有报道[19]指出,相同工艺和运行条件下的活性污泥分理出的EPS的蛋白质和碳水化合物含量要高于SMP,该结论证实了此处EPS掺杂程度高的推测.
在EPS的四个样品中,厌氧CASS的EPS电导值最高,这是因为厌氧培养中动力消耗少,可以更好地储存物质,其所分泌的代谢物也更多,包括有机大分子物质和可移动离子,所以厌氧培养下的CASS工艺污泥中提取的EPS样液电导值最高.这一推论也通过PACL沉降试验得以证实.
如图4所示,厌氧培养下的SMP和EPS中的大分子物质含量普遍高于好氧培养,且不同培养方式下EPS中的大分子物质含量均高于SMP,其中A2O活性污泥厌氧培养中提取的EPS中的大分子物质最多.这同时说明不同工艺来源污泥对SMP和EPS的性质影响不大,而有氧或厌氧的培养模式则对两者的性质影响较大.
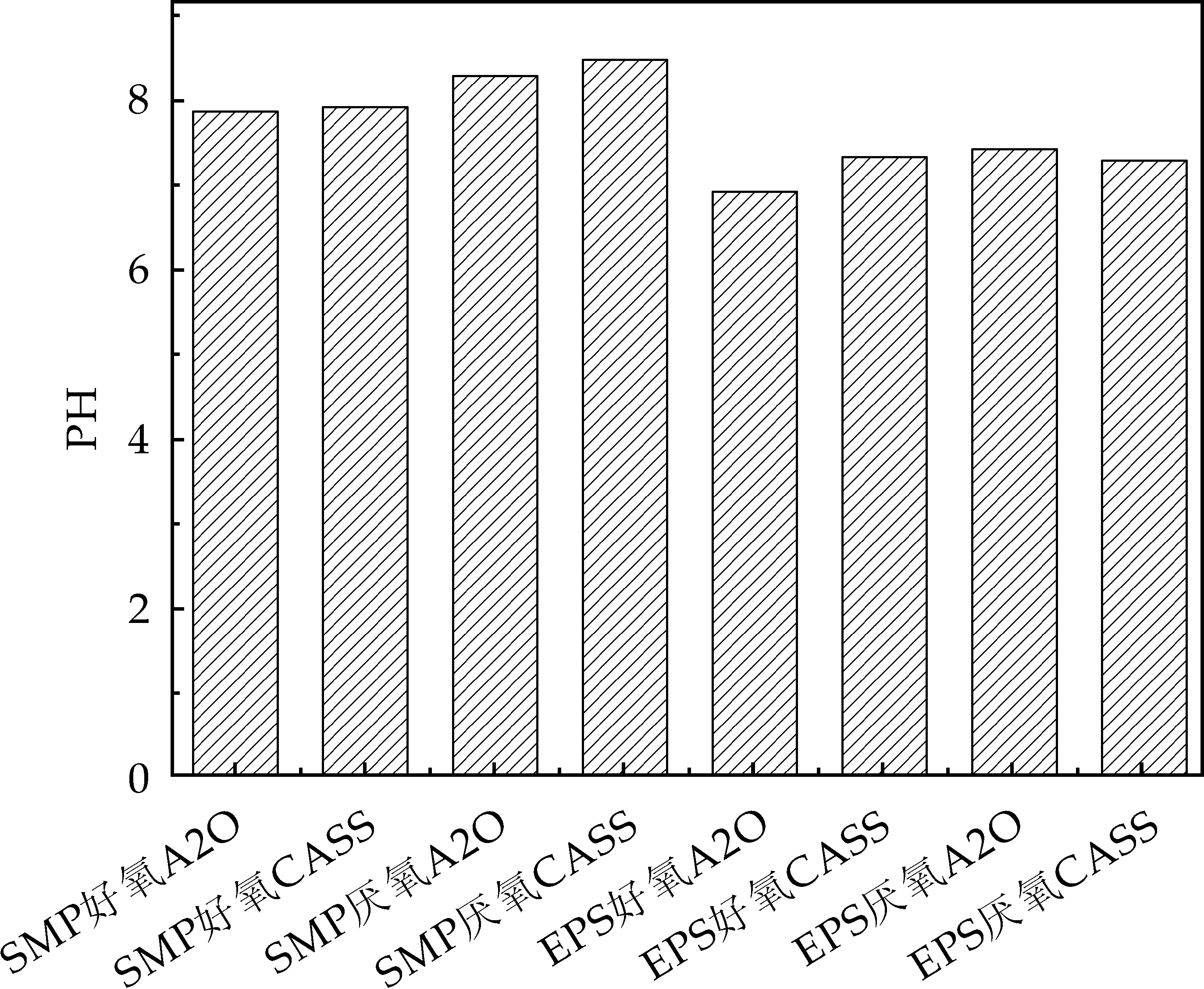
图2 不同处理SMP和EPS的pH值
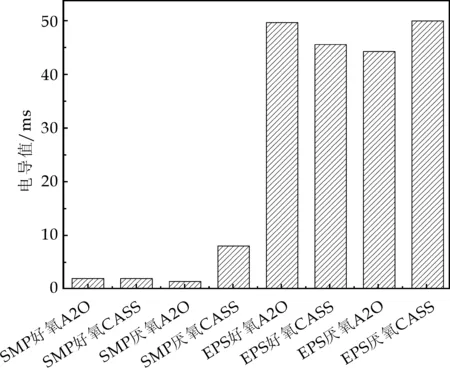
图3 不同处理SMP和EPS的电导值
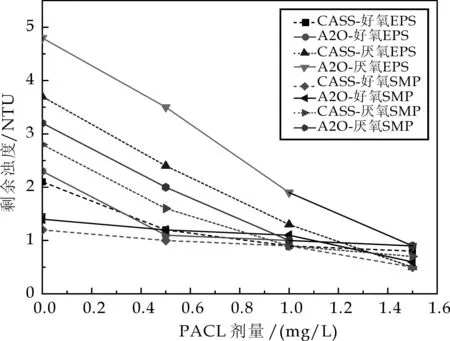
图4 不同处理SMP和EPS样液的PACl沉降结果
2.2SMP和EPS的红外分析
通过提取丙酮中分离的沉淀物质,将其干燥并进行傅里叶红外光谱分析,所得图谱如图5所示.从图5可以发现,好氧和厌氧所提取的SMP和EPS的波形相似度很高,其中所有图的出峰位置多集中在3 500 cm-1、2 900 cm-1、1 600 cm-1、1 400 cm-1、1 000 cm-1和500 cm-1.而在红外光谱分区中,第一峰区4 000~2 500 cm-1为X—H伸缩振动区(X=O,N,C,S);第二峰区2 500~2 000 cm-1为三键、累积双键伸缩振动区;第三峰区2 000~1 500 cm-1为双键伸缩振动区;第四峰区1 500~600 cm-1为X—Y伸缩、X—H变形振动区.
由此可知,本研究所得SMP和EPS中的物质多为蛋白质和多聚糖,相互间相似度很高.在相关研究中,有部分学者认为SMP和EPS是相互独立的两个范畴,它们之间并没有任何关系;还有部分学者认为,在混合废水中可溶性的EPS等同于松散的EPS结合在一起,也就是我们常说的SMP[20].本实验结果表明,SMP和EPS是一类多组分混合物,不同工艺和培养方式并未改变SMP和EPS的物质组成.
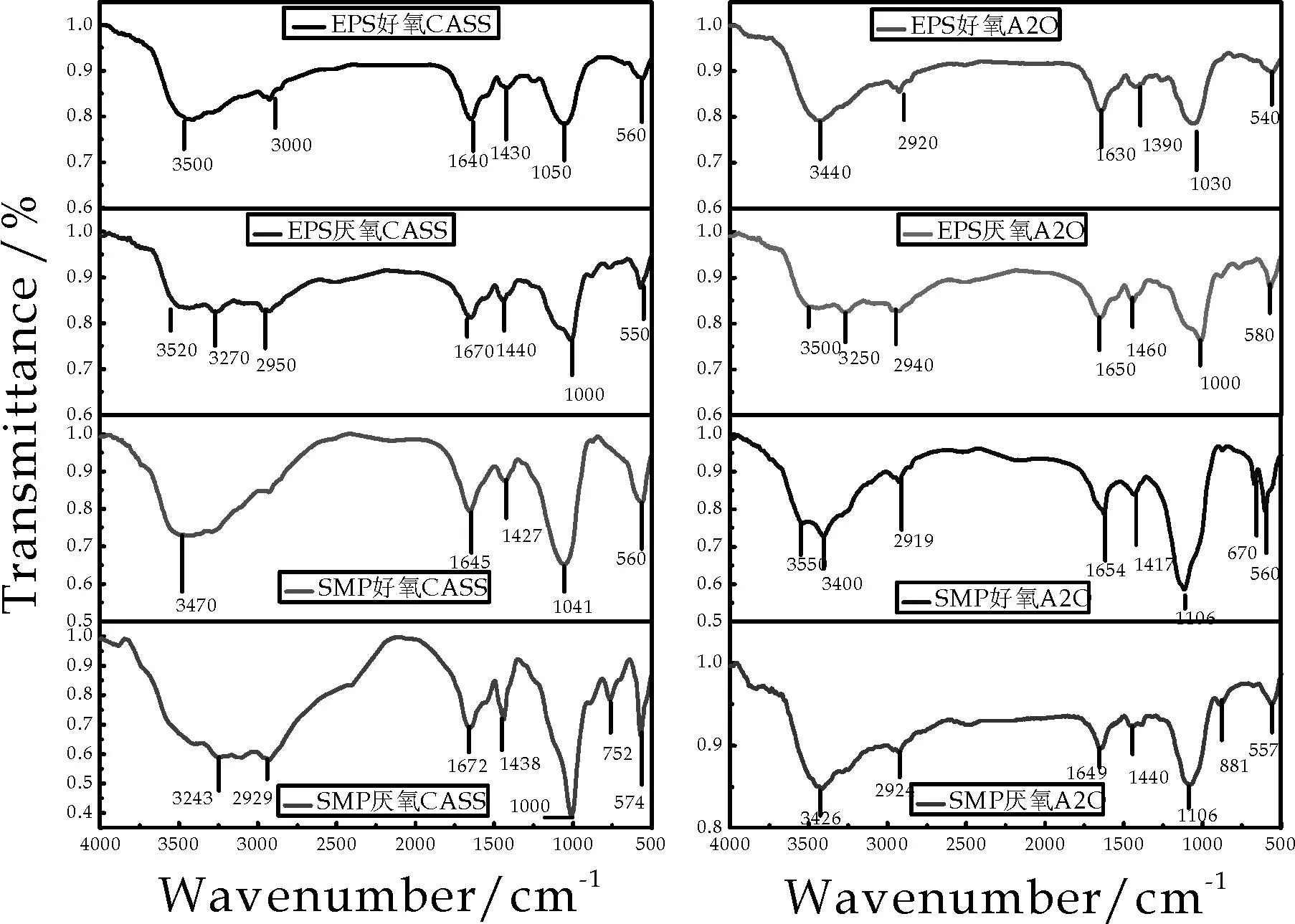
图5 不同处理SMP和EPS的傅里叶红外分析图
2.3SMP和EPS对MFC产电性能和染料脱色的影响
MFC与常规电池产能的原理基本相同,只是在电子产生及传递路径上稍有不同.目前,公认的微生物染料电池的电子转移机制有三种[21]:纳米导线、细胞膜蛋白介导和电子载体.前两者为直接传递;最后一种为间接传递,比较普遍.不同微生物能够分泌产生类型不同的电子载体,可能存在于SMP和EPS中.
由图6可知,添加SMP和EPS均能提高MFC的输出电压,其中厌氧培养提取的SMP和EPS对电压的提升更为明显,最高可达130 mV(EPS厌氧A2O).这是因为厌氧培养下积累的微生物代谢产物更多,可能包含更多的可溶性电子载体来进行电子的传递,这同章节2.1所述的结果相符;电压提升的持续时间普遍很短,因为在偶氮染料溶液MFC中分别只加入了4mL的EPS和SMP样液,从而起作用的电子载体摩尔浓度低,作用时间有限.
观察结果证实源自活性污泥的SMP和EPS中存在微生物分泌的外源电子载体,且能实现不同微生物种间共享,从而提高了MFC的电子转移速率和电能输出.但SMP和EPS中的氧化还原穿梭体为何种物质,还需要进一步地研究论证.
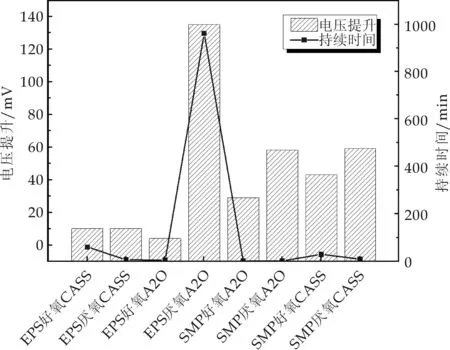
图6 不同处理SMP和EPS对MFC产电性能的影响
图7为SMP和EPS对MFC处理金橙I溶液时脱色率的影响结果.试验表明,SMP和EPS均可加快偶氮染料的脱色速度.EPS(厌氧A2O)的脱色率最高为93%,EPS(好氧CASS)的脱色率最低为69%.这说明SMP和EPS所带入的外源电子载体加快了电子转移速率,从而加快了微生物把从电子供体得到的电子用于攻击偶氮染料分子偶氮键的速率,最终表现为有限时间内脱色率的改善.
另一方面,如图7中折线所示,不同SMP和EPS添加造成了微生物培养物进入对数生长期的时间差异.所需时间最短的处理,即EPS(厌氧A2O),在有限时间内脱色效果最好.这说明SMP和EPS通过刺激微生物生长加快了脱色速率.
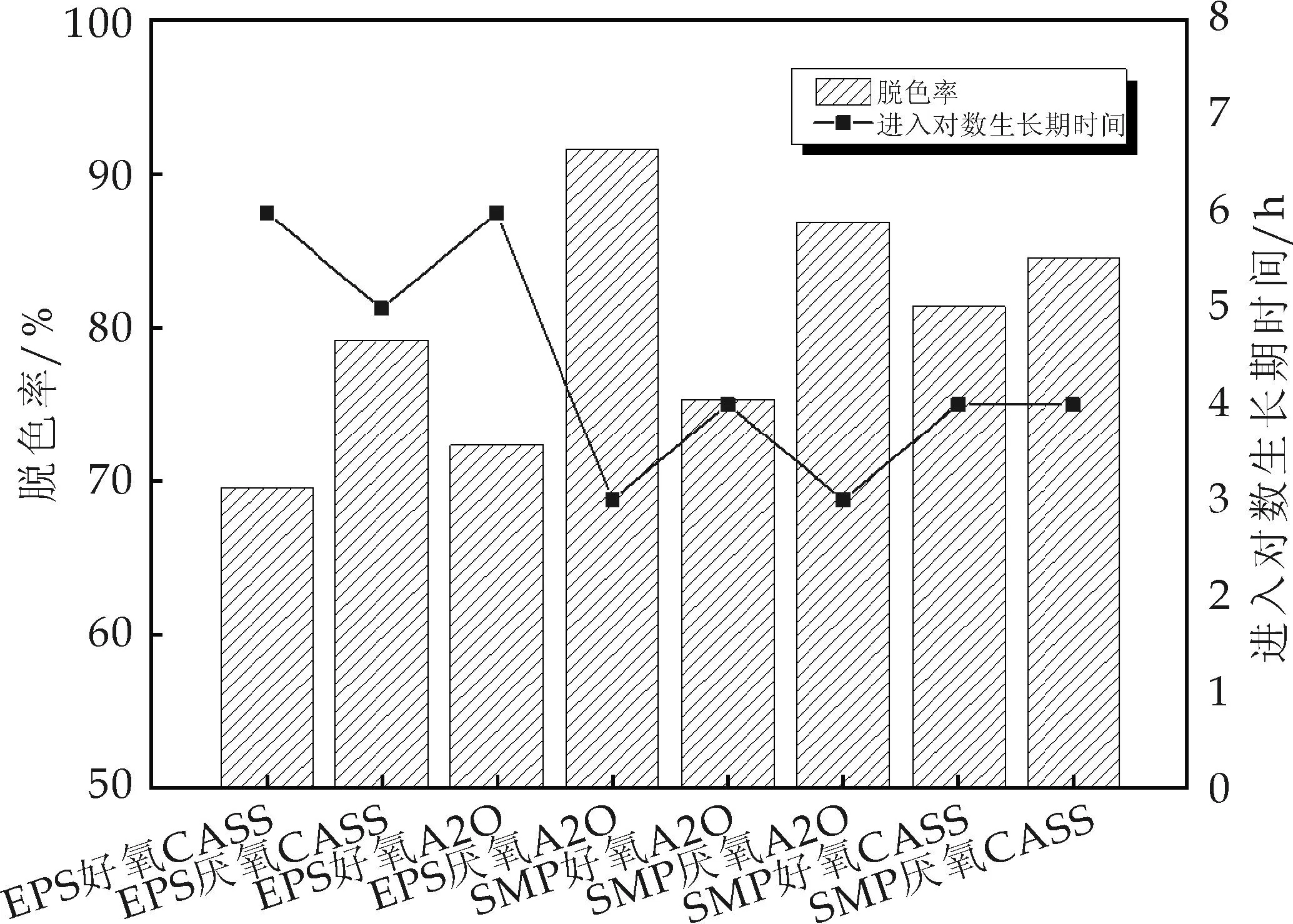
图7 不同处理SMP和EPS对MFC中偶氮染料脱色率的影响
3结论
本文通过对不同工艺来源的活性污泥进行好氧和厌氧饥饿培养,分别提取SMP和EPS并进行表征,研究了其对微生物燃料电池产电性能和对偶氮染料脱色的影响,主要结论如下:
(1)不同工艺和培养条件下SMP和EPS的物质组成基本一致,为蛋白质和多糖类,但存在大分子物质浓度和自由离子浓度的差异.
(2)SMP和EPS均可通过引入外源电子载体的方式来使微生物燃料电池中电子转移速率加快,从而电压提升.
(3)SMP和EPS均可以促进微生物的生长,使脱色菌更快地进入对数生长期和静止期,从而产生足量的偶氮还原酶,提高了有限时间内偶氮染料的脱色效率.
参考文献
[1] 陈宏字.生物反应器中SMP的特性及其对膜污染的影响[D].天津:天津大学,2007.
[2] 孟凡松,冯雷雨.污水厌氧处理系统中可溶性微生物产物的研究进展[J].工业水处理,2012,32(6):6-10.
[3] 孔晓英,李连华,孙永明.微生物燃料电池产能原理及输出功率的影响因素[J].现代化工,2007,27(2):282-286.
[4] Barker D.J.,Stuckey D.C..A review of soluble microbial products(SMP) in wastewater treatment systems[J].Water Res.,1999,33(14):3 063-3 082.
[5] Yao M,Ladewig B,Zhang K.Identification of the change of solublemicrobial products on membrane fouling in membrane bioreactor(MBR)[J].Desalination,2011,278(1):126-131.
[6] Berk R.S.,Canfield J.H..Bioelectrochemical energy conversion[J].Appl. Microbiol,1964,12(1):10-12.
[7] Rao J.R.,Richter G.J.,Von Sturm F.,et al.The performance of glucose electrodes and the haracteristics of different biofuel cell constructions[J].Bioelectrochem. Bioenerg,1976,3(1):139-150.
[8] Loqan B.E.,Hamelers B.,Rozendal R.,et al.Microbial fuel cells:Methodology and technology[J].Environ.Sci.Technol,2006,40(17):5 181-5 192.
[9] Mei X.J.,Wang Z.W.,Zheng X..Soluble microbial products in membrane bioreactors in the presence of ZnO nanoparticles[J].J.Membr.Sci.,2014,451(1):169-176.
[10] Lefebvre O.,Tan Z.,Shen Y.J..Optimization of a microbial fuel cell for wastewater treatment using recycled scrap metals as a cost-effective cathode material[J].Bioresour Technol,2013,127:158-64.
[11] Tommasi T.,Chiolerio A.,Crepaldi M..A microbial fuel cell powering an all-digital piezoresistive wireless sensor system[J].Microl.Technol.,2013,20(5):1 023-1 033.
[12] Jiang T.,Myngheer S.,Pauw D.J.W.,et al.Modelling the production and degradation of soluble microbial products(SMP)in membrane bioreactors(MBR)[J].Water Res.,2008,42(20):4 955-4 964.
[13] Largus T.A.,Khursheed K.,Muthanna H.A.,et al.Production of bioenergy and biochemicals from industrial and agricul tural waste[J].Trends Biotechnol.,2004,22(9):477-485.
[14] Ibeid S.,Elektorowicz M.,Oleszkiewicz J.A..Impact of electro-coagulation on the fate of soluble microbial products (SMP) in submerged membrane electro-bioreactor (SMEBR)[J].Annual Conference-Canadian Society for Civil Engineering (CSCE),2010,1:634-640.
[15] Laspidou C.S.,Rittmann B.E..Non-steady state modeling of extracellular polymeric substances, soluble microbial products and active and inert biomass[J].Water Res.,2002,36(8):1 983-1 992.
[16] Chen L.,Tian Y.,Cao C.Q.,et al.Interaction energy evaluation of soluble microbial products (SMP) on different membrane surfaces: role of the reconstructed membrane topology[J].Water Res,2012,46(8):2 693-2 704.
[17] Chang J.S.,Chen B.Y.,Lin Y.C..Stimulation of bacterial decolorization of an azo dye by extracellular metabolites from Escherichia coli strain NO3[J].Bioresour.Technol.,2004,91(3):243-248.
[18] Oh S.,Logan B.E..Proton exchange membrane and electrode surface areas as factors that affect power generation in microbial fuel cells[J].Appl. Microbiol.Biotechnol.,2006,70(2):162-169.
[19] Liang D,Wei J.,Song Y.H.,et al.The characteristics of extracellular polymeric substances and soluble microbial products in moving bed biofilm reactor-membrane bioreactor[J].Bioresour.Technol,2013,148(9):436-442.
[20] A.Ramesh,Duu Jong,Lee S.G.Hong. Soluble microbial products(SMP) and souble extracellular polymeric substances(EPS) from wastewater sludge[J].Appl.Microbiol and Biotechnol,2006,73(1):219-225.
[21] Bruce E.Logan.微生物燃料电池[M].冯玉杰,王鑫.北京:化学工业出版社,2009:18-30.
The effect of soluble microbial product on the decoloration and
concomitant electricity recovery of azodye-containing wastewater
ZHU Chao1, XIE Jing-kun1, WANG Yuan1, YI Wei-jie2
(1.College of Resources and Environment, Shaanxi University of Science & Technology, Xi′an 710021, China; 2.College of Agriculture, Guizhou University, Guiyang 550025, China)
Abstract:Soluble microbial product (SMP),being an important metabolite of the microbes in activated sludge system of wastewater treatment,plays an essential role in the formation of sludge flocs and the stable operation of treatment system.The characteristics of SMP and extracellular polymeric substances (EPS) from the sludge of Cyclic Activated Sludge System (CASS) and Anaeroxic-Anoxic-Oxic (A2O) treatment processes,cultured anaerobically and aerobically,were investigated after long-term (60 days) cultivation and used for the enhancement of the electricity generation and decoloring rate of the microbial fuel cell (MFC) to treat azodye-containing wastewater.The results showed that the SMP and EPS from different processes and cultivating methods were of high similarity in composition while the EPS had higher content of macromolecular substances than that in SMP according to the data of PACL sedimentation test.Both SMP and EPS were confirmed to be effective in enhancing the voltage to its peak value of 130 mV and the decoloring rate to 93% of the MFC for azodye-containing wastewater.The present study suggests that EPS and SMP are of valuable as auxiliary in the electricity reclamation from azodye-containing wastewater treatment.
Key words:soluble microbial product (SMP); extracellular polymeric substances (EPS); azodye; microbial fuel
中图分类号:X172
文献标志码:A
文章编号:1000-5811(2015)01-0036-06
作者简介:朱超 (1981-), 男, 陕西西安人,讲师, 博士,研究方向:污染环境微生物和微生物生态毒理学
基金项目:陕西省教育厅专项科研计划项目(2013JK072); 陕西科技大学博士科研启动基金项目(BJ12-29)
收稿日期:*2014-11-23

