双咪唑硝基衍生物配合物的合成及其生物活性研究
·化学与化学工程·
双咪唑硝基衍生物配合物的合成及其生物活性研究
杨莉宁1,黑嘉慧2,李立1,成昭1,余丽丽1
(1.西安医学院 药学院,陕西 西安710021;2.陕西航天职工大学,陕西 西安710100)
摘要:以2-甲基-4-硝基咪唑为原料按照文献方法合成了1,2-二[1-(2-甲基-4-硝基咪唑)]乙烷配体,进而制备了其铜、银配合物,通过紫外吸收光谱、荧光光谱及黏度法研究所合成的有机配体及其配合物与DNA相互作用模式,并以二倍稀释法研究抗厌氧菌的活性。结果表明,目标化合物与DNA相互作用方式可能为部分插入,并伴随有静电式结合。Cu,Ag配合物对两种厌氧菌菌株的抗菌性相对配体明显增强。
关键词:双咪唑硝基衍生物;金属配合物;与DNA相互作用;抗厌氧菌
收稿日期:2014-07-22
基金项目:国家自然科学基金资助项目(81302706);陕西省教育厅自然科学基金资助项目(14JK1631);西安医学院博士科研启动基金资助项目(2012DOC3)
作者简介:杨莉宁,女,陕西渭南人,副教授,从事生物无机化学及无机药物化学方面的研究。
中图分类号:O614
Synthesis and biological activity of complexes with flexible
bisimidazole nitro-derivative ligand
YANG Li-ning1, HEI Jia-hui2, LI Li1, CHENG Zhao1, YU Li-li1
(1. Department of Pharmacy, Medical University of Xi′an, Xi′an 710021, China;
2.Shaanxi Aerospace Staffs & Vocation University, Xi′an 710100, China)
Abstract:A flexible nitroimidazole derivative 1,2-di-[1-(2-methyl-4-nitroimidazolyl)] ethane was prepared according to the literature method, and its transition metal complexes were synthesized. The binding of the compounds with calf thymus DNA has been investigated by UV, fluorescence spectra and viscosity measurements. With the two-fold agar dilution method, the antiamoebic activities of nitroimidazole derivative and its copper, silver complexes have been determined, respectively. All of the results indicate that the ligand and complexes bind to DNA base pairs by partial intercalation and electrostatic attraction mode. Complexes have better effect of antiamoebic activity than ligand to two kinds of anaerobic bacteria strains.
Key words: flexible bisimidazole nitro-derivative; metal complex; DNA-binding; antiamoebic activity
硝基咪唑类药物是常见的抗厌氧菌类药物,尤其甲硝唑药物在临床上的应用非常广泛。但是,随着时间的推移,细菌的耐药性迅速增加,药物的毒副作用也突显出来,因而对硝基咪唑类药物的构效关系的研究日益深入。对金属配合物药物的抗菌性研究,为近年来生物无机化学的热门研究课题之一。目前这一方面的研究主要集中于Schiff碱过渡金属配合物[1],对硝基咪唑类药物配合物的抗厌氧菌活性的研究相对较少。本研究采用经典的二倍稀释法药物敏感实验原理,初步分析了新合成的硝基双咪唑衍生物及其铜、银配合物对两种厌氧菌变异链球菌(Streptococcus mutans)和伴放线放线杆菌(aggregatibacter actinomycetem)的体外抗菌活性,为进一步探讨硝基咪唑类药物的抗厌氧菌机理提供了丰富的实验素材。
1实验部分
1.1试剂与仪器
除小牛胸腺DNA(ct-DNA)为生化试剂,2-甲基-4-硝基咪唑为化学纯外,其他试剂均为分析纯。
德国Vario EL-IIIG型元素分析仪,EQUINOX55 型红外光谱仪,STA449C型热分析仪;日本1800紫外可见分光光度计,F-4500荧光分光光度计;上海Ubbeoldhe黏度计,DDS-307型电导仪。
1.2 配体及配合物的合成
配体1,2-二[1-(2-甲基-4-硝基咪唑)]乙烷(以下用L表示)的合成参照文献[2-3]。
其合成路线为:
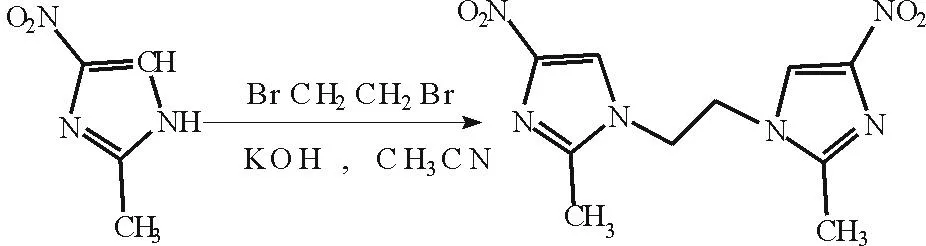
配合物[Cu(L)Cl2]·H2O(1)的合成:准确称取配体 0.140g(0.5mmol)于25mL烧杯中,加入10mL甲醇和5mL乙腈略微加热溶解得橙黄色溶液。再称取CuCl2·2H2O 0.091g (0.5mmol)于50mL烧杯中,加入10mL甲醇溶解,待完全溶解后,将配体溶液逐滴滴入CuCl2溶液中得到黄绿色溶液,持续搅拌3天,有蓝绿色粉末状沉淀析出,过滤,洗涤,固体粉末烘干后呈蓝绿色。
配合物[Ag(L)NO3](2)的合成方法与配合物(1)相似,但要避光搅拌3天,得粉色沉淀物。
1.3配体及配合物与DNA相互作用实验
采用已报道文献[4-5]的经典方法配制实验所需试剂、缓冲溶液以及进行与DNA相互作用实验操作。DNA浓度对化合物的紫外吸收光谱和荧光吸收强度的影响见图2,3,化合物浓度对DNA黏度的影响见图4。
1.4 配体及其配合物体外抗厌氧菌活性实验[6]
1.4.1实验材料实验所用标准菌株:变形链球菌(StreptococcusmutansUA159), 伴放线放线杆菌(ActinobacillusactinomycetemATCC 29523),均来自第四军医大学口腔医院牙体实验室。
1.4.2实验方法
1) 培养基的准备
称取37g培养基,加入950mL的三蒸水,加热溶解,再补水至1L,在121℃下高压灭菌15min,冷却至4℃保存。给所制备的1L培养液中加入15g琼脂粉,充分溶解后,高温高压消毒15 min,再冷却至50℃,取约20mL均匀地铺于培养皿中,常温下冷却,并于4℃保存。
2) 抗菌活性检测
取冻存的变形链球菌(S.mutans)和伴放线放线杆菌(A. a)分别划线接种于培养基表面,进行厌氧培养;挑取培养36 h的S.mutans和培养48 h的A. a菌落各自接种于培养液,其中前者培养24 h,后者培养48 h,备用。用少量DMSO配制各种配体及其Cu,Ag配合物待测抗菌剂,用无菌水对各种抗菌剂从1 280 mg/L到0.625 mg/L进行2倍梯度稀释;96孔板的每孔中分别加入上述各种浓度的待测抗菌剂溶液、细菌培养液和BHI培养液,用酶标仪进行OD值测定。取对照组(每孔以 PBS缓冲溶液代替待测抗菌剂溶液,其余同前) 100μL,进行10倍梯度稀释,取100μL稀释的菌液铺于BHI培养基表面,培养48 h,得到每孔中原细菌生存数(同时对3个复孔进行计数,取平均值)。再于厌氧箱中培养24 h。培养后,继续测定OD值,得到最小抑菌浓度(MIC)值。所有的试样均平行测试3次,取平均值。
2结果与讨论
2.1配合物的性质表征
1) 配合物的元素分析和摩尔电导率

表1 配合物的元素分析及摩尔电导率
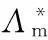
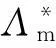
2) 配体及配合物的红外光谱分析
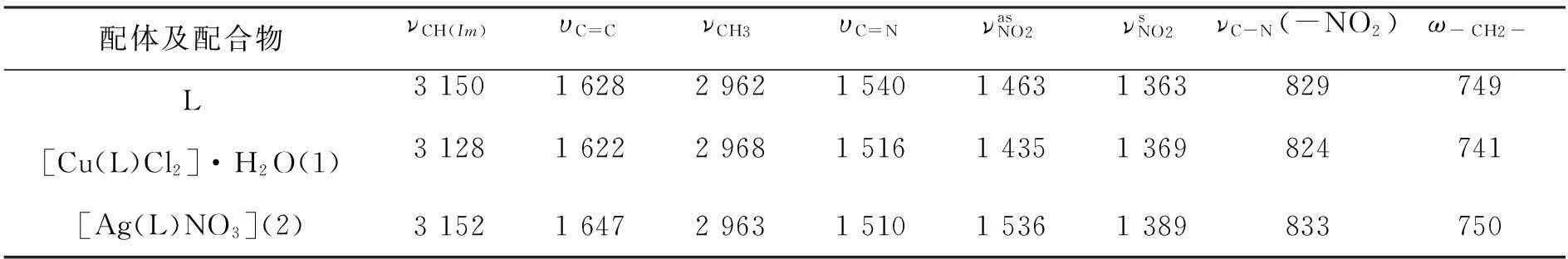
表2 配体及配合物的红外光谱数据(cm -1)
由表2可见,配体形成各配合物后的特征吸收峰发生偏移的主要表现在咪唑环上的振动吸收,其中的υC=N伸缩振动都向低波数发生了偏移,说明金属与咪唑环上的3位N发生了配位[8]。配合物(2)存在含氧酸根NO3-,在谱图上表现为4条谱带,尤其是NO3-的N-O伸缩振动峰在整个谱图的吸收峰是最强的,其指纹区谱带未增加,说明NO3-未参与配位。
采用元素分析、紫外、红外、电导率等方法,结合双咪唑配合物文献[9-10],初步推测各配合物的可能结构为图1所示。

图1 配合物(1),(2)的可能结构 Fig.1 The possible structure of the complexes
2.2配合物与ct-DNA相互作用研究
1) 配体及其配合物与DNA相互作用的紫外光谱分析
图2为配体及其配合物(1),(2)随着DNA浓度增加与DNA相互作用的紫外吸收光谱图。

曲线a→f DNA浓度(×10 -5mol/L)分别为: 0; 1.59; 3.16;4.71; 6.23; 7.74, 以下荧光图同 图2 DNA浓度对配体L及其配合物紫外光谱的影响 Fig.2 UV absorption spectra of L and its complexeswith increasing concentration of DNA
由图2可以看到,双咪唑硝基衍生物配体L及其铜配合物随着DNA浓度的增加,其紫外特征吸收峰表现为减色效应,而它的银配合物则表现为增色效应,最大吸收峰未发生明显的红移或蓝移,与DNA相互作用模式应该不是典型的插入作用[11]。根据减色率的大小,DNA对铜配合物的紫外光谱的影响比配体的紫外光谱影响要大。如果化合物小分子紫外-可见吸收光谱中的吸收峰强度表现为增色效应或减色不显著、无红移现象,则认为化合物小分子与DNA发生了非插入的静电作用或沟槽作用[12]。
2) 配体及其配合物与DNA相互作用的荧光光谱分析。
图3为配体及其配合物随着DNA浓度增加与DNA相互作用的荧光吸收光谱图。

图3 DNA浓度对配体L及其配合物荧光光谱的影响 Fig.3 Fluorescence spectra of L and complexes at different concentrations of DNA
如图3所示,随着DNA浓度的不断增加,配体及其配合物的荧光光谱强度都呈增加的趋势,但最大荧光吸收峰值变化不大,因此配体及其配合物与DNA的作用模式可能不是典型的插入式。根据增色率大小,配体及其铜配合物与DNA的作用力要强,这与根据紫外吸收强度变化所得到的结论基本一致。
3) 配体及其配合物与 ct-DNA 相互作用的黏度分析
黏度法是研究化合物与DNA相互作用模式的另一种有效的检测方法[13]。当配合物插入DNA之间,黏度增加;与DNA以部分插入方式作用时,DNA黏度变小;DNA溶液黏度变化不大,则与DNA以非插入方式作用[14-18]。如图4所示,配体L及其铜配合物(1)使DNA溶液黏度减小,说明配体L与DNA相互作用方式可能为部分插入;而其银配合物(2)使DNA黏度变化不大,则可能是以非插入方式与DNA相互作用,这些结果与光谱分析的结果是一致的。
2.3配体及其配合物抗厌氧菌活性研究
对所合成的硝基双咪唑衍生物配体及其Cu,Ag 配合物应用变异链球菌(S. mutans)和伴放线放线杆菌(A. a)进行抗菌活性试验,测试结果如表3所示。结果表明,参与抑菌实验的所有药物对伴放线放线杆菌(A. a)的抑菌效果要强于变异链球菌(S. mutans)。配体L对两种菌的抑菌效果都不如其配合物明显,对变异链球菌(S. mutans)抑菌性(2)>(1),而对伴放线放线杆菌(A. a)的抑菌性(1)>(2)。
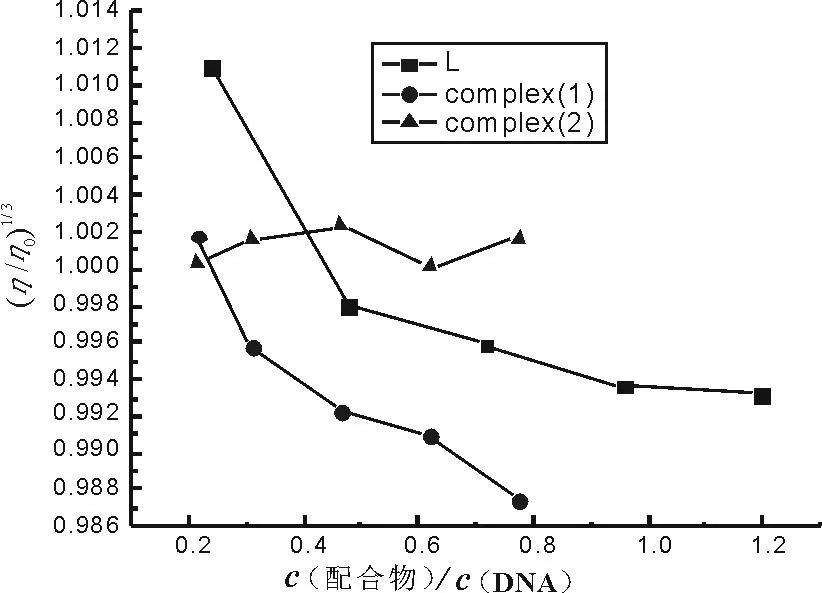
图4 配体L及其配合物浓度对DNA黏度的影响 Fig.4 Effects of increasing amount of L and complexes on the viscosity of DNA
表3化合物对S. mutans UA 159和A. a ATCC 29523的最小抑菌浓度MIC值
Tab.3MIC of test material on S. mutans UA 159 and A. a ATCC 29523

测试样MIC(S.mutans)/μg·mL-1MIC(A.a)/μg·mL-1L-320-160Ag配合物(2)40-2040-20Cu配合物(1)320-16020-10Ag+20-101.25-0.625Cu2+-20-10
硝基咪唑类药物发挥抗厌氧菌作用,是在细胞中的硝基还原酶的作用下,药物的硝基还原成羟胺衍生物后,再与DNA作用引起链损伤、断裂、解旋,导致细菌死亡[19-20]。依据硝基咪唑类药物的抗菌机制,可以认为硝基咪唑类药物抗厌氧菌的最终主要细胞内靶点为DNA。分析配体及其配合物与DNA之间相互作用的实验结果,其抗菌性与DNA相互作用结果并不完全一致,这是因为金属配合物的抑菌机理较复杂,包括干扰细胞的呼吸过程,破坏蛋白质的合成,进而抑制微生物的生长;正常的细胞生长过程受到配合物C=N基团与细胞活性中心间所形成氢键的影响等等。因此,配合物的抗厌氧菌活性并不完全受该药和DNA作用结果的影响。金属配合物的抗厌氧菌机理,以及抗菌活性和配合物与DNA相互作用之间的关系,还需要进一步分析研究。
参考文献:
[1]NITISS J L. Investigating the biological functions of DNA topoisomerases in eukaryotic cells[J]. Biochim Biophys Acta, 1998, 1400: 63-81.
[2]李润涛,曹胜利,孙万赋,等.1-烷基2-甲基-4-硝基咪唑类化合物的合成及生物活性[J]. 高等学校化学学报,1997,18(8):1325-1328.
[3]蔡娟,赵涛涛,安港,等.二(1-咪唑基)甲烷的合成研究[J]. 化学与生物工程, 2009,26(7):22-24.
[4]WU S S, YUAN W B, WANG H Y, et al. Synthesis, crystal structure and interaction with DNA and HAS of (N,N′-dibenzylethane-1,2-diamine)transition metal complexes[J]. J Inorg Biochem, 2008, 102(11):2026-2034.
[5]LIU M, YUAN W B, ZHANG Q, et al. Synthesis, characterization and DNA interaction studies of complexes of lanthanide nitrates with tris{2-[(3,4-dihydroxybenzylidene)imino]ethyl}amine[J]. Spectrochimica Acta Part a-Molecular and Biomolecular Spectroscopy, 2008, 70(5): 1114-1119.
[6]TONG Z, DONG L, ZHOU L, et al. Nisin inhibits dental caries-associated microorganism in vitro[J]. Peptides, 2010, 31:2003-2008.
[7]李珺.综合化学实验[M]. 西安: 西北大学出版社, 2003: 208-209.
[8]MOHANTY R R, ROUT K C, JENA S, et al. Dioxouranium(VI) and thorium(IV) complexes of a bidentate chelating biheterocycle, 1,1′-dimethyl-2,2′-biimidazole [J]. Polyhedron, 1994, 13(21): 2945-2952.
[9]DING J G, GE H Y, ZHANG Y M, et al. Syntheses, crystal structures and magnetic properties of three copper(II) coordination polymers with the flexible ligand 1,2-bis(1,2,4-triazol-1-yl)ethane or 1,2-bis(imidazol-1-yl)ethane[J]. Journal of Molecular Structure, 2006, 782: 143-149.
[10]LI F F, MA J F, SONG S Y. Syntheses, structures, and characterizations of four new silver(I)sulfonate coordination polymers with neutral ligands[J]. Crystal Growth& Design, 2006, 6(1): 209-215.
[11]卢艳梅,区志镔,刘海峰,等.三元TBZ/HPB-L-蛋氨酸配合物的合成、表征、抑菌活性及与DNA的作用[J].无机化学学报,2011, 27(4): 704-710.
[12]BAARTON J K, GOLDBERG J M, KUMAR C V, et al. Binding modes and base specificity of tris(phenanthroline)ruthenium(II) enantiomers with nucleic acids: tuning the stereoselectivity [J].J Am Chem Soc,1986,108(8):2081-2088.
[13]SATYANARAYANA S, DABROWIAK J C,CHAIRES J B. Neither-nor Λ-tris(Phenan-throline)ruthenium(Ⅱ)binds to DNA by classical intercalation [J].Biochem,1992,31(39):9319-9324.
[14]SIGMAN D S, MAZUMDER A, PERRIN D M. Chemical nucleases[J]. Chem Rev, 1993, 93:2295-2316.
[15]KUMAR R S, ARUNAEHALAM S, PERIASAMY V S, et al. DNA binding and biological studies of some novel water-soluble polymer-copper(Ⅱ)-phenanthroline complexes[J].Eur J Med Chem, 2008, 43: 2082-2091.
[16]洪显兰, 任健敏.[Ru(dipn)(tpy)](ClO4)2的合成、表征、DNA结合性质及与系列化合物之比较[J]. 无机化学学报, 2011,27(4):785-790.
[17]郭航鸣, 赵国良, 吴小勇,等. 3,4-二甲氧基苯乙酸邻菲咯啉锌配合物的合成及与DNA作用[J].无机化学学报, 2011, 27(5): 855-859.
[18]刘 峰, 张维平, 胡亭,等.二元配合物RE(HL)2ClO4与DNA作用的光谱研究[J].西北大学学报(自然科学版), 2008, 38(2): 237-242.
[19]MÜLLER M. Mode of action of metronidazole on anaerobic bacteria and protozoa[J]. Surgery,1983,93(1/2): 165-171.
[20]柏干荣, 胡友梅. 替硝唑的药理与临床应用进展[J]. 中国药房,1998, 9(1): 42-43.
(编辑任智卉)

