慢性炎症状态下成纤维细胞生长因子23与终末期肾病血管钙化的相关性
慢性炎症状态下成纤维细胞生长因子23与终末期肾病血管钙化的相关性
张艺马玲1肖业伟2余广2冯志强2盘强文2
(泸州医学院机能实验室,四川泸州646000)
摘要〔〕目的探讨炎症状态下成纤维细胞生长因子(FGF)23与终末期肾病(ESRD)血管钙化的关系。方法成年雄性SD大鼠随机分为对照组(Ctr)组、慢性肾功能不全(CRF)组和炎症伴慢性肾功能不全(CRF+I)组。Ctr组用生理盐水灌胃持续6 w,CRF组用腺嘌呤灌胃持续6 w构建大鼠CRF的动物模型,CRF+I组每天用腺嘌呤灌胃持续6 w并隔日皮下注射10%酪蛋白(Casein,1.2 g/kg)构建大鼠炎症伴CRF动物模型。检测各组血清肌酐、尿素氮、磷以及血管组织的钙含量、α-平滑肌肌动蛋白(α-SMA)蛋白表达量、FGF23 mRNA表达水平等指标。结果α-SMA 蛋白表达量,Ctr组明显高于CRF组和CRF+I组(P<0.05),CRF组明显高于CRF+I组(P<0.05);组织钙含量,CRF组和CRF+I组明显高于Ctr组(P<0.05),而CRF+I组明显高于CRF组(P<0.05);FGF23 mRNA表达,CRF+I组的相对表达量明显高于CRF和Ctr组(P<0.05),Ctr组和CRF组FGF23 mRNA的相对表达量无差异(P>0.05)。结论炎症除了可以直接引起ESRD血管钙化外还可以通过升高FGF23加剧ESRD血管钙化。
关键词〔〕终末期肾病;血管钙化;炎症;成纤维细胞生长因子23
中图分类号〔〕R692.5〔文献标识码〕A〔
基金项目:四川省教育厅项目(09ZC118)
通讯作者:盘强文(1971-),男,教授,硕士生导师,主要从事肾功能保护研究。
1漯河医学高等专科学校生理学教研室
2泸州医学院肾功能保护研究室
第一作者:张艺(1981-),女,实验师,硕士,主要从事肾功能保护研究。
终末期肾病(ESRD)患者心血管疾病发病率及病死率的增加与患者的血管钙化密切相关,而有研究表明高磷血症是慢性肾功能不全(CRF)患者血管钙化的重要诱因,与心血管死亡事件亦密切相关〔1〕。成纤维细胞生长因子(FGF)23目前普遍认为能通过作用于肾脏和抑制1α-羟化酶的表达和活性以达到降低血磷的作用。有学者〔2〕观察到FGF23也可能参与了CRF患者的血管钙化。同时终末期肾病(ESRD)患者体内存在微炎症状态并可能参与血管钙化的形成〔3〕。而ESRD患者的慢性炎症状态与FGF23是否存在关系则未见报道。本实验检测慢性炎症条件下CRF大鼠的血清磷、肌酐、尿素氮以及血管组织钙含量、血管平滑肌α-平滑肌肌动蛋白(α-SMA)蛋白表达量和FGF23 mRNA表达水平,探讨慢性炎症状态下FGF23与ESRD血管钙化的相关性。
1材料与方法
1.1材料与试剂腺嘌呤、酪蛋白(Casein)、硫代硫酸钠、硝酸银、核固红购自武汉博士德生物工程公司,血磷、血尿素氮和血肌酐试剂盒购自南京建成生物工程研究所,RNA提取试剂盒购自天根生物技术有限公司,RT-PCR试剂盒购自成都博瑞克生物技术有限公司,SP免疫组化试剂盒、DAB显色试剂盒均购自北京中杉金桥生物技术有限公司,单克隆小鼠抗α-SMA抗体购自武汉博士德生物工程公司。
1.2动物分组及模型制备8 w龄成年雄性SD大鼠30只,体重(200±20)g,由泸州医学院实验动物中心提供。随机分为对照组(Ctr,n=6)、CRF组(n=12)、CRF+炎症组(CRF+I,n=12)。Ctr组用生理盐水(10 ml/kg)灌胃,另两组用腺嘌呤(300 mg/kg)灌胃构建大鼠CRF动物模型,其中CRF+I组隔日以10% Casein(1.2 g/kg)皮下注射。6 w后,戊巴比妥钠腹腔注射麻醉大鼠后取材备检。
1.3取材及指标检测首先经腹主动脉取血用于测定血清肌酐、尿素氮和磷等指标,按试剂盒说明操作。然后分离并摘取腹主动脉,部分用 4%中性甲醛固定后做组织学观察,余下主动脉作钙定量及PCR检测基因表达等。血管组织按SP免疫组化试剂盒处理后用DAB显色液显色在光镜下随机观察5个视野,用Image Pro Plus 6.0软件进行半定量分析被检血管组织中α-SMA的阳性表达量;用Von Kossa染色观察血管组织钙沉积;以OCPC法检测血管组织钙浓度;用RT-PCR法扩增FGF23以测定血管组织中FGF23 mRNA的转录水平,反应条件为:94℃2 min,94℃30 s→ Tm℃30 s→ 72℃1 min,热循环30次,72℃延伸5 min。取PCR产物进行琼脂糖凝胶电泳后进行图像分析。
1.4统计学方法采用SPSS16.0统计软件进行单因素方差分析及LSD法(最小显著差异法)。
2结果
2.1三组肌酐和尿素氮测定及动物模型构建结果各组肌酐比较,CRF组(270.93±29)μmol/L和CRF+I组(270.63±24.54)μmol/L比Ctr组(66.85±1.5)μmol/L明显升高(P<0.05);各组尿素氮比较,CRF组(27.9±4.1)mmol/L和CRF+I组(33.65±8.26)mmol/L比Ctr组(6.62±0.28)mmol/L明显升高(P<0.05),CRF模型构建成功,CRF+I组使用连续6 w隔日皮下注射10% Casein(1.2 g/kg)的方法构建慢性炎症模型。
2.2炎症对CRF大鼠血清磷的影响CRF组(5.23±0.27)mmol/L及CRF+I组(5.37±0.42)mmol/L磷浓度均明显高于Ctr组(2.1±0.2)mmol/L(P<0.05),CRF组和CRF+I组相比,差异无统计学意义(P>0.05)。
2.3各组大鼠血管平滑肌细胞中α-SMA的阳性表达量α-SMA蛋白阳性表达呈淡黄色或棕色,定位于细胞质中。Ctr组α-SMA 蛋白表达量(0.16±0.01)明显高于CRF组(0.13±0.01)和CRF+I组(0.08±0.04)(P<0.05),CRF组α-SMA 蛋白表达量明显高于CRF+I组(P<0.05)。见图1。

图1 各组大鼠血管平滑肌细胞α-SMA阳性表达(DAB,×400)
2.4各组大鼠主动脉组织Von Kossa染色结果Ctr组和CRF组内皮细胞排列完整,弹性纤维无断裂,平滑肌排列整齐,未见黑色钙盐沉积,核固红复染为粉红色;CRF+I组平滑肌排列紊乱,部分弹性纤维断裂,中膜弹力层可见广泛分布的黑色钙盐沉积,间或聚集成团。见图2。
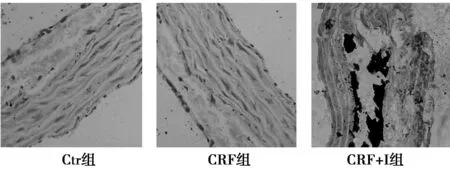
箭头所指为钙盐沉积 图2 大鼠胸主动脉Von Kossa染色结果(×200)
2.5大鼠动脉组织中钙含量变化CRF+I组(258.98±69.50)μmol/g动脉组织中钙含量高于CRF组(107.55±32.50)μmol/g和Ctr组(23.66±11.54)μmol/g(P<0.05),CRF组动脉组织中钙含量高于Ctr组(P<0.05)。
2.6炎症对CRF大鼠血管组织中FGF23 mRNA表达水平的影响CRF+I组(0.86±0.35)FGF23 mRNA的相对表达量均高于Ctr组(0.24±0.29)和CRF组(0.3919±0.33)(P<0.05)。Ctr和CRF组FGF23mRNA的相对表达量无差异(P>0.05)。见图3。
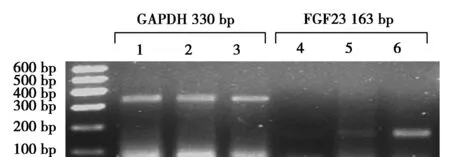
1、4:Ctr组,2、5:CRF组,3、6:CRF+I组 图3 FGF23 mRNA电泳结果
3讨论
本实验结果显示ESRD大鼠动脉组织Von Kossa钙染色和钙含量,CRF+I 组最高,CRF组次之,Ctr组最低,而动脉组织免疫组化结果显示,各组α-SMA蛋白表达量的差异则刚好相反,提示在ESRD时,炎症可作为一项独立的影响因素促进血管平滑肌细胞的转分化和钙化的进程,其可能机制:慢性炎症一方面促使细胞产生炎性因子,进而促进成骨细胞分化和增殖,另一方面刺激肝脏急性时相蛋白的合成同时减少Fetuin-A的合成。Fetuin-A作为血管钙化的主要循环系统抑制因子,它通过刺激吞噬细胞吞噬凋亡物质,抑制羟磷灰石的生成〔4〕。Fetuin-A的减少会造成血管内皮细胞紊乱和氧化应激等。
在慢性炎症和ERSD继发的高磷血症条件下骨形态蛋白(BMP)-2的表达增加。BMP-2与平滑肌细胞膜上的BMP-2受体结合,诱导一系列Smads的核内转移和磷酸化〔5〕,将信号转移到细胞核内,进而上调Cbfα-1等特异性成骨基因的转录活性,使平滑肌细胞表达成骨/成软骨细胞表型。BMP-2表达增加,促使其下游基因Msx2表达上调,增进Wnt3a的表达,使经典的Wnt3a/β连环信号通路加强〔6〕,从而抑制平滑肌细胞向脂肪细胞和软骨细胞分化,使其向成骨细胞分化、增殖并促使矿物质沉积增加而促进钙化的发生。
FGF23是重要的调磷因子,其作用的主要靶器官是肾脏。ESRD患者体内普遍存在高磷血症,血磷水平升高促进成骨细胞表达FGF23增加,FGF23通过血液循环到达肾脏作用于肾脏近曲小管,抑制NaPi-Ⅱ的表达减少磷的重吸收降低血磷;FGF23也可通过抑制1α-羟化酶的表达和活性,使1,25(OH)2D3生成减少,从而抑制肠道对磷的吸收实现机体稳定的血磷环境〔7〕。本实验提示此时FGF23表达增加不是由血清磷增高引起,而可能是由炎症刺激导致。
FGF23水平不仅是矿物质代谢异常引起的早期心血管病变的生物标志,有研究观察到,血液透析患者血浆FGF23水平的增加与主动脉钙化独立相关〔8〕。也有学者对其是否直接作用于心血管系统,导致心血管病变提出质疑〔9〕。最近还有报道在颈动脉不稳定斑块的平滑肌细胞发现FGF23及受体I的过表达〔10〕。本实验结果显示CRF+I 组血管组织钙含量明显高于CRF组,而CRF+I 组血管组织FGF23 mRNA表达量明显高于CRF组。由此推测,炎症刺激下高表达的FGF23与其受体结合后可能加剧动脉中膜平滑肌细胞钙化。
4参考文献
1Cozzolin M,Brancaccio D.Optimising the treament of hyperphosphatemia and vascular calcification in chronic kidney disease 〔J〕.Expert Opin Emerg Drugs,2007;12(3):341-3.
2颜佳毅,张敏芳,倪兆慧,等.成纤维细胞生长因子23与慢性肾脏病中晚期患者冠状动脉钙化的关系〔J〕.中华肾脏病杂志,2012;28(5):355-60.
3冯兵,杨旭,叶自林,等.尿毒症患者微炎症与血管功能损伤的关系〔J〕.中国动脉硬化杂志,2008;16(6):473-5.
4EL-Shehaby AM,Zakaria A,EL-Khatib M,etal.Association of fetuin-A and cardic calcification and inflammation levels in hemodialysis patients〔J〕.Scand J Clin Lab Invest,2010;70(8):575-82.
5西永明,贾连顺,赵鹏,等.Smad蛋白在BMP.2在诱导成骨分化过程中的作用〔J〕.青岛大学医学院学报,2007;43(6):482-4.
6Shao JS,Ala ZA,Lai CF,etal.Vascular Bmp MSX2 Wnt signaling and oxidative stress in arterial calcification〔J〕.Ann N Y Acad Sci,2007;1117(1):40-50.
7Shimada T,Hasegawa H,Ymazaki Y,etal.FGF-23 is a potent regulator of vitamin D metabolism and phosphate homeostasis〔J〕.J Bone Miner Res,2004;19(3):429-35.
8Chen Z,Chen X,Xie J,etal.Fibroblast growth factor 23 is a predictor of aortic artery calcification in maintenance hemodialysis patients 〔J〕.Ren Fail,2013;35(5):660-6.
9Kovesdy CP,Quarles LD.The role of fibroblast growth factor-23 in cardiorenal syndrome 〔J〕.Nephron Clin Pract,2013;123(3-4):194-201.
10Sigala F,Sawari P,Liontos M,etal.Increased expression of bFGF is associatded with caroid atherosclerotic plaques instability engaqing the NF-kappa B pathway〔J〕.J Cell Mol Med,2010;14(9):2273-80.
〔2014-06-19修回〕
(编辑安冉冉/曹梦园)

