紫杉醇联合卡铂单周新辅助化疗加曲妥珠单抗在HER2阳性乳腺癌的探讨
张钢龄,张培礼,朱敬军,任殿全,李 慧,樊佳妮
紫杉醇联合卡铂单周新辅助化疗加曲妥珠单抗在HER2阳性乳腺癌的探讨
张钢龄,张培礼,朱敬军,任殿全,李慧,樊佳妮
目的:观察紫杉醇联合卡铂行新辅助化疗加曲妥珠单抗方案在HER2阳性乳腺癌中的疗效及安全性。方法:42例HER2阳性的乳腺癌患者,均行4个疗程紫杉醇联合卡铂单周化疗方案加曲妥珠单抗的治疗;紫杉醇80 mg/m2,卡铂AUC= 1.5,d1静脉点滴,每周重复;每3周为1疗程,共12周;同时加曲妥珠单抗(赫赛汀)单周治疗;评价其疗效及不良反应,主要观察指标为pCR。结果:41例完成了4疗程的紫杉醇联合卡铂新辅助化疗加曲妥珠单抗治疗,临床总有效率97.6%,临床完全缓解25例(59.5%),肿瘤部分缓解16例(38.1%),病理完全缓解23例(54.8%);不良反应主要为骨髓抑制和脱发,无心脏毒副作用。结论:在HER-2阳性乳腺癌的新辅助化疗中,4疗程的紫杉醇联合卡铂单周化疗方案加曲妥珠单抗的治疗具有较好的疗效及耐受性。
紫杉醇联合卡铂;曲妥珠单抗;乳腺癌;新辅助治疗
乳腺癌的新辅助化疗是在手术加放疗的局部治疗前,以全身化疗为第一步治疗[1]。最初只应用于不可手术的局部晚期乳腺癌的标准治疗[2],近年来新辅助化疗在各期乳腺癌的涉及面越来越广。2013年6月—2015年3月,我们对42例人类表皮生长因子受体2(human epidermal growth factor receptor-2,HER2)阳性的乳腺癌患者应用紫杉醇联合卡铂行新辅助化疗加曲妥珠单抗治疗,取得了较好的疗效。
1 资料与方法
1.1一般资料本组共42例,先行空心针穿刺经病理组织学定性。均为女性,年龄31~68岁,中位年龄45.6岁。ECOG体能状态评分≤1。左侧29例,右侧13例。导管浸润癌39例,小叶浸润癌3例。II期27例,III期15例。免疫组化回报为任何雌激素受体和孕激素受体。化疗前均行腋窝淋巴结穿刺或行前哨淋巴结活检,证实腋窝淋巴结转移34例(表1)。
1.2治疗方法42例均行4个疗程紫杉醇联合卡铂单周化疗方案加曲妥珠单抗的治疗。紫杉醇80 mg/m2,溶于5%250 mL葡萄糖静滴,时间为6 h。卡铂AUC 1.5,溶于5%250 mL葡萄糖,静滴30~60 min。同时行曲妥珠单抗(赫赛汀)单周治疗,首次剂量4 mg/kg,第2周开始2 mg/kg,均d1静脉点滴,每周重复。每3周为1疗程,计划给予4个疗程,共12周。常规化疗前应用地塞米松预防过敏及使用止吐药物。化疗前日化验血常规和生化全项。第1周不用预防性升白,第2周开始根据化验结果决定是否进行预防与治疗性升白。常用药物G-CSF,300μg,第4 d皮下注射。升白的目标是维持白细胞计数/中性粒细胞绝对计数值分别在2.0~10/1.0~8.0×109/L。根据血常规调整升白药物剂量。每个周期结束后行乳腺彩超检查,每2个周期结束后行乳腺核磁(MRI)检查、心电图及心脏彩超检查。在乳腺彩超及MRI辅助诊断下,肿瘤缓解,则继续化疗。若肿瘤进展、稳定或心功能异常,则停止化疗。化疗结束后手术,术后辅助治疗依据NCCN乳腺癌诊疗规范进行并继续行曲妥珠单抗治疗满1年。
1.3评价方法及疗效采用乳腺彩超及MRI共同测量肿瘤大小,评价疗效。按世界卫生组织(WHO)制定的统一标准分为4类:(1)临床完全缓解(CR)为临床检查肿瘤完全消失;(2)临床部分缓解(PR)为肿瘤体积缩小≥50%;(3)病情稳定(SD)为肿瘤体积缩小<50%,或增加<25%;(4)疾病进展(PD)为肿瘤体积增加≥25%或出现新病灶。总有效率(OR)=CR+PR[3]。病理完全缓解(pCR)为手术标本中原发肿瘤区已无浸润癌细胞,同时腋淋巴结未见癌转移。
2 结果
本组42例,41例完成了4疗程的紫杉醇联合卡铂新辅助化疗加曲妥珠单抗治疗。1例2个疗程后,肿瘤SD终止治疗。临床总有效率97.6%。25例达到CR,完全缓解率59.5%。16例肿瘤PR,部分缓解率38.1%。化疗结束3周后手术,行改良根治术33例,保乳根治术9例。34例新辅助化疗前腋窝淋巴结证实有癌转移,新辅助化疗后28例腋窝淋巴结无癌转移。达到CR患者中,2例有癌残留,其中1例为肿瘤病灶残留,1例为腋窝淋巴结癌残留。病理完全缓解率54.8%。从TNM分期、病理性质及淋巴结状况分析pCR,均无统计学意义。见表1。
1.4统计学处理用 SPSS 17.0软件对计数资料进行χ2检验。以P<0.05为差异有统计学意义。根据WHO化疗毒副作用分级标准,所有患者无心脏不良事件,只有轻微恶心、呕吐、腹泻等消化道反应。11例出现3~4度中性粒细胞降低,发生率26.1%。其中1例发生中性粒细胞降低性发热,推迟1周治疗。1例出现严重血小板降低和贫血。2例发生l度以上的外周神经不良反应(表2)。
3 讨论
新辅助化疗的目的是使不能手术切除的患者变为可切除,本应行乳房切除的病例转成为可实行保乳手术[4]。许多随机试验结果均显示,新辅助化疗后的乳房切除的比例较术后辅助化疗减少,保乳比例增加。Bonadonna等[5]报道,在乳腺癌肿块>5 cm的病人中,新辅助化疗后有73%的病例采用了保乳手术治疗。
与辅助化疗相比,采用新辅助化疗根据化疗前后肿瘤的大小及生物学指标的变化,直观地了解具体肿瘤对化疗药物、方案是否敏感,有效。作为体内药敏实验,对于化疗不敏感的肿瘤,可及时调整、更换化疗药物、方案,提高化疗效果,避免术后辅助化疗的盲目性,防止了过度化疗和无效化疗。而且乳腺癌容易发生血行转移,通过“局部看全身”,更早地控制肿瘤的远处转移,达到提高患者长期生存的效果。NSABP B-18试验[6]随访16年的结果显示,原发肿瘤对化疗反应敏感及淋巴结转为阴性的患者生存率有明显提高。一项对照研究结果也初步显示:在局部晚期癌患者中,采用短程、密集新辅助化疗组的5年、10年生存率较术后辅助化疗组有明显提高,新辅助化疗中的远期疗效也有改善[7]。
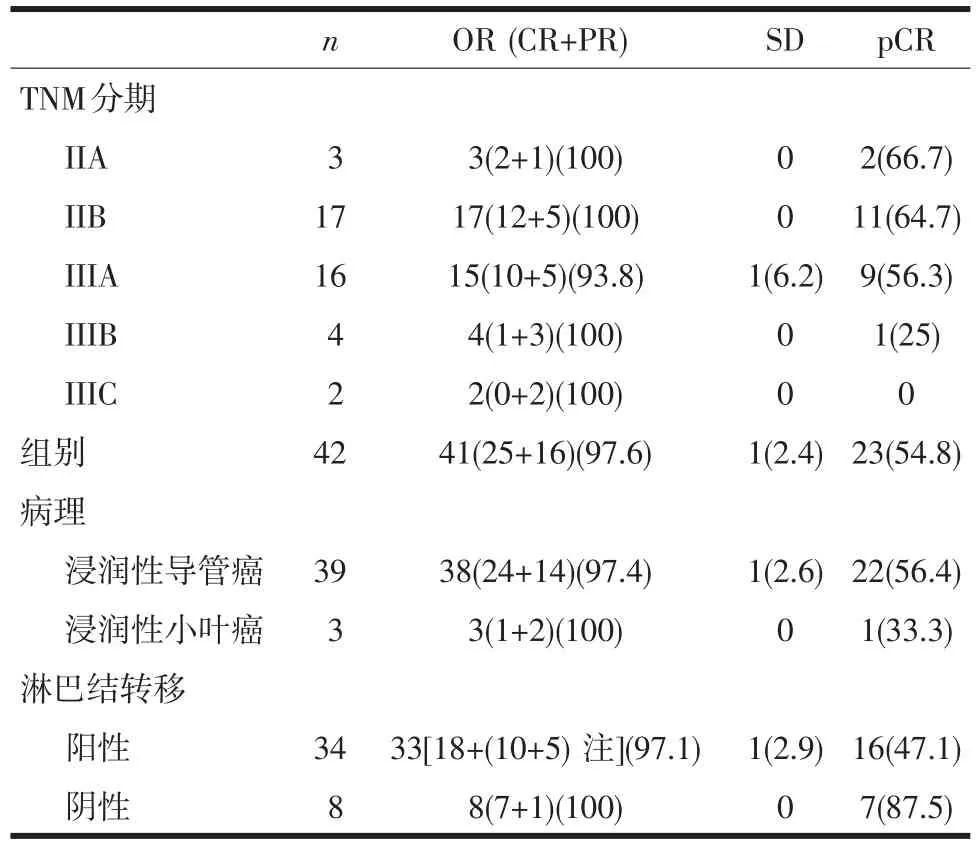
表1 42例乳腺癌新辅助治疗的疗效分析(n,%)

表2 42例乳腺癌新辅助治疗的主要不良事件(n)
由于新辅助化疗在乳腺癌治疗中的确切疗效,正被越来越多的乳腺外科医生采用。随着化疗药物的发展,不断寻找更为有效的新辅助化疗方案,是一个重要的研究方向。2013年,St Gallen会议专家共识推荐,新辅助化疗首选含紫杉类和蒽环类的化疗方案。因此,目前临床上绝大多数为蒽环和紫杉联合或序贯应用,但无标准化疗方案。
HER2蛋白的过度表达与肿瘤的侵袭性强、复发率高和死亡率高密切相关[8]。曲妥珠单抗是针对HER2阳性乳腺癌的人源化单克隆抗体,联合化疗可以显著提高乳腺癌患者的无病生存率和总生存率[9]。Valachis等[10]的一篇荟萃结果显示,Her-2阳性乳腺癌患者,新辅助化疗方案中增加曲妥珠单抗可显著增加pCR率。针对HER2阳性的乳腺癌,曲妥珠单抗联合不同的化疗方案有较多的研究[11]。与单独化疗组比较,联合曲妥珠单抗的新辅助化疗组患者的病理完全缓解率(31.7%~65.0%)显著高于单独化疗组(15.7%~26.3%)[12-13]。形成差异的原因,应该与各研究中肿瘤分型、分期、化疗方案的制定、疗程的不统一有关。体外试验显示,曲妥珠单抗与紫杉醇联合使用具有累加作用,与卡铂联合使用具有协同作用[14]。本研究选取42例HER2阳性乳腺癌,应用紫杉醇联合卡铂新辅助化疗加曲妥珠单抗治疗,其临床有效率高达97.6%,病理完全缓解率也有57.1%,达到了很好的治疗效果。
在化疗的不良事件中,心功能的损害是应用曲妥珠单抗最严重的不良反应,约4%~6%,而联合蒽环类药物时其发生率高达27%[15]。在骨髓抑制,胃肠道反应,口腔溃疡,脱发的发生率方面,化疗联合曲妥珠单抗与单独化疗组之间无明显差异[16-17]。本文42例治疗中没有出现消化道不良事件及心脏不良事件。这考虑与方案中不含蒽环类药物有一定关系。11例出现骨髓抑制严重,经G-CSF升白治疗后,继续进行治疗。其余不良事件反应较轻,经对症、支持治疗后均可较好耐受。
4疗程紫杉醇联合卡铂单周化疗方案加曲妥珠单抗的治疗,在HER2阳性的乳腺癌新辅助治疗中,有较高的临床有效率及病理完全缓解率,且无严重不良事件,故是一可选择的不含蕙环类药物的乳腺癌新辅助化疗方案。
[1]方志沂.乳腺癌[M].北京:北京大学医学出版社,2007:246-254.
[2]沈坤炜,廖宁.紫杉醇序贯表阿霉素新辅助化疗联合曲妥珠单抗显著提高病理完全缓解率[J].循证医学,2006,6(2):84-86.
[3]沈镇宙,柳光宇,苏逢锡,等.多西紫杉醇加表柔比星治疗局部晚期乳腺癌的多中心II期临床研究 [J].中华肿瘤杂志,2005,27(2):126-128.
[4]邵志敏.乳腺肿瘤学 [M].上海:复旦大学医学出版社 ,2013: 546-547.
[5]Bonadonna G,Valagussa P,Brambilla C,et al.Primary chemothera⁃py in operable breast cancer:Eight-year experience at yht Milan Cancer Institute[J].J Clin Oncol,1998,6:93-100.
[6]Fisher B,Bryant J,Wolmark N,et al.Effect of preoperative chemo⁃therapy on the outcome of women with operable breast cancer[J]. J Clin Oncol,1998,16(8):2672-2685.
[7]张斌,蔡玉娥,张奇,等.新辅助化疗用于可手术乳腺癌的10年疗效[J].中国肿瘤临床,2002,29(3):157-159.
[8]Perez EA,Suman VJ,Davidson NE,et al.HER2 testing by lo⁃cal,central,and reference laboratories in specimens from the North Central Cancer Treatment Group N9831 intergroup adjuvant trial[J].J Clin Oncol,2006,24(19):3032-3038.
[9]Yardley DA,Tripathy D,Brufsky AM,et al.Long-term survivor characteristics in HER2-positive metastatic breast cancer from reg⁃istHER[J].Br J Cancer,2014,110(11):2756-2764.
[10]Valachis A,Mauri D,Polyzos NP,et al.Trastuzumab combined to neoadjuvant chemotherapy in patients with HER2-positive breast cancer:a systematic review and meta-analysis[J].Breast,2011,20(6):485-490.
[11]Buzdar AU,Ibrahim NK,Francis D,et al.Significantly higher pathologic complete remission rate after neoadjuvant therapy with trastuzumab,paclitaxel and epirubicin chemotherapy:results of a randomized trial in human epidermal growth factor receptor 2-posi⁃tive operable breast cancer[J].J Clin Oncol,2005,23(16): 3676-3685.
[12]Untch M,Rezai M,Loibl S,et al.Neoadjuvant treatment with trastuzumab in HER2-positive breast cancer:results from the Ge⁃par Quattro study[J].J Clin Oncol,2010,28(12):2024-2031.
[13]廖宁,张国淳,李学瑞,等.联合曲妥珠单抗的新辅助化疗方案用于HER2阳性乳腺癌的Meta分析 [J].南方医科大学学报,2009,29(5):943-945.
[14]Pegram MD,Koneeny GE,O’Callaghan C,et al.Rational combina⁃tions of trastuzuumab with chemotherapeutic drugs used in the treatment of breast cancer[J].J Natl Cancer Inst,2004,96(10): 739-749.
[15]丁燕,吴洪斌.曲妥珠单抗的不良反应及处理 [J].药物不良反应杂志,2003,5(6):388-389.
[16]Gianni L,Eiermann W,Semiglazov V,et al.Neoadjuvant and ad⁃juvant trastuzumab in patients with HER2-positive locally ad⁃vanced breast cancer(NOAH):follow-up of a randomised con⁃trolled superiority trial with a parallel HER2-negative cohort[J]. Lancet Oncol,2014,15(6):640-647.
[17]肖宇,李惠平,侯宽永,等.40例乳腺癌新辅助化疗的疗效观察[J].癌症进展,2008,6(2):104-109.
(收稿:2015-02-06修回:2015-04-26)
(责任编辑张 瑾)
Study on Weekly Paclitaxel Plus CarboPlatin and Trastuzumab as Neoadjuvant Therapy for HER2 Positive Breast Cancers
ZHANG Gang-ling,ZHANG Pei-li,ZHU Jing-jun,et al.Department of Breast Surgery, Baotou Cancer Hospital,Baotou(014030),China
ObjectiveTo evaluate the clinical efficacy and safety of weekly paclitaxel plus carboplatin and trastuzumab as neoadjuvant therapy for HER2 positive breast cancers.MethodsForty-two patients with HER-2 positive breast cancer were assigned to receive four cycles of paclitaxel plus carboplatin and trastuzum⁃ab as neoadjuvant therapy with dose of paclitaxel 80 mg/m2and carboplatin AUC=1.5,given day1,out of every 3weeks for a total of 12 weeks;and were mainly for bone marrow suppression and hair loss.None of them suffered from severe cardiotoxicity. ConclusionThis four cycles therapy of weekly paclitaxel plus carboplatin and trastuzumab was highly effective and tolerable as neoadjuvant therapy for HER2 positive breast cancer.
weekly trastuzumab.Then the overall clinical efficacy and adverse reactions were observed.The primary end point was pCR.ResultsForty-one patients completed four cycles of paclitaxel plus carboplatin and trastuzumab as neoadjuvant therapy.The overall response(OR)rate was 97.6%, clinical complete response(CR)was achieved in 25 cases,partial response(PR)in 16 cases.The pCR was seen in 23 cases(54.8%).Adverse reactions
Paclitaxel plus carboplatin;trastuzumab;breast cancers;neoadjuvant therapy
R737.9
A
1007-6948(2015)05-0463-04
10.3969/j.issn.1007-6948.2015.05.007
内蒙古包头市科技发展研究基金(2014S2003-3-4)
内蒙古包头肿瘤医院乳腺外科(包头 014030)
张培礼,E-mail:zhangpeiliwm@263.com

