银粉末微电极的CV和EIS研究
张永强,郑会勤
(1.河南教育学院 化学与环境学院,河南 郑州 450046; 2.郑州大学 化学与分子工程学院,河南 郑州 450001)
银粉末微电极的CV和EIS研究
张永强1,2,郑会勤1
(1.河南教育学院 化学与环境学院,河南 郑州 450046; 2.郑州大学 化学与分子工程学院,河南 郑州 450001)
摘要:为了研究氧化还原过程中银电极的组成和结构的变化,将银粉制成粉末微电极.通过对银粉末微电极的循环伏安测试和电化学阻抗谱分析,得知反应过程中的银电极分为内、外两层.在不同的反应阶段,确定了内、外两层的组成和结构.
关键词:银粉末微电极;氧化还原;CV;EIS
0引言
粉末微电极实际上就是多孔电极与微电极的结合.将用作电极材料的粉末填入带微孔的铂微电极中即制成粉末微电极.粉末微电极的端面与铂微盘电极具有相同的表观面积,而电极的粉层部分具有多孔电极的性质.因此相对于平面微盘电极,粉末微电极的实际有效反应表面大为提高.采用粉末微电极技术可以显著提高电极反应的表观电流密度和表观可逆性.粉末微电极技术已成功地应用于电源、电催化以及生物电化学等领域的研究[1].
电化学阻抗谱(electrochemical impedance spectroscopy,EIS)是一种在电化学研究中应用极其广泛的技术,不仅可以研究包括扩散、传荷等步骤在内的电极过程[2-3],而且经常用来评价金属或合金材料表面无机陶瓷涂层[4-5]或有机涂层[6]的结构和性能.交流阻抗技术的优点是能够在不同的频率段分别得到涂层的电容、电阻及涂层与基底界面的电容、电阻等有关信息.根据测量得到的EIS数据和实际体系的物理化学过程,选择合适的等效电路模型,对电化学阻抗谱进行模拟解析,从而研究无机或有机涂层的组成和结构特性.
银的氧化和还原是一个复杂的过程,银从0价经过+1价氧化到+2价,再从+2价经+1价还原至0价.关于氧化还原过程中银电极的组成和结构变化的研究还未见报道.笔者将银粉制成粉末微电极,应用循环伏安法(cyclic voltammetry,CV)和EIS对银粉的氧化还原过程进行研究,以确定不同反应阶段银电极的组成和结构特征.
1实验
1.1试剂与仪器
试剂:丙酮、硝酸、盐酸、氢氧化钾和自制蒸馏水.实验中所用试剂均为分析纯.
仪器:CK-240超声波清洗机(长沙超科有限公司)、XSP-2C显微镜(上海光学仪器一厂)、CHI660C电化学工作站(上海辰华仪器有限公司).
1.2粉末微电极的制备
将直径100 μm的铂丝封入玻璃管内,然后将玻璃管末端依次在4#~6#金相砂纸上打磨,直至磨平并露出铂丝,再分别用蒸馏水和丙酮将电极末端超声清洗干净.将该微电极放入微沸的王水中腐蚀.一段时间后,用显微镜观察电极末端,直至电极末端腐蚀出深度为100 μm~200 μm的孔洞,将电极洗净烘干.在玻璃片上铺一层自制的银粉,用微电极在粉末上研磨,使孔洞内填满电极材料,即得银粉末微电极.
1.3CV测试
粉末微电极做工作电极,铂电极做辅助电极,Hg/HgO电极做参比,30%KOH溶液(质量比)做电解液,用CHI660C电化学工作站对银粉末微电极进行循环伏安测试.测试条件:扫描范围为0.1 V~1.0 V,扫描速度为0.8 mV/s,循环周数为3 w.
1.4EIS测试
粉末微电极做工作电极,铂电极做辅助电极,Hg/HgO电极做参比,30%KOH溶液(质量比)做电解液,用CHI660C电化学工作站分别对银粉末微电极不同氧化还原阶段的产物进行电化学交流阻抗测试,进而分析电极表面物质组成及结构的变化.测试条件:起始电位为-0.5 V,频率范围为10-2Hz~105Hz,振幅为5 mV.
2结果与讨论
2.1CV测试结果
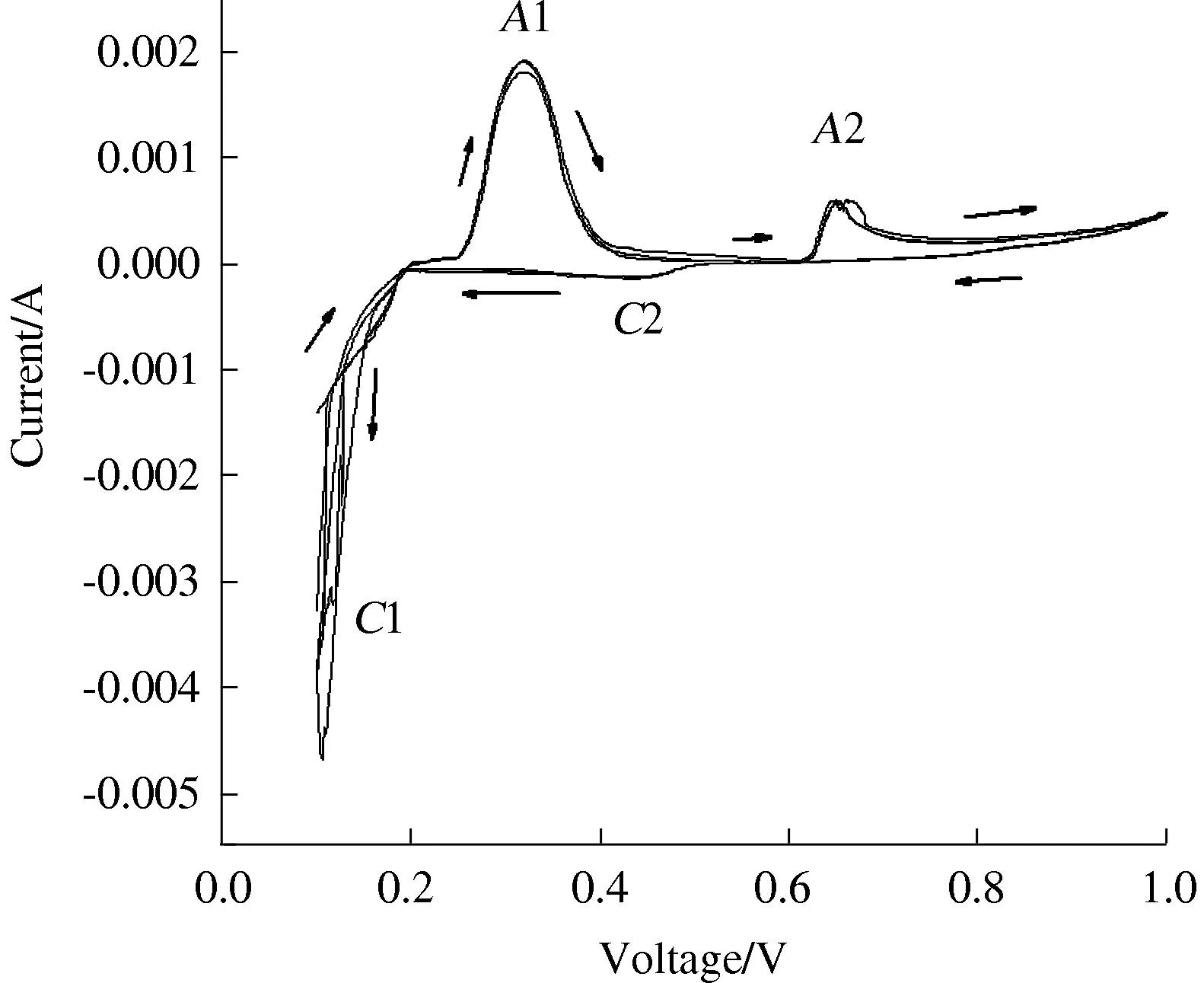
扫描速度:0.8 mV/s;循环周期: 3 weeks图1 银粉末微电极的循环伏安曲线 Fig.1 The CV curves of silver powders microelectrode
由图1可见,在扫描范围内出现了2个氧化峰和2个还原峰.向右扫的氧化过程中,在0.24 V左右出现第一个氧化峰,对应于Ag氧化为Ag2O的过程(A1), 峰面积(SA1)约为9.6×10-2C;在0.62 V左右出现第二个氧化峰,对应于Ag2O氧化为AgO的过程(A2),峰面积(SA2)约为1.1×10-2C.向左扫的还原过程中,在0.5V左右出现第一个还原峰,对应于AgO还原为Ag2O的过程(C2),峰面积(SC2)约为5.8×10-3C;在0.2 V左右出现第二个还原峰,对应于Ag2O 还原为Ag的过程(C1),峰面积(SC1)约为9.9×10-2C.4个峰的面积关系为:SC1>SA1>SA2>SC2.峰面积的变化可以解释为:A1过程中生成的Ag2O在A2步骤只有部分被氧化为AgO,因此A2消耗的电量小于A1;A2生成的AgO在C2中也只有部分被还原成Ag2O,因此C2消耗的电量小于A2;在C1中电极上除了Ag2O外,还有未被还原的AgO,因此当C1全部还原成Ag时,就需要比A1更多的电量.上述氧化还原过程中电量的变化情况,将为后面确定电极的成分提供证据.相关反应如下:
2Ag+2OH-=Ag2O+H2O+2e-,
(1)
Ag2O+2OH-=2AgO+H2O+2e-.
(2)
2.2EIS测试结果
分别对银粉末微电极在反应前和A1、A2、C2及C1峰出现后进行EIS测试,并找出合适的等效电路对交流阻抗谱进行拟合,得出各电路元件的拟合值,再通过对各元件拟合值的分析,研究电极表面物质的组成及结构的变化.等效电路的描述采用电路描述码,测试及拟合结果如图2.方框代表实验曲线,实线代表拟合曲线.采用所选的等效电路时,拟合曲线与实验曲线得到了很好的拟合.
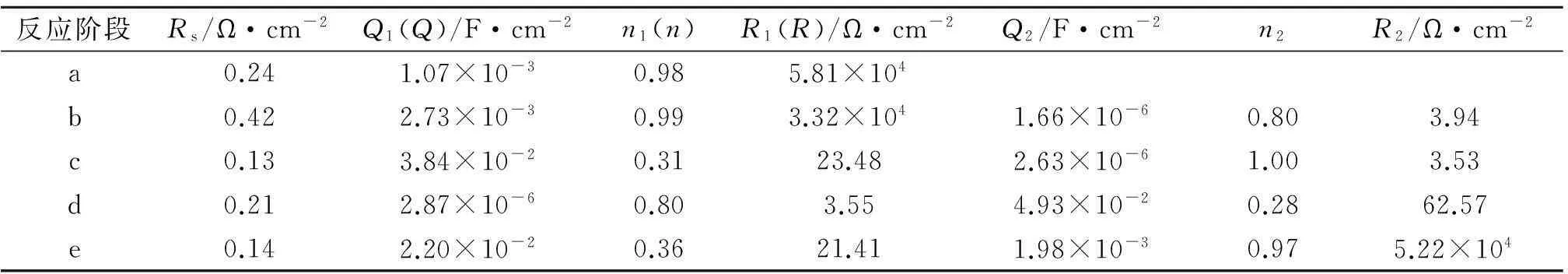
表1列出了各Bode图与反应阶段及等效电路的对应关系.由于电极层和界面双电层的电容并不完全是纯电容,所以用常相位角元件(constant phase angle element, CPE)Q代替绝大多数电容C.CPE的阻抗Z=Yo-1(jω)-n,其中包含CPE常数Yo和弥散指数n.Q与电极层的孔隙率和电介质有关,孔隙越多电介质的介电常数越大,则Q越大.由于Ag、Ag2O和AgO的介电常数远小于水和氢氧化钾的介电常数,所以电极层的电容主要取决于进入其中的水和氢氧化钾的多少.n与电极层的表面粗糙度有关,n越小,粗糙度越高[7];当n=1时,Yo=C,Q就相当于C.电极层电阻与电极的组成和附着量有关.
等效电路的物理模型如图3.反应前的电极层为一层,反应后的电极层分为内、外两层.当然,这种分层是相对的,内、外层间并不存在明显的物理界限,其中Rs为溶液电阻,C、R为一层电极的电容和电阻,C1、R1为电极外层的电容和电阻,C2、R2为电极内层的电容和电阻,Cdl、Rct为界面双电层电容和电荷传递电阻.
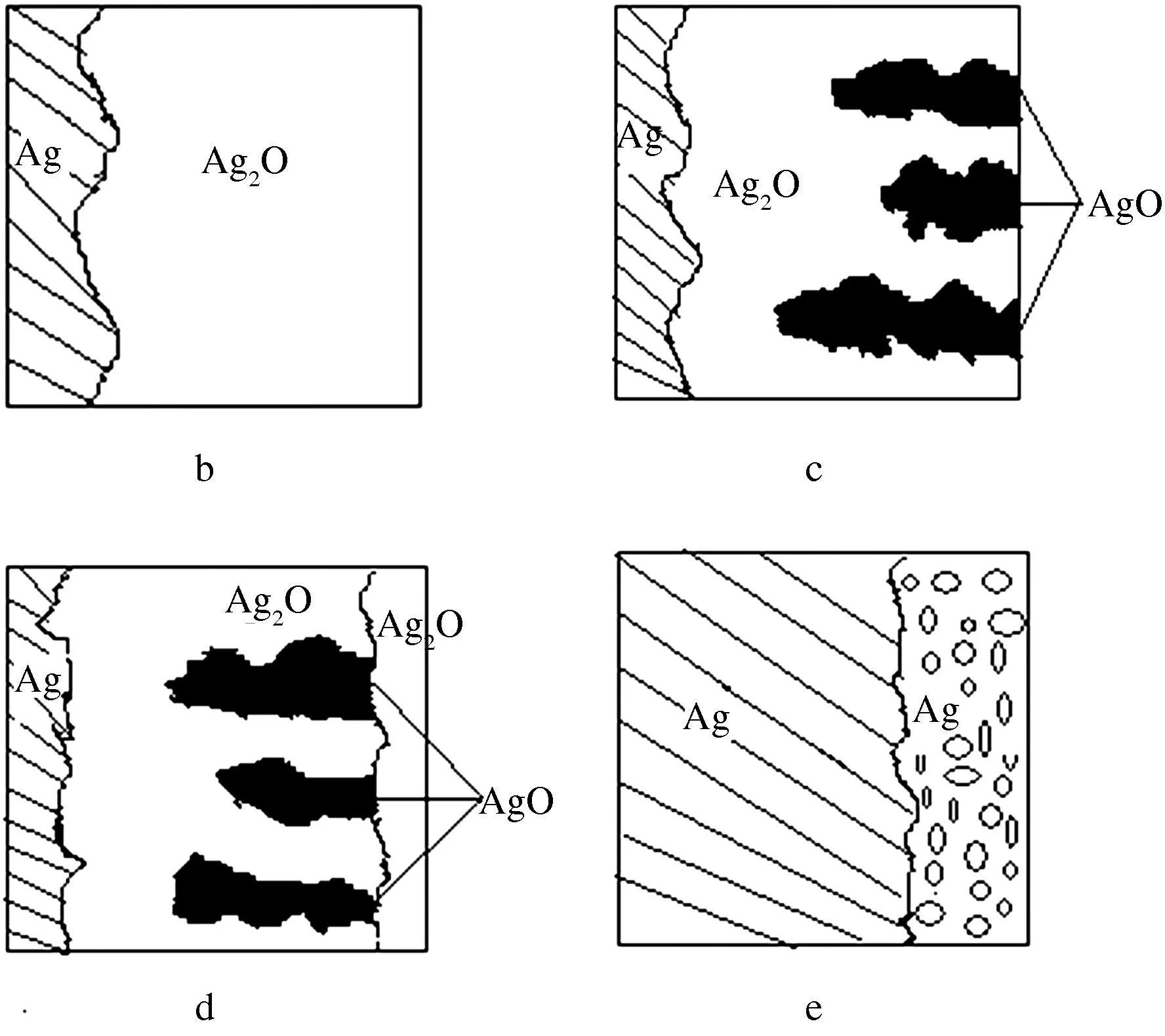
反应不同阶段等效电路各元件的拟合值如表2,表中只列出了溶液和电极层的电阻和电容.在反应的各阶段,溶液的电阻基本不变并且都较小.反应前(a阶段),银粉末电极形成一层表面光滑(n=0.98)、内部致密(电容小、孔隙率低)的电极层.当Ag2O生成后(b阶段),电极外层的电容增加(1.07×10-3F·cm-2→2.73×10-3F·cm-2),这可能是由于氧化过程需要OH-参与,其向电极层内部进行渗透,形成离子通道.水和OH-的进入,使电极外层的介电常数增大,电容升高.外层电阻受两方面因素的影响,一方面Ag2O的生成使电阻增加;另一方面,外层中碱液的进入,使得电阻减小,而后者占了上风,所以外层电阻减小(5.81×104Ω·cm-2→3.32×104Ω·cm-2).而电极内层的电容和电阻都较小,这是由内层未氧化的银形成的.b阶段形成的银电极的结构见图4b.
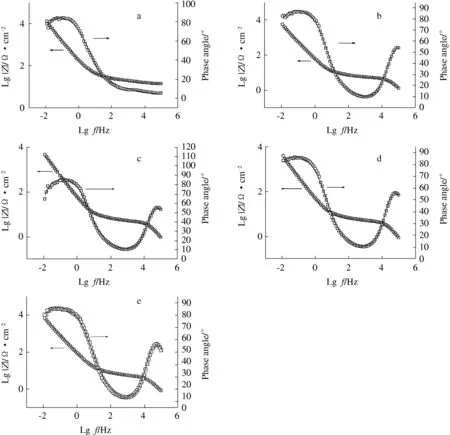
超始电位:-0.5 V; 振幅: 5mV; “□”:测量值;“—”:fitting value

表1 各Bode图与反应阶段及等效电路的对应关系
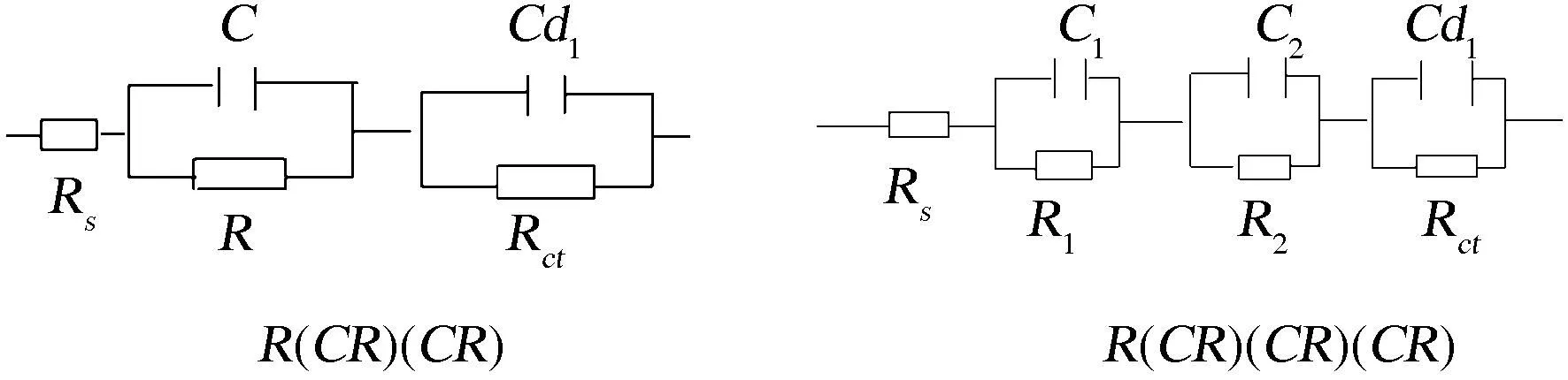
图3 等效电路物理模型 Fig.3 The physical models of equivalent circuit
Ag2O氧化为AgO后(c阶段),电极外层的电容明显增加(2.73×10-3F·cm-2→3.84×10-2F·cm-2).田昭武等[8]认为,Ag2O氧化为AgO时,并不是在Ag2O层表面均匀进行的,而是优先在Ag2O层表面电阻小的地方进行,Ag2O被氧化为AgO后,这些地方的电阻进一步减小,反应沿着AgO向电极纵深发展,在垂直于电极方向上形成若干个深洞.而AgO的密度比Ag2O大,深洞中AgO的体积将减小,在洞内出现较大的缝隙,将有更多的电解液进入缝隙内,使得外层电容迅速增加.同样,由于孔洞的出现,使得外层表面变得粗糙(n=0.31).AgO的电阻率比Ag2O小,同时由于孔洞内更多溶液的进入,使得外层电阻迅速下降(3.32×104Ω·cm-2→23.48 Ω·cm-2).且外层中只有部分Ag2O被氧化成AgO(见图1,SA2 表2 反应不同阶段等效电路各元件的拟合值 图4反应各阶段银电极的结构示意图 Fig.4The structural diagrams of the silver electrode for every stage AgO还原为Ag2O后(d阶段),电极外层的电容在减小(3.84×10-2F·cm-2→2.87×10-6F·cm-2),这是因为孔洞内的AgO被还原为Ag2O后,孔洞内的缝隙将被填满,新生成的Ag2O与原来的Ag2O联成一个整体,使得外层中的电解液减少,电容减小.同时,孔洞被填平,外层表面粗糙度降低(n=0.80).AgO还原为Ag2O后,外层电阻理应增大,但实际却在减小,这说明外层在变薄.且c阶段的外层中只有部分靠近溶液的AgO被还原为Ag2O(见图1,SC2 Ag2O还原成Ag后(e阶段),电极外层的电容增加,n减小,电阻增大;说明外层结构疏松,内部有较多的电解液,表面粗糙,外层变厚.电极内层的电容较小,n值大,电阻较大,与反应前(a阶段)的数值基本一致;说明内层结构致密,表面光滑,基本恢复至反应前的形貌.且由于AgO的存在,使得该阶段消耗的电量大于b阶段(见图1,SC1>SA1).e阶段形成的银电极的结构见图4e. 3结论 银电极的氧化还原过程共包含4个阶段,通过对银电极CV测试结果和EIS各元件拟合值的分析,可将银电极分为内、外两层,在不同的反应阶段,内、外两层的组成和结构发生相应的变化.具体内容如下: (1)Ag氧化为Ag2O后,外层是表面光滑,颗粒间渗透有碱液的Ag2O;内层是少量未反应的Ag. (2)Ag2O氧化为AgO后,外层由Ag2O和AgO形成的孔洞组成,表面粗糙,结构疏松;内层仍为未反应的Ag. (3)AgO还原为Ag2O后,外部由一薄层相对光滑、致密的Ag2O组成;内层由表面粗糙、结构疏松的Ag、Ag2O和AgO共同组成. (4)Ag2O还原为Ag后,外部是一薄层表面粗糙、结构疏松的Ag;内部是一厚层表面光滑、结构致密的Ag. 参考文献 [1]陈剑.粉末微电极用作生物传感器的理论与实践[M]. 武汉:武汉大学出版社,2012. [2]HARRINGTON D A, VAN DEN DRIESSCHE P. Impedance of multistep mechanisms: Equivalent circuits at equilibrium [J]. Electrochim Acta, 2011,44(24): 4 321-4 330. [3]BAKER B C, WEST A C. Electrochemical impedance spectroscopy study of nickel-iron deposition [J]. J Electrochem Soc, 2007, 144(1): 164-175. [4]BOVARD F S, BURLEIGH T D, SMITH A T. Electrochemical impedance spectroscopy of electrocoated aluminum food cans [J]. Electrochim Acta, 2005,40(2): 201-207. [5]PAN J, THERRY D, LEYGRAF C.Electrochemical impedance spectroscopy study of the passive oxide film on titanium for implant application [J].Electrochim Acta, 2006, 41(7): 1 143-1 153. [6]POPOY B N, ALWOHAIBI M A, WHITE R E. Using electrochemical impedance spectroscopy as a tool for organic coating solute saturation monitoring [J]. J Electrochem Soc, 2003, 140(4): 947-951. [7]张建民,杨长春,石秋芝.交流阻抗谱研究钙磷陶瓷电沉积层的结构[J]. 硅酸盐学报, 2003, 31(2): 127-132. [8]田昭武,陈衍珍.银电极大电流充放电的某些行为[J].厦门大学学报:自然科学版,1963,10(1):34-42. Study on CV and EIS of Silver Powders Microelectrode ZHANG Yong-qiang1,2, ZHENG Hui-qin1 (1.DepartmentofChemistryandEnvironment,HenanInstituteofEducation,Zhengzhou450046,China; 2.DepartmentofChemistryandMolecularEngineering,ZhengzhouUniversity,Zhengzhou450001,China) Abstract:The Ag powder microelectrode was made to survey the changes of its ingredients and structures during the redox process. The cyclic voltammetry and electrochemical impedance spectroscopy study on silver powders microelectrode were carried out and discovered that silver electrode can be divided into two layers, the external and the internal. In addition, the ingredients and structures of two layers were changed at different stages of reaction. Key words:Ag powder microelectrode; redox; CV; EIS 中图分类号:O646.54 文献标识码:A 文章编号:1007-0834(2015)02-0004-05 doi:10.3969/j.issn.1007-0834.2015.02.002 作者简介:张永强(1977—),男,河南焦作人,河南教育学院化学与环境学院副教授,主要研究方向:电化学. 基金项目:河南省自然科学基金项目(132102210161) 收稿日期:2015-01-25