M oO3纳米带/RGO复合材料的制备及其电化学性能研究
纪文旭 吴 迪 杨 蓉 丁维平 彭路明
(南京大学化学化工学院,介观化学教育部重点实验室,南京210093)
M oO3纳米带/RGO复合材料的制备及其电化学性能研究
纪文旭 吴 迪 杨 蓉 丁维平 彭路明*
(南京大学化学化工学院,介观化学教育部重点实验室,南京210093)
以水杨酸为模板剂和还原剂,采用水热法制备得到了一种MoO3纳米带/RGO复合材料。利用XRD、SEM、TEM、拉曼光谱、恒流充放电、交流阻抗等手段对样品的结构、形貌以及电化学性能进行表征。测试结果表明,MoO3纳米带/RGO复合材料作为锂离子电池负极材料,在50 mA·g-1的电流密度下可逆比容量为1 000 mAh·g-1,循环50次后比容量还保持在950 mAh·g-1,相比于MoO3纳米带其容量保持能力和循环性能得到了显著改善。
MoO3纳米带;还原氧化石墨烯;锂离子电池;负极材料
DO I:10.11862/CJIC.2015.111
0 引言
自1990年SONY公司正式向市场推出商品化的锂离子电池以来,锂离子电池技术和产业获得了飞速发展,已广泛应用于笔记本电脑、数码相机、移动电话等便携式设备当中。近年来,随着纯电动汽车(EVs)、混合动力汽车(HEVs)、航空航天、军用电子设备等的发展,新一代高比能量、大功率、长寿命、无污染及低成本的高性能动力电池正成为锂离子电池研究的热点和方向[1-4]。
石墨类碳材料由于导电性好、循环性能优异(>95%)、资源丰富、价格低廉,是目前市场上应用最为广泛的锂离子电池负极材料。然而在使用过程中,石墨类碳材料电极表面会有锂枝晶生成,导致电池短路,存在安全隐患,同时其理论比容量较低(372 mAh·g-1),人们期望能寻找到一种高比容量和高安全性的负极材料作为替代材料。过渡金属氧化物Fe2O3、Mn3O4、Co3O4和Fe3O4等作为锂离子电池负极材料时通常发生转化反应机理,其比容量一般为石墨类碳材料的2~3倍,因而受到研究人员的广泛关注[5-12]。其中α-MoO3以高达1 117 mAh·g-1的理论比容量、环境友好和成本较低等特点备受青睐。然而由于α-MoO3的导电性和锂离子扩散速率较差,且在锂离子嵌入/脱嵌过程中体积变化剧烈,导致材料粉化现象严重,造成α-MoO3容量保持能力不高,限制了其在锂离子电池中的商业应用前景。为了克服这些缺陷,研究人员们提出了许多策略,包括减小材料的尺寸到纳米级,以及将α-MoO3和导电材料进行掺杂或包裹复合等。Zhao等[13]采用电化学沉积的方法制备得到了一种多孔结构的MoO3薄膜,在70 mA·g-1的充放电电流密度下,首次放电容量为1 286 mAh·g-1,50次循环以后放电容量仍达803 mAh·g-1。Hassan等[14]成功地将MoO3纳米带和碳材料复合,材料表现出很好的电化学性能。Tao等[15]通过控制球磨法得到了一种MoO3和碳均匀分布的纳米复合物,该复合物在0.2C的倍率下表现出近700 mAh·g-1,电化学性能较为突出。
2004年,英国曼彻斯特大学的Geim和Novoselov[16]采用机械剥离的方法首次在实验中制备并观察到二维碳材料石墨烯。理想的石墨烯是由单层碳原子组成的二维结构材料,碳原子以sp2杂化方式互相键合形成蜂窝状结构排布,其厚度为0.35 nm,碳碳键长度约为0.142 nm。这种特殊的二维结构使得石墨烯具有高的理论比表面积(2 600 m2·g-1)、突出的电子迁移率(15 000 cm2·V-1·s-1)、良好的化学稳定性以及优异的力学性能等诸多特点[17-19]。这些特点使得石墨烯与过渡金属氧化物的复合可能解决过渡金属氧化物作为锂离子电池负极材料时存在的不足。到目前为止,诸如Mn3O4-graphene[20]、Fe2O3-graphene[21]、Fe3O4-graphene[22]、Co3O4-graphene[23]、SnO2-graphene[24]以及TiO2-graphene[25]等复合材料已经被合成出来,并且表现出优异的电化学性能。
本文采用水热法较为便捷地制得了一种MoO3纳米带/还原氧化石墨烯(RGO)复合材料。这种复合材料在50 mA·g-1的电流密度下表现出1 000 mAh· g-1的可逆比容量,循环50次后容量仍然有950 mAh·g-1,相对于纯MoO3纳米带而言,比容量得到很大的提升,体现了添加RGO对于提升MoO3电化学性能的巨大作用。
1 实验部分
1.1 氧化石墨(Graphite Oxide)的制备
采用Hummer法[26]制备氧化石墨。在干燥的平底烧瓶中加入23 mL浓硫酸(98%),冰浴冷却至0℃,加入1 g石墨粉末并搅拌。随后在冰浴下缓慢加入6 g高锰酸钾(分10次加入,每次间隔5 min)。继续冰浴搅拌2 h后,将烧瓶置于35℃油浴锅中搅拌30 min。接着在冰浴的条件下缓慢加入46 mL H2O,随后将烧瓶置于98℃油浴锅中搅拌30 min,最后加入140 mL H2O和10 mL 30%H2O2。所得溶液呈金黄色,趁热过滤并用5%的HCl溶液和蒸馏水充分洗涤至无SO42-(BaCl2溶液检测),产物在80℃干燥48 h。
1.2 M oO3纳米带/RGO复合材料的制备[27]
称取20 mg氧化石墨,分散在20 m L去离子水中(1 mg·mL-1),超声30 min后得到Graphene Oxide (GO)水溶液。称取1.21 g(5 mmol)Na2MoO4·2H2O以及3 g水杨酸钠,溶于40 m L H2O中,加入到上述GO水溶液中,搅拌10 min,用3 mol·L-1的HCl溶液调节pH=1。将上述溶液移至水热釜中,180℃水热24 h。将固体产物过滤、水洗及醇洗,于80℃真空干燥过夜。
1.3 材料表征
XRD表征采用Philips X′pert Pro型X射线衍射仪(Cu靶Kα辐射,λ=0.154 18 nm)。微观形貌表征采用Hitachi S-4800场发射扫描电子显微镜(FESEM)和JEOL JEM-2100高分辨透射电子显微镜,并结合EDX能量散射谱仪对样品的Mo、O、C元素分布情况进行检测。拉曼光谱表征采用Horiba LabRAM Aramis型共聚焦激光拉曼光谱仪。
1.4 极片的制备及电化学性能测试
按质量比为8∶1∶1分别称取活性物质、导电剂乙炔黑以及粘结剂PVDF,以N-甲基吡咯烷酮(NMP)为溶剂,取其适量将PVDF溶解,活性物质和乙炔黑混合均匀,置于研钵中研磨30 min,然后加入到PVDF的NMP溶液中,机械搅拌8 h以上,形成浆料。用刮刀将浆料均匀地涂抹在集流体铜箔上,然后放在普通烘箱中70℃干燥6 h,再用辊压机碾压烘干后的极片,并用冲片机将极片冲压成直径为15 mm的电极片,放在真空干燥箱中120℃真空干燥12 h。称取极片的重量,放进手套箱中等待组装成电池。
采用CR2032纽扣电池作为模拟电池,以金属锂片作为对电极,电解液采用1 mol·L-1LiPF6的DMC/EMC/EC(质量比为1∶1∶1)有机溶液(LB315),使用Celgard2300 PP/PE/PP三层微孔复合隔膜作为电池隔膜,以不锈钢垫片和弹簧片为填充物来增加极片与电池壳之间的接触,用封口机将电池密封。整个组装过程在氩气手套箱中完成。
采用武汉市鑫诺电子科技有限公司生产的Land-CT2001A型电池性能测试系统测试扣式电池的充放电性能和循环性能。采用扣式电池体系在上海辰华公司生产的CHI660D电化学综合测试仪上测试交流阻抗谱,测试频率范围为0.01 Hz~100 kHz,振幅为5 mV。
2 结果与讨论
2.1 结构及形貌分析
图1a是石墨粉末和氧化石墨的XRD特征图,可以看到,石墨粉末在26.5°处有1个尖锐的特征衍射峰,代表了石墨的(002)晶面,在54.7°附近有1个小峰,为石墨的(004)晶面。经Hummer法向石墨层间引入大量官能团与缺陷制得氧化石墨后,(002)和(004)晶面的衍射峰消失,而在10°附近出现1个新的强度较弱的衍射峰,表明石墨层的间距增加且结晶度变差。经过化学氧化处理后,石墨片层内及边缘处引入了大量的含氧基团,例如羟基(-OH),羧基(-COOH)等,造成石墨层间距加大。同时,由于含氧基团的引入,使得氧化石墨具有良好的亲水性,水分子进入到石墨层间,增大了石墨的层间距。此外,强酸作用破坏了石墨原本完美的晶型而产生大量缺陷,导致氧化石墨的结晶度变差,无序性增加,衍射峰的强度变弱[28-31]。以上结果表明,石墨得到了充分氧化变成氧化石墨。图1b为制备得到的MoO3纳米带/ RGO样品的XRD特征图,可以看出所有的衍射峰都可以归属为正交相MoO3的特征衍射峰(JCPDS:05-0508),表明制备得到的MoO3纳米带/RGO复合物较为纯净。
对得到的MoO3纳米带/RGO复合材料进行电镜表征,以观察样品的形貌,结果如图2所示。图2a~b是MoO3纳米带/RGO复合材料的SEM图片,可以看出MoO3纳米带形貌较为规整,宽度约200~300 nm,长度为几个微米。高分辨透射电镜照片(图2c)显示在MoO3纳米带边缘有RGO出现。由于MoO3能够与氨水反应生成可溶性钼酸铵(MoO3+ 2NH3·H2O→(NH4)2MoO4+H2O),借助这一特性用氨水除去MoO3纳米带/RGO复合材料中的MoO3纳米带,然后对残留物进行高分辨透射电镜表征,得到如图2d的电镜图片,可以很明显的看出残留物为大面积的薄片,并有皱褶和重叠出现,表明复合材料中确实有RGO存在。对MoO3纳米带/RGO复合材料进行EDX-Mapping表征,以观察RGO在复合材料中的分布情况,得到如图3所示的结果。可以看出钼、氧、碳3种元素在材料中的分布比较均匀,说明复合材料中RGO和MoO3纳米带的复合较为均匀。
为了进一步证实MoO3纳米带/RGO复合材料中是否存在RGO,对复合材料以及除去MoO3纳米带后的残留物分别进行拉曼光谱表征,结果如图4所示。图谱中100~1 200 cm-1之间的拉曼峰为MoO3的特征峰[32],而由于复合物中RGO的含量很低,出现在1 350和1 590 cm-1附近的拉曼特征峰强度非常弱。将MoO3纳米带用氨水溶解除去后,剩下的残留物在1 350和1 590 cm-1处有较强的拉曼峰,对应为RGO的的D带和G带,并且在2 700 cm-1附近出现2D带的特征峰,证实了RGO在复合材料中的存在[33]。
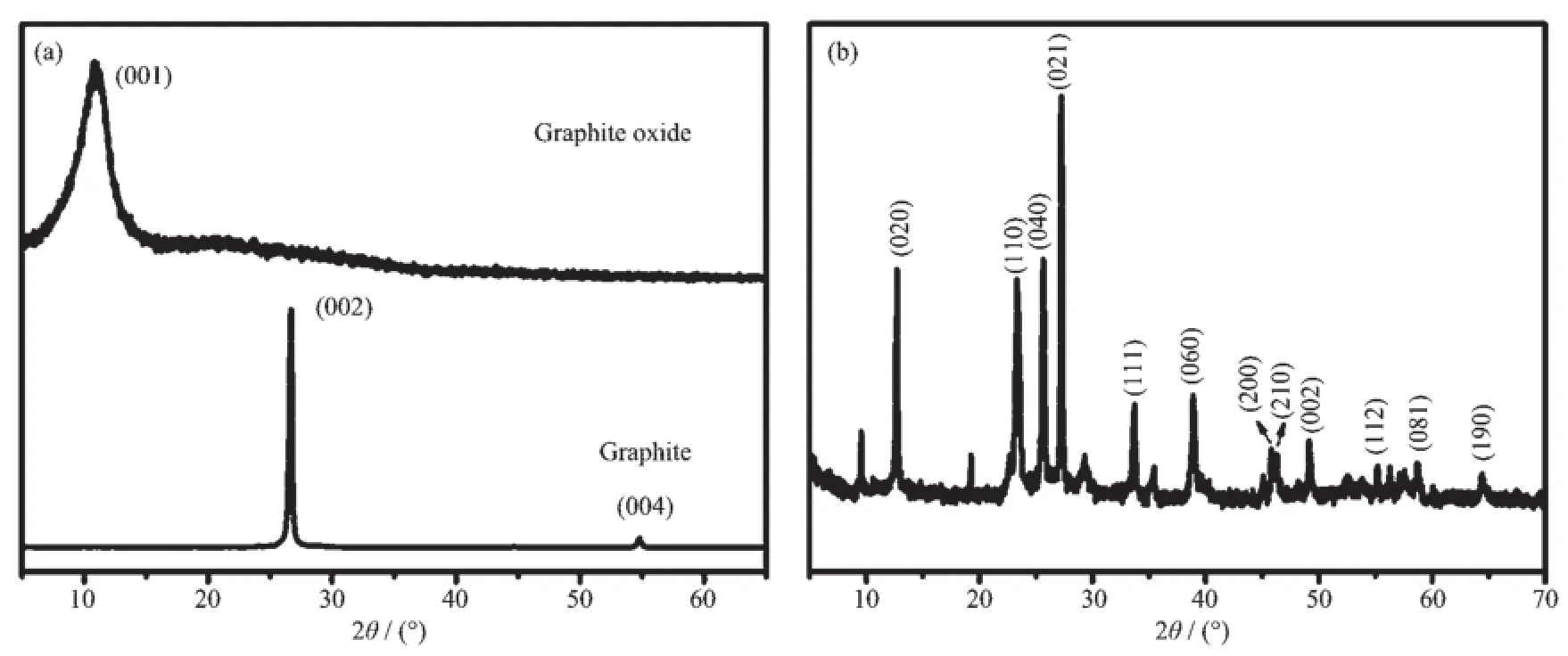
图1 (a)石墨和氧化石墨的XRD图;(b)MoO3纳米带/RGO复合材料的XRD图Fig.1 XRD patterns of(a)graphite and graphite oxide;(b)MoO3nanobelts/RGO

图2 MoO3纳米带/RGO复合材料的SEM图(a~b)和HR-TEM图(c);RGO(用氨水除去复合材料中的MoO3纳米带)的HR-TEM图(d)Fig.2 SEM images(a~b)and HR-TEM image(c)of the MoO3nanobelts hybrid composites;HR-TEM image(d) of RGO(MoO3nanobelts was removed by dissolving hybrid in ammonia)

图3 MoO3纳米带/RGO复合材料的EDX-Mapping图Fig.3 SEM image and corresponding carbon,oxygen and molybdenum elemental mapping of the MoO3nanobelts/RGO hybrid composites
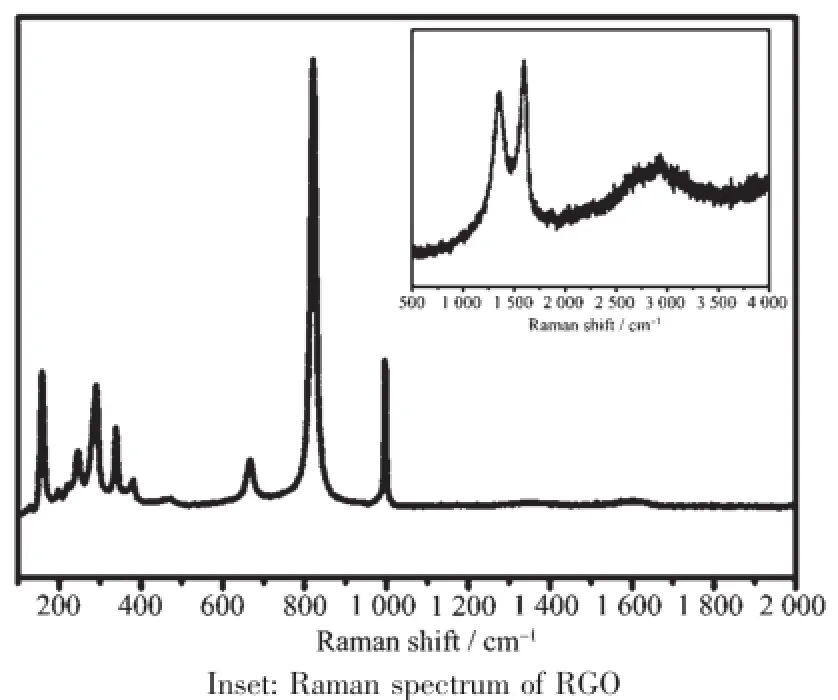
图4 MoO3纳米带/RGO复合材料的拉曼图谱Fig.4 Raman spectrum of the MoO3nanobelts/RGO hybrid composites
2.2 电化学性能分析
图5a~5b为不含RGO的MoO3纳米带的电化学性能测试结果,其合成方法除了不加入GO水溶液外,与制备MoO3纳米带/RGO复合材料的方法相同。可以看出,在50 mA·g-1的电流密度下MoO3纳米带的可逆容量约为550 mAh·g-1,比理论容量低了50%,这可能是由于MoO3纳米带的导电性差造成的。但可以看出MoO3纳米带的循环能力还不错,50次循环后容量只发生轻微衰减,而文献[11]中块体材料的MoO3容量一般会下降到330 mAh·g-1,这体现了纳米化对提升材料的电化学性能的作用:纳米化不但缩短了锂离子在材料中的扩散距离,而且一定程度了减缓了充放电过程中由于体积变化造成的应力变化。图5c~5d为MoO3纳米带/RGO复合材料的电化学性能测试结果。可以看出复合材料的首次放电容量为1 300 mAh·g-1,大于MoO3的理论比容量,这是由于首次充放电时材料表面会形成SEI膜而得到一部分不可逆容量[13,15]。在随后的循环中,MoO3纳米带/RGO表现出1 000 mAh·g-1的比容量,并持续40个循环不发生明显的衰减,之后发生缓慢衰减,第50次循环时,材料的比容量还超过950 mAh·g-1,显示出相当好的容量保持能力和循环性能。相对于纯的MoO3纳米带,复合材料的电化学性能得到显著的提升,这应该与添加的RGO在提升了MoO3的导电性有关。
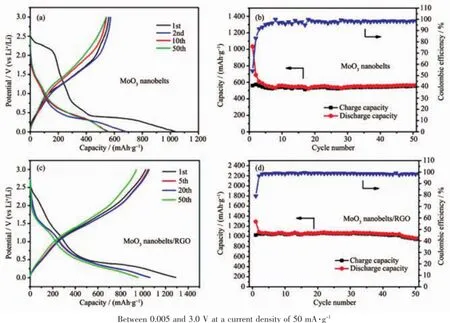
图5 MoO3纳米带和MoO3纳米带/RGO复合材料的恒流充放电曲线和循环性能曲线Fig.5 Electrochemical performance of bare MoO3nanobelts and the MoO3nanobelts/RGO hybrid composites
对MoO3纳米带/RGO复合材料的第五次充放电曲线进行偏微分处理,得到如图6所示的微分电容曲线。从图中可以看出,有2对氧化还原峰0.28/ 1.22 V和1.55/1.77 V,它们对应着由于锂离子在MoO3纳米带中的嵌入/脱嵌过程所造成的相变过程[13]。对MoO3纳米带/RGO复合材料和MoO3纳米带进行交流阻抗测试和等效电路拟合(图7),可以看出,MoO3纳米带/RGO和MoO3纳米带的阻抗谱图均由一个中高频区的半圆弧和一条低频区的直线组成。MoO3纳米带/RGO的半圆弧直径远小于MoO3纳米带的半圆弧直径,表明前者的接触电阻(Rf)和电荷迁移电阻(Rct)远小于后者,MoO3纳米带/RGO的导电性更好,因而其电化学性能也更好,体现了RGO在增强材料的导电性方面的巨大作用。
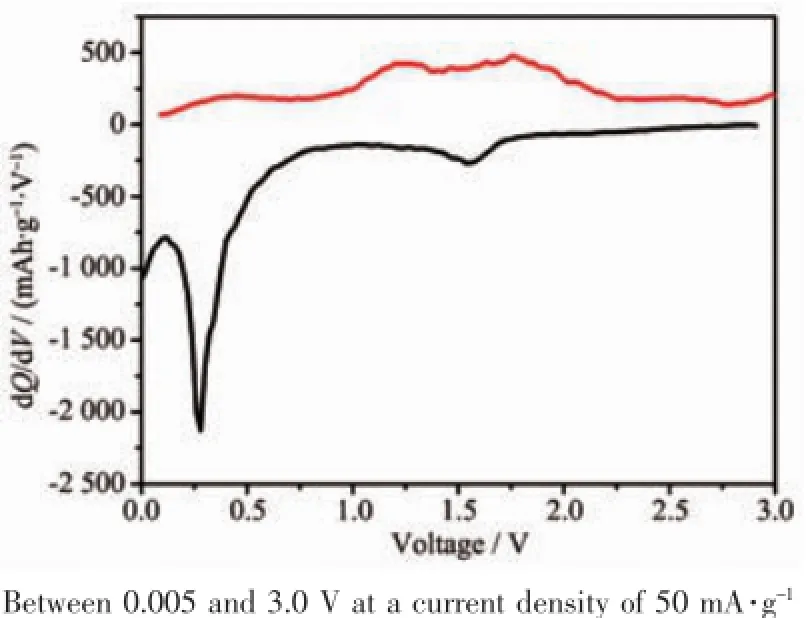
图6 MoO3纳米带/RGO复合材料的微分电容曲线Fig.6 Differential capacity curve of the MoO3nanobelts/ RGO hybrid composites for the fifth cycle
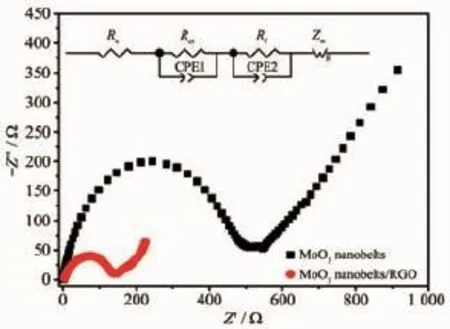
图7 MoO3纳米带/RGO和MoO3纳米带的交流阻抗图谱Fig.7 Electrochemical impedance spectra of the MoO3nanobelts/RGO hybrid composites and bare MoO3nanobelts

表1 M oO3纳米带/RGO和MoO3纳米带的交流阻抗分析结果Table1 Analysis data of EIS spectra for the M oO3nanobelts/RGO hyb rid com posites and bare MoO3nanobelts
3 结论
以水杨酸同时作为合成纳米带的模板剂和还原GO的还原剂,采用水热法较为便捷地制备得到了一种MoO3纳米带/RGO复合材料。这种复合材料作为锂离子电池的负极材料时,表现出优异的电化学性能:在50 mA·g-1的电流密度下可逆比容量为1 000 mAh·g-1,循环50次后比容量还有950 mAh· g-1。上述结果表明,将MoO3纳米化不但缩短锂离子的扩散距离,提高了锂离子扩散速率,而且为锂离子嵌入/脱嵌过程中发生的体积变化提供了缓冲空间,缓解了材料的粉化现象;同时RGO的超高导电性也增强了MoO3纳米带的导电性,从而使得MoO3的电化学性能得到提升。
[1]Kang B,Ceder G.Nature,2009,458:190-193
[2]Tarascon J M,Armand M.Nature,2001,414:359-367
[3]Kang K,Meng Y S,Bréger J,et al.Science,2006,311:977-980
[4]ZHANG Huan(张欢),QI Lu(其鲁),GAO Xue-Ping(高学平), et al.Chinese J.Inorg.Chem.(无机化学学报),2010,26(9): 1539-1543
[5]Poizot P,Laruelle S,Grugeon S,et al.Nature,2000,407:496 -499
[6]Taberna P L,Mitra S,Poizot P,et al.Nat.Mater.,2006,5: 567-573
[7]Nam K T,Kim D W,Yoo P J,et al.Science,2006,312:885-888
[8]Wang B,Chen J S,Wu H B,et al.J.Am.Chem.Soc.,2011, 133:17146-17148
[9]LIU Xiao-Feng(刘晓峰),MI Chang-Huan(米常焕),ZHANG Wen-Qing(张文庆).Chinese J.Inorg.Chem.(无机化学学报), 2014,30(2):242-250
[10]Gao J,Lowe M A,Abruna H D.Chem.Mater.,2011,23:3223 -3227
[11]Ji W,Shen R,Yang R,et al.J.Mater.Chem.A,2014,2:699 -704
[12]XUE Hai-Rong(薛海荣),ZHAO Jian-Qing(赵建庆),WANG Tao(王涛),et al.Chinese J.Inorg.Chem.(无机化学学报), 2012,28(8):1601-1608
[13]Zhao G,Zhang N,Sun K.J.Mater.Chem.A,2013,1:221-224
[14]Hassan M F,Guo Z P,Chen Z,et al.J.Power Sources, 2010,195:2372-2376
[15]Tao T,Glushenkov A M,Zhang C F,et al.J.Mater.Chem., 2011,21:9350-9355
[16]Novoselov K S,Geim A K,Morozov S V,et al.Science,2004, 306:666-669
[17]Chae H K,Siberio-Perez D Y,Kim J,et al.Nature,2004,427: 523-527
[18]Zhang Y,Tan Y W,Stormer H L,et al.Nature,2005,438: 201-204
[19]Mcallister M J,Li J L,Adamson D H,et al.Chem.Mater., 2007,19:4396-4404
[20]Wang H L,Cui L F,Yang Y A,et al.J.Am.Chem.Soc., 2010,132:13978-13980
[21]Zhu X J,Zhu Y W,Murali S,et al.Acs Nano,2011,5:3333-3338
[22]Zhou G M,Wang D W,Li F,et al.Chem.Mater.,2010,22: 5306-5313
[23]Wu Z S,Ren W C,Wen L,et al.Acs Nano,2010,4:3187-3194
[24]Paek S M,Yoo E,Honma I.Nano Lett.,2009,9:72-75
[25]Wang D H,Choi D W,Li J,et al.Acs Nano,2009,3:907-914
[26]Hummers W S,Offeman R E.J.Am.Chem.Soc.,1958,80: 1339-1339
[27]Yang X F,Lu C Y,Qin J L,et al.Mater.Lett.,2011,65: 2341-2344
[28]He H,Klinowski J,Forster M,et al.Chem.Phys.Lett.,1998, 287:53-56
[29]Lerf A,He H,Forster M,et al.J.Phys.Chem.B,1998,102: 4477-4482
[30]Cai W,Piner R D,Stadermann F J,et al.Science,2008, 321:1815-1817
[31]Gao W,Alemany L B,Ci L,et al.Nat.Chem.,2009,1:403-408
[32]Mai L Q,Hu B,Chen W,et al.Adv.Mater.,2007,19:3712-3716
[33]Guo X,Fan Q,Yu L,et al.J.Mater.Chem.A,2013,1:11534-11538
M oO3Nanobelts/Reduced Graphene Oxide(RGO)Com posites as a H igh-Performance Anode Material for Lithium Ion Batteries
JI Wen-Xu WU Di YANG Rong DING Wei-Ping PENG Lu-Ming*
(Key Laboratory of Mesoscopic Chemistry of Ministry of Education,School of Chemistry and Chemical Engineering,Nanjing University,Nanjing 210093,China)
MoO3nanobelts/RGO composites were obtained through a facile and efficient hydrothermal procedure by using organic compound sodium salicylate as both structure-directing agent and reducing agent.The crystal structure,morphologies and electrochemical performances of the as-prepared samples were characterized by powder X-ray diffraction(XRD),scanning electron microscopy(SEM),transmission electron microscopy(TEM), Raman spectroscopy,galvanostatic charge/discharge test and electrochemical impedance spectroscopy(EIS).The hybrid material shows a high specific capacity of 1 000 mAh·g-1with a good cycling stability as an anode material for lithium ion batteries,which has a much enhanced performance compared to bare MoO3nanobelts.
MoO3nanobelts;reduced graphene oxide(RGO);lithium ion batteries;anode materials
O614.61+2
A
1001-4861(2015)04-0659-07
2014-11-18。收修改稿日期:2015-01-22。
国家重大科学研究计划青年科学家专题(No.2013CB934800);国家自然科学基金(No.21222302)资助项目。*

