以硅藻为模板合成TiO2微胶囊及其可见光催化性能
陈志刚,张玉珠,钱君超,王盟盟,陆秋月
(1.江苏大学材料科学与工程学院,镇江 212013;苏州科技学院2.江苏省环境功能材料重点实验室; 3.化学生物与材料工程学院,苏州 215009)
0 引 言
随着生物学的发展,人们逐渐认识到大自然是一个庞大的实验室,它以蛋白质、糖类、核酸为基础,通过进化,构造出了无数奇特的精密生物结构[1],这些结构可以富集环境中的化学物质从而高效迅速地完成所需的化学反应,这值得人们去研究、探讨并加以模仿。近年来,生物模板法作为合成纳米材料一种全新方法逐渐受到科学工作者的重视。以各种生物如鸡蛋膜[2]、鱼鳞[3]、植物纤维[4]、昆虫翅膀[5]、花瓣[6]和DNA[7]等为模板复制具有特殊形貌的分级多孔生物组织结构,并将这些分级多孔特殊结构与无机功能材料的特性相结合,便能获得性能优越且具有独特功能的仿生材料。
Chow等[8]以香樟叶和夹竹桃叶为模板,并浸渍于硝酸铈溶液,煅烧后制备出了具有高储氧能力的仿叶形CeO2;此外,他们还以甘蔗、玉米、小麦、豇豆等的叶片为模板,先经稀盐酸处理脱去钾、钙等元素,再由TiCl3和Ti(OBu)4的乙醇溶液两步浸渍,最后在500℃煅烧制得了生物形态的TiO2,且绿叶含有的氮元素通过自掺杂进入材料,从而获得了较为优良的集光能力[9]。随后,他们又将海草作为模板,制得了掺杂氮、碘的仿海草形貌TiO2,其光催化效率远高于普通TiO2的[10]。可见模仿常见的能够进行光合作用的生物组织结构,可获得集光性能优良的微纳米结构。而最常用的方法,就是以廉价的生物为模板,浸渍于相应的金属盐溶液从而制备出氧化物材料。
已有大量文献报道了制备多孔TiO2胶囊的方法,如溶胶-凝胶法、水热法、水解法和沉积技术法等[11-14],但这些传统方法步骤繁琐、耗时长、模板的制备环节成本较高,并对环境造成严重污染。
羽纹硅藻呈长方形或舟形,花纹排列成两侧对称,表面有线纹,壳面中央呈加厚状,且细胞壁中富含多种孔道,较为适合用作模板来制备分级多层多孔材料。因此,作者以羽纹硅藻为模板,经钛盐浸渍后煅烧制备了一种全新的高效光催化剂——多孔TiO2微胶囊,研究了它的结构特性及其在可见光下降解亚甲基蓝的催化性能。
1 试样制备与试验方法
1.1 试样制备
试验用四氯化钛(质量分数为98%)、无水乙醇、亚甲基蓝、过氧化氢等均为分析纯试剂,国药集团化学试剂有限公司产;P25粉(TiO2粉,Degussa)为市售;去离子水为实验室自制。
从湖水中采集水体进行培养,并制作培养液的水封片进行镜检,确定硅藻种属,利用毛细管分离法将羽纹硅藻分离到硅藻培养基中,进行光照培养,当硅藻繁殖72 h后,即可通过离心分离得到硅藻。
将约1 g羽纹硅藻放入200 mL超纯水中,并浸入冰水混合物中,然后将2 mL四氯化钛逐滴滴入硅藻溶液中并搅拌;加入10 mL无水乙醇,用盐酸调节溶液pH至3;然后在28℃下恒温浸渍72 h,再用去离子水洗涤,并离心分离获取下层硅藻,如此重复离心洗涤3次,所得产物在50℃下干燥一段时间后放入马弗炉中,以2℃·min-1的升温速率在空气气氛中升温至550℃,保持恒温2 h,煅烧除去硅藻模板后得到多孔TiO2微胶囊。
1.2 试验方法
采用XL-30型环境扫描电子显微镜观察硅藻模板的形貌;采用S-4800型场发射扫描电子显微镜及JEOL JEM 2010型高分辨透射电子显微镜观察TiO2微胶囊的形貌;采用D/max2500PC型X射线衍射仪测TiO2微胶囊的物相;采用电镜附带的能谱仪(EDS)测TiO2微胶囊的化学成分;采用UV-2450型紫外-可见漫反射光谱仪测TiO2微胶囊和P25粉的紫外-可见光漫散射图谱;采用ESCALAB 250型X射线光电子能谱仪测TiO2微胶囊的XPS谱。
采用ASAP-2010C型自动吸附仪,通过容量法以氮气为吸附质在液氮温度77 K下对TiO2微胶囊进行吸附测定,根据测得的等温吸附曲线用BET法计算表面积,用BJH方程计算得到TiO2微胶囊的孔径分布。
在400 mL 20 mg·L-1的亚甲基蓝溶液中加入100 mg多孔TiO2微胶囊,将其置于暗室中搅拌30 min,达到吸附-脱附平衡,然后加入2 mL H2O2,在可见光照射下进行光催化降解。按同比例,以加入P25粉和H2O2及仅加入H2O2的亚甲基蓝溶液,在相同条件下进行光催化降解的对比试验。每隔一定时间取样,经离心后取上层清液,每隔一段时间吸取3 mL溶液,离心分离,取上清液,在波长664 nm处测定亚甲基蓝的吸光度。以脱色率(D)表示亚甲基蓝的光催化降解率。

式中:A0为光照前亚甲基蓝的吸光度;A为亚甲基蓝在光照t时刻的吸光度。
2 试验结果与讨论
2.1 产物的形貌与组成
由图1(a)可见,扁平的硅藻细胞上密布有较为有规则的孔道,并显出凹坑的特殊形貌,其长度大致为22 μm。经过550℃煅烧,模板被除去,生成了具有仿硅藻形貌的多孔TiO2微胶囊,如图1(b)所示,其上分布有细密规则的孔道结构,由于高温作用,得到的微胶囊长度收缩至12 μm左右。由图1(c~d)可以看出,TiO2微胶囊是由直径5~15 nm的晶体颗粒堆积而成,富含大量介孔结构,其孔径在5~15 nm。
从图2(a)可以看出,在衍射角2θ为25.2°,37.5°,48°,53.3°和62.2°处出现了强的衍射峰,分别对应于锐钛矿TiO2(JCPDS 21-1272)的(101),(004),(200),(105)和(204)晶面,硅藻本身应初期就获得了较高的脱色率,100 min后脱色率超过了80%。由于多孔TiO2微胶囊继承了硅藻独特的分级多孔结构,其丰富的孔道结构和较大的比表面积能提高催化剂捕捉光的能力;此外,掺杂含有的TiO2并未在图中显示出特征峰,这是由于它的含量过低或是呈无定形态。由图2(b)可知,多孔TiO2微胶囊中有氮元素掺杂,而硅因为质量分数低于2%而未能被检出。

图1 硅藻模板及多孔TiO2微胶囊的微观形貌Fig.1 Morphology of diatom template and porous TiO2capsule:(a) diatom,SEM morphology;(b) porous TiO2capsule,SEM morphhology;(c)porous TiO2capsule,TEM morphology at low magnification and(d) porous TiO2capsule,TEM morphology at high magnification
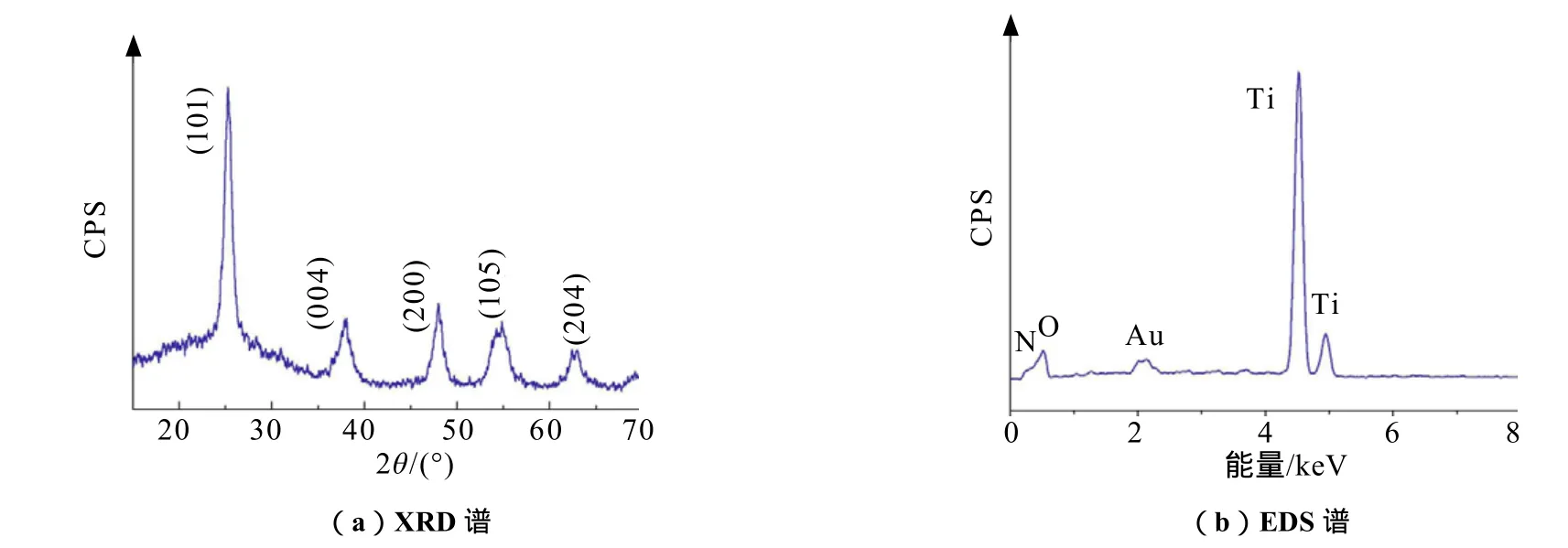
图2 多孔TiO2微胶囊的XRD谱和EDS谱Fig.2 XRD pattern(a) and EDS pattern(b) of porous TiO2capsule
2.2 氮气吸附脱吸附曲线及孔径分布曲线
由图3(a)可以看出,多孔TiO2微胶囊吸附脱附等温曲线为Ⅳ型,并具有H3型的回滞环,是典型介孔结构的吸附等温曲线;用BET法计算得到其比表面积约为100.5 m2·g-1。由图3(b)可知,TiO2微胶囊的孔径集中分布于6 nm左右,这与TEM的观察结果一致,充分表明了材料中含有大量的介孔结构。发达的孔结构能富集污染物,为TiO2的光催化提供高浓度有机环境,从而提高光催化活性,加快反应速度。
2.3 光催化性能
由图4可见,亚甲基蓝溶液在仅有H2O2而无催化剂的情况下,溶液的脱色率极低,100 min后脱色率还不到5%;P25粉对亚甲基蓝溶液的光催化活性稍好,100 min后脱色率近50%;在加入多孔TiO2微胶囊和H2O2的条件下,亚甲基蓝溶液在反的氮元素相当于在TiO2的能级中加入了一个杂质能级,使得其吸收区拓展到了可见光波长区,因此它对光的利用能力较高。加入的H2O2是有效的导带电子捕获剂,既可以有效捕获光生电子使电子和空穴分离,达到提高光量子产率的目的,又促进了超氧基及羟基自由基的生成,加速光催化反应。制备的多孔TiO2微胶囊不仅具有良好的吸附性能,还具有较高的催化活性。
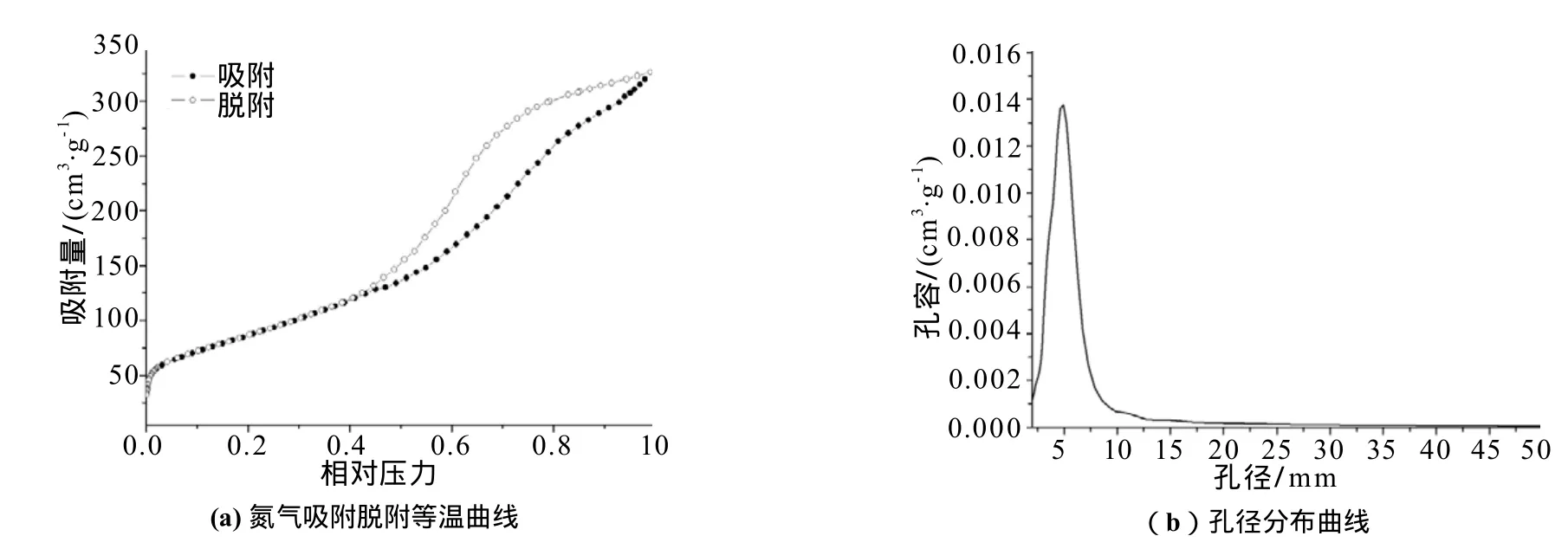
图3 多孔TiO2微胶囊的氮气吸附脱吸附等温曲线及相应的孔径分布曲线Fig.3 Nitrogen adsorption-desorption isotherms(a) and corresponding pore size distribution plot(b) of porous TiO2capsule
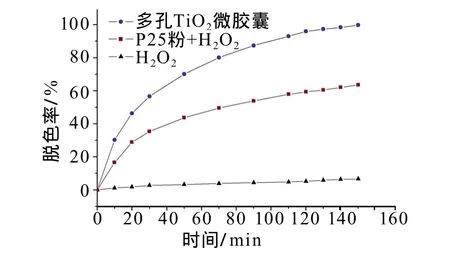
图4 不同催化剂条件下亚甲基蓝溶液的脱色率Fig.4 Decolourization ratio of methylene blue using different catalysts
从图5(a)可以看到,因为掺入氮的影响,TiO2微胶囊的吸收边发生了红移,充分说明TiO2微胶囊对可见光吸收能力增强。从图5(b)可看到,掺入氮的芯能级主要分布于400 eV。理论上N2p与O2p,C2p与O2p均存在杂化现象,当宽禁带半导体中掺杂入碳和氮等原子后,可以减小禁带宽度。氮原子掺杂分为替代型(Substitutional N doping)和间隙型掺杂(Interstitial N doping),其对应的N—O及N—N键可将价带分别提高0.14 eV和0.74 eV,这类掺杂也能显著提高半导体晶粒中氧空位的浓度,提高光催化效率,而400 eV处的XPS峰一般代表掺入的N—N键,价带发生了改变,禁带宽度缩小,因此可被能量更低、波长更长的光激发,产生光生电子,这类掺杂可促进材料漫散射谱的红移,与图5(a)的结果相符。
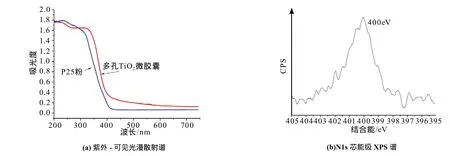
图5 多孔TiO2微胶囊和P25粉的紫外-可见光漫散射谱以及TiO2微胶囊N1s芯能级XPS谱Fig.5 UV-visible diffuse reflectance spectra of porous TiO2capsule and P25(a) and N1s core level XPS spectrum of TiO2capsule(b)
3 结 论
(1)以羽纹硅藻为模板,在四氯化钛的溶液中浸渍后于550℃下煅烧,可得到具有仿硅藻形貌的TiO2,TiO2微胶囊富含介孔结构,由晶体颗粒堆积而成,增强了捕捉光的能力。
(2)煅烧后生物体中存在的氨基酸转化为氮元素掺杂入TiO2中,等同掺入一个杂质能级,使其增强了对可见光波段的吸收,提高了可见光催化降解亚甲基蓝的能力。
[1]FAN T X,CHOW S K,ZHANG D.Biomorphic mineralization∶from biology to materials[J].Progress in Materials Science,2009,54(5):542-659.
[2]YANG D,QI L,MA J.Eggshell membrane templating of hierarchically ordered macroporous networks composed of TiO2tubes[J].Advanced Materials,2002,14(21):1543-1546.
[3]王炜,陈志刚,陈丰.以鱼鳞为模板合成仿生氧化铈及其性能[J].机械工程材料,2012,36 (12):17-20.
[4]MACEDO J S,OTUBO L,FERREIRA O P.Biomorphic activated porous carbons with complex microstructures from lignocellulosic residues[J].Microporous and Mesoporous Materials,2008,107(3):276-285.
[5]GALUSHA J W,JORGENSEN M R,BARTL M H.Diamond-structured titania photonic-bandgap crystals from biological templates[J].Advanced Materials,2010,22(1):107-110.
[6]QIAN J,CHEN F,ZHAO X.China rose petal as biotemplate to produce two-dimensional ceria nanosheets[J].Journal of Nanoparticle Research,2011,13(12):7149-7158.
[7]ZHAO K,CHANG Q,CHEN X.Synthesis and application of DNA-templated silver nanowires for ammonia gas sensing[J].Materials Science and Engineering:C,2009,29(4):1191-1195.
[8]CHOW S,FAN T,DING J.Meso/macroporous ceria with enhanced surface oxygen activity via plant-leaf mineralization[J].Journal of the American Ceramic Society,2010,93(1):40-43.
[9]LI X,FAN T,ZHOU H.Enhanced light-harvesting and photocatalytic properties in morph-TiO2from green-leaf biotemplates[J].Advanced Functional Materials,2009,19(1):45-56.
[10]COHEN-HADAR N,LAGZIEL-SIMIS S,WINE Y.Restructuring protein crystals porosity for biotemplating by chemical modification of lysine residues[J].Biotechnology and Bioengineering,2011,108(1):1-11.
[11]SHEN J,YAN B,SHI M.One step hydrothermal synthesis of TiO2-reduced graphene oxide sheets[J].Journal of Materials Chemistry,2011,21(10):3415-3421.
[12]FLAHERTY D W,DOHNÁLEK Z,DOHNÁLKOVÁ A.Reactive ballistic deposition of porous TiO2films:growth and characterization[J].The Journal of Physical Chemistry:C,2007,111(12):4765-4773.
[13]OZASA K,NEMOTO S,LI Y.Contact angle and biocompatibility of sol-gel prepared TiO2thin films for their use as semiconductor-based cell-viability sensors[J].Surface and Interface Analysis,2008,40(3/4):579-583.
[14]WANG T H,NAVARRETE-LÓ PEZ A M,LI S.Hydrolysis of TiCl4:initial steps in the production of TiO2[J].The Journal of Physical Chemistry:A,2010,114(28):7561-7570.

