多活性中心协同加氢纳米催化剂的设计和制备
朱丽华,孙菡蕾,曹志凯,郑进保,张诺伟,陈秉辉
多活性中心协同加氢纳米催化剂的设计和制备
朱丽华,孙菡蕾,曹志凯,郑进保,张诺伟,陈秉辉
(厦门大学化学化工学院,福建厦门 361005)
基于催化剂多活性中心分工协同作用可活化两种或多种反应物,本研究工作以一种新的制备策略对贵金属-过渡金属-过渡金属氧化物催化剂进行合理设计,构筑金属与金属氧化物双活性中心。结果发现,贵金属负载于过渡金属/过渡金属氧化物(NM-TM/TMO)结构的催化剂在加氢反应中具有优异的催化活性。同时,热处理方法可有效调控催化剂微观结构,并对此构效关系进行了较为深入的研究。
纳米催化剂;分工协同;加氢;构效关系
引 言
贵金属催化剂往往表现出其他金属催化剂难以达到的优异催化性能,但贵金属储量少,价格昂贵是目前贵金属催化剂的重大问题之一。因此,通过贵金属与过渡金属或载体之间的“协同作用”是降低催化剂成本并提高其催化性能的有效途径之一。
单贵金属催化剂的金属活性位与载体往往存在协同作用[1-5]。一个典型的例子是Au/TiO2催化剂,通过Au-TiO2界面与TiO2的分工协同作用实现CO高效催化氧化[1]。随着研究的深入,更多的研究者也发现其他过渡金属氧化物(TMO)作为贵金属催化剂的载体有利于催化活性的提高,这主要得益于贵金属与过渡金属氧化物之间的电子传递所带来的协同作用,如Au/ZnO[6]、Au/Fe3O4[7]、Pt/FeO[8]、Ir/FeO[9]、Pd/Fe3O4[10]、Ag/MnO[11]等催化剂。研究也表明双贵金属催化剂也常存在协同作用[12-14]。如Pt-Pd催化剂通过高指数晶面与电子结构的协同作用获得了优异的甲酸催化氧化活性[13]。为降低贵金属(NM)的用量,引入过渡金属(TM)替代部分贵金属,在大幅降低贵金属用量的同时保持甚至提高单一贵金属原有的催化活性,成为研究的热点之一,如Pt3Ni(111)在电化学氧还原反应中(ORR)的活性远高于Pt(111)[15]。
围绕NM-TM催化剂的组成、纳米结构进行可控合成,以获取高活性的催化剂,已多见报道。在此基础上,本课题组在贵金属与过渡金属氧化物之间引入过渡金属,以加氢反应为对象,通过对NM-TM/TMO催化剂的合理设计,开发了低贵金属用量、高活性及稳定性好的加氢催化剂,并可应用于多个加氢反应。
1 催化剂的设计
1.1 催化剂的设计思路
多活性位的协同效应在多相催化中扮演着重要角色。贵金属基加氢催化剂往往存在多活性中心的协同作用,如Pt、Rh、Pd与Ru基催化剂,以及双(多)金属基催化剂,如Pt-Pd[16]及Au-Pd[17]等。Han等[18]利用胍类离子液体(TMGL)将Pd纳米颗粒固定于分子筛上,通过Pd纳米颗粒、TMGL离子液体与分子筛的协同作用显著提高了其催化环己烯、己烯与环己二烯加氢的活性与稳定性。
对于更为复杂的芳烃加氢过程,实现不同活性位的协同作用则更具有挑战性。Song等[19]发现苯加氢制环己烷反应在Pd/C与氯代1-甲基-3-丁基咪唑-三氯化铝(Lewis酸离子液体)复合催化剂中进行时,氢气在Pd活性位上吸附与活化,富含电子的苯分子容易受亲电试剂进攻,因此在Lewis酸离子液体的作用下,苯容易被吸附活化。利用Pd/C与Lewis酸离子液体之间的协同作用显著地提高了其催化苯加氢性能。类似地,可认为苯分子也将较易吸附在带有正电荷的固体表面,如具有正电荷空位的p型半导体NiO,而氢气易于在贵金属如Ru上吸附与活化。
基于此,本研究以苯加氢反应为例,提出了一种多活性位分工协同作用的催化剂的设计理念(图 1)[20-21]。
以Ru、Pt、Pd、Rh等为贵金属,Ni、Cu、Fe、Co等为过渡金属,将NM纳米颗粒负载于TM/TMO催化剂上,形成新型的NM-TM/TMO催化剂。该催化剂具有优异的芳烃加氢性能,这归结于多活性中心(贵金属、过渡金属与过渡金属氧化物)的分工协同作用。其中,贵金属如Ru含量很低且粒径相对较小,将优先吸附与活化氢气;带有正电荷空穴的NiO等过渡金属氧化物有可能起着活化富含π电子的芳烃化合物作用;而过渡金属如Ni物种则可作为氢溢流作用的“桥梁”。
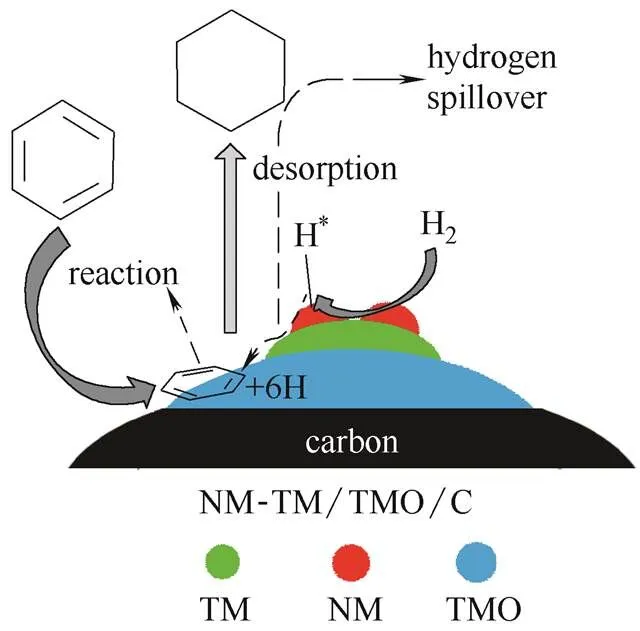
图1 新型含协同多活性中心NM-TM/TMO催化剂设计图
1.2 催化剂的制备
NM-TM/TMO/C催化剂的制备主要采用水合肼还原法及化学置换法,制备流程简述如下。过渡金属前驱体溶液在PVP保护下,与氢氧化钠反应生成过渡金属氢氧化物;同时,根据所生成过渡金属氢氧化物的解离性质,采用水合肼不断还原解离的过渡金属离子。控制过渡金属离子的还原速率,以使所还原物种可迅速被保护剂PVP所包裹,并负载于过渡金属氢氧化物;由于原溶液有添加载体如炭黑,因此,易得到TM/TMOH/C催化剂;随后,将贵金属还原在TM/TMO/C表面,经热处理,即可得NM-TM/TMO/C或NM-TM/C催化剂。图2为Ru-Ni/NiO/C与Ru-Ni/C催化剂的制备过程。
1.3 催化剂的表征
样品的XRD测试在Rigaku UltimaⅣ X射线衍射仪上进行。仪器的工作参数为:以Cu Kα为X射线源(= 0.15406 nm),工作电压为35 kV、电流为20 mA。采用荷兰FEI公司的Tecnai F30(Tecnai F20)型号和日本电子株式会社的JEOL JEM 2100F透射电子显微镜获得催化剂纳米颗粒的大小、形貌与高分辨像(HRTEM),加速电压为300 kV(200 kV)。采用Tecnai G2 F30(20)透射电子显微镜对催化剂进行高角度环形暗场扫描透射(HAADF STEM)分析及EDS元素面扫与线扫分析,加速电压为300 kV(200 kV)。催化剂的表面原子种类和组成采用高灵敏低能离子散射(high-sensitivity low-energy ion scattering spectroscopy,HS-LEIS)测试。仪器,IonTOF Qtac100。实验条件为:采用初始动能5 keV20Ne+离子束为溅射离子源,样品电流为1.6 nA。

图2 Ru-Ni/NiO/C与Ru-Ni/C催化剂的合成过程示意图[20]
2 催化剂的活性及其纳米结构
2.1 催化剂的结构表征
下面以Ru-Ni/NiO/C与Ru-Ni/C催化剂为例,介绍催化剂的结构特征。基于上述制备方法,室温下以水合肼还原法合成Ni/Ni(OH)2/C;将贵金属负载于Ni/Ni(OH)2/C表面得Ru-Ni/Ni(OH)2/C催化剂,在N2或N2+H2混合气气氛下380℃焙烧后分别得Ru-Ni/NiO/C和Ru-Ni/C催化剂。
由HRTEM表征[图3(a)]可知,Ru-Ni/NiO/C催化剂存在fcc结构的NiO(111)晶面与hcp结构的Ru(002)(晶格条纹间距分别为0.240和0.214 nm)。结果表明Ru主要是以纳米颗粒、团簇或单原子的形式存在。而Ru-Ni/C催化剂可能以Ru-Ni合金的形式存在,一个较明显的证据是金属物种的晶格条纹间距(0.210 nm)介于Ru(100)及Ni(111)之间[图3 (b)],同时发现在Ru-Ni/C催化剂中也存在着Ru/Ni相分离的结构。因此,HRTEM结果表明Ru-Ni/C主要存在Ru-Ni合金与Ru/Ni相分离纳米颗粒。
为了确定催化剂最表层的原子种类和组成,采用Ne+为溅射源对样品进行低能离子散射(HS-LEIS)测试,结果如图4所示。由图可知,在Ru-Ni/NiO/C催化剂中Ru主要在催化剂的最表层;同时,最表层也有少量Ni的信号峰,这表明Ru可能是以小岛状的形式负载于Ni/NiO纳米颗粒上,但未完全包裹住Ni/NiO纳米颗粒。

图3 Ru-Ni/NiO/C (a)和Ru-Ni/C (b)催化剂的HRTEM图[20]

图4 Ru-Ni/NiO/C催化剂的5 keV20Ne+低能离子散射谱图[20]
因此,结合以上表征结果可知,Ru-Ni/NiO/C催化剂中Ru将主要以小岛的形式负载于Ni/NiO纳米颗粒上,而Ru-Ni/C催化剂主要以Ru-Ni合金和Ru/Ni相分离的形式存在。
2.2 Ru-Ni/NiO/C催化剂的芳烃加氢活性
上述所制催化剂的苯加氢制环己烷性能如表1所示。Ru-Ni/NiO/C(Ru质量分数1.25%、总Ni质量分数1.40%)催化剂对环己烷的产率为100%,TOF(转化频率)高达18210.3 h-1,为Ru-Ni/C催化剂的55倍(TOF327.8 h-1)。而Ru-Ni/Ni(OH)2/C催化剂的活性很低(TOF25.4 h-1),原因是催化剂未经焙烧,未分解的PVP阻止了反应物扩散到催化剂表面。为了与Ru-Ni/NiO/C催化剂性能形成对比,分别评价了Ru/C和Ni/NiO/C催化剂催化苯加氢制环己烷性能,结果为:Ru/C的TOF为1706.0 h-1,环己烷产率为9.4%;Ni/NiO/C催化剂和碳载体在相同反应条件下,基本没有任何催化活性。
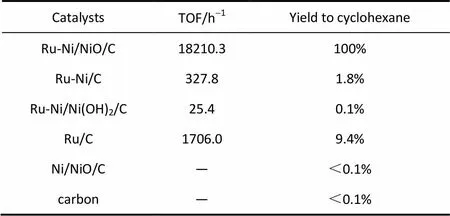
表1 各催化剂催化苯加氢制环己烷性能[20]
Note: Reaction conditions, benzene 10 ml, H2pressure 5.3 MPa; reaction time, 1 h; reaction temperature, 60℃.
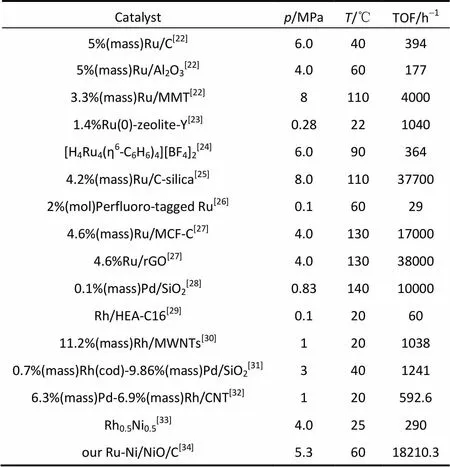
表2 其他文献中非负载型与负载型金属催化剂催化苯加氢制环己烷性能[20]
此外,与现有文献所报道的负载型及非负载型Ru基、Pd基、Rh基或双金属催化剂相比,本研究中的Ru-Ni/NiO/C催化剂在相似反应条件下具有更优越的苯加氢性能(表2)。
Ru-Ni/NiO/C催化剂具有优异催化活性,这与其所特有的纳米结构密切相关。小岛状Ru纳米颗粒负载于Ni/NiO纳米颗粒有利于实现多活性位的分工协同作用。尺寸较小的Ru纳米颗粒优先活化氢气,与之相邻的Ni物种可传输所活化的氢物种;而与Ni紧挨的NiO物种一般带有正电荷,这将有利于活化芳烃,最终已活化的H物种使芳烃加氢生成烷烃。而Ru-Ni/C与Ru/C催化剂不存在这种多活性位的分工协同作用,相应地,其催化芳烃加氢性能相对较低。此外,根据本组之前工作,Ru-Ni双金属催化剂在苯加氢反应中具有较高的稳定性[35-36]。
Ru-Ni/NiO/C催化剂也可应用于甲苯、对二甲苯等其他芳烃加氢的反应,结果见表3, Ru-Ni/NiO/C催化剂在温和反应条件下(反应温度30℃与反应压力5.3 MPa)仍具有较高的加氢性能。这说明Ru-Ni/NiO/C催化剂可适用于多种芳烃化合物的加氢反应。

表3 低温下Ru-Ni/NiO/C催化剂对其他芳烃的加氢性能
① Yield to methyl cyclohexane.② Yield to dimethylcyclohexane.
Note: Reaction conditions, substrate 10 ml, H2pressure 5.3 MPa; reaction temperature, 30℃; catalyst, 0.05 g.
2.3 其他NM-TM/TMO/C催化剂的加氢性能
应用上述同样的设计方法,以Pd、Rh、Pt等替代Ru,或者以Co替代Ni,制备了一系列相应的催化剂。催化活性见表4,在一定的反应条件下,Pd-Ni/NiO/C、Rh-Ni/NiO/C、Pt-Ni/NiO/C及Ru-Co/ Co3O4/C催化剂的苯加氢制环己烷的TOF分别为2606.7、4071.8、3022.1及91051 h-1,均(远)高于其相应的Pd-Ni/C、Rh-Ni/C、Pt-Ni/C与Ru-Co/C催化剂性能。总之,NM-TM/TMO/C催化剂催化苯加氢制环己烷的性能高于NM-TM/C,这归因于NM、TM与TMO的分工协同作用,侧面说明了TMO的重要性。同时说明本研究中催化剂设计与制备方法可用于其他贵金属-过渡金属催化剂体系中。
3 催化剂的结构调控及其活性
大量研究表明,双金属催化剂结构对其性能有着重要的影响[37]。为了提高双金属催化剂的活性、选择性与稳定性,众多科研工作者设计并制备了各种不同结构的催化剂(如合金、核壳或颗粒负载于颗粒结构等),如Enache等[37]合成了Au-Pd合金负载于TiO2的纳米催化剂,该催化剂在醇选择性氧化制醛的反应中比单金属催化剂具有非常优异的活性。
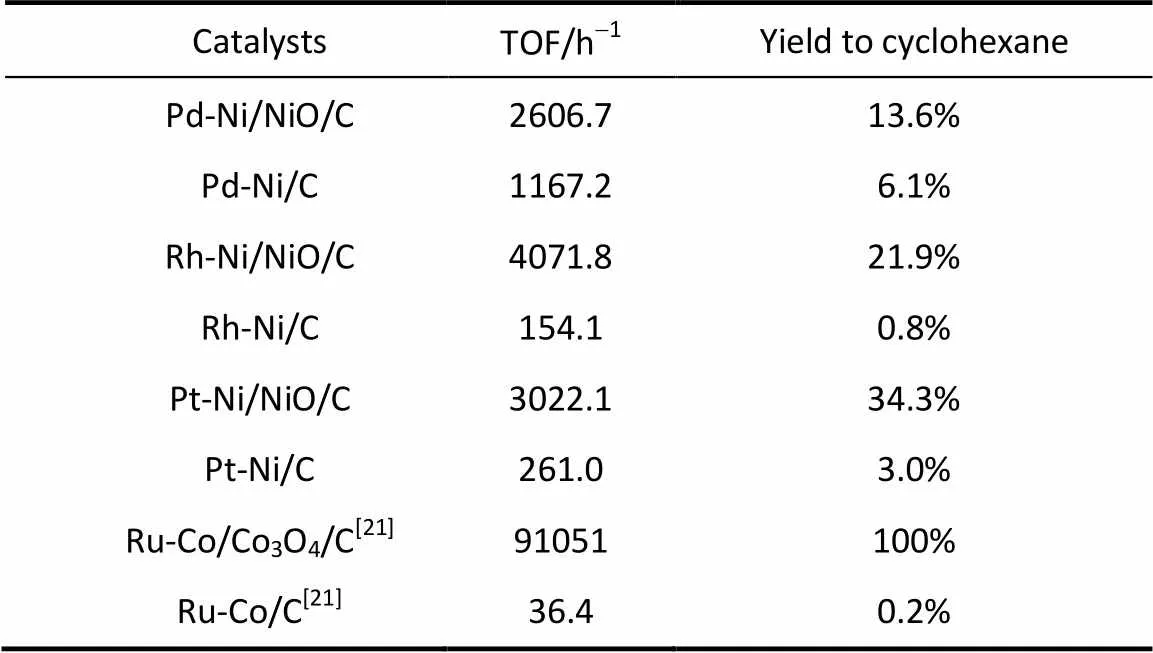
表4 NM-TM/TMO/C与NM-TM/C催化剂催化苯加氢制环己烷性能
Note: Reaction conditions: reaction pressure, 5.3 MPa H2; catalyst, 0.05 g; reaction temperature, 60℃; reaction time, 1 h; benzene, 10 ml.
合成不同纳米结构的Ru-Ni纳米颗粒已有报道,如Chen等[38]采用种子生长法成功制备了具有双功能磁性Ni@Ru核壳结构纳米颗粒,并用于氨硼烷氢解反应,其催化性能高于单金属Ni或Ru催化剂。另外,该研究小组又采用溶胶化学合成法制备了Ru-Ni合金纳米颗粒,同样是较好的氨硼烷氢解制氢催化剂[39]。Li等[40]采用CTAB为导向剂自组装合成了Ru-Ni双金属催化剂,并用于乙酰丙酮加氢反应。而本文重点阐述Ru-Ni纳米结构的演变规律及其与催化性能之间的内在关系[35]。
3.1 催化剂的结构调控
以Ru0.04Ni0.96/C(Ru质量分数1.25%、总Ni质量分数15.57%)为催化剂,Ru0.04Ni0.96/C催化剂前驱体Ru-Ni/Ni(OH)2/C在N2+H2中经不同热处理条件可调控Ru0.04Ni0.96催化剂纳米结构-Ru-Ni合金、小岛状Ru负载于Ni纳米颗粒与Ru@Ni核壳结构-壳较厚[35]。催化剂的XRD表征结果如图5所示,从图中可知,Ru-Ni/Ni(OH)2/C催化剂经230或280℃处理后,Ni(100)、Ni(200)的衍射峰均发生左移,表明Ru原子融入Ni晶格中形成了Ru-Ni键(Ru-Ni合金),导致晶格膨胀。随着处理温度继续升高至380℃,微弱的Ru(100)晶面特征衍射峰出现。当处理温度为480℃时,Ru与Ni金属衍射峰强度增强。焙烧温度继续升高(580或680℃),Ni与Ru的特征衍射峰均向较低的2方向移动,表明高温处理易导致晶格膨胀[41];且随着催化剂焙烧温度的升高,各衍射峰的强度增强,半峰宽减小,表明热处理温度的升高使得Ru-Ni双金属纳米颗粒的结晶度变好,尺寸变大。
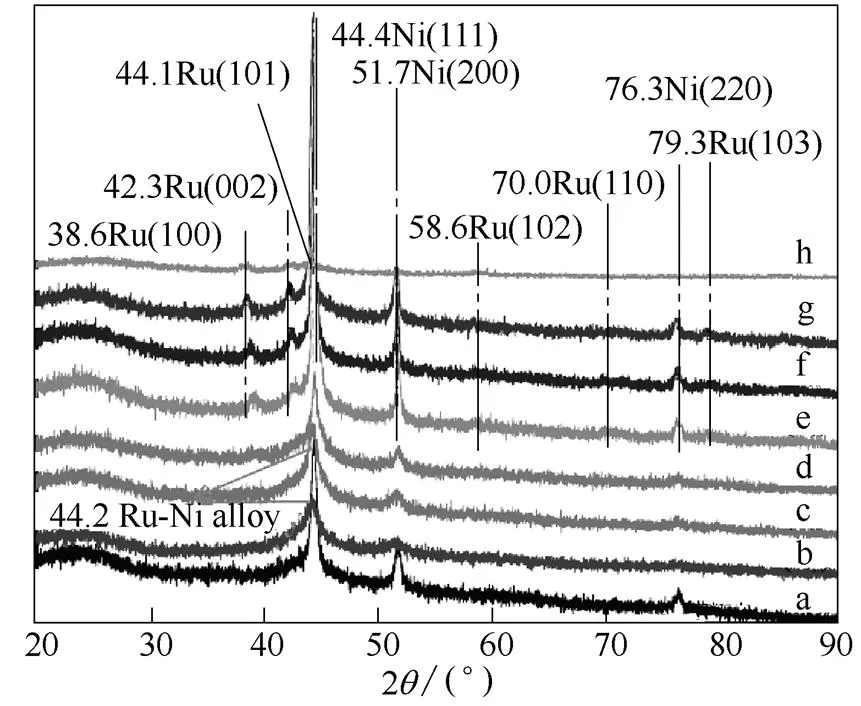
图5 Ru-Ni/Ni(OH)2/C催化剂不同温度热处理后的XRD图[35]
(a) 16.84%Ni/C pretreated at 380℃, Ru-Ni/Ni(OH)2/C pretreated at (b) 230℃, (c) 280℃, (d) 380℃, (e) 480℃, (f) 580℃, (g) 680℃,(h) 2.5%Ru/C pretreated at 600℃
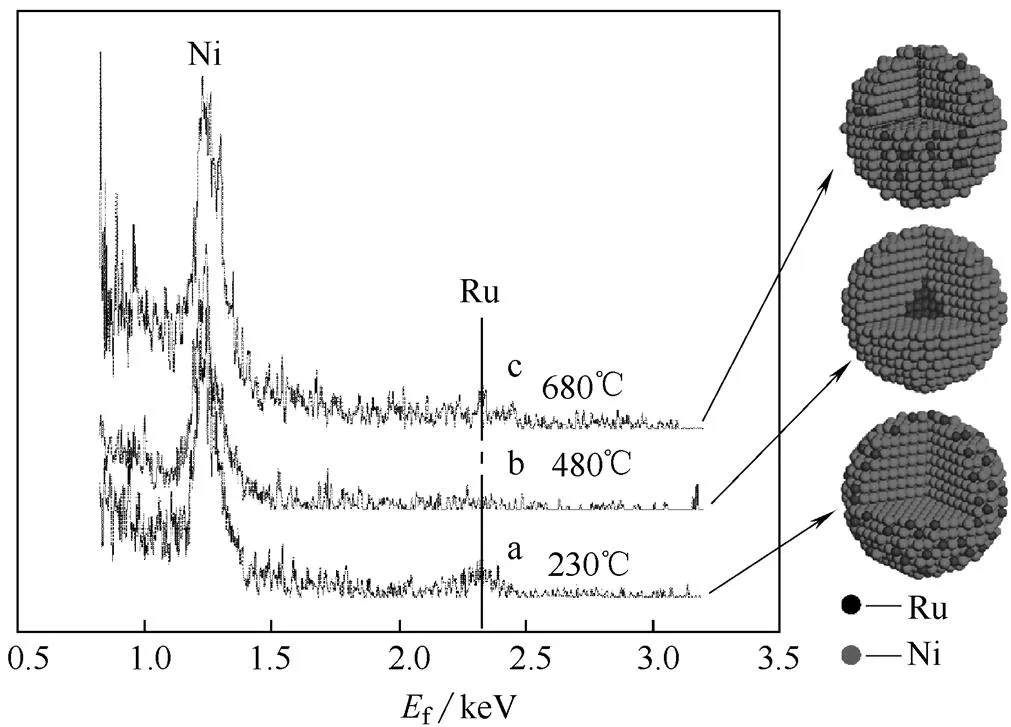
图6 Ru-Ni/Ni(OH)2/C催化剂经不同温度热处理后的HS-LEIS图[35]
为了研究催化剂最表层的原子种类和组成,采用Ne+为溅射源对样品进行了低能离子散射(HS-LEIS)测试,结果如图6所示。从图中可知,Ru0.04Ni0.96/C-230催化剂表面Ru与Ni原子同时存在,结合其XRD结果可知,该催化剂中Ru0.04Ni0.96纳米合金颗粒;Ru0.04Ni0.96/C-480催化剂的最表层仅有Ni原子,且其XRD结果表明Ru与Ni发生相分离,说明Ru0.04Ni0.96纳米颗粒可能为Ru@Ni核壳结构;Ru0.04Ni0.96/C-680的HS-LEIS谱图[图6 (c)]显示催化剂的最表层同时存在Ru与Ni原子,结合其XRD结果可认为小岛状Ru纳米颗粒负载于Ni纳米颗粒。
3.2 催化剂的活性
催化活性的测试结果(图7)表明Ru0.04Ni0.96/C催化剂在N2+H2中的热处理温度影响着其催化苯加氢制环己烷性能。Ru0.04Ni0.96/C-230催化剂对环己烷的产率为9.25%,活性相对较高,TOF约为Ru0.04Ni0.96/C-480催化剂的18倍。同样地,Ru0.04Ni0.96/C-680催化剂具有相对较高的活性,但仍比Ru0.04Ni0.96/C-230催化剂低,其环己烷的收率为6.77%。从以上结果可知,Ru0.04Ni0.96/C-催化剂催化苯加氢制环己烷活性顺序为:Ru0.04Ni0.96/C-230(Ru-Ni合金)>Ru0.04Ni0.96/C-680(小岛状Ru负载于Ni纳米颗粒)Ru0.04Ni0.96/C-480(Ru@Ni核壳结构-壳较厚)。
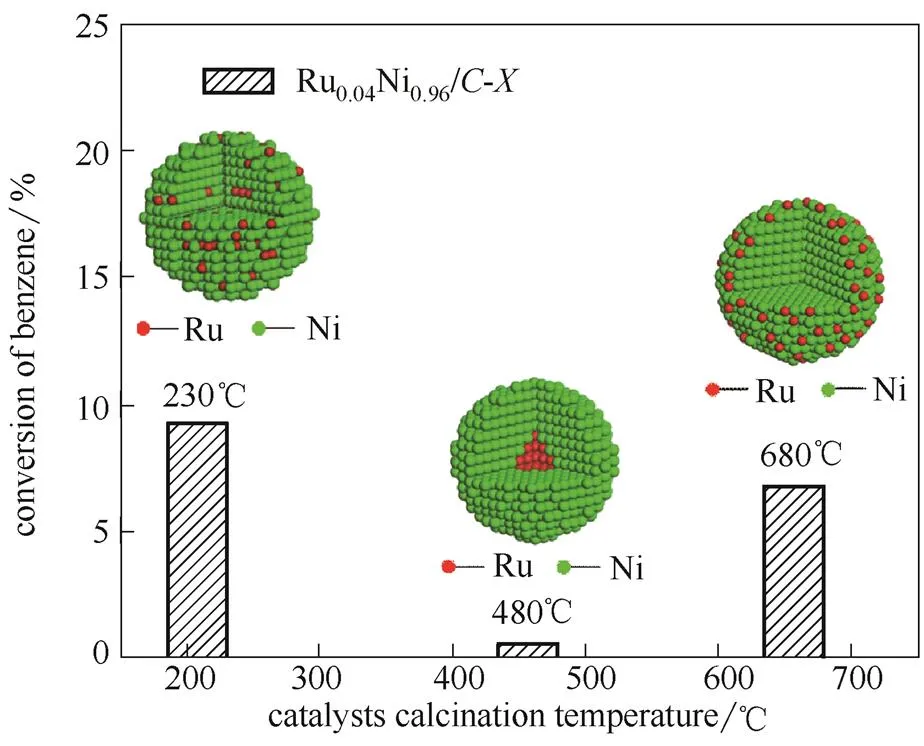
图7 Ru0.04Ni0.96/C催化剂的催化苯加氢制环己烷性能[35]
因此,综上所述,不同的热处理条件可调控Ru0.04Ni0.96/C-催化剂金属颗粒的纳米结构,并进一步决定其催化性能。
4 结 论
针对特定的催化反应科学设计催化剂是值得挑战的难题。基于催化剂多活性中心的分工协同作用,本研究合理设计了用于加氢反应的贵金属-过渡金属-过渡金属氧化物(NM-TM/TMO)催化剂,通过XRD、HRTEM、HS-LEIS等表征手段,证实了具有优异加氢活性的NM-TM/TMO催化剂原因是:较小尺寸的贵金属颗粒有利于活化氢气,且过渡金属可作为氢溢流作用的媒介;而芳香化合物可在具有空穴的NiO等过渡金属氧化物上实现活化。该催化剂设计理念可拓展至其他反应。同时,研究还发现,在不同热处理条件下可实现双金属催化剂的纳米结构的有效调控并影响其催化性能,从而建立催化剂的“构效关系”。
[1] Green I X, Tang W, Neurock M, Yates Jr J T. Spectroscopic observation of dual catalytic sites during oxidation of CO on a Au/TiO2catalyst [J]., 2011, 333 (6043): 736-739.
[2] Li H, Bian Z F, Zhu J, Huo Y, Li H, Lu Y F. Mesoporous Au/TiO2nanocomposites with enhanced photocatalytic activity [J]....., 2007, 129 (15): 4538-4539.
[3] Fujitani T, Nakamura I. Mechanism and active sites of the oxidation of CO over Au/TiO2[J]....., 2011, 50 (43): 10144-10147.
[4] Bennett R A, Stone P, Bowker M. Pd nanoparticle enhanced re-oxidation of non-stoichiometric TiO2: STM imaging of spillover and a new form of SMSI [J]..., 1999, 59 (2/4): 99-105.
[5] Baker L R, Kennedy G, Van Spronsen M, Kennedy G, Spronsen M V, Hervier A, Cai X, Chen S, Wang L L, Somorjai G A. Furfuraldehyde hydrogenation on titanium oxide-supported platinum nanoparticles studied by sum frequency generation vibrational spectroscopy: acid-base catalysis explains the molecular origin of strong metal-support interactions [J]....., 2012, 134 (34): 14208-14216.
[6] Li P, Wei Z, Wu T, Peng Q, Li Y. Au-ZnO hybrid nanopyramids and their photocatalytic properties [J]....., 2011, 133 (15): 5660-5663.
[7] Wang C, Yin H, Dai S, Sun S. A general approach to noble metal-metal oxide dumbbell nanoparticles and their catalytic application for CO oxidation [J]..., 2010, 22 (10): 3277-3282.
[8] Qiao B, Wang A, Yang X, Allard L F, Jiang Z, Cui Y, Liu J, Li J, Zhang T. Single-atom catalysis of CO oxidation using Pt/FeO[J]..., 2011, 3 (8): 634-641.
[9] Lin J, Wang A, Qiao B, Liu X, Yang X, Wang X, Liang J, Li J, Liu J, Zhang T. Remarkable performance of Ir/FeOsingle-atom catalyst in water gas shift reaction [J]....., 2013, 135 (41): 15314-15317.
[10] Chen S, Si R, Taylor E, Janzen J, Chen J. Synthesis of Pd/Fe3O4hybrid nanocatalysts with controllable interface and enhanced catalytic activities for CO oxidation [J]...., 2012, 116 (23): 12969-12976.
[11] Huang Z, Gu X, Cao Q, Hu P, Hao J, Li J, Tang X. Catalytically active single-atom sites fabricated from silver particles [J]....., 2012, 51 (17): 4198-4203.
[12] Deng Y J, Tian N, Zhou Z Y, Huang R, Liu Z L, Xiao J, Sun S G. Alloy tetrahexahedral Pd-Pt catalysts: enhancing significantly the catalytic activity by synergy effect of high-index facets and electronic structure [J]..., 2012, 3: 1157-1161.
[13] Wang A Q, Liu X Y, Mou C Y, Zhang T. Understanding the synergistic effects of gold bimetallic catalysts [J]..., 2013, 308: 258-271.
[14] Liu X, Liu M H, Luo Y C, Mou C Y, Lin S D, Cheng H, Chen J M, Lee J F, Lin T S. Strong metal-support interactions between gold nanoparticles and ZnO nanorods in CO oxidation [J]....., 2012, 134 (24): 10251-10258.
[15] Stamenkovic V R, Fowler B, Mun B S, Wang G, Ross P N, Lucas C A, Markovic N M. Improved oxygen reduction activity on Pt3Ni (111)increased surface site availability [J]., 2007, 315 (5811): 493-497.
[16] Pawelec B, La Parola V, Navarro R M, Murcia-Mascarós S, Fierro J L G. On the origin of the high performance of MWNT-supported PtPd catalysts for the hydrogenation of aromatics [J]., 2006, 44 (1): 84-98.
[17] Venezia A M, Parola V L, Pawelec B, Fierro J L G. Hydrogenation of aromatics over Au-Pd/SiO2-Al2O3catalysts: support acidity effect [J]...:., 2004, 264 (1): 43-51.
[18] Huang J, Jiang T, Gao H, Han B, Liu Z, Wu W, Chang Y, Zhao G. Pd nanoparticles immobilized on molecular sieves by ionic liquids: heterogeneous catalysts for solvent-free hydrogenation [J]....., 2004, 43 (11): 1397-1399.
[19] Deshmukh R R, Lee J W, Shin U S, Lee J Y, Song C E. Hydrogenation of arenes by dual activation: reduction of substrates ranging from benzene to C60fullerene under ambient conditions [J]....., 2008, 47 (45): 8615-8617.
[20] Zhu L, Jiang Y, Zheng J, Zhang N, Yu C, Li Y, Pao C W, Chen J L, Jin C, Lee J F, Zhong C J, Chen B H. Ultrafine nanoparticle-supported Ru-nanoclusters with ultrahigh catalytic activity [J].,2015. DOI: 10.1002/smll.201500654.
[21] Zhu L, Yang Z, Zheng J, Hu W, Zhang N, Li Y, Zhong C J, Ye H, Chen B H. Decoration of Co/Co3O4nanoparticles with Ru nanoclusters: a new strategy for design of highly-active hydrogenation [J]...., 2015, 3 (22): 124-132. DOI: 10.1039/C5TA02452H.
[22] Miao S, Liu Z, Han B, Huang J, Sun Z, Zhang J, Jiang T. Ru nanoparticles immobilized on montmorillonite by ionic liquids: a highly efficient heterogeneous catalyst for the hydrogenation of benzene [J]....., 2006, 45 (2): 266-269.
[23] Zahmakiran M, Özkar S. Intrazeolite ruthenium(0) nanoclusters: a superb catalyst for the hydrogenation of benzene and the hydrolysis of sodium borohydride [J]., 2008, 24 (14): 7065-7067.
[24] Dyson P J, Ellis D J, Welton T, Thomas W. Arene hydrogenation in a room-temperature ionic liquid using a ruthenium cluster catalyst [J]..., 1999, (1): 25-26.
[25] Su F, Lv L, Lee F Y, Liu T, Cooper A I, Zhao X S. Thermally reduced ruthenium nanoparticles as a highly active heterogeneous catalyst for hydrogenation of monoaromatics [J]....., 2007, 129 (46): 14213-14223.
[26] Niembro S, Donnici S, Shafir A, Vallribera A, Buil M L, Esteruelas M A, Larramona L. Perfluoro-tagged rhodium and ruthenium nanoparticles immobilized on silica gel as highly active catalysts for hydrogenation of arenes under mild conditions [J]..., 2013, 37 (2): 278-282.
[27] Yao K X, Liu X, Li Z,Li C C, Zeng H C, Han Y. Preparation of a Ru-nanoparticles/defective-graphene composite as a highly efficient arene-hydrogenation catalyst [J]., 2012, 4 (12): 1938-1942.
[28] Domínguez-Quintero O, Martínez S, Henríquez Y, D’Ornelas L, Krentzien H, Osuna J. Silica-supported palladium nanoparticles show remarkable hydrogenation catalytic activity [J]....:., 2003, 197 (1/2): 185-191.
[29] Schulz J, Roucoux A, Patin H. Stabilized rhodium(0) nanoparticles: a reusable hydrogenation catalyst for arene derivatives in a biphasic water-liquid system [J]...., 2000, 6 (4): 618-624.
[30] Pan H B, Wai C M. Sonochemical one-pot synthesis of carbon nanotube-supported rhodium nanoparticles for room-temperature hydrogenation of arenes [J]...., 2009, 113 (46): 19782-19788.
[31] Barbaro P, Bianchini C, Dal Santo V, Meli A, Moneti S, Pirovano C, Psaro R, Sordelli L, Vizza F. Benzene hydrogenation by silica-supported catalysts made of palladium nanoparticles and electrostatically immobilized rhodium single sites [J]., 2008, 27 (12): 2809-2824.
[32] Yoon B, Pan H B, Wai C M. Relative catalytic activities of carbon nanotube-supported metallic nanoparticles for room-temperature hydrogenation of benzene [J]...., 2009, 113 (4): 1520-1525.
[33] Duan H, Wang D, Kou Y, Li Y. Rhodium-nickel bimetallic nanocatalysts: high performance of room-temperature hydrogenation [J]..., 2013, 49 (3): 303-305.
[34] Zhu L, Sun H, Fu H, Zheng J, Zhang N, Li Y, Chen B H. Effect of ruthenium nickel bimetallic composition on the catalytic performance for benzene hydrogenation to cyclohexane [J]....., 2015, 499 (25): 124-132. DOI: 10.1016/j.apcata.2015.04.016.
[35] Zhu L, Cao M, Li L, Tang Y, Zhang N, Zheng J, Zhou H, Li Y, Yang L, Zhong C J, Chen B H. Synthesis of different ruthenium nickel bimetallic nanostructures and an investigation of the structure-activity relationship for benzene hydrogenation to cyclohexane [J]., 2014, 6 (7): 2039-2046.
[36] Zhu L, Zheng L, Du K, Fu H, Li Y, You G, Chen B H. An efficient and stable Ru-Ni/C nano-bimetallic catalyst with a comparatively low Ru loading for benzene hydrogenation under mild reaction conditions [J].., 2013, 3 (3): 713-719.
[37] Enache D I, Edwards J K, Landon P, Solsona-Espriu B, Carley A F, Herzing A A, Watanabe M, Kiely C J, Knight D W, Hutchings G J. Solvent-free oxidation of primary alcohols to aldehydes using Au-Pd/TiO2catalysts [J]., 2006, 311 (5759): 362-365.
[38] Chen G, Desinan S, Nechache R, Rosei R, Rosei F, Ma D. Bifunctional catalytic/magnetic Ni@Ru core-shell nanoparticles [J]..., 2011, 47 (22): 6308-6310.
[39] Chen G, Desinan S, Rosei R, Rosei F, Ma D. Synthesis of Ni-Ru alloy nanoparticles and their high catalytic activity in dehydrogenation of ammonia borane [J]...., 2012, 18 (25): 7925-7930.
[40] Yang Y, Gao G, Zhang X, Li F. Facile fabrication of composition- tuned Ru-Ni bimetallics in ordered mesoporous carbon for levulinic acid hydrogenation [J].., 2014,4 (5): 1419-1425.
[41] Solliard C, Flueli M. Surface stress and size effect on the lattice parameter in small particles of gold and platinum [J]..., 1985, 156 (1): 487-494.
Design and synthesis of hydrogenation nanocatalyst with synergetic multiple catalytic sites
ZHU Lihua, SUN Hanlei, CAO Zhikai, ZHENG Jinbao, ZHANG Nuowei, CHEN Binghui
Department of Chemical and Biochemical EngineeringCollege of Chemistry and Chemical EngineeringXiamen UniversityXiamenFujianChina
As synergic multiple active sites catalysts can theoretically activate two or more reactant or substrates simultaneously resulting in significantly increase of activity and stability of catalysts, we herein develop a novel catalysts preparation strategy to design and construct noble metal-transition metal-transition metal oxide (NM-TM/TMO) to form bi-active catalytic sites. The experimental results show that such a catalyst has excellent performance in catalytic hydrogenation,.. aromatic compounds hydrogenation as the case studies. It was also found that the nanostructure of catalyst can be tunedthermal treatments, which are investigated and the relationship between structure and activity is explored to some extent.
nanocatalyst; synergistic; hydrogenation; relationship of nanostructure-activity
2015-05-26.
Prof.CHEN Binghui, chenbh@xmu.edu.cn
10.11949/j.issn.0438-1157.20150702
O 643.38
A
0438—1157(2015)08—3091—07
陈秉辉。
朱丽华(1987—),男,博士研究生。
国家自然科学基金项目(20973140,201106118,21303140)。
2015-05-26收到初稿,2015-06-10收到修改稿。
supported by the National Natural Science Foundation of China (20973140, 201106118, 21303140).
——庆祝中国共产党成立一百周年贵金属纪念币展

