基于PARAFAC分析的二级出水DOM臭氧化特性研究
金 鑫,金鹏康,孔 茜,白 雪,王晓昌
(西安建筑科技大学环境与市政工程学院,陕西 西安 710055)
基于PARAFAC分析的二级出水DOM臭氧化特性研究
金 鑫,金鹏康*,孔 茜,白 雪,王晓昌
(西安建筑科技大学环境与市政工程学院,陕西 西安 710055)
基于三维荧光平行因子分析(PARAFAC analysis),对污水处理厂二级出水溶解性有机物(DOM)在不同臭氧投加量下的反应特性进行了研究,PARAFAC分析确定了污水厂二级出水中共有3个荧光组分,其中组分1为蛋白质类物质,组分2和3为腐殖质类物质.当臭氧为0.98mgO3/mgTOC时,3个组分中的荧光基团均可以和臭氧发生比较彻底的反应.线性回归分析表明,臭氧与组分1和组分2中荧光基团的反应可以很好地解释臭氧化对色度、UV254、UV280的去除.HPLC-SEC的结果进一步验证了PARAFAC的分析结果.同时,对于蛋白类物质组分1而言,臭氧主要和其中小分子物质的荧光基团发生反应,与其大分子物质几乎不发生反应.
二级出水;臭氧氧化;平行因子分析;荧光特性
二级出水(污水处理厂二沉池出水)中溶解性有机物(DOM)含有一定量的腐殖质类,蛋白质类等物质[1],这类有机物的存在对后续深度处理工艺会造成一定的影响,如导致膜过滤工艺中膜污染和消毒过程中消毒副产物的生成[2-3],因此需对这一类物质进行处理,使其性质发生改变,降低其对后续处理工艺的影响.通常情况下,臭氧氧化被用于水中有机物的性质改变,改善后续处理工艺的处理效果.
目前,对于二级出水溶解性有机物臭氧特性评价的研究手段多种多样,其中三维荧光光谱在近些年来被广泛应用于溶解性有机物的定性分析上[4].由于溶解性有机物的三维荧光图谱(EEM)通常是由若干相互叠加的荧光团组成,传统的识谱方法并不可靠,有些峰可能无法识别[5].利用平行因子分析法(PARAFAC)对EEM图谱进行分析可以解决传统识谱方法的问题,该方法最大的优点是它的分解具有唯一性.在PARAFAC分解过程中,只要选择正确的因子数而且信噪比合适,分解的结果便可以反应真实的谱图[6].
本文通过PARAFAC分析对西安市某污水处理厂二级出水臭氧化前后的EEM图谱进行了分析,同时采用凝胶排阻色谱法(HPLC-SEC)对臭氧化前后EEM图谱中的不同组分进行了分析,探究不同臭氧投加量下臭氧与污水厂二级出水溶解性有机物的反应特性.
1 材料与方法
1.1 污水处理厂二级出水及其臭氧化
实验所用水样取自西安市某污水处理厂二沉池出水,该污水处理厂进水主要来自城市生活污水,采用A2O处理工艺,出水水质特征如表1所示.本研究采用图1所示装置进行二级出水的臭氧化,该装置主体反应器有效体积为1.5L,臭氧发生器(南京沃环,WH-S-B2)出口流量通过气体流量计调节控制在40L/h,未反应的气体通入20%KI进行吸收.整个反应装置通过水浴调节使得反应温度在15℃,反应结束时,利用氮气将未反应的臭氧进行吹脱,该臭氧系统通过调节不同的反应时间来实现臭氧投加量的调节.

图1 臭氧化反应系统Fig.1 The setup of ozonation system
1.2 分析方法
1.2.1 样品预处理 污水处理厂沉淀池出水及臭氧化后的水样在进行进一步分析前均需进行0.45μm滤膜过滤处理,样品的后续分析均使用3~5个平行样.
1.2.2 臭氧投加量的确定 进入反应器和未反应的臭氧含量通过碘量法进行测定,臭氧投加量为系统输入和未反应臭氧差值与水样TOC的比值,单位为mgO3/mgTOC,通过对反应时间的调节,本研究确定了3个不同的臭氧投加量,即0.45,0.98,2.15mgO3/mgTOC.
1.2.3 有机物浓度测定 对水样用硫酸酸化至pH<3并用氮气吹脱3min,随后水样采用岛津公司生产的TOC-V CPH型总有机碳分析仪测定TOC含量.
1.2.4 UV254,UV280及SUVA测定 采用北京谱析通用仪器有限责任公司生产的TU-1901双光束紫外可见分光光度计测定UV254,UV280及SUVA(单位浓度TOC的紫外吸光度值).
1.2.5 色度的测定 色度的测定采用分光光度铂钴比色法[7].
1.2.6 三维荧光光谱 采用日本JASCO公司生产的FP6500型荧光分光光度计,对臭氧化前后样品进行分析.如表1所示,所有样品UV254均小于0.3cm-1,因此没有内滤效应[8],所有样品可不用稀释直接进行三维荧光分析.激发波长范围为220~480nm,发射波长范围为280~550nm.激发和发射扫描间隔分别为5nm和2nm,扫描速度为2000nm/min.
1.2.7 PARAFAC模型分析 PARAFAC模型分析采用MATLAB R2010a中的DOMFluor 工具箱[9],该工具箱首先将检测样本中的异常值去除,随后进行数据导入,三维荧光图谱中拉曼及瑞丽散射的去除.工具箱程序将通过一分为二法及残差分析法对样本进行2~7个组分的模型模拟,最终确定适用于该样本的正确组分数,完成PARAFAC模型的建立.
PARAFAC分析将一个三维数据矩阵 X 分解为得分矩阵 A,载荷矩阵 B 和C.分解模型如方程(1)所示:
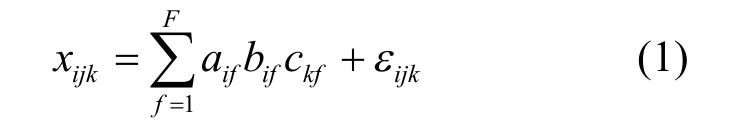
平行因子模型解析三维荧光谱图时,公式中xijk是第 i 个样品在第 j 个发射波长,第 k 个激发波长处的荧光强度值;F 代表因子数,表示有实际贡献的独立荧光成分数,也就是荧光图谱的实际组分数;aif,bjf,ckf分别为载荷矩阵A,B,C中的元素,分别代表荧光组分浓度,发射光谱和激发光谱;εijk为三线性模型用于最小化模型中的残差的平方和.在经典 PARAFAC 算法中,使用交替最小二乘法(ALS)来实现三线性模型的分解.分解的目标是使损失函数即残差矩阵中元素的平方和(RSS)达到最小.平行因子分析的分解是唯一的,成功的解决了由于组分间化学结构相似导致的组分难辨别的问题[10].
1.2.8 HPLC-SEC分子量分布分析 HPLCSEC分析由岛津公司生产的LC-2010AHF型高效液相色谱测定,采用荧光检测器,检测波长分别设置为Ex/Em290/376,Ex/Em350/424nm和Ex/Em400/476nm,色谱柱为Zenix SEC-100凝胶色谱柱,流动相为150mM PBS缓冲溶液,流速0.8mL/min.
2 结果与讨论
2.1 臭氧化前后二级出水水质特性
由表1可以看出,臭氧在3个臭氧投加量下对TOC的去除均非常有限,氧化前后TOC变化不大,臭氧化后UV254和UV280均有了明显去除,且随着臭氧投加量的增加UV254和UV280的值逐渐降低.同时,臭氧化后二级出水的色度也随着投加量的增加而逐渐降低,当投加量为0.98mgO3/mgTOC时,色度的去除率已经达到75%左右,体现了臭氧良好的脱色性能.SUVA是水样UV254与TOC的比值,是表示水中有机物的共轭不饱和及芳香程度的指标,SUVA值越大,说明水中有机物不饱和键含量越高,芳香性越强.表1的结果表明,臭氧化后SUVA随投加量的升高逐渐降低,经过臭氧化后有机物的不饱性和及芳香程度得以降低,臭氧起到了改变有机物结构的作用,而二级出水中的生色物质正是一些不饱和且具有较高芳香程度的有机物,因此SUVA的降低就可以解释臭氧化后水中色度的降低.

表1 二级出水臭氧化前后水质特性Table 1 The water quality variation before and after ozonation
2.2 臭氧化前后三维荧光EEM谱图
由图2可以看出,原水中主要存在2个峰,分别为Ex/Em225/340nm (峰A)和Ex/Em350/440nm(峰B).经过臭氧化后,这2个峰的峰强明显减弱,在低臭氧投加量下(0.45mgO3/mgTOC),臭氧与二级出水中有机物的荧光基团发生了反应,破坏了荧光基团的结构,当投加量为0.98mgO3/mgTOC时,峰B消失,当投加量为2.15mgO3/mgTOC时,峰A的位置发生蓝移,这可能是因为在臭氧投加量较大时,二级出水中有机物中苯环及共轭键的数量减少,所以其峰A产生了一定程度的蓝移[11].

图2 二级出水臭氧化前后EEM图谱Fig.2 The EEM spectra of raw water before and after ozonation in three different ozone dosages
2.3 三维荧光PARAFAC分析
2.3.1 样品荧光组分的确定 通过一分为二分析及残差分析[9],样品中荧光组分数得以确定.由图3可以看出,当组分数为3时,即公式(1)中的F值为3时,其残差平方和明显小于组分为1和2时的残差平方和,而当组分数大于3时,其残差平方和与组分数为3时变化不大,因此确定该PARAFAC模型的因子数为3.
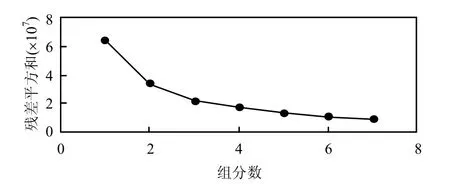
图3 PARAFAC分析残差平方和分析Fig.3 Residual sum of square analysis for PARAFAC analysis
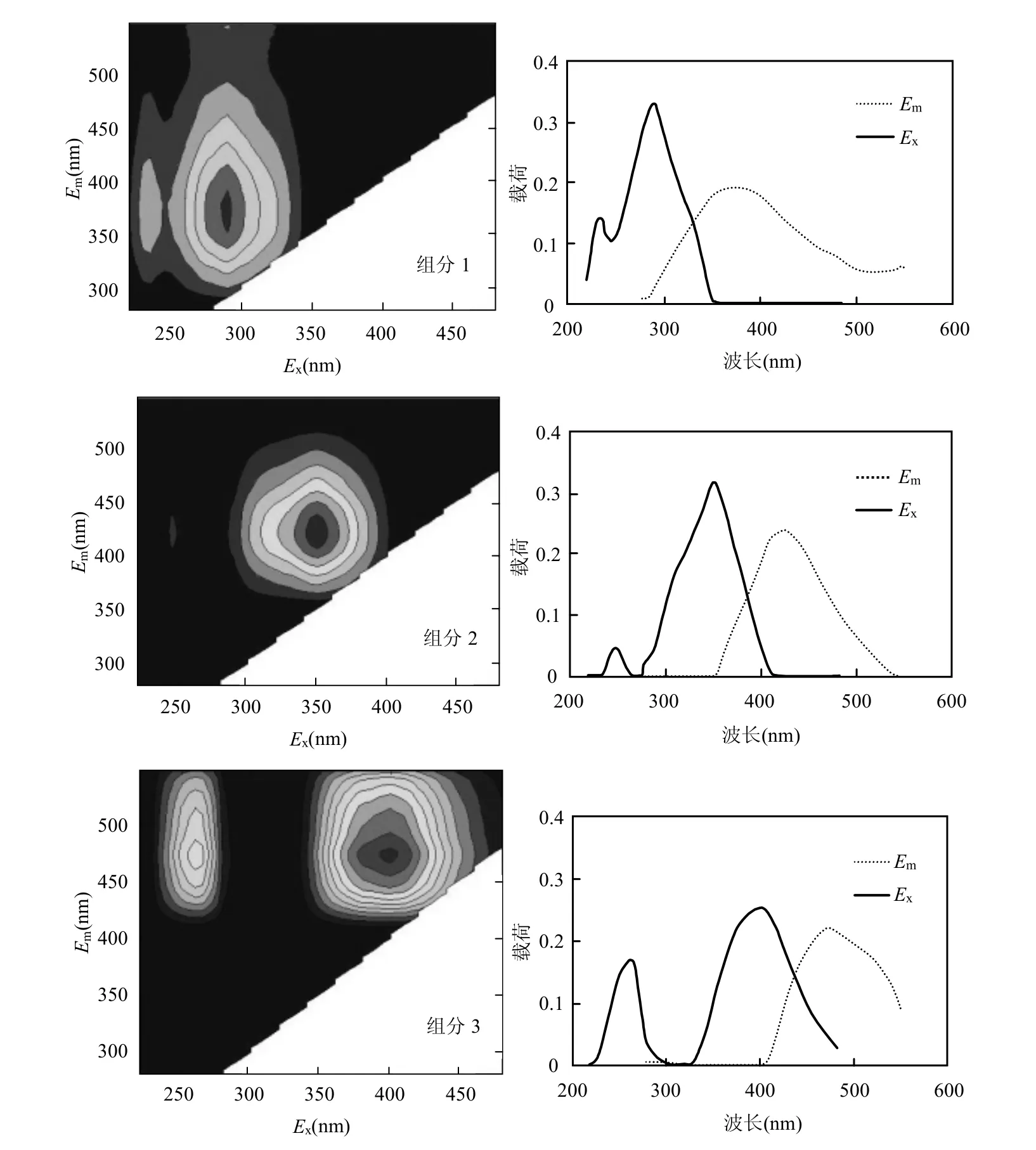
图4 PARAFAC 模型鉴别出的3个荧光组分及其激发/发射载荷Fig.4 The identified three components from PARAFAC model and their excitation/emission loadings
通过PARAFAC模型的计算,其3个荧光组分的EEM谱图及激发,发射载荷见图4.由图4可以看出,组分1属于类蛋白荧光物质,组分2和3为类腐殖质类物质[12-13],这3种荧光组分的荧光特征见表2.其中,组分1在激发波长290nm和235nm处分别具有一个峰,该组分与Stedmon等[14]研究中的组分5非常相似,该组分含有环状结构的色氨酸,与微生物代谢产物有关[15],是污水处理厂二级出水中主要的成分之一[16].组分2在激发波长350nm处有较强的峰,在激发波长245nm处有非常弱的一个小峰,从发射波长的范围来看,其属于腐殖质类物质[12-13],有研究表明,该物质为陆源腐殖质类物质[15-17].组分3同样具有2个峰,分别在激发波长260,400nm处,组分3同样为一种大分子陆源腐殖质类物质,在很多水环境中均有发现[18],而组分3中的发射波长与前2种组分相比均发生了红移,这说明组分3中含有更多的苯环及其他共轭结构基团[19].
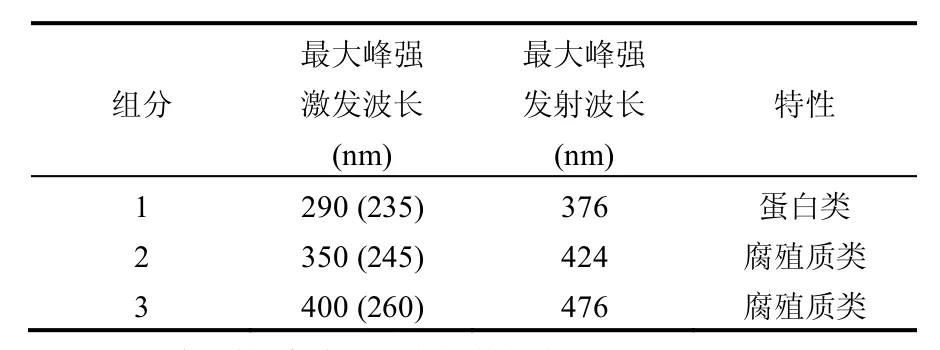
表2 3种组分荧光特征Table 2 Fluorescence characteristics of the 3components
对比常规的三维荧光图谱分析和PARAFAC的分析结果可以看出,常规的三维荧光图谱分析方法得到的信息仅局限于峰的位置及强度等常规信息,而PARAFAC得到的结果更加丰富,可以得到组成荧光图谱的若干种物质及其相应的荧光特性[6],更有利于进行水样中不同组分有机物的反应特性,动力学规律及分子量分布特性等进一步研究.
2.3.2 臭氧化与荧光组分的反应特性 三种荧光组分与臭氧的反应特性可以通过其EEM图谱中的荧光强度最大值Fmax来表征[20].由图5可以看出,在原水中腐殖质类物质组分2的荧光强度最大,在0.45mgO3/mgTOC的臭氧投加量下,其荧光强度迅速减弱,组分1和3在低臭氧投加量下与臭氧反应后荧光强度均有减少,但减少幅度小于组分2,其中大分子的腐殖质类物质组分3的减少幅度最小,这说明了在低臭氧投加下组分2会优先与臭氧反应,使其荧光强度迅速降低.当臭氧投加量小于0.98mgO3/mgTOC时,随着臭氧投加量的增加,组分1和组分2的荧光强度均有较大幅度降低,而组分3虽有降低,但降低不明显.投加量为2.15mgO3/mgTOC时,3种组分的荧光强度变化不大,说明此时3种荧光组分中大部分易于与臭氧反应的荧光基团结构已经得到了改变.
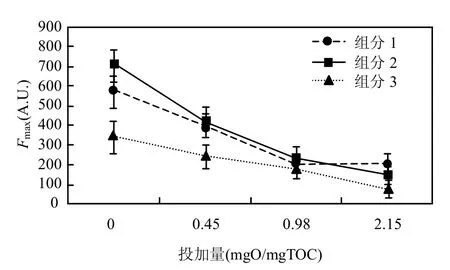
图5 三种荧光物质与臭氧的反应情况Fig.5 The reaction between three fluorescent component and ozone
基于上述3种荧光物质与臭氧反应情况,通过一级动力学模型拟合来表征3种组分荧光强度去除的动力学规律,结果如图6所示,由图6可知,组分2和组分3可以较好地用一级动力学模型来表征,而对于组分1而言,其拟合效果不是很好,这是因为组分1在投加量为2.15mgO3/ mgTOC时,其荧光强度与0.98mgO3/mgTOC相比几乎不变,这使得组分1的一级动力学拟合在较大投加量时不能很好表征.由图6结果可以看出,与图5的分析结果一致,类腐殖质类物质组分2与臭氧的反应速率最快,进一步说明了在低臭氧投加下组分2会优先与臭氧反应,使其荧光强度迅速降低.
2.3.3 荧光特性与水质指标线性回归分析 由表3可以看出,对于3个组分而言,TOC与其荧光特性的相关性很差,也就是说TOC与各个组分的荧光特性的关系不大,而3个组分Fmax值与色度,UV254及UV280具有很好的线性关系,其中组分1和组分2与这3项水质指标的R2均在0.95以上,因此二级出水臭氧化后组分1和组分2中荧光强度的降低可以很好地解释臭氧化对色度、UV254、UV280的去除.
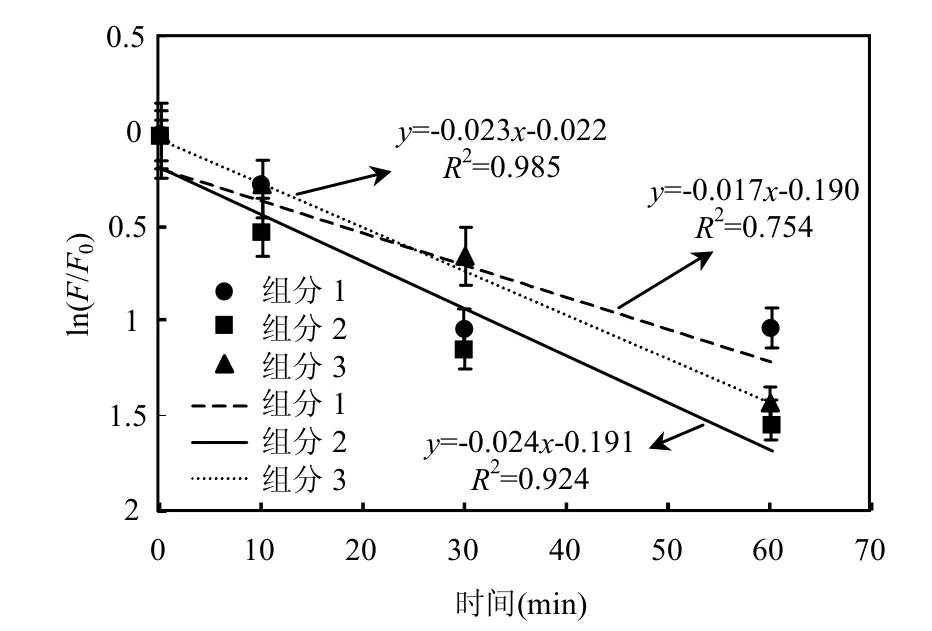
图6 3种组分以及动力学拟合Fig.6 First-order kinetic fit for reaction between three fluorescent components and ozone

表3 荧光特性与水质指标线性回归分析结果Table 3 The relationship between Fmaxand water quality
2.4 HPLC-SEC分析
由图7可以看出,对于3种组分而言,当臭氧投加量为0.98mgO3/mgTOC时,其荧光强度均明显降低,对于蛋白类物质组分1而言,其大分子物质响应值变化不大,但是其小分子物质的响应值显著降低,由此可知组分1小分子物质此时与臭氧发生了反应,使得其荧光基团结构发生改变.当投加量升高到2.15mgO3/mgTOC时,与投加量0.98mgO3/mgTOC相比,3种组分的响应值变化不大,尤其是腐殖质类物质组分2和组分3,该结果也与图5所示的3种荧光物质Fmax与臭氧投加的关系一致,进一步说明了在投加量为0.98mgO3/mgTOC时,二级出水中3种组分的荧光基团就会与臭氧发生比较彻底的反应.

图7 HPLC-SEC对3种荧光组分的分析Fig.7 HPLC-SEC analysis results of three components
3 结论
3.1 根据PARAFAC分析结果,污水厂二级出水中共有3个荧光组分,其中组分1为蛋白质类物质,组分2和3为腐殖质类物质,组分1和组分2的荧光强度较强.
3.2 臭氧与腐殖质类物质的荧光基团在低臭氧投加量下就有明显的反应,其中与腐殖质类物质(组分2)的反应最为明显.当臭氧为0.98mgO3/ mgTOC时,2种腐殖质类物质与一种蛋白质类物质中的荧光基团均可以和臭氧发生比较彻底的反应,当臭氧投加量提高至2.15mgO3/mgTOC时,3种物质的荧光强度变化不大.
3.3 线性回归分析表明,臭氧化前后蛋白质类物质(组分1)和腐殖质类物质(组分2 )的荧光强度与二级出水臭氧化前后色度、UV254、UV280具有很好的线性关系,因此臭氧化后这两类物质中荧光强度的降低可以很好解释水质臭氧化对色度、UV254、UV280的去除.
3.4 HPLC-SEC的结果进一步验证了PARAFAC的分析结果,同时,对于蛋白类物质组分1而言,臭氧主要和其中小分子物质的荧光基团发生反应,与其大分子物质几乎不发生反应.
[1]Chen W, Westerhoff P, Leenheer J A, et al. Fluorescence Excitation-Emission Matrix regional integration to quantify spectra for dissolved organic matter [J]. Environ. Sci. Technol., 2003,37(24):5701-5710.
[2]Guo J, Peng Y, Guo J, et al. Dissolved organic matter in biologically treated sewage effluent (BTSE): Characteristics and comparison [J]. Desalination, 2011,278(1-3):365-372.
[3]郑晓英,王俭龙,李鑫玮,等.臭氧氧化深度处理二级处理出水的研究 [J]. 中国环境科学, 2014,34(5):1159-1165.
[4]Li W T, Chen S Y, Xu Z X, et al. Characterization of Dissolved Organic Matter in Municipal Wastewater Using Fluorescence PARAFAC Analysis and Chromatography Multi-Excitation/ Emission Scan: A Comparative Study [J]. Environ. Sci. Technol., 2014,48,2603-2609.
[5]郭卫东,黄建平,洪华生,等.河口区溶解有机物三维荧光光谱的平行因子分析及其示踪特性 [J]. 环境科学, 2010,31(6):1419-1427.
[6]李卫华.废水生物处理过程的紫外与荧光光谱解析 [D]. 合肥:中国科学技术大学, 2008.
[7]曾凡亮,罗先桃.分光光度比色法测定水样色度 [J]. 工业水处理, 2006,26(9):69-77.
[8]Miller M P, Simone B E, McKnight D M, et al. New light on a dark subject: comment [J]. Aqu. Sci., 2010,72(3):269-275.
[9]Stedmon C A, Bro R. Characterizing dissolved organic matter fluorescence with parallel factor analysis: A tutorial [J]. Limnol. Oceanogr.: Methods, 2008,6:572-579.
[10]吕桂才,赵卫红,王江涛.平行因子分析在赤潮藻滤液三维荧光光谱特征提取中的应用 [J]. 中国分析化学, 2010,38(8):1144-1150.
[11]Swietlik J, Sikorska E. Application of fluorescence spectroscopy in the studies of natural organic matter fractions reactivity with chlorine dioxide and ozone [J]. Water Research, 2004,38(17):3791-3799.
[12]Murphy K R, Hambly A, Singh S, et al. Organic matter fluorescence in municipal water recycling schemes: toward a unified PARAFAC model [J]. Environ. Sci. Technol., 2011,45(7):2909-2916.
[13]Fellman J B, Miller M P, Cory R M, et al. Characterizing dissolved organic matter using PARAFAC modeling of fluorescence spectroscopy: a comparison of two models [J]. Environ. Sci. Technol., 2009,43(16):6228-6234.
[14]Stedmon C A, Markager S, Bro R. Tracing dissolved organic matter in aquatic environments using a new approach to fluorescence spectroscopy [J]. Marine Chemistry, 2003,82(3/4):239-254.
[15]Coble P G, Del Castillo C E, Avril B. Distribution and optical properties of CDOM in the Arabian Sea during the 1995 Southwest Monsoon [J]. Deep-Sea Res., Part 2, 1998,45:2195-2223.
[16]Baker A. Fluorescence excitation-emission matrix characterisation of some sewage impacted rivers [J]. Environ. Sci. Technol., 2001,35: 948-953.
[17]Holbrook R D, Yen J H, Grizzard T J. Characterizing natural organic material from the Occoquan watershed (Northern Virginia, US) using fluorescence spectroscopy and PARAFAC [J]. Science of the Total Environment, 2006,361(1-3):249-266.
[18]Stedmon C A, Markager S. Resolving the variability in dissolved organic matter fluorescence in a temperate estuary and its catchment using PARAFAC analysis [J]. Limnology and Oceanography, 2005,50(2):686-697.
[19]Sharma A, Schulman S G. Introduction to Fluorescence Spectroscopy [M]. New York: Wiley, 1999.
[20]Nancy P S, Andrew T S, Christopher M M. Assessment of dissolved organic matter fluorescence PARAFAC components before and after coagulation-filtration in a full scale water treatment plant [J]. Water Research, 2013,47:1679-1690.
Ozonation characteristics of DOM in secondary effluent based on fluorescence PARAFAC analysis.
JIN Xin, JIN Peng-kang*, KONG Qian, BAI Xue, WANG Xiao-chang
(Department of Environmental and Municipal Engineering, Xi'an University of Architecture and Technology, Xi'an 710055, China).
China Environmental Science, 2015,35(2):427~433
The characteristics of DOM in secondary effluent at different ozone dosages were investigated based on EEM parallel factor analysis. There were three fluorescent components in secondary effluent. Component 1was protein-like substances and the other two components were humic-like substances. The three components will react with ozone intensively at ozone dosage 0.98mgO3/mgTOC. Linear regression analysis showed that the reaction between ozone and component 1and 2could account for the removal of color, UV254and UV280. In addition, the HPLC-SEC analysis confirmed the PARAFAC analysis results and revealed that ozone will react preferentially with small molecular weight substances in component 1. However, there was little reaction between ozone and high molecular weight substances in component 1.
secondary effluent;ozonation;parallel factor analysis;fluorescence characteristics
X703
A
1000-6923(2015)02-0427-07
金 鑫(1987-),男,陕西兴平人,西安建筑科技大学博士研究生,主要从事水处理理论与技术研究.发表论文2篇.
2014-05-29
国家自然科学基金资助项目(51378414,51178376);教育部新世纪优秀人才支持计划(NCET-12-1043);陕西省污水处理与资源化创新团队(IRT 2013KCT-13)
* 责任作者, 教授, pkjin@xauat.edu.cn

