石斛碱的研究进展
王亚芸,任建武,2*
1.北京林业大学生物科学与技术学院食品科学与工程系,北京100083
2.林业食品加工与安全北京市重点实验室(北京林业大学),北京100083
石斛碱的研究进展
王亚芸1,任建武1,2*
1.北京林业大学生物科学与技术学院食品科学与工程系,北京100083
2.林业食品加工与安全北京市重点实验室(北京林业大学),北京100083
石斛是一种常用的名贵中药材,我国石斛药材植物来源众多。石斛有效成分的研究,对有效利用石斛资源具有重要意义。文中主要综述了石斛中有效成分石斛碱的组成结构、作用功效以及生物合成途径的研究进展。
石斛碱;合成途径;研究进展
石斛(Dendrobium nobile Lindl)为兰科石斛属多种药用植物的总称,具有调节机体免疫作用、生津益胃、抗白内障、抗肿瘤等功能。生物碱是一类含氮有机化合物,大多数具有较复杂的氮杂环结构,并具有生理活性和碱性。从广义上讲,生物界除去生物体必须的有机化合物,如氨基酸、多肽、蛋白质和B族维生素等外,其他所有的含氮有机化合物都可视为生物碱。生物碱是中药材中众多有效化学成分种类之一,其药理作用甚为广泛,石斛碱是从金钗石斛中获得的主要生物碱类,它的生物活性与木防己毒素(Picrotoxin)相似,通过化学与光谱方法检测确定石斛碱具有一种木防己毒烷(Picrotoxane)的骨架。石斛碱是第一种被检测到的Picrotoxane-type的生物碱。
石斛碱具有止痛、解热作用,可降低心率、血压、减慢呼吸,可产生中度的高血糖,具强壮作用并可解巴比妥中毒[1],具有较高的研究开发价值。目前,临床应用的生物碱就有80多种。当前除了提取分离生物中大量的生物碱,并测定它们的结构式外,生物碱的全合成和半合成工作也是重要的研究领域,而且发展的速度很快。生物碱类成分是最早从石斛属植物中分离得到的化合物,含量较低,石斛碱(Dendrobine)为1932年铃木秀干等人[2]首次从金钗石斛中分得的生物碱,其含量为0.52%[3]。而我国对药材石斛化学成分的研究始于二十世纪三十年代[4],1935年,陈克恢再次从金钗石斛中分离得到该成分[5]。铁皮石斛的总生物碱含量较低,一般在0.0083%~0.0241%之间[6]。
1 石斛碱的结构组成
Porter[7]和Coscia[8]分别描绘出了六种石斛碱以及一种石斛盐的结构,尽管这些石斛碱远比大多数的木防己毒烷的结构简单,但是也只有在1960年光谱分析变得通用之后这些石斛碱的结构确定才变得可行。1964年,不少于3组日本研究团队运用降解反应和光谱数据分析联合的方法独立地完成了金钗石斛中主要的生物碱-石斛碱的结构确定。到目前为止,共从14种石斛属植物中分离获得34个生物碱,其中有7种植物含有石斛碱类生物碱(即倍半萜类生物碱)21个,石斛碱类生物碱是石斛中最主要的生物碱,根据其分子结构的母核类型判断此类生物碱属于倍半萜类生物碱。不同石斛属植物中含有的石斛碱成分有着很大不同,金钗石斛(D.nobile Lindl)中含有的石斛碱种类有Dendrobine(1)、Dendrobine-N-oxide(2)、N-Methyldendrobinium salt(3)、N-Isopentenyl-dendrobinium salt(4)、6-Hydroxy-dendrobine(5)、Dendrine(7)、Dendronobiline A(8)、Nobilonine(9)、6-Hydroxy-nobilonine(10)、Dendroxine(11)、N-Isopentenyldendroxinium salt(12)、6-Hydroxy-dendroxine(13)、N-Isopentenyl-6-hydroxyden-droxinium salt(14)、4-Hydroxy-dendroxine(15)、13-Hydroxy-14-oxodendrobine(19);樱石斛(D.linawianum)、棒节石斛(D.findlayanum)、D.hildebrandii中都含有石斛碱Dendrobine(1);此外棒节石斛中含有2-Hydroxy-dendrobine(6);D.hildebrandii中还含有石斛碱(5)、(9)、(10)、(12)、(14);D. friedricksianum中含有石斛碱(1)、(5)、(9)、(10)、(12)、(14);大苞鞘石斛(D.wardianum)中含有石斛碱(1)、Dendrowardine(20);细茎石斛(D.moniliforme)含有石斛碱(10)、Moniline(21);春石斛(D.Snowflake)中含有Mubironine A(16)、Mubironine B(17)、MubironineC(18)。

图1 石斛碱结构式Fig.1 The structural formula of dendrobine
2 石斛碱的作用功效
生物碱的药理作用主要表现在抗肿瘤,对心血管、胃肠道抑制作用及止痛退热等作用[9,10]。1995年韩国学者Lee等报道金钗石斛的乙酸乙酯提取物对肿瘤细胞株A-549、SK-OV-3和HL-60有显著的细胞毒性作用[11]。2000年日本学者Morita等从金钗石斛分得的Picrotoxane倍半萜型生物碱Flakinins A和B以及Mubironine C,具有小鼠白细L1210的细胞毒性作用,体外IC50分别为4.0 μg·mL-1,8.5 μg·mL-1,2.6 μg·mL-1[12]。1994年Chen等研究发现粉花石斛的甲醇提取物可明显抑制兔血小板凝集的作用。同年施红等研究发现大剂量的石斛碱可降低兔、豚鼠的心肌收缩力,降低血压并抑制呼吸[13]。石斛碱对猫血压有类似毒覃碱作用及烟碱的兴奋作用[14,15]。不论浓度高低,石斛浸膏对离体蟾蜍的心脏均有抑制作用[16]。2001年,陈晓梅等研究发现石斛碱还能抑制离体兔肠管活动[17],推测这是由于石斛能使血中胃泌素浓度升高,石斛可以直接刺激G细胞,引起胃泌素的释放增加,使血清中的胃泌素浓度升高。胃泌素刺激壁细胞,使胃酸分泌增加,从而明显降低小鼠胃肠推动作用。1991年李满飞等从粉花石斛中分离出的生物碱石斛宁和石斛宁定能抑制大鼠肾脏微粒体Na+-K+-ATP酶,该酶是基础代谢下产生热能最主要的酶[10]。2001年陈晓梅等研究发现铁皮石斛和金钗石斛药液对大鼠肾脏微粒体Na+-K+-ATP酶的活性有抑制作用[13]。中医的阳虚内热是由于Na+-K+-ATP酶活性过高的一种表现,石斛能抑制肾脏微粒体Na+-K+-ATP酶活性的药理作用与其滋阴清热的功效是相吻合的[9]。另外,石斛碱还有一定的止痛解热作用,与非那西汀相似[16]。
金钗石斛多糖和生物碱均能降低肾上腺素所致的小鼠血糖升高[18]。其生物总碱可改善脂多糖诱导的大鼠学习记忆功能减退[19]。2009年,Q.Wang等人[20]通过将新生大鼠原代培养神经元OGD/RP损伤后测定乳酸脱氢酶(LDH)释放和噻唑蓝(MTT)液比色吸光度,评价神经元活性,观察不同浓度的石斛碱对于离体脑损伤的保护作用,发现石斛碱可有效减轻OGD/RP对脑片的缺血性损伤,并对于OGD/RP原代神经元具有显著的保护作用。2011年,Yanfei Li等人[21]发现石斛碱能够抑制由于脂多糖引起的记忆损伤问题。
2012年L.Fitria等人[22]发现石斛碱对生育力增强起着重要的作用,实验材料是提取野生植物鸽子兰(D.crumenatum)的假鳞茎汁,其研究目的是用与女性生殖功能类似的Wistar大鼠作为动物模型来研究鸽子兰假鳞茎汁的作用效果。结果表明口服的鸽子兰假鳞茎果汁能显著提高Wistar大鼠雌激素水平,增加三级卵泡的数量。此外金钗石斛对眼科疾病有明显的治疗作用,其生物碱具有较好的抗糖性白内障作用,可下调iNOS基因的表达,显著抑制NOS的活性,减少NO的产生,从而减轻氧化损伤作用,达到抗白内障作用[23]。体外研究表明金钗石斛的总生物碱和粗多糖均有一定的抗白内障作用,而总生物碱的作用优于粗多糖[24]。
3 石斛碱的生物合成途径
迄今为止,石斛碱的七种全合成和五种表全合成被报道出来(其中全合成指从原料开始到最终产物的制备和反应路线全部都是由一个科研组独立设计完成的途径;表全合成又叫接力全合成指反应路线有一部分是完全拷贝他人以及完成的工作而实现的全合成)。

图2 Kaneko等人的合成途径Fig.2 Kaneko's synthetic route
1970年,Kaneko等人报道了石斛碱[25],他们合成了Dendrobine的三环骨架结构(8a,8b)。起始材料是可以很容易由香芹酮转化得到的二氢黄蒿萜酮1(图2)[26],这个反应的先决条件是完成EPC合成(EPC是Enantiomeric Purity Compound的缩写,指的是对映纯化合物的合成),它的关键步骤是是路易斯酸催化丁二烯和二氢香芹酮分子间的Diels-Alder反应(简称IMDA,由共轭双烯与烯烃或炔烃反应生成六元环的反应),然后通过如图2所示一系列反应,最终在200℃、50个大气压下环化得到两个三环胺结构的非对映体混合物8。
1972年,Yamada等人报道了完整的石斛碱的合成途径[27]。Yamada等人以四氢萘酮9[28]为初始料,经Ac2O-p-TsOH回流处理转变为烯醇乙酸酯类物质10(图3),随后将10臭氧化得到一种醛类物质11,利用Corey-Chaykovsky条件然后冷凝使链伸长,再经含草酸水溶液的甲基酮水解处理得到一种烯醇醚类物质12,通过酮体保护形成环状缩酮13,随后经过如图3所示的一系列反应顺序生成酮酯类混合物质24和25,然后分离得到25后在NaBH4、Glyme存在时环化得到②,之后还原得到Dendrobine①,从9到获得石斛碱①总共需要23步,只有1.2%的获得率。除此之外还可以将25溴化后水解得到26,然后经一系列反应得到③,再经Eschweiler-Clark甲基化反应得到石斛酮碱④。

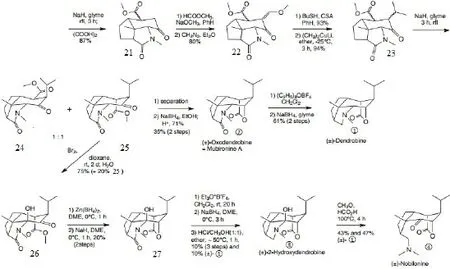
图3 Yamada等人的合成途径Fig.3 Yamada's synthetic route
1974年,Inubushi等人对石斛碱的合成发表了一个完整的描述[29]。此次合成的初始材料为二氢茚酮衍生物28(图4)[30],通过对甲苯磺酰氯及氰化钠的作用将28转化为氰化物29,然后在氢气、碳酸锶作用下形成顺式八氢印酮30,将30进行溴化处理,结果发现在C(5)上容易发生溴化,只能得到20%的不饱和羰基化合物31,可以得到68%的同分异构体29,将31用强水基团水解得到羧酸物质32,在高温酸性条件下转化为酮酯33,在30%的甲胺水溶液及CH3NH3+Cl-存在条件下185℃高温作用2 d得到34,经过多次尝试在KHSO4存在时高温处理得到烯烃物质35,在碘、醋酸、醋酸银存在条件下,经Collin试剂皂化和一系列氧化得到36、37(2:1)的混合物,将34通过Nagata氢氰化反应转化为38,之后38通过如图4所示两种途径转化为含氧石斛碱②。最后通过Borch反应转化为石斛碱①。


图4 Inubushi等人的合成途径Fig.4 Inubushi's synthetic route
20世纪60年代末和70年代初,Yamada和Inubushi对全合成途径的研究证明了复杂、拥挤的分子结构是可以被合成得到的。
Kende对于石斛碱外消旋体的合成途径是比较简短的[31],Kende等人起始材料用麝香草酚(图5)[32],然后通过百里香醌转化和Thiele-Winter-乙酰氧基化形成已知的物质1、2、4-triacetoxy-3-异丙基-6-甲基苯(42)。通过皂化反应,三元醇被FeCl3氧化得到羟基醌43,醌和丁二烯发生分子间的狄尔斯阿尔德反应不仅新生成的两个手性中心的相对构型而且定量产量三取代双键(与Kaneko的关键步骤相比),之后利用CH3I甲基化烯醇44,通过二羟基化作用及连续的醇醛缩合作用得到45,在Kaneko的途径中,即使催化,溶解和温度条件发生改变时醇醛缩合也没有表现出区域选择性,然后在较温和的酸性条件下利用CH3NH3+Cl-和NaBH3CN将46氨基化,生成47、48。饱和胺48可以自发地转化为具有石斛碱三环骨架结构的49,49在LiAlH4存在时被还原为不饱和羰基化合物50,51在NaOCH3存在时转化为一部分初始材料和一部分51的同分异构体52,之后按图5条件反应得到石斛碱。

图5 Kende等人的合成途径Fig.5 Kende's synthetic route
此外,1975年,Borch等人以Diels-Alder反应作为关键步骤成功合成4-Epi-dendrobine[33,34];Roush也运用IMDA反应作为关键步骤成功地合成了外消旋体的石斛碱[35,36],他通过避免形成三元双键消除了关键步骤中的空间立体结构所产生的障碍;1989年,Martin等人对外消旋体石斛碱合成的尝试研究[37,38,39],实验以由初始材料二烯单元物质转化生成的二烯烃氨基化合物与三元取代烯烃类物质发生的IMDA反应作为主要步骤合成石斛碱;1992年,Takano等人通过EPC合成石斛碱的三环骨架结构,证明了Pauson-Khand反应的有效性[40];1997年Sha等人第一个发表了左旋-石斛碱的合成途径[41];1999年,Zard等人又以反式-烯醇作为初始材料,以Pauson-Khand反应作为主要步骤完成了石斛碱的EPC合成[42,29];最近关于石斛碱合成的报道是由Padwa等人发表的,它的关键步骤是引发串联反应的IMDA反应[43,44]。
4 结语
石斛碱是石斛中重要的药用活性成分,具有较高的药用价值。但是目前对于石斛碱的结构及合成途径报道较为少见。石斛属植物具有多方面的药理活性,我国石斛属植物种类较多,从中筛选具有临床应用价值的药物具有广阔的前景。但在野生石斛植物资源遭到严重破坏的今天,更应该注意资源保护,对拟开发利用的药用种类进行人工培植,以达到可持续发展的利用资源。不同种的药用石斛具有不同的药理及临床功效,因此有必要根据有效成分和药理临床实验,对所有药用石斛进行整理和归纳,制定相应的质量标准,把所有药用石斛的临床功效尽可能充分发挥,以确保临床疗效。
[1]王宪楷,赵同芳.石斛属植物的化学成分与中药石斛[J].药学通报,1986,21(11):666-669
[2]铃木秀干.中药金石斛生物碱的研究[J].药学杂志,1932,52(12):1049-1060
[3]WANG X K,ZHAO T F.Chemical constituents in Dendrobium species and Chinese traditional medicine SHIHU[J]. Chin Pharm Billk,1986,21(11):666-669
[4]马继兴.神农本草经辑注[M].北京:人民卫生出版社,1995
[5]沈关桢.石斛治百病[M].浙江:科学技术出版社,2004
[6]丁亚平,杨道麒,吴庆生,等.安徽霍山三种石斛总生物碱的测定及其分布规律研究[J].安徽农业大学学报,1994,21(4):503-506
[7]Porter L A.Picrotoxinin and Related Substances[J].Chem Rev,1967,67(4):441-464
[8]Coscia C J.Picrotoxin[C]//Cyclopentanoid Terpene Derivatives.Taylor,W I,Battersby,A R(eds.).New York:Dekker,1969:147-201
[9]叶庆华,赵维民,秦国伟.石斛属植物化学成分及生物活性研究进展[J].药物化学进展,2004(3):113
[10]陈照荣,来平凡,林巧,等.不同炮制方法对石斛中石斛碱和多糖溶出率的影响[J].浙江中医学院学报,2002,26(4):79
[11]Lee Y H,Park J D,Baek N I,et al.In vitro and vivo antitumoral phenanthrenes from the aerial parts of Dendrobium nobile[J].Planta Med,1995,61:178
[12]Hiroshi M,Masako F.New Picrotoxini-type and Dendrobine-type Sesquiterpenoids from Dendrobium Snowflake RedStar[J].Tetrahedron,2000,56:5801-5805
[13]Chen C C,Wu LG,Ko FN,et al.Antiplatelet aggregation principles ofDendrobium loddigesii[J].Nat Prod,1994,57(9):1271
[14]施红,黄玲.石斛抗衰老作用的研究[J].中草药,1993,24(1):534
[15]方泰惠.石斛对大鼠肠系膜的动脉血管的作用[J].南京中医学院学报,1991,7(2):100
[16]江苏新中医学院.中药大药典[M].上海:上海科学技术出版社,1985:586
[17]陈晓梅,郭顺星.石斛属植物化学成分和药理作用的研究进展[J].天然产物研究与开发,2001,13(l):70-75
[18]李菲,黄琦,李向阳,等.金钗石斛提取物对肾上腺素所致血糖升高的影响[J].遵义医学院学报,2008,31(1):11-12
[19]林智诚,施红,刘福英,等.石斛复方制剂长期毒性的研究[J].福建中医学院学报,1996,6(4):33-35
[20]Wang Q,Gong Q,Wu Q,et al.Neuroprotective effects of Dendrobium alkaloids on rat cortical neurons injured by oxygen-glucose deprivation and reperfusion[J].Phytomedicine,2010,17:108-115
[21]Yanfei Li,Fei Li,Qihai Gong,et al.Inhibitory Effects of Dendrobium Alkaloids on Memory Impairment Induced by Lipopolysaccharide in Rats[J].PlantaMed,2011,77:117-121
[22]Fitria L,Ridhowati A.Reproductive function in female Wistar rats(Rattus norvegicus Berkenhout,1769)after oral administration of Pigeon Orchid(Dendrobium crumenatum Swartz,1799)pseudobulb juice[C].Bandung:International Conference on Biomedical Science(ICBS),2012
[23]魏小勇,龙艳.金钗石斛生物碱对糖性白内障大鼠诱导型一氧化氮合酶基因的调控[J].解剖学研究,2008,30(3)177-180
[24]魏小勇,龙艳,詹宇坚,等.金钗石斛提取物抗白内障的体外实验研究[J].现代中药研究与实践,2008,22(2):27-31
[25]Yamamoto K,Kawasaki I,Kaneko T.Synthetic studies of dendrobine I synthesis of the skeleton of dendrobine[J]. Tetrahedron Letters,1970,11(56):4859-4861
[26]Ireland RE,Bey P.Homogeneous catalytic hydrogenation:dihydrocarvone[J].Org Synth Coll,1988,6:459-459
[27]Yamada K,Suzuki M,Hayakawa Y,et al.Total synthesis of(±)-dendrobine[J].Journal of the American Chemical Society,1972,94(23):8278-8280
[28]Ruzicka L,Sternbach L.Zur Kenntnis der Diterpene.(42.Mitteilung).Dehydrierung von Oxydationsprodukten der Abietinsäure zu 1-Methyl-7-oxy-phenanthren und 1,5-Dimethyl-6-oxy-naphtalin.Synthese von 1,5-Dimethyl-7-oxyund von 1,6-Dimethyl-7-oxy-naphtalin[J].Helvetica Chimica Acta,1940,23(1):355-363
[29]Inubushi Y,Kikuchi T,Ibuka T,et al.Total Synthesis of the Alkaloid(±)-Dendrobine[J].Chemical&pharmaceutical bulletin,1974,22(2):349-367
[30]Acklin W,Prelog V,Prieto A P.Reaktionen mit Mikroorganismen.2.Mitteilung.Die stereospezifische Reduktion von(±)-Δ4,9-8-Methyl-hexahydro-indendion-(1,5)[J].Helvetica Chimica Acta,1958,41(5):1416-1424
[31]Kende A S,Bentley T J,Mader R A,et al.Simple total synthesis of(±)-dendrobine[J].Journal of the American Chemical Society,1974,96(13):4332-4334
[32]a)Kremers E,Wakeman N,Hixon R M.Thymoquinone[J].Organic Syntheses.Collective,1941:1.b)Blatchly JM,Green RJS,McOmie JFW.Thiele-Winter acetoxylation of quinones.Part IV.Quinones containing one or more t-butyl groups[J].J.Chem.Soc.,Perkin Trans.1,1972:2286-2291
[33]Borch R F,Evans A J,Wade J J.Synthesis of 8-epi-dendrobine[J].Journal of the American Chemical Society,1975,97(21):6282-6284
[34]Borch R F,Evans A J,Wade J J.Synthesis of 8-epi-Dendrobine[J].Journal of the American Chemical Society,1977,99(5):1612-1619
[35]Roush W R.Total synthesis of(+)-dendrobine[J].Journal of the American Chemical Society,1978,100(11):3599-3601
[36]Roush W R.Total synthesis of(+)-dendrobine[J].Journal of the American Chemical Society,1980,102(4):1390-1404
[37]Martin S F,Li W.General methods for alkaloid synthesis via intramolecular Diels-Alder reactions.A concise formal total synthesis of(±)-dendrobine[J].The Journal of Organic Chemistry,1989,54(2):265-268
[38]Martin S F,Li W.Applications of intramolecular Diels-Alder reactions to alkaloid synthesis.A formal total synthesis of(±)-dendrobine[J].The Journal of Organic Chemistry,1991,56(2):642-650
[39]Lynch V M,Li W,Martin S F,et al.Structure of the ABC ring subunit of 3-hydroxy-2-oxodendrobine[J].Acta Crystallographica Section C:Crystal Structure Communications,1990,46(6):1159-1161
[40]Takano S,Inomata K,Ogasawara K.A facile chiral approach to the dendrobine skeleton by intramolecular Pauson-Khand reaction[J].Chemistry Letters,1992,21(3):443-446
[41]Sha C K,Chiu R T,Yang C F,et al.Total Synthesis of(±)-Dendrobine via α-Carbonyl Radical Cyclization[J].Journal of the American Chemical Society,1997,119(18):4130-4135
[42]Cassayre J,Zard S Z.A Short Synthesis of γ-Lycorane using Ni/AcOH Mediated Radical Cyclisation[J].Synlett,1999,1999(4):501-503
[43]Padwa A,Dimitroff M,Waterson A G,et al.Diels-Alder Reaction of 2-Amino-Substituted Furans as a Method for Preparing Substituted Anilines[J].The Journal of Organic Chemistry,1997,62(12):4088-4096
[44]Padwa A,Brodney M A,Dimitroff M.A New Method for the Formation of Octahydroindole Alkaloids via the Intramolecular Diels-Alder Reaction of 2-Amidofurans[J].Journal of organic chemistry,1998,63(16):5304-5305
The Progress of Study on Dendrobine
WANG Ya-yun1,REN Jian-wu1,2*
1.Department of Food Science and Engineering,College of Biological Sciences and Biotechnology,Beijing Forestry University,Beijing 100083,China
2.Key Laboratory of Forest Food Processing and Security,Beijing Forestry University,Beijing 100083,China
Dendrobium is a commonly used herbal medicine material,which has numerous sources of medicinal plants.The research of active ingredients in Dendrobium is crucial to the effective utilization of Dendrobium resources.This paper mainly reviewed the Dendrobium in three aspects:composition,medicinal effects and biosynthetic pathways of Dendrobium base.
Dendrobine;biosynthetic pathways;research progress
R284
A
1000-2324(2015)01-0152-07
2013-04-13
2013-04-22
北京市园林绿化局计划项目(Y1HH200900304)
王亚芸(1990-),女,在读研究生.Email:wyy3127986@163.com
*通讯作者:Author for correspondence.E-mail:jianwur@sina.com

