硅溶胶的制备及其影响因素
张 翠 李绍纯 金祖权 赵铁军
(青岛理工大学土木工程学院,山东 青岛 266033)
0 引言
硅溶胶是二氧化硅的胶体粒子分散于水中或溶剂中的一种胶体溶液,又名硅酸溶液或二氧化硅水溶液[1]。根据pH值的不同硅溶胶分为酸性硅溶胶和碱性硅溶胶。其基本成分为无定型的二氧化硅,分子式mSiO2·nH2O,胶团结构如图1所示。

图1 胶团结构示意图
硅溶胶含有大量的水合胶体,这些胶体呈化学惰性,因此硅溶胶无臭、无味、无化学腐蚀;硅溶胶的胶团为纳米级别,具有较大的比表面积和吸附能力,使得硅溶胶具有较好的粘结性、亲水性和憎油性。与此同时,硅溶胶还具有较好的分散性以及良好的透光性。这一系列优异的性能使得硅溶胶得到人们的关注并广泛应用于涂料、粘结剂、耐火绝热材料、纺织、冶金精铸、制药等行业[2-4]。
1 溶胶—凝胶法制备硅溶胶
溶胶-凝胶法以金属醇盐或其化合物为原料,在酸性或碱性催化剂的作用下,进行水解缩聚反应,使溶液由溶胶变为凝胶。其制备过程是醇盐的水解与聚合同时反应的物理化学过程。
实验室利用溶胶-凝胶法制备硅溶胶一般是以正硅酸乙酯(TEOS)为前驱体,乙醇为溶剂,酸或碱为催化剂,DMF(N-N—二甲基甲酰胺)为添加剂,去离子水,按一定比例混合,在一定温度下搅拌制得硅溶胶[5]。正硅酸乙酯在不同的水解条件下进行水解和缩合,得到的产物有所不同。完全水解时生成二氧化硅和乙醇,不完全水解的情况下则有中间产物存在[5-12]。
硅溶胶反应过程:
(1)水解
正硅酸乙酯(TEOS)在水中的水解反应如式(1)所示[14-16]:
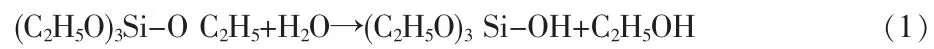
根据催化剂的不同,水解反应又可分为亲电性取代和亲核性取代,当酸作催化剂时发生亲电性取代,水解速率与H+成正比,具体取代过程如下:
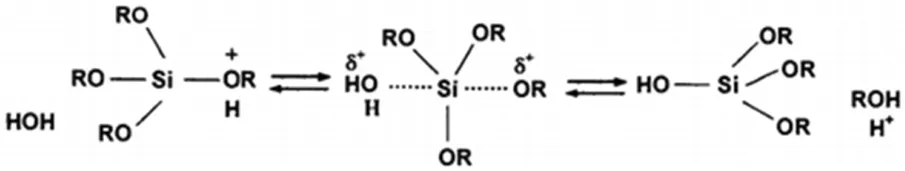
在酸的催化条件下,H+首先进攻正硅酸乙酯分子中的一个OR基团并使之质子化,造成电子云向该OR集团偏移,使硅原子核的另一侧面空隙加大并呈亲电子性,因此,负电性较强的阴离子得以进攻硅离子,使TEOS水解。
碱为催化剂时发生亲核性取代,其水解速率与OH-浓度成正比,具体过程如下:

OH-直接对硅原子发动亲核进攻,并导致电子云向另一侧的OR基团偏移,致使该基团的Si-O键削弱而断裂,完成水解反应[17]。
(2)聚合
聚合分为脱水和脱醇两步反应:
脱水缩聚,如式(2)所示。
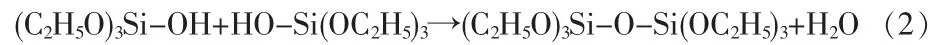
脱醇缩聚,如式(3)所示。

水解缩聚反应进行之后所得到的溶胶只是初步形成了网络结构,网络交联不完善,存在不稳定性,需在室温下静置一段时间后放入70℃的去离子水中进行老化[18]。
2 稳定性影响因素
硅溶胶是一种胶体,它具有胶体溶液的一切性质,包括不稳定性。通常以硅溶胶在一定温度下不凝胶、稳定存在的时间长短为指标来评判硅溶胶稳定性的好坏。凝胶时间是指溶胶从配制完成到倾斜45°不流动所需要的时间[19-20]。
溶胶的稳定性决定于促使溶胶粒子相互聚结的粒子间相互吸引的能量和阻碍其相互聚结的相互排斥的能量这两方面的总效应。凝胶时,体系失去聚结稳定性,但宏观上胶粒仍分布于三维空间,此时硅溶胶胶粒依靠硅氧烷形成的化学键(Si-O-Si)相结合,连成极稳定的空间网络结构[21-22]。
研究表明,影响硅溶胶稳定性的因素主要有温度、pH值、去离子水用量、乙醇用量、添加剂、催化剂种类、二氧化硅粒径等。
2.1 温度
大量实验研究表明,随着反应温度的升高,溶胶的稳定性降低。这是由于温度升高,物质的布朗运动加剧,增加了物质间相互碰撞的几率,水解和缩聚反应加快,温度升高有利于水解反应的进行,使溶胶体系含有更多的交联点,加速了粒子在溶胶体系中的熟化,与此同时,温度的升高,使溶剂挥发加快,缩聚反应产生的聚合物含量增大,促使进一步的凝胶过程进行,因而稳定性降低。有研究表明,在30℃及以下的温度制备硅溶胶较为合适,平均凝胶时间随着温度升高而缩短,并且当温度超过30℃时,溶胶稳定时间缩短速率明显变快,稳定性变差[23-24]。
2.2 pH值
正硅酸乙酯可在酸或碱的催化剂作用下发生水解和缩聚反应,根据催化剂的不同,溶胶分为酸性硅溶胶和碱性硅溶胶。硅溶胶的稳定性与pH的关系如下图,在酸性环境中,在2<pH<4范围内,存在一个亚稳区,为酸性硅溶胶的制备提供给了可能;在碱性环境中,随着pH的增大,硅溶胶的稳定性逐渐增加,pH为6.3时,溶胶稳定性最差。根据胶体化学双电层理论,硅溶胶吸附层和紧密层的电位差决定着胶体的稳定性,随体系pH的变化,溶液中H+的浓度也在发生变化,溶液呈酸性或碱性时,溶胶粒子表面的强电荷使得粒子间产生静电斥力,溶胶具有较高的稳定性,但当pH约为6.3时,紧密层吸附层内的电性被完全饱和,电位降到最低,达到了等电点,胶粒双电层消失,因此硅溶胶在该体系中极不稳定[25-26]。
有文献报道,在酸性硅溶胶中,不同酸对二氧化硅溶胶稳定性的影响大小依次为 HAC>H2SO4>HCl>HNO3>HF[24]。

图2 pH对硅溶胶稳定性的影响[27]
赵庆祥[27]通过实验发现,在酸性硅溶胶中,随pH值的增大,溶胶的稳定性先逐渐增加,随后保持稳定,最后再增加。这是因为,催化剂的增加是为了增加正硅酸乙酯的水解,当氢离子较多时,正硅酸乙酯都得到了充分的水解,使得每个原硅酸分子都可作为成核物质进行缩合,从而使溶胶稳定性增加。
高建东等[28]对碱性催化剂作用下的水解缩合进行了研究,发现碱性催化剂下进行的水解缩合,反应剧烈且随着反应的进行,体系越来越向酸性方向进行,使得溶胶体系的稳定性降低,其所得溶胶液无法得到有效存储。
2.3 水用量
在制备二氧化硅溶胶的过程中,水既以溶剂的形式存在,又以反应物的形式存在。用水量对溶胶性能的影响主要通过水与TEOS的摩尔比n来定性判断,水量较少时,一般当摩尔比m≤7时,水主要作为反应物与正硅酸乙酯发生水解,体系的粘度较大,平均凝胶时间较短,溶胶的稳定性较差;增加用水量,摩尔比m>7时水解更为充分,有相当一部分水以溶剂的形式存在,溶胶体系的粘度下降,溶胶离子之间距离增大,使缩聚反应几率变小;用水量继续增大,对溶胶的稳定性影响变小[27-29]。
2.4 乙醇用量
在以正硅酸乙酯为原料制备硅溶胶的试验中,正硅酸乙酯在水中的溶解度不大,而在乙醇中的溶解度则要大的多,乙醇既可以溶于水,又可溶解正硅酸乙酯的性质使得整个反应可以在均匀的液相中进行。一般研究乙醇用量对硅溶胶性能的影响是通过乙醇与TEOS的摩尔比m来定性判断的,随着摩尔比m的增加,硅溶胶的凝胶时间逐渐延长,稳定性增加。

图3 乙醇与TEOS的摩尔比对硅溶胶稳定性的影响[30]
根据扩散双电层理论,溶胶的介电常数与双电层厚度成正比,随着乙醇用量的增加,胶粒的介电常数增大,双电层厚度增加,溶胶稳定性增加;同时,由于乙醇是正硅酸乙酯的水解产物,可抑制水解反应的正向进行,最后,乙醇的加入使得溶液得到稀释,水解产物之间碰撞几率变小,降低了缩聚反应速率,几种作用综合,最终使溶胶的稳定性增加[30-31]。
2.5 添加剂
在制备二氧化硅溶胶的试验中,常用的添加剂为N,N一二甲基甲酰胺(DMF),随着DMF的增加,溶胶的稳定性增加,这是因为,溶胶中的氢离子可以和DMF发生氢键作用,氢键的形成使得进入紧密层的氢离子减少,从而导致胶团的电势增加,溶胶发生凝聚的势垒也相应增加,进而导致溶胶的稳定性升高。不仅如此,DMF的加入还可以抑制醇盐的水解,提高凝胶的缩聚速率,提高凝胶固含量。同时,DMF的加入也使得溶液得到稀释,提高溶胶稳定性[29-32]。
2.6 SiO2粒径
二氧化硅粒径是影响硅溶胶稳定性的一个重要因素,二氧化硅胶粒的大小和分布是硅溶胶质量高低的重要指标,影响着产品的浓度、稳定性。硅溶胶粒子直径在一定范围内,粒径越均匀,粒径分布范围越小,硅溶胶的稳定性越好。许念强认为在酸性硅溶胶体系中,溶胶的粒径与稳定性呈“S”型,如下图:
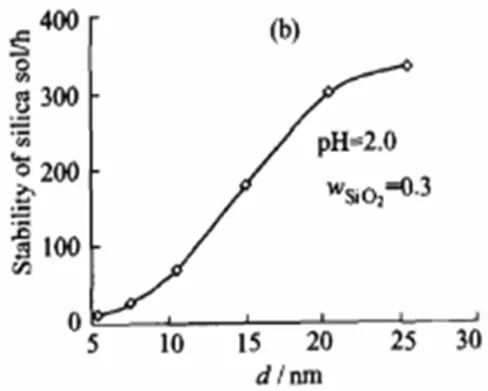
图4 粒径对酸性硅溶胶稳定性的影响[31]
二氧化硅胶粒粒径较小时,溶胶的稳定性比较低,随着粒径的增大,平均凝胶时间延长,稳定性提高,在粒径为10~20nm之间时,硅溶胶的稳定性与胶粒大小近似成正比。这是由于粒径的增大使得硅溶胶表面的羟基集团活性降低,胶粒比表面积降低,吸附分子的能力也相应的减弱,从而使凝胶过程变缓[31]。
2.7 电解质
电解质对溶胶的稳定性也有一定的影响,由硅溶胶的胶团结构可知,在酸性条件下,进入紧密层的为H+,碱性条件下进入紧密层的为金属离子。电解质中含有的离子可以吸附在溶胶胶团分散层,使分散层变薄,当电解质含量超过一定限度后,分散层为厚度零,胶粒凝结化,稳定性降低[31]。
许念强[26]等认为,在电解质盐浓度一定时,硅溶胶的稳定性随二氧化硅粒径的增大增大而减弱,当二氧化硅粒径较小时,电解质盐的浓度对稳定性产生较大影响。当硅溶胶中的含盐量降低到一定值时,电解质对溶胶稳定性的影响可忽略不计。
3 总结
硅溶胶的应用类型很多,对于硅溶胶的性能要求也不尽相同,而制备方法在很大程度上决定了硅溶胶的性能。目前,关于采用溶胶—凝胶法制备硅溶胶还存在一系列的问题有待解决:
(1)硅溶胶稳定性受很多因素影响,在制备硅溶胶过程中难以精确控制反应;
(2)硅溶胶的反应机理研究还不够系统、深入,应深入研究溶胶稳定性的因素,创建溶胶稳定化结构理论,为制备稳定溶胶提供理论依据;
(3)反应原材料正硅酸四乙酯价格偏高,而且在实验过程中需加入乙醇作为溶剂,成本相对较高;
(4)溶胶凝胶法制备的硅溶胶浓度范围在10%~20%,浓度过高硅溶胶产品易变质。
[1]陈连喜,田华,叶春生,等.硅溶胶制备与应用研究进展[J].山西化工,2008(8):9-17.
[2]田立朋,孙道兴,王力.硅溶胶的制备及其在涂料中的应用[J].上海涂料,2006(11):23-26.
[3]马纯超,郑典模,硅溶胶的制备与应用[J].无机硅化合物,2008:22-26.
[4]Gilliland J W,Yokoyama K,Yip W T.Comparative study of guest chargecharge interactions within silica sol-gel[J].J Phys Chem B,2005(11):4816-4823.
[5]WANG Yu-young.HSIEH T-E.Preparation and properties of p.yacrylate/clay photo cured nanocomposite materials[J].Chem Mater,2005,17(13):333l-3337.
[6]PERCY M J,BARTHET C,LOBB J C,et a1.Synthesis and characterization of vinyl polymer-silica colloidal nanocomposites[J].Langmuir,2000.16(17):6913-6920.
[7]ZHANG Shengwen,ZHOU Shu xue.WENG Yuming,et a1.Synthesis of SiO2/polystyrene nanocomposite particles viaminiemulsion polymerization[J].Langmuir,2005,21(6):2124-2128.
[8]BOURGEAT-LAMI E,LANG J.Encapsulation of inorganic particles by dispersion polymerization in polar media(2):Effect of silica size and concentration on the morphology of silica-polystyrene composite particles[J].Journal of Colloid and interface Science,1999,210(2):281-289.
[9]LUNA-XAVIER J-L,BOURGEAT-I AM I E,GUYOT A.The role of initiation in the synthesis of silica/poly(methyl methacrylate)nanocomposite latex particles through emulsion polymerization[J].Colloid & Polymer Science,2001.279(10):947958.
[10]I UNA-XAVIER J-L,GUY()T A,BOURGEAT-I AM I E.Preparation of nano—sized silica/poly(methyl methacrylate) composite latexes by heter0c0agulati0n:Comparison of three synthetic routes[J].Polymer International,2004,53(5):609-6l7.
[11]SCHMID A,FUJII S,ARMES S P.Polystyrene silica nano-composite particles via alcoholic dispersion polymerization using a cationicazo initiator[J].Langmuir,2006,22(11):4923-4927.
[12]KAI ININAO.KU M ACH EVA E.A “core-shell” approach to producing 3D polymer nanocomposites[J].Macromoleculesl999,32(12):4l22-4l29.
[13]黄志良,陈巧巧,陈常连,等.酸性硅溶胶稳定性的正交试验[J].武汉工程大学学报,2013(1):60-64.
[14]Guo Jian-jun,Liu Xue-hui,Cheng Yu-chuan.Size-controllable synthesis of mono-dispersed colloidal silica nano-particles via hydrolysis of elemental silicon[J].Journal of Colloid and Interface Science,2008,326:138-142.
[15]Duan Qing-jiao,Zhang Jian,Tian Jia,Silica nanorings on the surfaces of layered silicate[J].Langmuir,2011,27(21):13212-13219.
[16]Won Bun Naa:Hyung Mi Lim:Soo Hyun Huh.Effect of the average particlesize and the surface oxidation layer of silicon on thecolloidal silica particle through direct oxidation[J].Materials Science and Engineering,2009,163:82-87.
[17]张霞,高大明.二氧化硅纳米粒子制备的工艺参数研究[J].安徽师范大学学报,2008(5):257-261.
[18]PAN Q X,PAN H H,CHEN J H.Sol-Gel technology and preparation of nano sized materials[J].Mater Res,2001,15(12):40-42.
[19]Won Bun Naa;Hyung Mi Lim;Soo Hyun Huh.Effect of the average particle size and the surface oxidation layer of silicon on the colloidal silica particle through direct oxidation[J].Materials Science and Engineering,2009,163:82-87.
[20]秦英,武鹏,吕毅军,等.硅溶胶的制备及其性能指标分析[J].天津化工,2013(5):4-7.
[21]邱春阳,张克铮.二氧化硅溶胶稳定性的研究[J].辽宁石油化工大学学报,2005(6):1-4.
[22]Wilhelm.The Physical chemistry of the silicate Chicago[M].The University of Chicago Publishing House,1954:426.
[23]江云波,李小霞,张克铮.正交试验法研究ZrO2/SiO2复合溶胶稳定性[J].石油化工高等学校学报,2010(12):64-67.
[24]杨靖,陈杰璐,等.二氧化硅溶胶的制备及性能影响研究[J].硅化物文摘.
[25]朱慧仙,王力.酸性硅溶胶的制备、性质及其稳定性研究进展[J].广东化工,2008,35(2):19-22.
[26]刘娟娟,王元政.硅溶胶稳定性能的影响因素分析[J].石化技术与应用,2009(9):421-423.
[27]赵庆祥,齐笑梅,等.SiO2无机涂抹液稳定性的研究[J].玻璃与搪瓷,2013(10):1-5.
[28]高建东.无机富锌底漆固化剂影响因素的研究[J].涂料工业,1998(3):11-13.
[29]王兴利,邱国民,等.SiO2溶胶稳定性的正交试验[J].辽宁石油化工大学学报,2006(3):30-33.
[30]张丹,王世敏,等.硅溶胶稳定性影响因素的研究进展[J].胶体与聚合物,2011(6):88-90.
[31]刘羽,吴东兵,等.Sol—Gel法二氧化硅溶胶的制备及稳定性研究[J].延安大学学报,2009(9):70-73.
[32]Schwartz R W,Voigt J A,Control of thin film processing behavior through precursor structural mcktifications[R].US:department of energy,1998.

