秦巴杜仲雄花总黄酮的提取及抗氧化稳定性研究
史 娟,李 江,葛红光
(陕西理工学院化学与环境科学学院,陕西汉中723000)
秦巴杜仲雄花总黄酮的提取及抗氧化稳定性研究
史娟,李江,葛红光
(陕西理工学院化学与环境科学学院,陕西汉中723000)
以秦巴杜仲雄花为原料,采用微波预处理-乙醇回流法,在不同的乙醇浓度、提取温度、提取时间和料液比下,探讨秦巴杜仲雄花总黄酮的提取工艺。通过清除DPPH自由基法测定总黄酮的抗氧化活性,并研究不同条件下总黄酮抗氧化稳定性。结果表明,乙醇浓度为60%,温度为80℃,时间为2.5 h,料液比为1∶60时,杜仲雄花总黄酮得率最高,达到2.983%。温度和金属离子Na+、K+、Ca2+、Mg2+对杜仲雄花总黄酮清除DPPH自由基的能力影响不大;金属离子Cu2+、Zn2+以及pH、光照对抗氧化能力影响较大。
杜仲雄花,总黄酮,提取,抗氧化,稳定性
秦巴山区是中国自然环境的十字交叉带,兼有东西南北复杂的生态环境特点,药用植物资源丰富。杜仲是杜仲科(Eucommiaceae)、杜仲属,多年生落叶乔木,在陕南秦巴山区资源丰富。因其产量大、质量佳、药效高,居全国四大名杜仲之首,被誉为“秦巴杜仲”。杜仲在中药古典《神农本草经》、《本草纲目》中就被列为药之上品,是中国特有的珍贵木本药用植物,传统以皮入药[1]。目前,对于杜仲的研究主要集中在杜仲皮、杜仲叶中黄酮等有效成分的提取及含量测定[2-4]。现代研究表明:杜仲黄酮具有抗自由基、抗氧化、抑菌、降脂减肥、抗病毒等作用[5]。
杜仲为雌雄异株植物,雄株占40%~60%。杜仲在我国栽种面积约36×104hm2,花量大,据估计每年有30 kt的产花量,资源丰富[6]。研究证明,杜仲雄花的黄酮类化合物含量高于杜仲皮和叶,并富含绿原酸、矿质元素和多种氨基酸,具有较高的营养价值及医疗保健作用[7]。目前,有关杜仲雄花中黄酮有效成分的提取、抗氧化活性研究较少[8-10],研究外界因素对其抗氧化稳定性影响的报道尚未见到。为此,本文对秦巴杜仲雄花总黄酮进行提取、并对其抗氧化稳定性进行分析,以期为杜仲雄花可能作为抗氧化剂来源的开发应用提供基础数据。
1 材料与方法
1.1材料与仪器
杜仲雄花采于汉中市陕西理工学院院内;芦丁对照品中国药品生物制品检定所;DPPH(1,1-二苯基-2-苦肼基)美国Sigma-Aldrich公司;无水乙醇、亚硫酸钠、硝酸铝、浓盐酸、氢氧化钠、氯化钠、氯化钾、氯化钙、氯化镁、氯化铜、氯化锌等试剂均为分析纯。
DGG-9140B型电热恒温鼓风干燥箱上海森信实验仪器有限公司;AL204-IC型电子分析天平梅特勒-托利多仪器上海有限公司;TDL-5台式离心机上海安亭科学仪器厂;WP700型微波炉佛山市格兰仕微波炉电器有限公司;RE-2A型旋转蒸发仪上海亚荣生化仪器厂;722-E型紫外可见分光光度计上海精密仪器科学有限公司。
1.2实验方法
1.2.1提取工艺流程新鲜杜仲雄花→烘干→研碎→微波预处理→乙醇回流→抽滤提取液→得黄酮提取物。
1.2.2芦丁标准曲线的绘制精确称取经105℃干燥至恒重的芦丁标准品7.5 mg,加乙醇溶解并定容至50 mL,配成150 mg/L的芦丁标准溶液。准确吸取标准品溶液0.0、0.5、1.0、1.5、2.0、2.5、3.0、3.5 mL,移入10 mL刻度比色管中,分别加入5%亚硝酸钠0.3 mL,摇匀后放置6 min;加入10%硝酸铝溶液0.3 mL,摇匀后放置6 min;加入4%氢氧化钠溶液2 mL,用乙醇溶液定容至刻度,10 min后在510 nm处测定不同浓度芦丁的吸光度,得到芦丁浓度C(mg/mL)与吸光度A的回归方程。
1.2.3杜仲雄花总黄酮提取及含量测定精确称取1.0 g干燥杜仲雄花粉末,置于250 mL圆底烧瓶中加入一定体积及浓度的乙醇溶液,在固定微波功率(500 W)下处理5 min后,在一定温度下、回流一定时间后,抽滤并定容至50 mL容量瓶中,510 nm处测定提取液的吸光度,并计算其总黄酮得率。总黄酮得率(%)=总黄酮浓度×提取体积×稀释倍数/杜仲雄花重量×100。
1.2.4杜仲雄花总黄酮提取的单因素实验
1.2.4.1乙醇浓度对总黄酮得率的影响杜仲雄花总黄酮提取中,固定微波预处理时间5 min,料液比1∶40,回流温度60℃,提取时间2 h,改变乙醇浓度为30%、45%、60%、75%、90%,研究溶剂浓度对得率的影响。
1.2.4.2提取温度对总黄酮得率的影响以60%乙醇为溶剂,杜仲雄花微波预处理时间5 min后,固定料液比1∶40,提取时间2 h,改变提取温度为50、60、70、80、90℃,考察温度对总黄酮得率的影响。
1.2.4.3提取时间对总黄酮得率的影响杜仲雄花总黄酮提取中,以60%乙醇为溶剂,样品微波预处理5 min后,固定料液比1∶40,提取温度80℃,改变提取时间为1、1.5、2、2.5、3 h,考察时间对得率的影响。
1.2.4.4料液比对总黄酮得率的影响以60%乙醇为溶剂对杜仲雄花微波处理5 min后,设置提取温度为80℃,浸提时间2 h,改变料液比1∶20、1∶30、1∶40、1∶50、1∶60,研究料液比对总黄酮得率的影响。
1.2.5杜仲雄花总黄酮提取的正交实验在单因素实验的基础上,以乙醇浓度、提取温度、提取时间和料液比为因素,设计L9(34)实验确定微波预处理-乙醇回流法的最佳提取工艺,因素水平见表1。
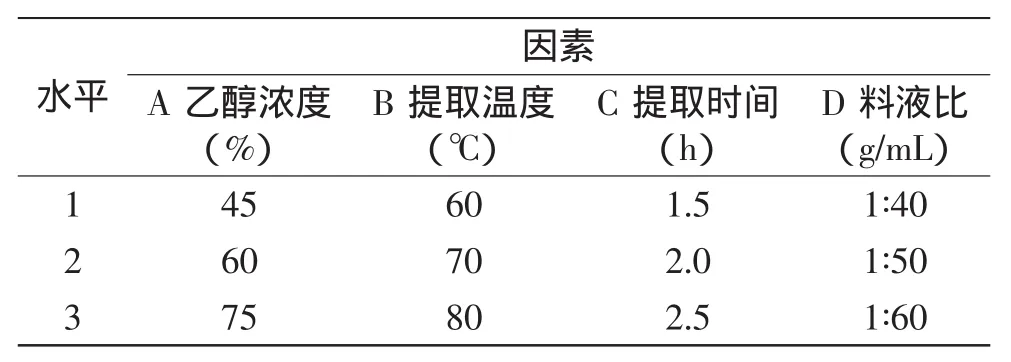
表1 L9(34)正交实验因素水平表Table 1 Factors and levels of L9(34)orthogonal experiments
1.2.6杜仲雄花总黄酮对DPPH自由基的活性测定采用清除DPPH自由基的能力,测定杜仲雄花总黄酮抗氧化活性[11]。测定时,在10 mL比色管中依次加入2.0 mL 2.0×10-4mol/L DPPH溶液和2.0 mL无水乙醇,混匀、静置30 min后,用1 cm比色皿在510 nm波长处,测吸光度值,记为A0;加入2.0 mL 2.0×10-4mol/L的DPPH溶液和2 mL杜仲雄花总黄酮试样混匀后测定吸光度值,记为Ai。杜仲总黄酮试样浓度设置6个梯度,每一吸光度平行测定3次,取其平均值,按下公式计算清除率:清除率(%)=[(A0-Ai)/A0]×100。
以样品浓度为横坐标,以清除率为纵坐标作图,得到杜仲雄花总黄酮浓度与自由基清除率的关系。
1.2.7杜仲雄花总黄酮抗氧化稳定性
1.2.7.1温度对杜仲雄花总黄酮抗氧化稳定性的影响取5 mL质量浓度为380 μg/mL的杜仲雄花总黄酮溶液(据1.2.6实验结果选择)置于有盖试管中,分别于40、50、60、70、80、90、100℃的恒温水浴中加热1、3、6 h,以不做温度处理的总黄酮溶液为对照,测定其对DPPH自由基的清除率。
1.2.7.2光照对杜仲雄花总黄酮抗氧化稳定性的影响取5 mL质量浓度为380 μg/mL的杜仲雄花总黄酮溶液置于烧杯,在日光灯箱内连续照射,并以未光照样品作对照,每隔3 d测定1次其对DPPH自由基的清除率。
1.2.7.3pH对抗氧化稳定性的影响取5 mL质量浓度为380 μg/mL的杜仲雄花总黄酮溶液6份,分别置于6个小烧杯中,用稀盐酸和氢氧化钠溶液调整pH为2、6、7、8、10、12。室温下放置2 h后,取样测定其对DPPH自由基的清除率。
1.2.7.4金属离子对抗氧化稳定性的影响取5 mL质量浓度为380 μg/mL的杜仲雄花总黄酮溶液,分别添加浓度为50、100、150、200、250、300、350 mg/L的Na+、K+、Mg2+、Ca2+、Zn2+、Cu2+溶液,室温下放置2 h后,取样测定其对DPPH自由基的清除率,以不加金属离子的提取液作为对照。
1.3数据分析
实验数据均为3次重复,取平均值,数据分析采用Origin8.0软件。
2 结果与分析
2.1芦丁标准曲线
以芦丁浓度C(mg/mL)为横坐标,吸光度A为纵坐标,得到回归方程式:A=17.519C-0.011,R2=0.9993,表明芦丁浓度与吸光度有良好的线性关系,可将其应用于总黄酮得率的测定中。
2.2杜仲雄花总黄酮提取的单因素实验结果
2.2.1最佳乙醇浓度的选择通过改变乙醇浓度,研究其对总黄酮得率的影响。如图1所示,在乙醇浓度为30%~60%内,随着乙醇浓度的增大,杜仲雄花总黄酮的得率逐渐增加,这是因为黄酮类化合物较易溶于乙醇,乙醇含量越大,杜仲雄花中黄酮化合物的析出就越多。当乙醇浓度为60%时,得率最大。但当乙醇浓度过高时,会导致其他脂溶性物质杂质同时溶出,干扰黄酮类化合物的测定[12]。故提取杜仲雄花总黄酮时,选择最佳乙醇浓度为60%。
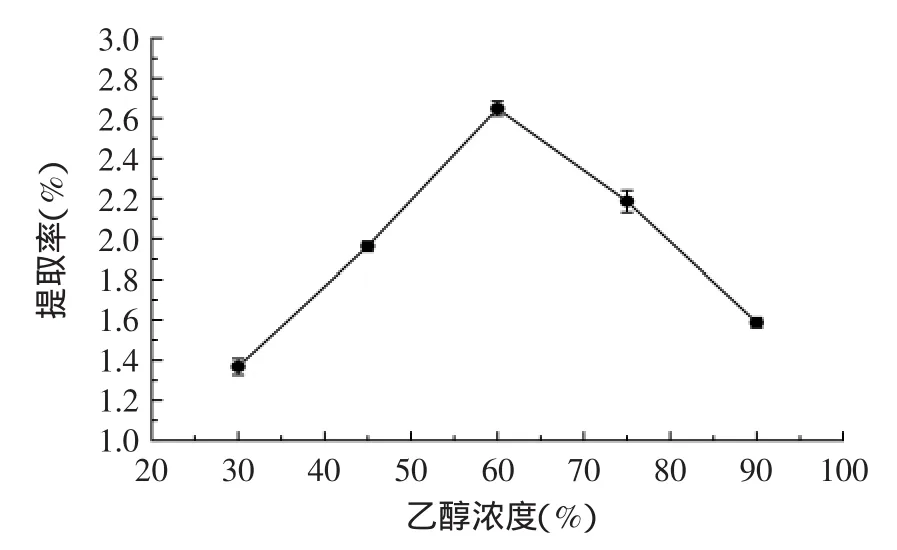
图1 乙醇浓度对总黄酮得率的影响Fig.1 Effect of ethanol concentration on the yield of total flavone
2.2.2最佳提取温度的选择在图2中,随着温度升高,杜仲雄花总黄酮得率呈增加趋势,因为随温度升高,分子运动加快,溶质分子与溶剂分子能够充分接触,黄酮类化合物更易从细胞中转移至溶剂[11-12]。当温度高于70℃时,杜仲雄花总黄酮得率下降;因为过高的提取温度,可能导致活性成分结构遭到破坏,且杂质溶出量也相应增大。所以,选择最佳提取温度为70℃。
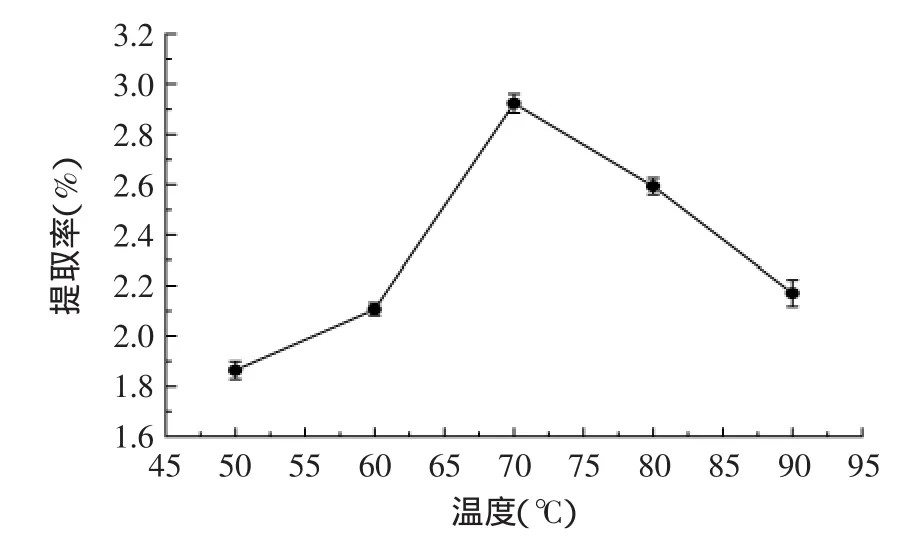
图2 提取温度对总黄酮得率的影响Fig.2 Effect of extraction temperature on the yield of total flavone
2.2.3最佳提取时间的选择图3的实验结果表明:在一定范围内,随着提取时间的增长,杜仲雄花总黄酮的得率随之上升,在2.0 h时达到最大值。主要原因是时间过短,黄酮类化合物还未充分溶出,时间在2.0 h时黄酮类化合物溶出已达到平衡;再延长时间,一些热敏性组分被破坏,或者溶剂挥发导致乙醇浓度降低,而使黄酮类化合物得率降低。所以2.0 h为提取较适宜时间。
2.2.4料液比对总黄酮得率的影响如图4所示,随着料液比的增大,杜仲雄花总黄酮的得率逐渐增大,在1∶50时得率最大;再增加料液比,总黄酮得率下降。因此,在保证提取效果的同时,应尽量减少溶剂的用量,降低减压浓缩消耗的能量。选择料液比1∶50为适宜条件。
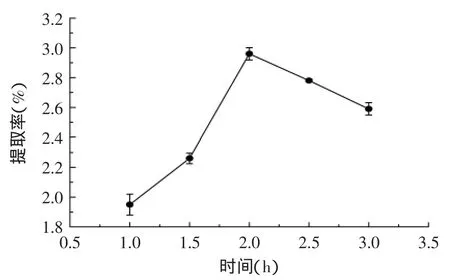
图3 提取时间对总黄酮得率的影响Fig.3 Effect of extraction time on the yield of total flavone
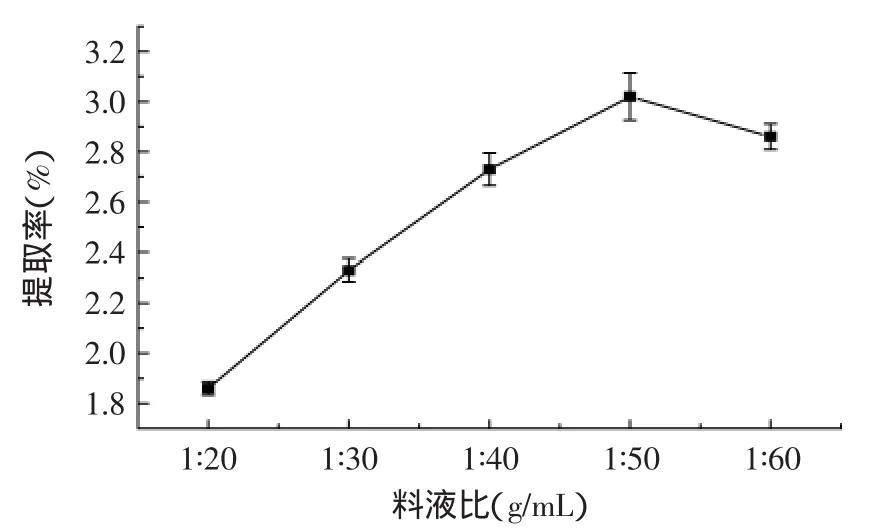
图4 料液比对总黄酮得率的影响Fig.4 Effect of material/liquid ratio on the yield of total flavone
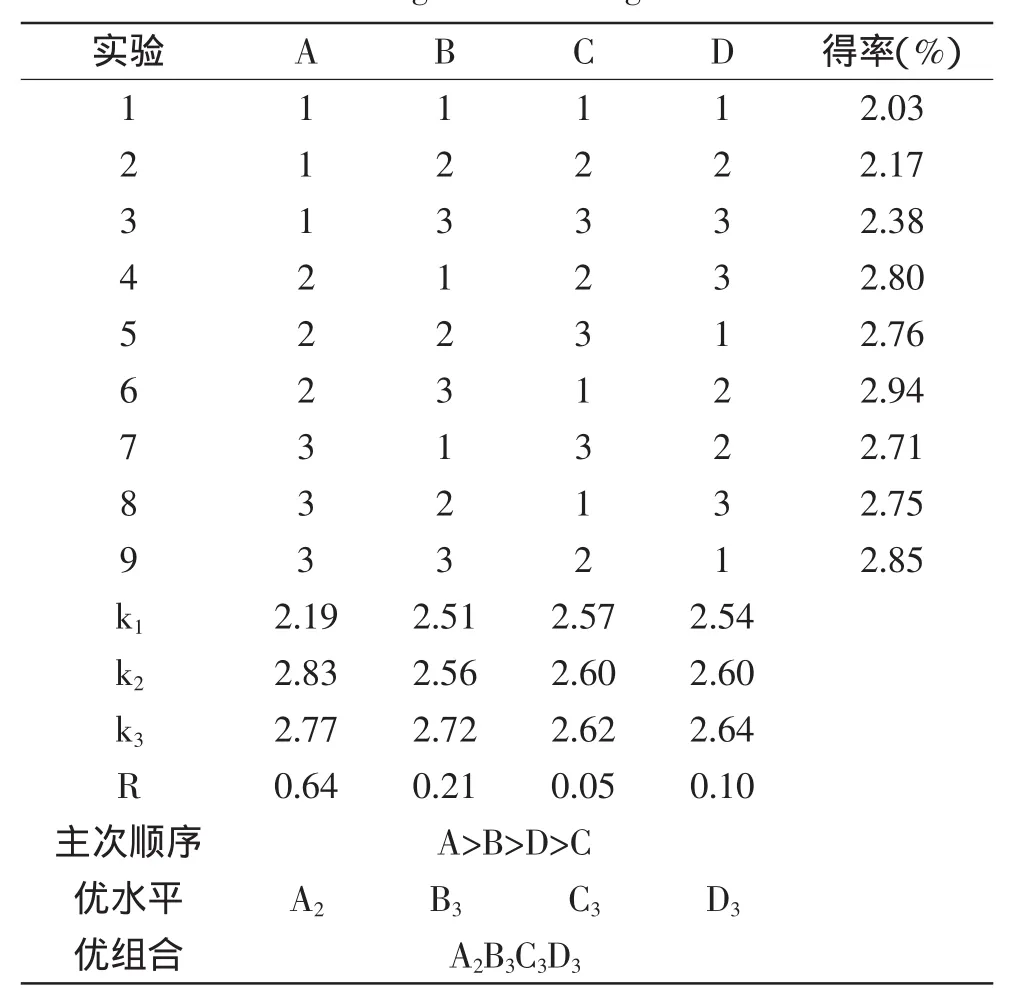
表2 正交实验结果Table 2 Orthogonal test design and results
2.3正交实验结果
2.3.1正交实验结果由表2可知,各因素对杜仲雄花总黄酮得率的影响大小是A>B>D>C,即乙醇浓度影响最大,提取温度影响其次,时间影响最小。杜仲雄花有效成分的最佳提取工艺是A2B3C3D3,即乙醇浓度为60%,提取温度为80℃,时间为2.5 h,料液比为1∶60。表3方差分析结果显示,乙醇浓度对黄酮得率的影响最大,为显著性因素。
2.3.2验证性实验为进一步考察上述优选工艺的稳定性,按上述最佳条件:乙醇浓度为60%,提取温度为80℃,时间为2.5 h,料液比为1∶60,进行三次平行实验。用紫外分光光度法测定其吸光度,并计算出杜仲雄花总黄酮的得率,得到的平均得率为2.983%。
2.4杜仲雄花总黄酮清除DPPH自由基能力
采用清除DPPH自由基的能力,测定杜仲雄花总黄酮抗氧化活性,结果如图5所示。在设定的浓度范围内,杜仲黄酮清除自由基的能力与样品浓度具有较好浓度-效应依赖关系。拟合方程为Y=0.00922X+ 2.512(R2=0.9906)。
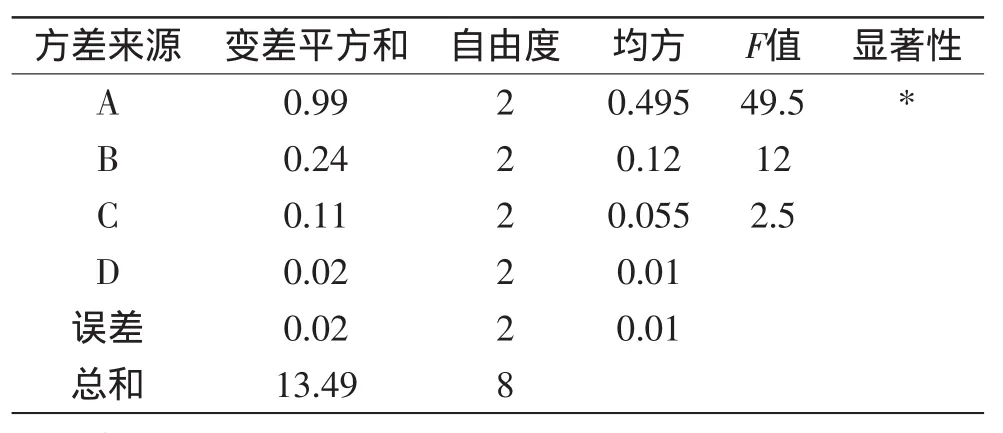
表3 正交实验方差分析Table 3 Analysis of variance
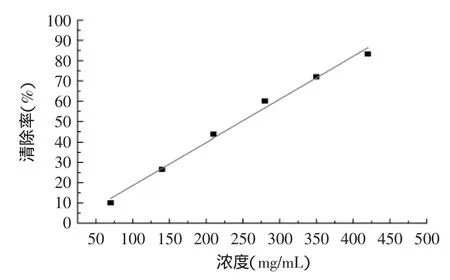
图5 杜仲雄花总黄酮对DPPH自由基清除的能力(n=3)Fig.5 Scavenging ability of total flavone from male flowers of Eucommia ulmoides(n=3)
2.5杜仲雄花总黄酮抗氧化稳定性
2.5.1温度对抗氧化稳定性的影响与室温未做加热处理杜仲黄酮清除率相比(清除率保持在82.1%~83.4%),图6的40~100℃范围内,杜仲雄花总黄酮对DPPH自由基的清除作用随着温度的升高,缓慢下降。且下降幅度同时还受热处理时间的影响:时间越长,抗氧化稳定性下降越大。但总体而言,杜仲雄花总黄酮在高温下仍可表现出较强的抗氧化性,温度对抗氧化能力的影响不明显。
2.5.2光照对抗氧化稳定性的影响在图7中,杜仲雄花总黄酮对DPPH自由基的清除作用随着光照时间的延长,不断减弱;直至光照8 d后下降至54.1%,此后趋于平缓。光照实验前后,清除率下降达28.3%;而未光照样品的对照组,清除率下降仅有5.2%。说明杜仲雄花总黄酮在光照条件下不稳定。主要是因为黄酮类化合物结构中多含有酚羟基,光照下易被氧化为醌类物质,从而导致其抗氧化性减弱。
2.5.3pH对抗氧化稳定性的影响由图8可知,杜仲雄花总黄酮对DPPH自由基的清除作用在酸性条件下较稳定,抗氧化能力较强。当pH大于7时,清除率迅速下降,至pH为12时,清除率仅为39.7%。这主要受到黄酮类化合物自身结构的影响,在碱性条件下,结构中所含酚羟基已被破坏,而导致抗氧化活性降低。
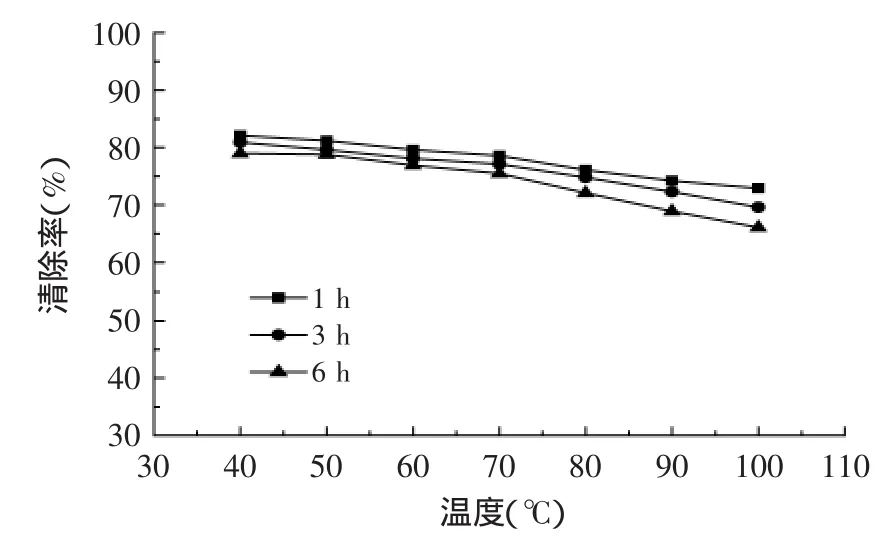
图6 温度对杜仲雄花总黄酮清除DPPH自由基的影响Fig.6 Effect of temperature on antioxidant stability of total flavone from male flowers of Eucommia ulmoides
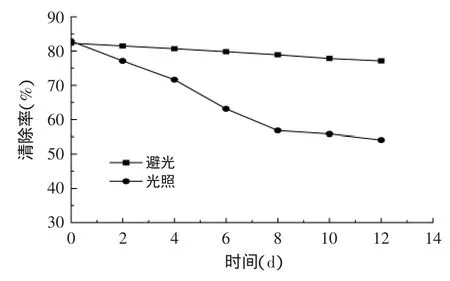
图7 光照对杜仲雄花总黄酮清除DPPH自由基的影响Fig.7 Effect of illumination on antioxidant stability of total flavone from male flowers of Eucommia ulmoides
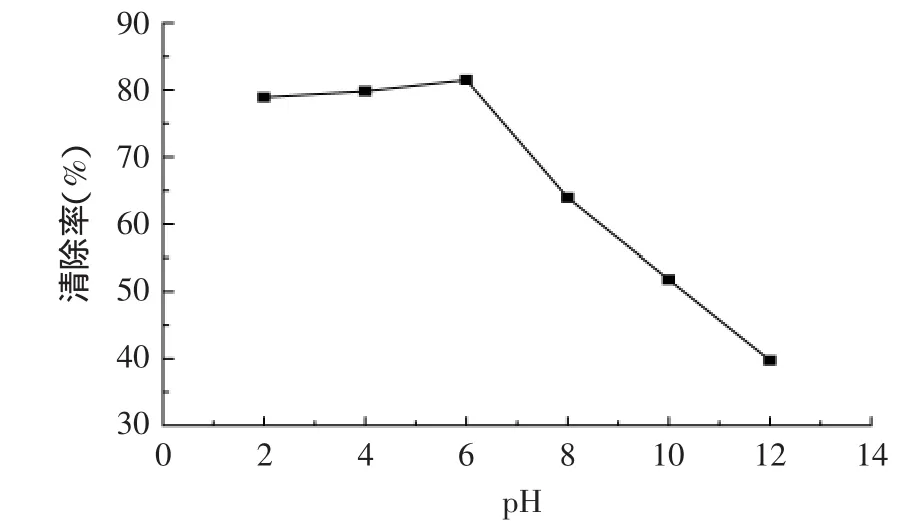
图8 pH对杜仲雄花总黄酮清除DPPH自由基的影响Fig.8 Effect of pH on antioxidant stability of total flavone from male flowers of Eucommia ulmoides
2.5.4金属离子对抗氧化稳定性的影响在表9所示的实验浓度范围内,Na+、K+、Mg2+、Ca2+对杜仲雄花总黄酮清除DPPH自由基活性影响较小;而Zn2+、Cu2+影响较大,且随着金属离子浓度的增加,抗氧化活性呈下降趋势。分析原因,可能与黄酮类化合物结构中所含酚羟基或羰基,可与某些金属离子进行络合致使其性质发生改变,从而降低了抗氧化活性。
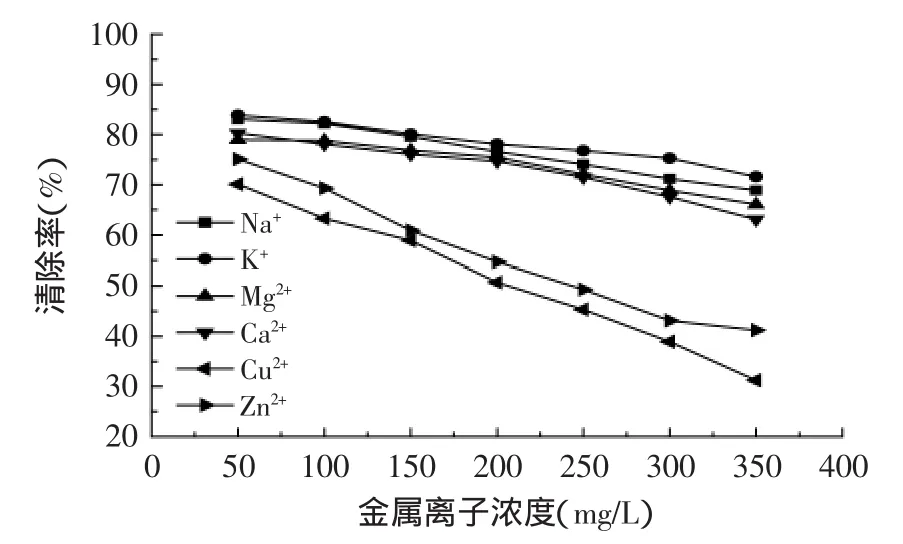
图9 金属离子对杜仲雄花总黄酮清除DPPH自由基的影响Fig.9 Effect of metal ions on antioxidant stability of flavone from male flowers of Eucommia ulmoides
3 结论
通过微波预处理-乙醇回流法对杜仲雄花黄酮进行了提取,得到最佳提取工艺是乙醇浓度60%,提取温度80℃,时间为2.5 h,料液比1∶60,该条件下杜仲雄花总黄酮得率为2.983%。温度及Na+、K+、Ca2+、Mg2+四种金属离子对总黄酮清除DPPH自由基的能力影响不大;而金属离子Cu2+、Zn2+以及pH、光照对抗氧化能力影响较大。因此,在对杜仲雄花总黄酮的制备和使用过程中,应避免强碱或强光条件下保存;同时要注意避免与一些高浓度金属离子Cu2+、Zn2+的接触。
[1]管淑玉,苏薇薇.杜仲化学成分及药理活性研究进展[J].中药材,2003,26(2):124-129.
[2]孙兰萍,马龙张斌,等.杜仲黄酮类化合物的研究进展[J].食品工业科技,2009,30(3):359-363.
[3]赵文红,范青生,马永花,等.杜仲叶中总黄酮的醇提工艺[J].南昌大学学报:理科版,2007,31(1):69-72.
[4]刘军海,任惠兰,裘爱泳,等.杜仲叶中总黄酮提取工艺研究[J].食品与机械,2007,34(4):92-95.
[5]晏媛,郭丹.杜仲叶的化学成分及药理活性研究进展[J].中成药,2003,25(6):491-492.
[6]董发明,白喜婷.响应面法优化超声提取杜仲雄花中黄酮类化合物的工艺参数[J].食品科学,2008,29(8):227-231.
[7]董娟娥,梁宗锁,张康健,等.杜仲雄花中次生代谢物合成积累的动态变化[J].植物资源与环境学报,2005,14(4):7-10.
[8]丁艳霞,郭洋静,任莹璐.杜仲雄花中黄酮类化学成分及其抗氧化活性研究[J].中草药,2014,45(3):323-327.
[9]李旭,刘停.杜仲叶总黄酮微波辅助提取工艺的优化及其抗氧化活性研究[J].食品工业科技,2013,34(4):243-248.
[10]白喜婷,朱文学,罗磊,等.杜仲雄花茶中黄酮类化合物的提取工艺研究[J].食品研究与开发,2008,29(11):96-100.
[11]程一鑫,马龙,张斌,等.大豆异黄酮抗氧化稳定性研究[J].食品研究与开发,2011,32(9):144-146.
[12]刘军海.杜仲叶中总黄酮类成分提取工艺研究[J].食品研究与开发,2006,27(8):129-132.
Extraction of flavone from male flowers of Qinba Eucommia ulmoides and their antioxidant stability
SHI Juan,LI Jiang,GE Hong-guang
(School of Chemistry and Environment Science,Shaanxi University of Technology,Hanzhong 723000,China)
The extraction process of flavone in male flowers of Qinba Eucommia ulmoides assisted by microwave pretreatment was studied.The flavone extraction from the different ethanol concentration,extraction time,extraction temperature and solid-to-liquid ratio were studied.And the antioxidant stability of total flavonoe was assessed by its capacity to scavenge the DPPH free radical under different treatments.The results showed that the best extraction process condition was:ethanol concentration 60%,abstracting temperature 80℃,abstracting time 2.5 h and the ratio of solid to extracting liquid 1∶60(g/mL).The total flavone extraction yield could reach 2.983%in the optimum conditions.The temperature and metal ions(Na+,K+,Ca2+,Mg2+)did not produce a great reduction of scavenging capacity.While the Zn2+,Cu2+,pH and illumination had a bigger influence to the antioxidation stability of flavone in male flowers of Qinba Eucommia ulmoides.
male flowers of Eucommia ulmoides;total flavone;extraction;antioxidant;stability
TS201.1
B
1002-0306(2015)16-0252-05
10.13386/j.issn1002-0306.2015.16.043
2014-12-08
史娟(1978-),女,在读博士,副教授,研究方向:天然产物化学和有机合成,E-mail:hzhshijuan@126.com。
国家自然科学基金(21373132);教育厅2012年科学研究项目(12JK0633)。

