以特异性皮损为首发症状的急性单核细胞白血病一例
崔晶 倪明 董正邦 陈梅 王飞
·病例报告·
以特异性皮损为首发症状的急性单核细胞白血病一例
崔晶 倪明 董正邦 陈梅 王飞
患者男,78岁,因全身泛发丘疹20余天于2014年3月11日入我院。入院20余天前胸部无明显诱因出现红色丘疹、结节,无疼痛、瘙痒、破溃,压之不褪色,逐渐遍及全身,伴双上肢及口周麻木。既往体质差,有前列腺癌、心律失常、颈椎病、白内障、高血压病史,无家族遗传性疾病病史。
体检:结膜、口唇苍白。无发热,未触及肝、脾、淋巴结肿大,牙龈无增生。无皮下出血。全身泛发性丘疹、结节(图1),绿豆至蚕豆大小,淡红色至棕色,质韧,表面光滑,浸润明显,无破溃及出血。实验室及辅助检查:血常规白细胞26.49×109/L,血红蛋白144 g/L,血小板77×109/L。尿粪常规未见异常。生化检查无异常。皮损组织病理检查:表皮基本正常,未见细胞移入,真皮内弥漫性肿瘤细胞浸润,与表皮间隔以无细胞浸润带(图2)。肿瘤细胞在胶原束间呈线状浸润,细胞呈单核细胞样,部分核大异形(图3)。免疫组化:髓过氧化物酶(MPO)(图 4)、CD56、溶菌酶、CD68、CD163 均阳性,CD34、CD117、CD3、CD20 均阴性,ki67> 90%阳性。骨髓穿刺:骨髓增生极度活跃,粒系占31.6%,红系占3.6%。单核细胞显著增生,幼稚单核细胞占42.4%,其他细胞胞体大小不一,胞质较丰富,色灰蓝,偶见空泡,可见天青颗粒;核大,不规则,染色质较粗,部分有扭曲、折叠、条索感,偶见核仁。成熟单核细胞比例增高。细胞组化检查:过氧化酶染色(POX)51%(± ~ +),过碘酸雪夫染色(PAS)(±),α 醋酸萘酚酯酶(α-NAE)染色(±),氟化钠(NaF)抑制(+)。骨髓细胞流式细胞仪检测 HLA-DR+24.44%,CD38+26%,CD13+56.02% ,MPO+58.08% ,CD10+38.10% ,CD15+70.56% ,CD11b+83.88%,CD4+24.97%,CD56+26.35%。基因遗传学检测:BCR-ABL阴性,早幼粒细胞白血病-维甲酸α受体融合基因(PML-RARα)阴性,FLT3/ITD、C-KIT D816V、NPM1、CEBPA突变均为阴性。染色体核型分析未见异常。诊断:以特异性皮损为首发症状的急性单核细胞白血病。
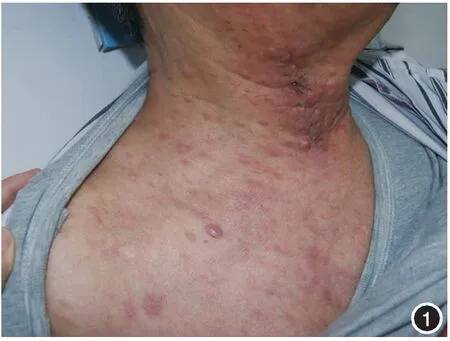
图1 患者全身泛发淡红色至棕色、质韧、大小不一的充实性丘疹、结节
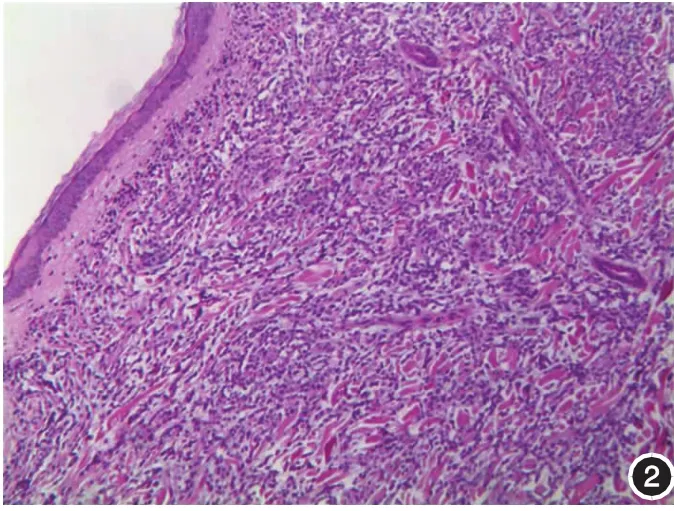
图2 真皮内弥漫性淋巴样肿瘤细胞浸润,真皮乳头层与表皮间形成明显无浸润带(HE×100)
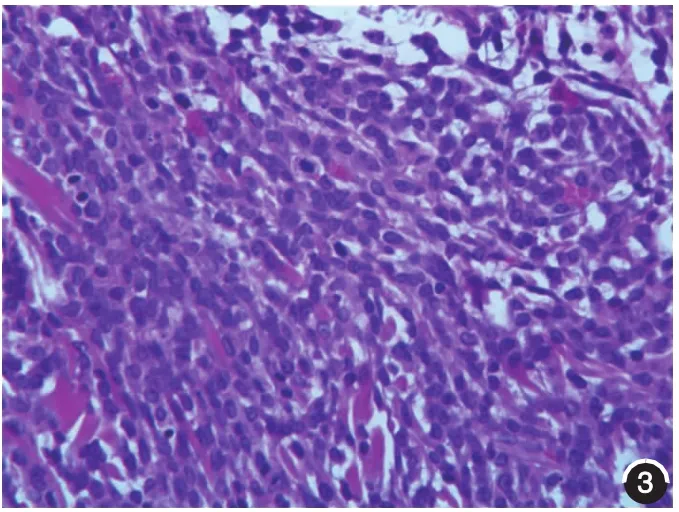
图3 肿瘤细胞胶原束间呈线状浸润,细胞呈单核细胞样,部分核大异形(HE×400)
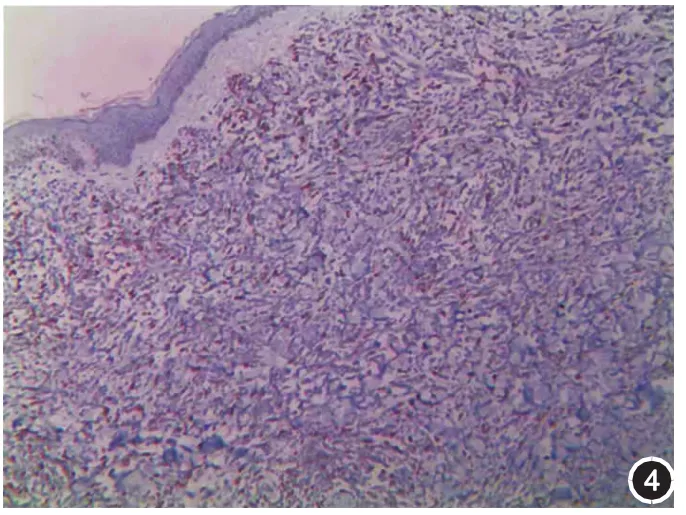
图4 皮损免疫组化染色,髓过氧化物酶阳性(DAB×100)
治疗过程:入院后予以小剂量CAG(阿糖胞苷+阿克拉霉素+粒细胞集落刺激因子)化疗,1个疗程后,皮疹逐步消退,无色素沉着。化疗结束后15 d,原发病(急性单核细胞白血病)部分缓解。其后患者多次复发,均伴有全身泛发性丘疹、结节,皮损逐渐密集,浸润明显。复发时感觉异常症状同前。相继予以CAG方案、IDA方案(去甲氧柔红霉素+阿糖胞苷)、DA-EPOCH(依托泊甙+多柔比星+长春新碱+环磷酰胺+地塞米松)、大剂量阿糖胞苷方案化疗。均可部分缓解,但易复发,缓解期短(仅2周左右)。缓解期皮疹可完全消退,不留痕迹。白血病确诊4个月后,患者出现黑便、肝功能损害、胆酶升高、左上肢肌力下降等表现。
讨论 白血病的皮肤表现称为皮肤白血病,常见于急性髓系白血病(AML)的法美英(FAB)分级中 M4、M5 亚型[1],包括特异性和非特异性损害。特异性皮损常表现为丘疹、斑疹、结节等,含有异常白细胞;非特异性皮损成多形性,无白血病细胞浸润。本例患者表现为全身泛发的红色充实性丘疹、结节,皮损组织病理可见弥漫性肿瘤细胞浸润;免疫组化MPO及溶菌酶阳性,提示为髓系来源;且血液学复发时皮损同步出现。故此患者皮肤改变为皮肤白血病的特异性皮损。
白血病的特异性皮损通常出现于白血病的最后阶段。极少数情况下,皮肤白血病出现在白血病的血象和骨髓象改变之前[2]。
作者单位:210009南京,东南大学附属中大医院皮肤性病科(崔晶、董正邦、陈梅、王飞),血液科(倪明)
表达CD56的髓系白血病被认为是一种具有高度侵袭性的恶性疾病,有预后差、易复发、易发生中枢浸润的特点。本病例为CD56阳性的急性单核细胞白血病(AML-M5),初期即出现大面积皮损,同时伴有麻木,提示存在周围神经浸润;化疗后期出现黑便等广泛浸润表现,可能与CD56表达相关。但其病理组织在镜下可见大量粒细胞及少量单核细胞浸润,在这些单核细胞中均有CD68及CD163的表达。
患者BCR-ABL融合基因,即t(9;22)(q34;q11)阴性,可排除慢性粒细胞白血病(CML);PML-RaRa融合基因,即t(15;17)(q22;q21) 阴性,可排除急性早幼粒细胞白血病(APL)。FLT3/ITD和C-KIT突变提示预后不良,NPM1和CEBPA双突变提示预后良好[3]。此患者染色体核型分析未见异常,预后基因检测为阴性。
[1]Chang H,Shih LY,Kuo TT.Primary aleukemic myeloid leukemia cutis treated successfully with combination chemotherapy:report of a case and review of the literature[J].Ann Hematol,2003,82(7):435-439.
[2]Hansen RM,Barnett J,Hanson G,et al.Aleukemic leukemia cutis[J].Arch Dermatol,1986,122(7):812-814.
[3] O′Donnell MR,Abboud CN,Altman JK,et al.Acute myeloid leukemia[J].J Natl Compr Canc Netw,2012,10(8):984-1021.
10.3760/cma.j.issn.0412-4030.2015.08.017
王飞,Email:ffwangfei@163.com
2014-10-13)
(本文编辑:颜艳)

