实验室条件下乙苯脱氢制苯乙烯反应条件研究
张淑霞 文萍


摘 要:苯乙烯是重要的有机化工原料。随着需求量的逐渐增加,苯乙烯的生产规模在逐渐的增大,生产方法也在不断的改进。乙苯脱氢法仍是其中的主要生产方法。在实验室的条件下,采用等温式乙苯催化脱氢小型装置,考察反应温度以及水和乙苯的进料比对实验结果的影响,并根据实验结果找出实验室条件下最佳的反应温度范围以及合适的进料比范围。
关 键 词:乙苯;苯乙烯;催化剂;反应温度;进料比
中图分类号:TQ 241.1 文献标识码: A 文章编号: 1671-0460(2015)06-1288-03
Study on Reaction Conditions for Preparing Styrene
via Dehydrogenation of Ethylbenzene at Laboratory
ZHANG Shu-xia, WEN Ping
(College of chemical Engineering, China University of Petroleum,Shandong Qingdao 266580,China)
Abstract: Styrene is an important organic chemical raw material. With gradual increase of demand, the production scale of styrene increases gradually, the production method is continually improved. But ethylbenzene dehydrogenation method is still a main production method. In this paper, under the laboratory condition, the influence of different process parameters on the experimental results was studied, and finally the best reaction conditions were obtained.
Key words: Ethylbenzene;Styrene;Catalysts;Reaction temperature;Feed ratio
苯乙烯是高分子合成材料的一種重要单体,是重要的基本有机原料,是三大高分子合成材料的重要单体,其用途十分广泛。近年来,苯乙烯的需求在逐年增加,苯乙烯的生产规模和成本也在逐年增加。目前,苯乙烯生产方法主要有乙苯脱氢法、乙苯共氧化法、甲苯为原料合成苯乙烯法、乙苯氧化脱氢法等,用的最多的就是乙苯脱氢法[1,2]。
乙苯脱氢反应是个复杂反应,从热力学上讲,裂解反应比脱氢反应有利,加氢裂解反应也比脱氢反应有利,即使在高温下,加氢裂解的平衡常数仍然很大[3,4]。故乙苯在高温下进行脱氢时,主要产物是苯,而要使主反应顺利进行,必须采用高活性、高选择性的催化剂。
本次实验选用的是铁系催化剂,主要组分为活性相Fe3O4,助剂为K2O和Cr2O3[5,6]。使用之前先将催化剂活化,使之具有活性,活化温度要在反应时的最高温度之上,如果活化程度不够,那么苯乙烯的收率会较低。反应结束后要继续通水蒸气进行清焦,大约半小时,消除反应过程中的积碳,延长催化剂使用寿命。
本文利用等温式乙苯催化脱氢小型实验装置,以乙苯和水为原料,选用氧化铁系催化剂,考察不同的反应温度和进料比对乙苯的转化率、苯乙烯的选择性和收率的影响[7,8]。
1 实验部分
1.1 主要实验原料
乙苯、蒸馏水。
1.2 主要实验仪器
乙苯脱氢制苯乙烯实验装置、气相色谱仪GC-950,主要流程见图1。
图1 实验装置及流程简图
Fig.1 The experimental device and flow diagram
1-气体钢瓶;2-减压阀;3-稳压阀;4-转子流量计;5-预热炉;6-预热器;7-反应炉;8-固定床反应器;9-冷凝器;10-气液分离器;11-取样器;12-湿式流量计;13-加料罐;14-进料泵
1.3 实验方法[9]
将乙苯和水通过计量泵进入预热器,预热器温度为300 ℃,使乙苯和水混合并汽化,之后进入到反应器,在装有催化剂的反应器中发生反应,反应产物经过循环冷却水冷凝,使气液分离,通过分离器分离气液两相,液相的粗产品通过分液漏斗去除水层,得到油层,油层部分用气相色谱分析其组成。
气相色谱采用氢火焰离子化检测器,氮气为载气,分析条件为:柱温120 ℃,汽化温度:150 ℃,检测器温度:150 ℃,柱前压0.07 MPa,进样量1 μL,催化剂用量为50 mL。
1.4 产物分析
实验所得到的粗产品用色谱分析后,得到其组分主要有苯、甲苯、乙苯和苯乙烯。其中苯和甲苯是主要的副产物。
2 结果分析与讨论
2.1 反应温度的影响
2.1.1 反应温度对反应产物组成的影响
控制预热器温度为300 ℃,乙苯进料速度0.5 mL·min-1,水进料速度0.75 mL·min-1,反应温度控制在540、560、580、600、620 ℃,考察不同温度下反应产物组成的变化,色谱分析数据结果见图2。
图2 反应产物主要组分随温度变化关系表
Fig.2 Change of main component in reaction product with temperature
由图2可以看出,反应产物中主要组分有苯、甲苯、乙苯和苯乙烯,其中苯和甲苯是主要的副产物,当反应温度由540 ℃升到620 ℃时,苯的含量由0.3%升到2%,甲苯的含量由1%升到4.3%,当温度升到600 ℃以后,由于副反应的加剧,副产物的含量增加的较快。随着温度升高,乙苯的含量下降加快,由540 ℃的85%下降到620 ℃的52%,下降幅度为60%。 因为此反应为吸热反应,温度越高,转化率也越高,由于受到实验室条件的限制,整个反应乙苯的转化率不是较高。苯乙烯的浓度也是逐渐升高,由540 ℃的12%升高到620 ℃的34%,增加了2.83倍,但是由图中可以看出,超过600 ℃以后苯乙烯的浓度增加的变慢。
2.1.2 反应温度对乙苯转化率、苯乙烯选择性、苯乙烯收率的影响
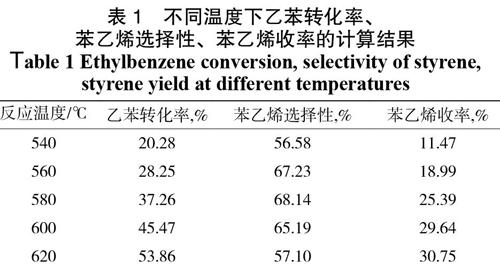
控制预热器温度为300 ℃,乙苯进料速度0.5 mL?min-1,水进料速度0.75 mL?min-1,反应温度控制在540~600 ℃,考察不同温度对乙苯转化率、苯乙烯选择性、苯乙烯收率的影响,数据结果见表1。
由表1可以看出,在540~620 ℃范围内,乙苯的转化率随温度的升高而升高,基本呈直线上升,由540 ℃时的20.28%升高到620 ℃的53.86%,提高了2.66倍。苯乙烯的选择性随温度的升高开始也升高,由540 ℃的56.58%升高到580 ℃的68.14%,提高了1.2倍,之后开始下降,到620 ℃下降为57.10%,主要原因是高温下发生了较多的副反应,致使苯乙烯的选择性开始下降,由表中曲线也可以看出苯乙烯的选择性随温度的变化影响不是很大。苯乙烯的收率随着温度的升高逐渐上升,超过600 ℃以后增加的开始变慢,主要原因是苯乙烯的选择性下降了。
表1 不同温度下乙苯转化率、
苯乙烯选择性、苯乙烯收率的计算结果
Table 1 Ethylbenzene conversion, selectivity of styrene, styrene yield at different temperatures
由上面实验结果可以看出,要得到较高转化率,就要求溫度较高,而高温时苯乙烯的选择性开始下降,所以综合这两个结果,找出一个实验室条件下的较合理的反应温度,使苯乙烯的收率较高,合理的温度范围应为560~600 ℃。
2.2 进料比的影响
控制预热器温度为300 ℃,反应器温度为580 ℃,考察不同的进料比条件下对乙苯转化率、苯乙烯选择性、苯乙烯收率的影响,进料比(V水∶V油)范围控制在1.2∶1~2.2∶1,实验结果见表2。
由表2可以看出,水和乙苯的进料比在1.2∶1到2.0∶1范围内,乙苯的转化率逐渐增大,由31.59%增加39.52%,增加了1.25倍,增幅不是很大,进料比超过2.0∶1后,乙苯的转化率开始下降。苯乙烯的选择性随着进料比的变化基本保持不变。苯乙烯收率随着进料比增加而缓慢上升,进料比增加到2.0∶1后收率也逐渐下降。
由此可以看出,进料比对乙苯转化率有影响,但是幅度不大;进料比对苯乙烯的选择性基本影响不大。由此根据节能和最佳收率的条件,确定实验室条件下最佳的进料比范围1.6∶1~1.8∶1。
表2 不同的进料比乙苯转化率、
苯乙烯选择性、苯乙烯收率的计算结果
Table 2 Ethylbenzene conversion rate, selectivity of styrene, styrene yield under different feed ratios
3 结 论
(1)根据乙苯催化脱氢的反应原理,我们分析了不同的反应温度和进料比对乙苯的转化率、苯乙烯的选择性以及苯乙烯收率的影响,实验结果表明反应温度的影响结果大于进料比。
(2)随着反应温度的升高,乙苯的转化率逐渐增大,苯乙烯的选择性和收率都是先增大后减小,主要原因是高温下副产物增多,得出最佳的反应温度为560~600 ℃。
(3)进料比对整个反应的影响不是很大,乙苯的转化率随着进料比增加稍微也增大,但是在进料比大于2后转化率开始下降,再综合考虑能耗的因素,确定最佳的进料比为1.6~1.8∶1。
参考文献:
[1]廖仕杰,陈铜,缪长喜,杨为民,谢在库,陈庆龄.乙苯脱氢制苯乙烯工业催化剂的失活原因[J].催化学报,2008,29(2):179-184.
[2] 邱宝军,李红娟.乙苯催化脱氢制苯乙烯技术研究进展[J].辽宁化工,2007,36(12):861-865.
[3] 童淮荣.苯乙烯及乙苯脱氢制苯乙烯催化剂的现状和发展[J].化学反应工程与工艺,2005,21(5):459-462.
[4] 魏狄,许峥,张继炎.乙苯脱氢制苯乙烯催化剂及工艺进展[J].石油化工,1995,24(3):215-220.
[5] 印会鸣,林宏,王继龙,王涛,姚文君,胡晓丽,柏介军,辛国萍.乙苯脱氢催化剂的发展现状[J].工业催化,2012,20(1):13-18.
[6]Zhu Xiaomeng,Schon M,Bartmann U.The Dehydrogenation of Ethylbenzene to Styrene Over a Potassium-Promoted Iron Oxide-based Catalyst:A Transient Kinetic Study[J].Appl Catal,A,2004,266(1):99-108.
[7]盛奎龙,毛元燕,裴松,郑立辉.乙苯脱氢制苯乙烯反应条件的研究[J].河南化工,2006,23(11):24-26.
[8] 徐志刚,钱志毅,俞丰,陈建春,李瑞江,朱子彬,朱中南.乙苯脱氢制苯乙烯反应器的技术进展[J].化学世界,2004,(1):49-52.
[9] 王彦杰,郭延红,高彩虹,朱晓龙.固定床乙苯脱氢制苯乙烯工艺条件的研究[J].化学与生物工程,2010,27(3):35-37.

