烤烟在惰性和含氧气氛中的热分析动力学研究
张晓宇等

摘要:采用热重分析法,以烤烟为材料,分别在纯氮气、氧气浓度为5%、10%的氮氧混合气氛中,对样品的热失重过程进行分析,并利用Flynn-Wall-Ozawa方法计算了热降解动力学参数。结果表明:在含氧气氛中,烟草样品的热分解主要包括5个热失重阶段,而在惰性气氛中,则表现为4个热失重阶段;在相同的升温速率下,氧气浓度的变化,对样品的第Ⅰ、Ⅲ 2个热失重阶段的温度范围、质量变化均没有明显的影响,而对后面的几个热失重阶段,尤其是对主反应区产生了较大的影响;动力学分析结果进一步显示,氧气浓度的变化没有改变前2个阶段的活化能,但却明显导致了主反应区活化能的变化。
关键词:烟草;热失重;氧气浓度;动力学
中图分类号: TS41+2文献标志码: A文章编号:1002-1302(2015)09-0323-04
卷烟的燃烧伴随着十分复杂的化学反应,其燃烧过程不仅依赖于烟草本身,而且也受燃烧环境条件的制约。卷烟的燃烧区域包括2个明显的反应区,即燃烧区和热解/蒸馏区[1]。在燃烧区中,氧气与焦炭化的烟草发生反应主要生成二氧化碳、一氧化碳、氢气以及水蒸汽等小分子气体物质,并释放出热量,从而维持卷烟的可持续性燃烧;在热解/蒸馏区中,化学反应是复杂的,卷烟烟气中的绝大多数化学成分都是在这一区域内产生的。研究表明,无论是燃烧区还是热解/蒸馏区都是缺氧的,卷烟中烟草的燃烧速率主要由进入烟草表面氧气的质量转移速率所控制,燃烧区域氧气浓度的高低不仅会影响卷烟的燃烧过程,也会对燃烧产物,即卷烟烟气产生明显的影响[2-4]。热重分析是指在程序控制温度下测量待测样品的质量与温度变化关系的一种热分析技术,已经成为研究包括烟草在内的生物质材料燃烧、热解过程及其动力学行为的有效技术手段[5-7]。因此,利用热重分析技术,对烟草在惰性和含氧气氛中的热失重行为和动力学过程进行比较研究,有助于深入了解氧气对卷烟燃烧过程的影响,从而为调控卷烟的燃烧提供理论基础。
1材料与方法
1.1材料与仪器
试验所用的材料为产自昆明市的2007年C2F烟叶。试验前,先将烟叶在40 ℃下经2h烘干后粉碎并过40目筛,密闭保存,备用。
试验仪器包括Netzsch STA 449C同步热分析仪(德国Netzsch公司);氧化铝坩埚(德国Netzsch公司);CP224S电子天平(感量:0.000 1 g,德国Satorius公司)。
1.2样品的热失重分析
取大约20 mg的烟叶粉末,置于氧化铝坩埚中进行热重分析。热解气氛为纯氮气、氧气的浓度分别为5%、10%的氧/氮混合气,所有载气的总流量均为100 mL/min;试验温度范围为30~1 000 ℃;升温速率分别为5、10、15、 20 ℃/min。为消除系统误差,保证试验结果的精确性,在每次样品测试之前做一个相同条件的基线校准。
2结果与分析
2.1惰性和含氧气氛中的热失重过程比较
图1-a至图1-d给出了升温速率分别为5、10、15、20 ℃/min 时,烟草样品在不同气氛中的热重(TG)及热失重(DTG)曲线。从图1中的DTG曲线可以清楚地看出,在各升温速率下的含氧气氛中,随着热解温度的不断升高,烟草样品均经历了5个明显的热失重阶段;而在惰性气氛中,则表现为第Ⅳ个热失重过程的消失,仅经历了4个热失重阶段。据文献报道[8-9],在含氧条件下烟草样品的5个热失重阶段质量损失的原因分别为:吸附水散失、挥发分析出并伴随着烟草组分的热分解、烟草生物聚合物的分解、焦炭燃烧、焦炭重排。因此,与含氧气氛相比较,烟草样品在惰性气氛中热解的一个明显的差异是焦炭燃烧过程的消失。
图1显示,各升温速率下,样品在不同气氛热解的TG和DTG曲线在第Ⅰ和第Ⅱ 2个失重阶段基本重合;数据分析结果进一步表明,在所有试验条件下,第I个热失重阶段质量的损失率为5.7%左右,第Ⅱ个热失重阶段为17.5%~22.4%,而且这2个热失重阶段质量的损失与氧气的存在与否无关,这表明热解气氛中氧气的存在及其浓度的高低对烟草样品热降解的前2个热失重阶段基本没有影响。
在第Ⅲ个热失重阶段,氧气对烟草样品热解的影响开始变得比较明显,这表现在各升温速率下的不同气氛中TG和DTG曲线开始出现分离;而且从DTG曲线上看,氧气的存在
及其浓度的升高会导致这一失重阶段移向低温区,表明此阶段氧气已经参与了化学反应,并促进了烟草生物聚合物的热解,这一观察结果与Senneca等在相近的试验条件下所报道的结果[10]相一致。随着反应温度的继续升高,氧气对样品热解的影响变得更加强烈,与惰性气氛中相比,氧气的存在导致了第Ⅳ个热失重阶段的出现,而且随氧气浓度的增加,第Ⅳ个热失重阶段的温度范围明显变窄,这表明氧气浓度的升高会加速燃烧反应的进行。另外,在所有的升温速率下,烟草样品在惰性气氛中第Ⅲ个热失重阶段质量损失为42.7%~468%;而在氧化气氛中第Ⅲ、第Ⅳ个热失重阶段质量损失分别为30.0%~39.0%、29.3%~35.1%。因此,从质量的损失率情况看,惰性气氛中的第Ⅲ个热失重阶段以及氧化气氛中的第Ⅲ、第Ⅳ个热失重阶段为烟草样品的热解主反应区。由于惰性气氛中第Ⅲ个热失重阶段的温度范围与氧化气氛中第Ⅲ、第Ⅳ 2个热失重阶段的温度范围是相对应的,因此在该温度区间内,氧化气氛中的质量损失要明显较惰性气氛中高。
在最后一个热失重阶段,所有的升温速率下惰性气氛中烟草样品的质量损失为6.0%~10.3%;而氧化气氛中,烟草样品的质量损失为2.7%~3.2%。因此,热解气氛对这一失重阶段仍然具有一定影响。在热降解结束后,惰性气氛中会留下大约23%的残留质量,而在氧化气氛中残留质量仅为6%左右,且与升温速率关系不大。
2.2惰性和含氧气氛中的动力学比较分析
非等温热分析动力学方法从操作方式上可分成单重扫描速率的非等温法和多重扫描速率的非等温法2大类[11]。单重扫描速率的非等温法是通过在同一加热速率下,对反应测得的一条热分析曲线上的数据点进行动力学分析的方法,这是长期以来热分析动力学的主要数据处理方法;多重扫描速率的非等温法是指用不同加热速率下所测得的多条热分析曲线来进行动力学分析的方法,用这种方法可以在不涉及动力学机理函数的前提下获得较为可靠的活化能Ed值。因此,多重扫描速率法是目前国际热分析协会大力推荐的热分析动力学的研究方法。由于烟草是由许多物质组成的复杂体系,在热解过程中不同的温区段可能对应不同的机理函数,为了避免因反应机理函数的假设不同而可能带来的误差,本研究将采用多重扫描速率非等温法中的Flynn-Wall-Ozawa方法[12,13]对烟草样品在惰性和含氧气氛中的热分解动力学进行分析。
对于一个等速升温的非等温热分解过程,其动力学方程通常可用如下形式表示:
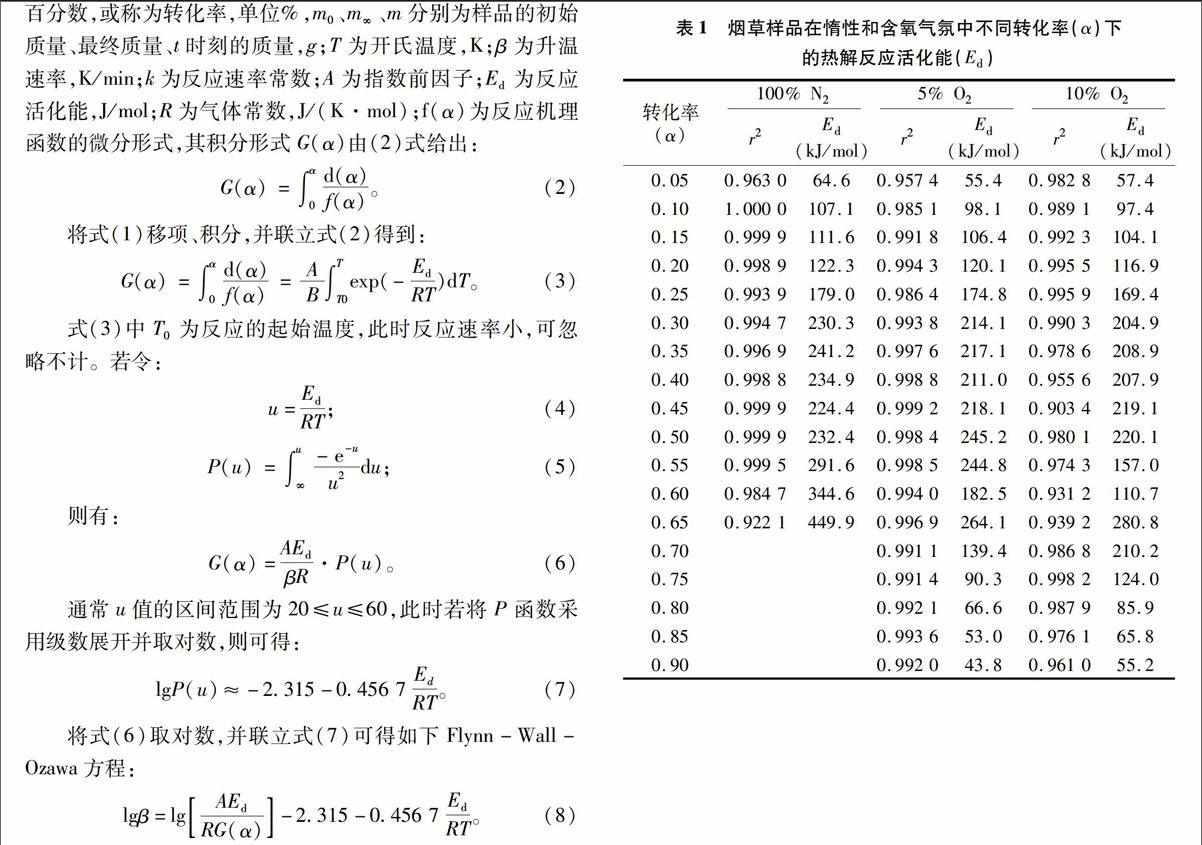
由于在相同的热解气氛中和不同的升温速率β下,选择相同的转化率α值,G(α)为一恒定值,这样由式(8)以lg(β)对1/T作图则可以得一直线,从直线的斜率即可求出活化能Ed值。在此选择α=0.05,0.10,0.15,0.20,……,0.90等一系列的值进行求解,所得结果列于表1中,其中r2值为通过作图法所得直线的决定系数。从表1中可以看出,在所有转化率α相同的条件下,lg(β)与 1/T之间都有较好的线性关系,这表明所得到的活化能Ed值是可靠的。
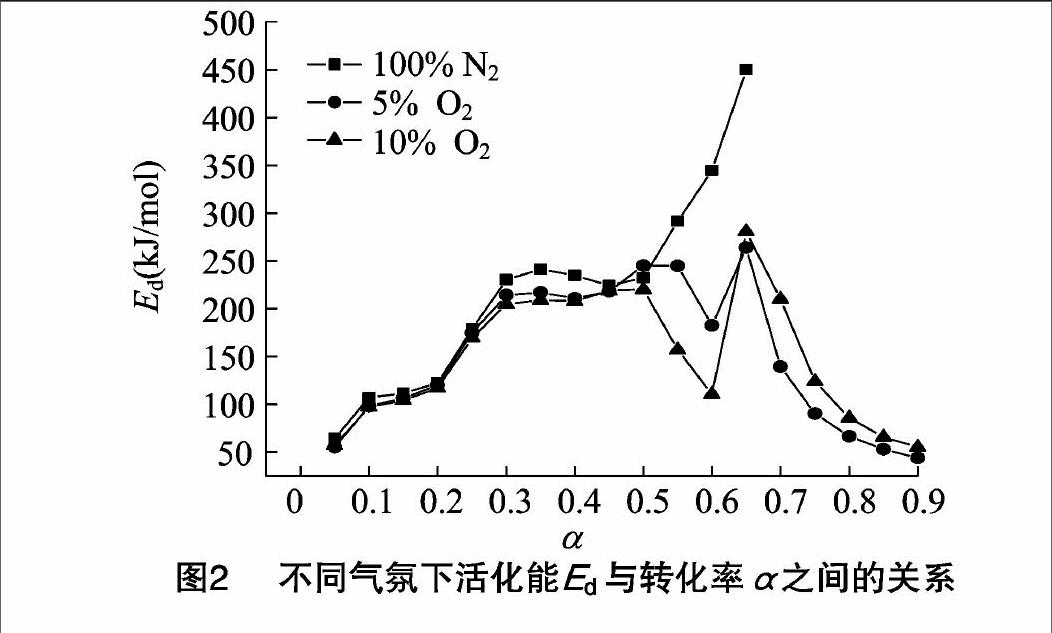
为了直观表达活化能Ed与转化率α之间的关系,将Ed对α作图,如图2所示。从图2中可以清楚地看出,在惰性气氛中,随转化率α的增大,活化能Ed值总体表现为上升的变化趋势。当α为0.05时,活化能Ed值是最低的,此时在4个升温速率的TG曲线上所对应的温度均在第Ⅰ个热失重(吸附水的蒸发)阶段的温度范围内,这显示烟草样品中水分的散失过程是最容易发生的。转化率α为0.10~0.20的范围是与样品热降解的第Ⅱ个热失重(挥发分的析出)阶段相对应的,在此范围内随着α值的增大,活化能Ed值缓慢上升,表明随着温度的升高,烟草样品中挥发性成分的析出是分阶段进行的,低温下一些易挥发性的物质首先析出,随着温度的上升一些难挥发性的物质随后释放。数据分析结果进一步表明,当转化率α为0.25时,在升温速率为20、15 ℃/min的TG曲线上所对应的温度均处于第Ⅱ个热失重阶段的温度范围内,而在升温速率为10、5 ℃/min的TG曲线上所对应的温度则均处于第Ⅲ个热失重阶段的温度
范围内,因此,α=0.25是样品的第Ⅱ个热失重和第Ⅲ个热失重阶段的过渡阶段,与转化率α分别为0.10、0.15、0.20时相比,此时活化能Ed值跳跃上升。在样品的第Ⅲ个热失重阶段,活化能Ed值随转化率α的变化可以分成2个区域,第1个区域位于转化率α为0.3~0.5的范围内,其活化能Ed值呈现出波动的复杂变化趋势;第2个区域位于转化率α为0.55~0.65的范围内,相应的活化能Ed值则快速上升。烟草是一个十分复杂的化学体系,其中除了含有非聚合物外,还含有许多纤维素、半纤维素、胶质和木质素等生物聚合物成分。由于在第Ⅲ个热失重阶段,质量的损失主要与烟草内源性生物聚合物的热降解相关,而不同生物聚合物的热分解过程和动力学行为是不同的。因此,当反应进入第Ⅲ个热失重阶段后,不同生物聚合物的热分解导致了第1个区域内活化能Ed值呈现出了较为复杂的变化趋势;至于在第2个区域内活化能Ed值的快速上升,则可能与第1个区域生物聚合物热解产生的焦炭和反应气氛相关,当生物聚合物在经历了第1个区域的裂解后,样品的表面上会形成大量的焦炭,由于反应是在惰性气氛中进行的,没有燃烧反应发生,这些焦炭很难发生进一步的热分解,随着反应温度的升高和转化率的增加,生物聚合物的热解反应逐渐发生完毕,因此在第2个区域内相应的反应很难发生,其活化能也就会快速增加。
另外,从图2中还可以发现,在转化率α值为0.05至025的范围内,不同热解气氛中的Ed与α关系曲线基本重合,这说明热解气氛中氧气的存在及其浓度的变化并没有改变样品的第Ⅰ和第Ⅱ 2个热失重阶段的反应动力学机理。然而当转化率α值大于0.25后,不同热解气氛中得到的Ed与α关系曲线彼此出现明显的分离。数据分析显示,在含氧气氛中,转化率范围为α=0.3~0.5时对应的温度段处于样品的第Ⅲ个热失重阶段的温度范围内;转化率α=0.55是样品的第Ⅱ、第Ⅲ2个热失重阶段的过渡阶段;而当转化率范围为α=0.60~0.90时的温度段则与样品的第Ⅳ个热失重阶段相对应。图2显示,热解气氛中氧气的存在,温和地降低了样品在第Ⅲ个热失重阶段的活化能,而且氧气浓度的增加会使得这一活化能的降低得到增强。在转化率α=0.55的过渡阶段以及转化率α=0.60的燃烧反应的前期阶段,氧气的存在及其浓度的高低对反应活化能降低的影响是十分强烈的,因此在有氧的条件下,当样品经历了生物聚合物的热解阶段后,其燃烧反应是很容易发生的,而且热解气氛中氧气浓度的升高也有利于燃烧反应的发生。然而,在转化率α=0.60时,活化能却出现了1个跳跃性的增加,随后又会逐渐下降,并且在α=0.65~0.90范围内,氧气浓度的增加会导致其活化能也有较为明显的上升。焦炭的燃烧阶段,活化能的跳跃上升及其随氧气浓度升高而增大的现象,在Zhao等研究氧气浓度对泥煤热失重过程的影响时也被发现[14],然而他们并没有对这一现象进行解释。笔者认为从反应机理上讲,氧化气氛中烟草样品的第Ⅳ个热失重阶段应该包括2个燃烧过程:第1个燃烧过程为气态可燃物的燃烧;第2个燃烧过程为固态焦炭的燃烧。气态可燃物的燃烧是一个均相的自由基反应过程,其活化能通常较低;而焦炭的燃烧是一个多相反应过程,其活化能则相对较高,因此在这2个燃烧过程的转化阶段,反应体系的活化能会出现跳跃性上升;随着反应温度的继续升高,焦炭的燃烧反应会进一步加强,其释放出的热量也会逐渐增多,从而导致了α=0.65~0.90范围内随着转化率的增大活化能逐渐降低的现象;至于在上述转化率范围内,反应活化能随氧气浓度的升高而增大,则可能与不同热解气氛中所形成的焦炭的组成和内部结构相关。
3结论
含氧气氛中,随着热解温度的不断升高,烟草样品均经历了5个明显的热失重阶段;而在惰性气氛中,则表现为第Ⅳ个热失重过程的消失,仅经历了4个热失重阶段。
热解气氛中氧气的存在及其浓度的变化对第Ⅰ、Ⅱ 2个热失重阶段没有明显的影响;而随着温度的升高,在后面的几个热失重阶段,尤其是在样品热解的主反应区,氧气的浓度对样品热降解的影响会十分明显。
热降解动力学分析结果进一步表明,在惰性气氛中活化能随转化率的增大表现出不断上升的变化趋势,在含氧气氛中活化能随转化率则呈现出复杂的变化规律;另外,热解气氛中氧气的存在及其浓度的变化并没有改变样品在前2个热失重阶段的反应活化能,而对主反应区的活化能影响较为明显,这预示着主反应区中氧气浓度的变化可能会导致其反应路径的变化,进而也会导致热解产物发生变化。
参考文献:
[1]Baker R R. Product formation mechanisms inside a burning cigarette[J]. Progress in Energy and Combustion Science,1981,7(2):135-153.
[2]Senneca O,Ciaravolo S,Nunziata A. Composition of the gaseous products of pyrolysis of tobacco under inert and oxidative conditions[J]. Journal of Analytical and Applied Pyrolysis,2007,79(1/2):234-243.
[3]Baker R R. The kinetics of tobacco pyrolysis[J]. Thermochimica Acta,1976,17(1):29-63.
[4]Gugan K. Natural smoulder in cigarettes[J]. Combustion and Flame,1966,10(2):161-164.
[5]Wongsiriamnuay T,Tippayawong N. Non-isothermal pyrolysis characteristics of giant sensitive plants using thermogravimetric analysis[J]. Bioresource Technology,2010,101(14):5638-5644.
[6]Gronli M G,Varhegyi G,di Blasi C. Thermogravimetric analysis and devolatilization kinetics of wood[J]. Industrial & Engineering Chemistry Research,2002,41(17):4201-4208.
[7]Longanezi T,Campos M P,Mothé C G. Thermal investigation of uncased and cased tobacco[J]. Thermochimica Acta,2002,392/393:51-54.
[8]Oja V,Hajaligol M R,Waymack B E. The vaporization of semi-volatile compounds during tobacco pyrolysis[J]. Journal of Analytical and Applied Pyrolysis,2006,76(1/2):117-123.
[9]Fenner R A. Thermoanalytical characterization of tobacco constituents[J]. Rec Adv Tob Sci,1988,14:82-113.
[10]Senneca O,Chirone R,Salatino P,et al. Patterns and kinetics of pyrolysis of tobacco under inert and oxidative conditions[J]. Journal of Analytical and Applied Pyrolysis,2007,79(1/2):227-233.
[11]胡荣祖,史启祯. 热分析动力学[M]. 北京:科学出版社,2001:136-126.
[12]Ozawa T. A new method of analyzing thermogravimatric data[J]. Bulletin of the Chemical Society of Japan,1965,38(11):1881-1886.
[13]Flynn J H,Wall L A. A quick,direct method for the determination of activation energy from thermogravimetric data[J]. J Polym Sci,1966,4(5):323-328.
[14]Zhao W T,Chen H X,Liu N A,et al. Thermogravimetric analysis of peat decomposition under different oxygen concentrations[J]. Journal of Thermal Analysis and Calorimetry,2014,117(1):489-497.

