温度对氯化胆碱/多元醇型低共熔溶剂物性的影响
何志强,鄢浩,王骑虎,余兴露,吴凯,徐毅
(上海大学环境与化学工程学院,上海 200444)
温度对氯化胆碱/多元醇型低共熔溶剂物性的影响
何志强,鄢浩,王骑虎,余兴露,吴凯,徐毅
(上海大学环境与化学工程学院,上海200444)
合成了4种氯化胆碱多元醇型低共熔溶剂,并在303~343 K时分别测定了4种低共熔溶剂的密度、黏度、电导率等物性随温度变化的规律.结果表明:4种低共熔溶剂的密度随温度的变化均符合简单的线性关系,黏度随温度的升高而下降,电导率随温度的升高而快速增加;无论是黏度还是电导率,它们与温度的关系均较好地符合阿伦尼乌斯指数关系.另外,根据阿伦尼乌斯公式计算了4种低共熔溶剂的黏度活化能和电导率活化能,并采用循环伏安法测定了333 K时4种低共熔溶剂的电化学窗口.
低共熔溶剂;密度;黏度;电导率;电化学窗口
胆碱类低共熔溶剂(deep eutectic solvent,DES)是一种由一定化学计量比的胆碱盐和配位剂组合成的低共熔混合物[1].研究表明,低共熔溶剂具有与离子液体相似的高导电性、宽电化学窗口等特性,且制备简单、价格低廉,对多种金属盐及金属氧化物有良好的溶解性[2].自2003年英国的Abbott等[3]首次合成氯化胆碱和尿素组成的胆碱类低共熔溶剂以来,低共熔溶剂作为一种可以替代传统溶剂和离子液体的新型绿色溶剂,在金属电沉积应用方面得到了广泛关注.Zn,Au,Ag,Cu等金属已经成功地从DES中电沉积制备得到[4-7].解析溶剂的物理化学特性是其应用的前提,因此对低共熔溶剂物性的研究已引起了众多学者的重视.Abbott研究小组率先研究了一系列胆碱类低共熔溶剂在某一温度下的熔点、黏度、电导率等物性与组成之间的关系[3,8-9].2010年,卢海君等[10]用甜菜碱盐酸盐和尿素合成了低共熔溶剂,并表征了其物化性质,讨论了密度、黏度以及电导率随温度变化的关系.2013年,Wang等[11-12]合成了氯化胆碱/尿素/氯化镍类低共熔溶剂和氯化胆碱/尿素/氯化镁类低共熔溶剂,并研究了其物理性质与温度以及组成之间的关系.最近,邓丽华等[13]制备了ZnCl2-ChCl-MgCl2类离子液体,并对其物性进行了讨论.
研究表明,除了尿素外,乙二醇等多元醇同样可以作为氢键供体与氯化胆碱形成较低熔点的混合物[14].氯化胆碱多元醇型低共熔溶剂不仅具有常规离子液体的优点,而且价格便宜,对水和空气也能够保持长久的稳定性.采用该类低共熔溶剂作为电化学反应介质电沉积锌镍、锌锡等合金的研究实例被相继报道[15-16],但探讨氯化胆碱多元醇型低共熔溶剂的物性与温度二者关系的相关文献还较少.
本工作合成了4种摩尔比为1∶2的氯化胆碱多元醇型低共熔溶剂,重点测定了4种低共熔溶剂的密度、黏度、电导率等物性随温度的变化关系,并使用线性方程、阿伦尼乌斯方程对密度、黏度和电导率进行数据处理,计算得到了黏度活化能和电导活化能等热力学数据.另外,还采用电化学方法测定了4种低共熔溶剂的电化学窗口,为在该体系中进行的电化学反应提供数据支持.
1 实验部分
1.1试剂
氯化胆碱(ChCl)、无水乙醇、乙二醇(EG)、1,2-丙二醇(PG)、1,3-丁二醇(BG)、甘油(GL),以上试剂均为分析纯,由国药集团化学试剂有限公司提供.
1.2氯化胆碱/多元醇类低共熔溶剂的配制
低共熔溶剂是按照文献[14]所给出的步骤配制的.首先,将氯化胆碱用无水乙醇重结晶,真空抽滤,旋转蒸发后得到较为干燥的粉末,真空干燥48 h;然后,将干燥的氯化胆碱与4种多元醇分别按照摩尔比1∶2进行配比混合,并分别置于80℃的油浴下加热;最后得到的透明均一的液体即分别为氯化胆碱/乙二醇(ChCl/EG)、氯化胆碱/1,2-丙二醇(ChCl/PG)、氯化胆碱/1,3-丁二醇(ChCl/BG)、氯化胆碱/甘油(ChCl/GL).
1.3仪器和测定方法
使用Avater370傅里叶红外光谱仪(由美国尼高力仪器公司提供)测定表征低共熔溶剂的结构,使用附温型比重瓶(25 mL)测定低共熔溶剂的密度,使用DV-II+Pro型黏度计(由美国Brookfield公司提供)测定低共熔溶剂的黏度,采用DDS-307数显电导率仪(由上海越磁电子科技有限公司提供)测定低共熔溶剂的电导率,使用CH660a电化学工作站(由上海辰华仪器有限公司提供)采用循环伏安法测定低共熔溶剂的电化学窗口.
2 结果与讨论
2.1DES的红外表征
图1为4种氯化胆碱多元醇型低共熔溶剂的傅里叶红外光谱.可以看出,ChCl/GL的傅里叶红外光谱在3 200~3 600 cm-1之间形成了较强的宽峰,这表明氯化胆碱与甘油形成了O—H···O,O—H···Cl等分子间氢键,而1 483.06 cm-1与954.84 cm-1的强峰分别为CH2和C—C键.同样,其他3种二元醇形成的DES红外光谱在3 200~3 600 cm-1之间也形成了与ChCl/GL类似的宽峰,这说明在这3种DES中也形成了大量的氢键.氢键对于形成低共熔溶剂是非常重要的.氢键的形成可以降低氯化胆碱的晶格能,使氯化胆碱和多元醇混合物的熔点大大降低,从而形成均一的液体混合物.此外,从图1还可以看出,3种二元醇形成的DES的氢键吸收峰位置按照ChCl/EG,ChCl/PG,ChCl/BG的顺序向波数减小的方向迁徙,且强度依次减小,这表明氢键供体的不同,多元醇与氯化胆碱形成的氢键强弱也不同.
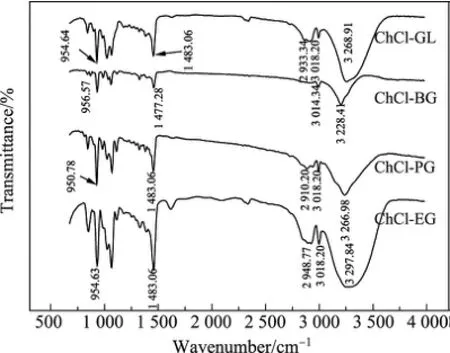
图1 4种DES的傅里叶红外光谱Fig.1 FTIR spectra of the four DESs
2.2DES密度的测定
在电沉积金属时,电解质与金属之间的密度差不但决定电解槽的结构形式,还对电流效率有显著影响.因此,低共熔溶剂密度的数据测定对在该溶剂中进行的电化学反应工艺设计非常重要.在293 K时,本研究测得的ChCl/GL密度为1.179 g·cm-3,这与Abbott等[17]所给出的值1.181 g.cm-3基本一致.图2为4种低共熔溶剂密度和温度之间的变化关系.由图2可知,在303~343 K时,4种低共熔溶剂的密度均随温度的升高而减小,但总的变化不大.4种低共熔溶剂的密度和温度均呈如下线性关系[18]:

式中,ρ为密度,T为温度,a和b为与DES种类有关的常数.
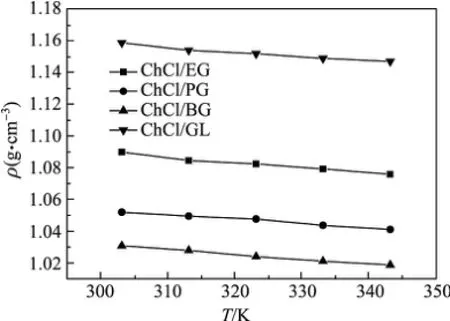
图2 温度对4种低共熔溶剂密度的影响Fig.2 Influence of temperature on the densities of the four DESs
由图2可知,在同一温度下4种低共熔溶剂的密度按照ChCl/GL,ChCl/EG,ChCl/PG,ChCl/BG(1.0308~1.0187)的顺序减小.产生上述密度变化趋势可能是由于作为氢键供体的多元醇的密度按照GL,EG,PG和BG的顺序依次减小的缘故,因为在温度为293 K时GL,EG,PG和BG的密度分别为1.303,1.113,1.037,1.005 g·cm-3.
2.3DES的黏度
黏度是溶剂的重要物性之一.黏度较低的电解质有利于物质的扩散,提高反应的速率.本研究测定了4种低共熔溶剂的黏度随温度变化的规律(见图3).可以看出,低共熔溶剂的黏度受温度的影响变化较大.在303~343 K时,4种低共熔溶剂的黏度均随着温度的升高而降低.与Abbott采用空穴理论模型得到的低共熔溶剂的热传输性质类似,温度的升高将赋予低共熔溶剂更高的能量,从而提高了溶剂分子的流动性[17,19].一般情况下,液体的黏度随温度的变化规律[20]可表示为

式中,η为黏度,η0为与液体特性有关的常数,Eη为黏度活化能,R为气体常数,T为液体的温度.
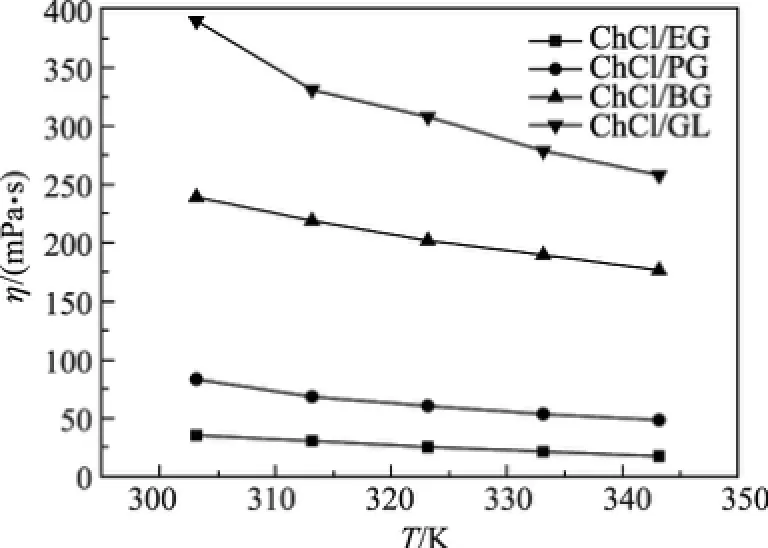
图3 温度对4种低共熔溶剂黏度的影响Fig.3 Influence of temperature on the viscosity of the four DESs
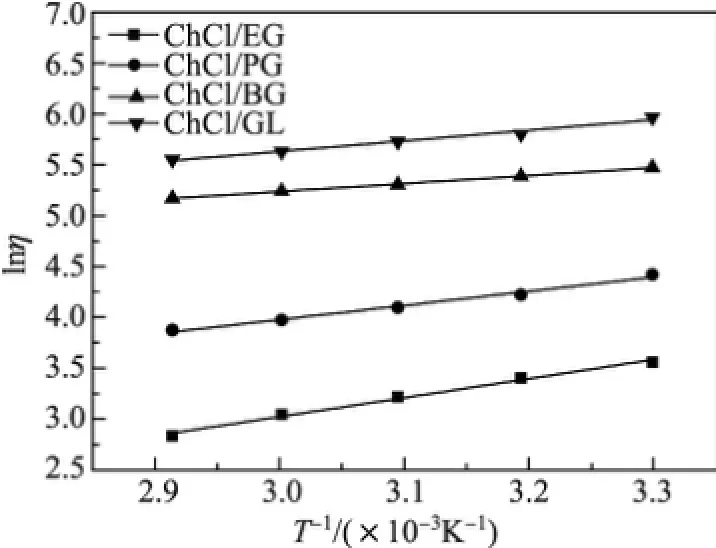
图4 lnη和T-1的关系Fig.4 Relationship of lnη and T-1
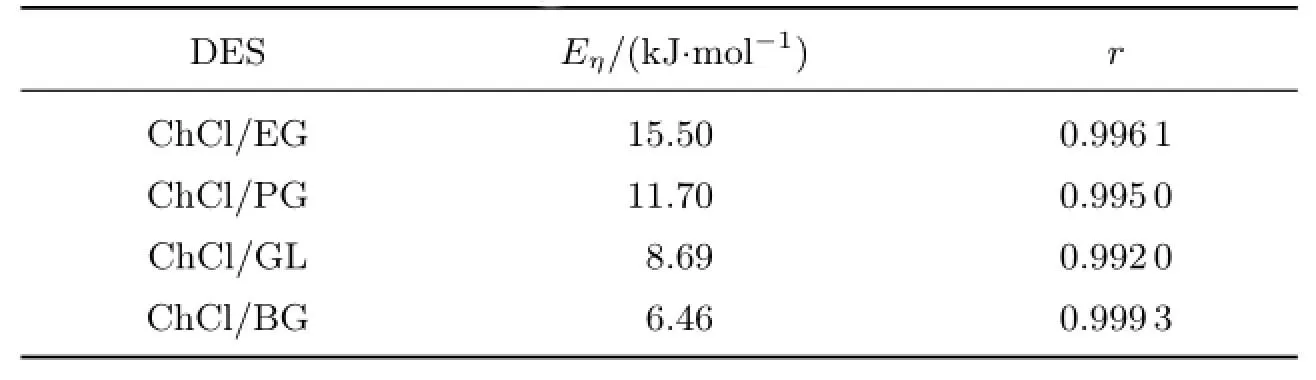
表1 DES的黏度活化能和相关系数Table 1 Activation energies for DES and correlation coefficients
图4是4种低共熔溶剂在303~343 K时lnη和T-1的关系.表1给出了4种低共熔溶剂的黏度活化能Eη及相关系数r.结果表明,4种低共熔溶剂的相关系数r均大于0.99.因此,测得的数据可以很好地用式(2)表示,即4种低共熔溶剂的黏度在303~343 K时展现出阿伦尼乌斯行为,由此可以根据Eη,采用式(2)来估算低共熔溶剂的黏度.此外,由表1和图4可以看出,低共熔溶剂的黏度活化能值越大,其流动性越差.Wang等[11]在研究氯化胆碱/尿素/氯化镍类离子液体物性时,也指出了该类液体的黏度与黏度活化能呈反比的特性.黏度活化能的测定结果有助于大致判断DES的黏度,为设计低黏度低共熔溶剂提供支持.
在温度相同时,4种低共熔溶剂的黏度按照ChCl/EG,ChCl/PG,ChCl/BG,ChCl/GL的顺序增大,这可能是由于提供氢键供体的EG,PG,BG,GL的黏度依次增大的原因,因为在293 K时EG,PG,BG和GL的黏度分别为26,61,130和945 mPa·s.因此,选择黏度低的氢键供体有利于合成低黏度的低共熔溶剂.
2.4DES的电导率
电化学反应能够实现的必要条件是反应体系必须导电,且能够溶解一定浓度的电解质.电导率表示物质导电的性能,电导率越大则物质的导电性能越强,越有利于电化学反应的实现.电解质的导电性主要与导电离子数目、离子迁移的速率有关.因此,可以简单地把电导率[21]表达为

式中,κ为电导率,ni,µi,qi分别为带电荷离子i的数目、迁移速率和电荷数.
低共熔溶剂的电导率一般为0.1~10 mS/cm,且大小与温度有关.由于ChCl/BG在低于323 K时有结晶析出,故本实验只测定了另外3种DES的电导率在298~333 K时的变化情况(见图5).由图5可见,ChCl/EG的电导率从7.3 mS/cm增加到12.3 mS/cm,ChCl/PG从2.79 mS/cm增加到6.07 mS/cm,ChCl/GL从1.0 mS/cm增加到3.56 mS/cm.3种DES的电导率均高于常用的室温离子液体BMimBF4(303 K,2.01 mS/cm)和BMIMPF6(303 K,1.17 mS/cm)[22],显然更适合于电化学反应.另外,3种DES的电导率均随着温度的升高而快速升高.DES的电导率与温度的关系[20]可以表示为

式中,κ为电导率,κ0为极限温度下的极大电导率,EΛ为电导活化能,T为温度,R为气体常数.活化能是与溶液体系发生化学反应的热力学条件有关的常数,在水相体系中可以看成是离子克服周围水分子和共存离子相互作用发生迁移所需的最低能量,用于“活化”离子并使之表现出导电性.这个过程需要破坏原有的离子与溶剂分子、离子与共存离子之间的相互作用力,为离子在溶液体系中的自由移动以及形成新物质提供能量保证.因此,通过电导活化能可以量化离子迁移的难易程度.通过图6所示的阿伦尼乌斯图可以计算得到不同多元醇构成的DES的电导活化能(见表2).可以看出,3种DES的电导活化能按照ChCl/EG,ChCl/PG,ChCl/BG的顺序逐渐增大,这是因为氢键供体的黏度越大,合成的DES的黏度也越大,离子迁移变慢,电导率降低,活化能增大.因此,通过电导活化能可以大致判断DES电导率的相对大小以及DES中离子迁移的难易程度.
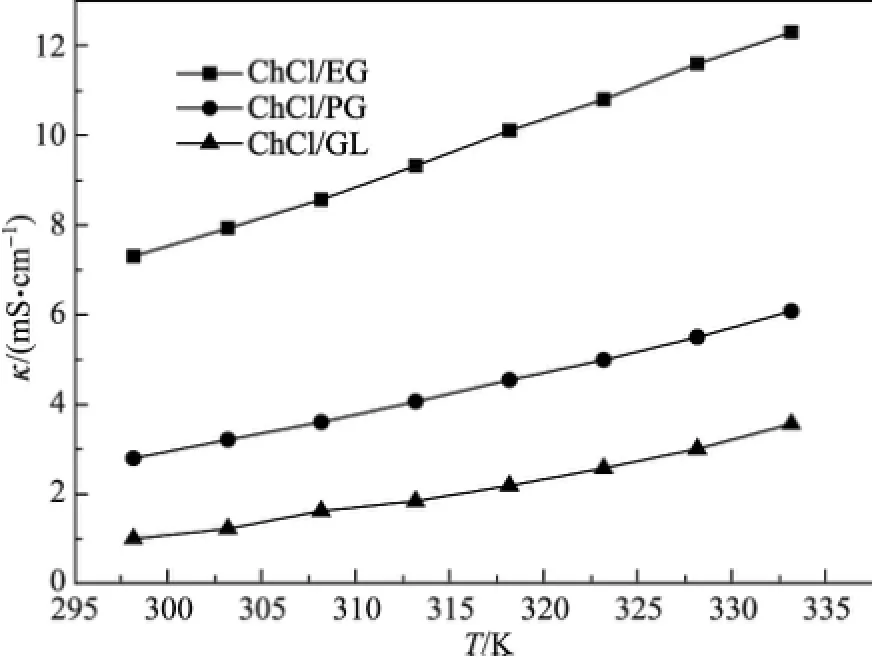
图5 温度对3种低共熔溶剂电导率的影响Fig.5 Influence of temperature on the conductivity of three DESs
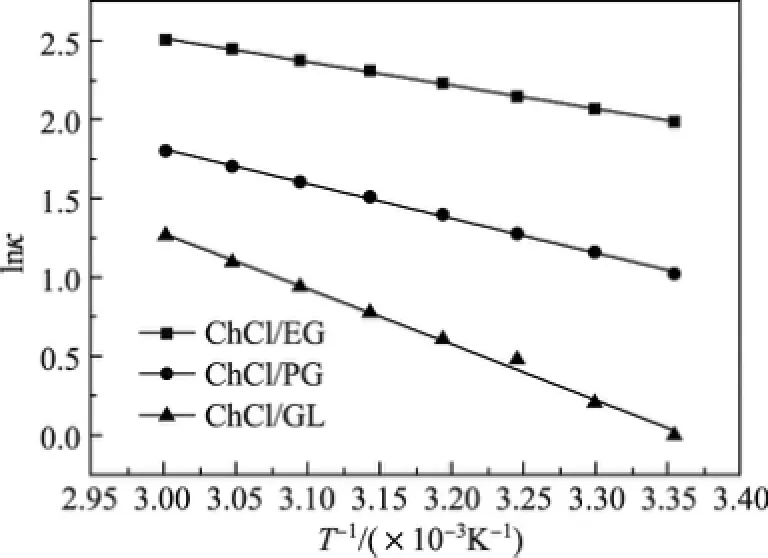
图6 lnκ和T-1的关系Fig.6 Relationship of lnκ and T-1
此外,对比表1与2所给出的DES的黏度活化能和电导活化能可以发现,电导活化能按照ChCl/EG,ChCl/PG,ChCl/BG的顺序依次增大,黏度的活化能则按照ChCl/EG,ChCl/PG,ChCl/BG的顺序依次减小,这一规律与高温熔盐的电导活化能和黏度活化能的关系[23]类似.
在同一温度下,ChCl/EG,ChCl/PG,ChCl/GL的电导率依次减小,且随着分子量的增大而减小.由DES的黏度测定结果可知,ChCl/EG,ChCl/PG,ChCl/GL的黏度依次增大,溶剂中带电离子的迁移速率也依次减小.根据式(3)可知,DES的电导率依次减小.根据氢键供体黏度的不同,DES的黏度和电导率呈相反的变化趋势.
2.5DES的循环伏安分析
溶剂的电化学窗口是溶剂开始发生氧化反应时的电势和开始发生还原反应时的电势的差值,其大小对溶剂作为电化学反应介质的应用具有重要作用.DES作为一种潜力巨大的绿色溶剂可以应用于诸多领域,同时也可以用作电解质,因此研究DES的电化学窗口是很有必要的.图7为4种多元醇类DES在333 K时的循环伏安曲线.电化学窗口的测定以银丝为参比电极,铂片为工作电极,铂丝为辅助电极,扫描速率为50 mV/s,扫描电压为-1.0~1.5 V.
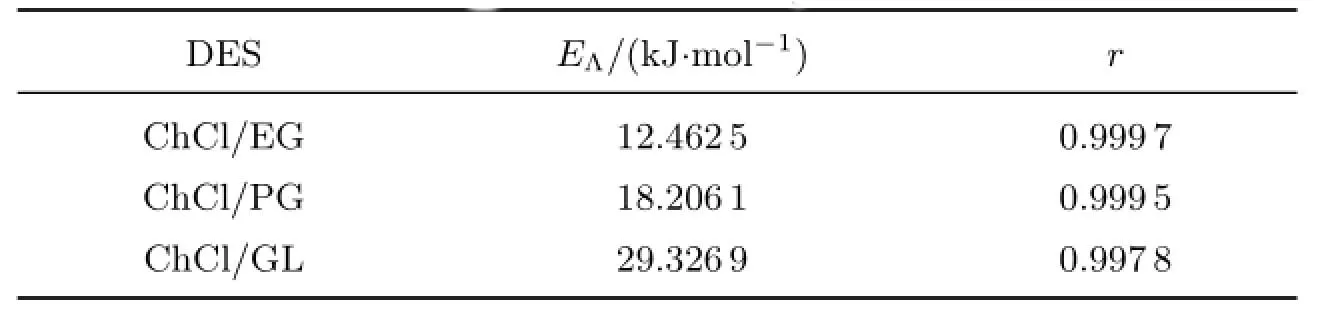
表2 DES电导活化能和相关系数Table 2 Activation energies for conductivity and correlation coefficients
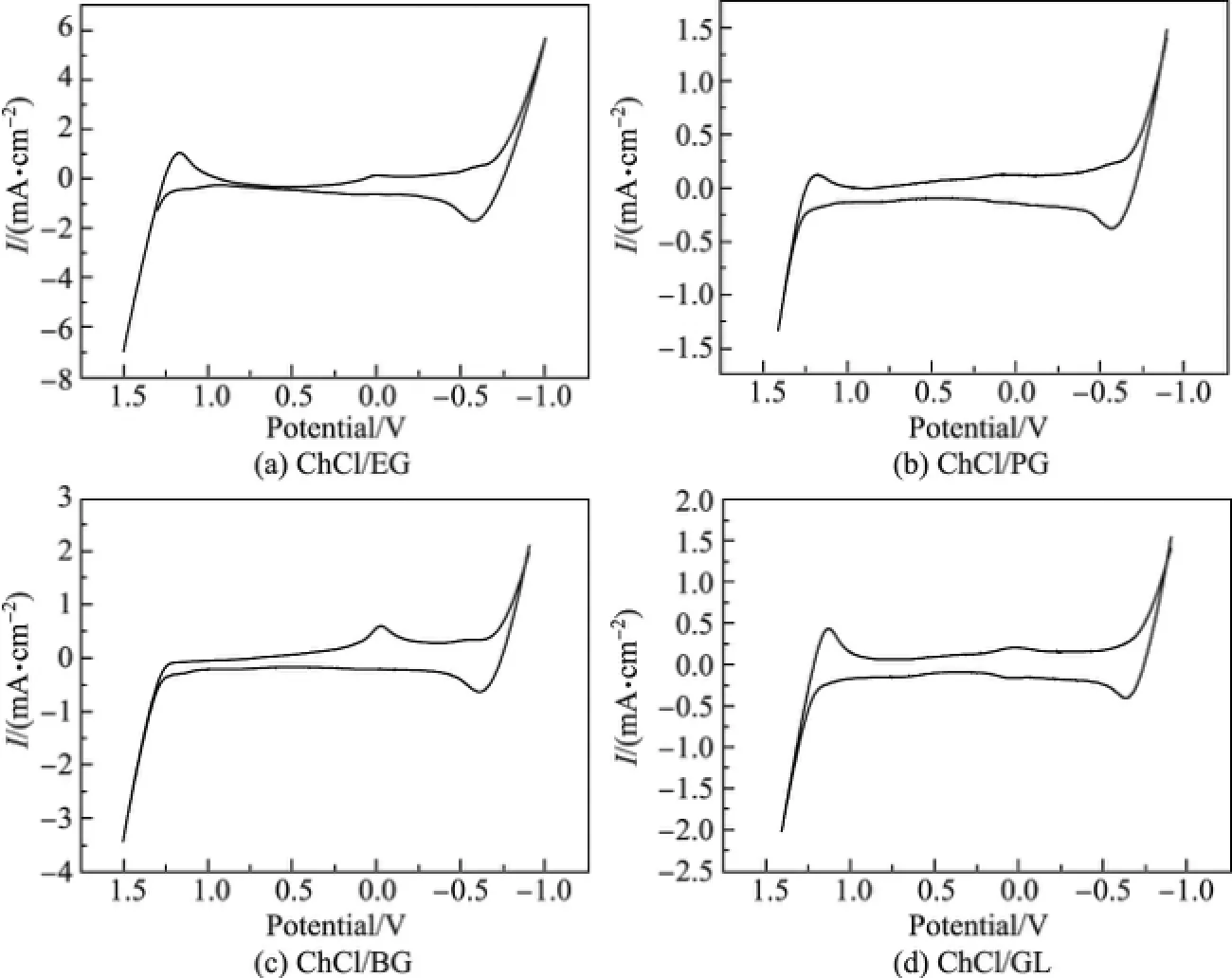
图7 333 K时4种低共熔溶剂的循环伏安曲线Fig.7 Cyclic voltammetry curves of four DESs at 333 K
从图7可以看出,4种多元醇型DES的电化学窗口均大于1 V,其中ChCl/PG和ChCl/GL的电化学窗口为1.5 V左右,这与Abbott给出的值[17]一致.虽然4种多元醇型DES的电化学窗口比大部分的室温离子液体(4 V左右)小,但比水的电化学窗口(1.229 V)略大.这说明4种DES电解时均比水溶液稳定,可以替代水、挥发性有机溶剂等传统的电化学反应介质应用于电沉积反应等领域.
3 结论
本研究测定了303~343 K时4种氯化胆碱/多元醇型低共熔溶剂的物化性质,并得到以下结论.
(1)红外表征表明ChCl/EG,ChCl/PG,ChCl/BG,ChCl/GL中存在大量的氢键,且由于氢键的供体不同,4种DES中氢键的强弱也不同.
(2)ChCl/EG,ChCl/PG,ChCl/BG,ChCl/GL的密度均随着温度的增大而减小,且密度与温度呈线性关系.
(3)ChCl/EG,ChCl/PG,ChCl/BG,ChCl/GL的黏度随着温度的升高而减小,且黏度与温度的关系较好地符合阿伦尼乌斯关系式.因此,选择低黏度的氢键供体有利于低黏度低共熔溶剂的合成.
(4)ChCl/EG,ChCl/PG,ChCl/GL的电导率均随着温度的升高而增大,且在同一温度下氢键供体的黏度越大,所合成的DES电导率越小.电导率与温度的关系较好地符合阿伦尼乌斯关系式,因此可以根据电导活化能的相对大小判断DES电导率的大小.
(5)循环伏安曲线测定结果表明ChCl/EG,ChCl/PG,ChCl/BG,ChCl/GL均具有大于1 V的电化学窗口,因此4种DES具有较为稳定的电化学性能,适合用作电化学反应介质.
[1]张盈盈,陆小华,冯新,等.胆碱类低共熔溶剂的物性及应用[J].化学进展,2013,25(6):881-892.
[2]Abbott A P,Capper G,Davies D L,et al.Solubility of metal oxides in deep eutectic solvents based on choline chloride[J].J Chem Eng Data,2006,51(4):1280-1282.
[3]Abbott A P,Capper G,Davies D L,et al.Novel solvent properties of choline chloride/urea mixtures[J].Chemical Communications,2003(1):70-71.
[4]Whitehead A H,Polzler M,Gpllas B.Zinc electrodeposition from a deep eutectic system containing choline chloride and ethylene glycol[J].J Electrochem Soc,2010,157(6):328-334.
[5]Abbott A P,Barron J C,Ryder K S.Electrolytic deposition of Zn coatings from ionic liquids based on choline chloride[J].Transactions of the Institute of Metal Finishing,2009,87(4):201-207.
[6]Mele C,Catalano M,Taurino A,et al.Electrochemical fabrication of nanoporous goldsupported manganese oxide nanowires based on electrodeposition from eutectic urea/choline chloride ionic liquid[J].Electrochimica Acta,2013,87:918-924.
[7]Abbott A P,Ttaib K E,Frisch G,et al.Electrodeposition of copper composites from deep eutectic solvents based on choline chloride[J].Physical Chemistry Chemical Physics,2009,11(21):4269-4277.
[8]Abbott A P,Boothby D,Capper G,et al.Deep eutectic solvents formed between choline chloride and carboxylic acids:versatile alternatives to ionic liquids[J].Journal of the American Chemical Society,2004,126(29):9142-9147.
[9]Abbott A P,Harris R C,Ryder K S,et al.Glycerol eutectics as sustainable solvent systems[J].Green Chemistry,2011,13(1):82-90.
[10]卢海君,华一新,李艳,等.以甜菜碱盐酸盐和尿素合成低共熔溶剂的研究[J].昆明理工大学学报:理工版,2010,35(6):11-14.
[11]Wang H,Jia Y,Wang X.Physical-chemical properties of nickel analogs ionic liquid based on choline chloride[J].Journal of Thermal Analysis and Calorimetry,2014,115:1779-1785.
[12]王怀有,景燕,吕学海,等.含氯化镁的类离子液体结构和物理化学性质[J].化工学报,2011,62(S2):21-25.
[13]邓丽华,贾永忠,景燕,等.ZnCl2-ChCl-MgCl离子液体的制备、结构及性质研究[J].盐湖研究,2013,21(2):43-51.
[14]Abbott A P,Gruffith J,Satvinder N,et al.Sustained electroless deposition of metallic silver from a choline chloride-based ionic liquid[J].Surf Coat Technol,2008,202:2033-2039.
[15]Wang Z L,Yang Y X.A study on electroplating of zinc nickel alloy with hedp plating bath[J].Russian Journal of Electrochemistry,2006,42(1):22-26.
[16]Abbott A P,Capper G,Mckenzie K J,et al.Electrodeposition of zinc-tin alloys from deep eutectic solvents based on choline chloride[J].Journal of Electroanalytical Chemistry,2007,599(2):288-294.
[17]Abbott A P,Harris R C,Ryder K S.Application of hole theory to define ionic liquids by their transport properties[J].Journal of Physical Chemistry B,2007,111(18):4910-4913.
[18]Kareem M A,Mjalli F S,Hashim M A,et al.Phosphonium-based ionic liquids analogues and their physical properties[J].Journal of Chemical and Engineering Data,2010,55(11):4632-4637.
[19]Endres F,Macfarlane D,Abbott A P.Electrodeposition from ionic liquids[M].Weinheim:Wiley-VCH,2008:39-41.
[20]Bockris J,Reddy A.Modern electrochemistry[M].New York:Plenum Press,1970.
[21]Every H,Bishop A G,Forsyth M,et al.Ion diffusion in molten salt mixtures[J].Electrochimica Acta,2000,45(8/9):1279-1284.
[22]张冰,陈松,陈亮.BMIMBF4和BMIMPF6二元复合离子液体的特性[J].北京联合大学学报:自然科学版,2012,26(2):51-54.
[23]张明杰,王兆文.熔盐电化学原理与应用[M].北京:化学工业出版社,2006:36.
Effect of temperature on physic-chemical properties of deep eutectic solvent based on choline chloride and polyols
HE Zhi-qiang,YAN Hao,WANG Qi-hu,YU Xing-lu,WU Kai,XU Yi
(School of Environmental and Chemical Engineering,Shanghai University,Shanghai 200444,China)
Four kinds of deep eutectic solvents(DESs)based on choline chloride and polyols were prepared.Density,viscosity and conductivity of the four DESs were measured as functions of temperature in the range of 303~343 K.The results show that the densities of the four DESs sare linearly dependent on temperature.Viscosities decrease with increasing temperature,and conductivities increase rapidly with increasing temperature,both obeying the Arrhenius exponential law.The activation energy of viscosity and conductivity were calculated with the Arrhenius formula.The electrochemical windows of the four DESs were also tested by using cyclic voltammetry at 333 K.
deep eutectic solvent;density;viscosity;conductivity;electrochemical window
O 646.54
A
1007-2861(2015)03-0384-09
10.3969/j.issn.1007-2861.2014.03.005
2014-03-21
国家自然科学基金资助项目(20604015,21176152)
鄢浩(1974—),女,副教授,博士,研究方向为绿色化工与技术、流体物性测定等. E-mail:hao-yan@shu.edu.cn

