姜黄挥发油β-环糊精包合物的制备与验证及稳定性考察
张超,韩丽,欧小群,张芳,杨秀梅,郝月莆
姜黄为姜科植物姜黄Curcuma longa L.的干燥根茎[1],主要分布于福建、广东、广西、云南、四川、湖北等地。姜黄性温而味辛、苦,具有破血行气,通经止痛的功效。临床常用于胸腹胀痛、肩臂痹痛、月经不调、跌打损伤等症[2]。姜黄主要含挥发油和姜黄素类,据测定,姜黄中挥发油含量可达4.0%~6.0%,姜黄素为1.8%~5.4%。目前关于姜黄素的研究报道较多,主要集中在抗炎、抗氧化、抗肿瘤、抗血管生成等方面,而作为姜黄重要活性部位的姜黄挥发油研究很少,现代药理研究表明,姜黄挥发油具有良好的抗菌、消炎、祛痰、止咳、抗癌等生物活性[3~5],在食品、医药、日化等行业中具有广泛的应用前景。
但是,挥发油作为中药有效成分,由于极易挥发,对光和热的不稳定,且具有较强的气味,影响了其临床药效的发挥和患者用药的顺应性,因此,为了提高姜黄挥发油的稳定性,掩蔽其不良气味,将其制备成 β-环糊精(β-CD)包合物。本试验采用饱和水溶法制备姜黄挥发油 β-环糊精包合物,通过正交试验筛选最佳包合工艺,采用薄层色谱法和紫外分光光度法对包合产物进行验证,并对其稳定性进行考察,为含姜黄挥发油的相关制剂的制备提供理论依据。
1 材料
85-2型数显恒温磁力搅拌器( 金坛市大地自动化仪器厂) ,Sar-torious BP 211D型电子天平(德国) ;UV-6100型双光束紫外可见分光光度计( 上海美谱达仪器有限公司) ,姜黄挥发油(实验室自制) ;β-环糊精( 成都市科龙化工试剂厂) ;硅胶G薄层板(实验室自制) ;其他试剂均为分析纯。
2 方法与结果
2.1 姜黄挥发油包合物的制备工艺研究
2.1.1 姜黄挥发油β-CD包合物的制备 采用饱和水溶液法制备[6],精密称取适量的 β-CD置于三角瓶中,加入适量蒸馏水,在规定温度下加热使溶解,配制成饱和水溶液,于设置一定转速的磁力搅拌器上恒温搅拌,精密量取挥发油适当体积,按1:1用无水乙醇稀释,配成50%(v/v)的姜黄挥发油乙醇溶液,在搅拌的同时将其缓慢滴加入含 β-CD的饱和水溶液中,恒温搅拌至规定时间,搅拌结束后待包合物冷却至室温,将形成的包合物混悬液置于冰箱冷藏24 h后,抽滤,弃去滤液,滤饼先用少量蒸馏水冲洗,再用石油醚(30~60 ℃)洗涤3次(每次10 mL),抽干后40℃减压干燥5 h,即得包合物,称定重量,备用。姜黄挥发油与 β-CD物理混合物的制备[7]按包合时对应的物料比,称定适量挥发油和β-CD,共同置于研钵中研磨混匀,即得一定颜色的粉末状混合物。
2.1.2 评价指标[8]挥发油包合率是衡量包合效果的重要指标,挥发油包合率越高,包合效果越好。而包合物收得率在实际生产中也具有重要意义,因此试验中综合考虑两指标,采用加权综合评分法,根据各指标的重要性确定挥发油包合率和包合物收得率的加权系数分别为0.8、0.2,按下列公式计算挥发油包合率和包合物收得率,并进行综合评分,得到最佳工艺。
挥发油包合率( % ) = (包合物中实际含油量) / (挥发油加入量×空白回收率)×100%
包合物收得率( %) = 包合物实际质量/ (β-CD质量+挥发油加入量)×100%
综合评分Y(%)= 挥发油包合率(%)×0.8+包合物收得率(%)×0.2
2.1.3 包合物中实际含油量测定 将制得的姜黄挥发油包合物,置于500 mL圆底烧瓶中,加入蒸馏水200 mL,按挥发油测定法( 2010年版《中国药典》一部附录XD甲法)[9]进行水蒸气蒸馏提取挥发油,至油量不再增加时停止加热,放置1 h,读取挥发油量即可。
2.1.4 挥发油空白回收率测定[10]精密量取3份挥发油各1 mL,分别置于500 mL圆底烧瓶中,按“2.1.3”项下方法测定,读取挥发油量,计算空白回收率。结果得到挥发油的量分别为0. 89,0. 90,0. 91 mL,挥发油空白回收率为90. 0%,RSD为1.11%。
2.1.5 正交设计优化包合工艺 根据文献及预实验,本研究采用较为常用、成本低廉的饱和水溶液法制备包合物,选择对挥发油包合影响较大的挥发油与β-环糊精(β-CD)的配比、包合时间、包合温度为主要因素,各因素分设3个水平,采用L9(34)正交表进行试验,以包合物收得率和挥发油包合率为评价指标对包合工艺进行优选,因素水平见表1,正交试验安排及结果见表2,方差分析见表3。

表 3 姜黄挥发油β-CD包合物制备工艺正交试验方差分析
由表2极差R的大小可知:RA>RB>RC,各因素对姜黄挥发油β-CD包合工艺的影响程度依次为A>B>C,即挥发油:β-环糊精>包合温度>包合时间。其中表3方差分析结果表明挥发油与β-环糊精的比例对包合效果有显著影响,且差异具有统计学意义(P<0.05),包合温度、包合时间对包合效果影响不大。综合考虑,确定姜黄挥发油的最佳包合工艺为:A3B3C2,即1 mL 姜黄挥发油与8 g β-环糊精进行包合,包合物温度50℃,包合时间90 min。
2.1.6 验证试验 精密量取姜黄挥发油3份,平行操作,按筛选出的最佳包合工艺A3B3C2进行验证试验,结果,得到的挥发油包合率分别为48.22%,47.76%,49. 54%,平均包合率48.51%,RSD1.91%。包合物收得率分别为67.43%,68.76%,69. 28%,平均收得率68.49%,RSD1.39%。结果表明,优选包合工艺稳定可行,具有良好的重现性。
2.2 姜黄挥发油 β-CD包合物的验证
2.2.1 薄层色谱法[11]取姜黄挥发油1 mL,作为样品1; 取适量包合物提取的挥发油,作为样品2; 取包合物、姜黄挥发油与 β-CD的物理混合物、β-CD各1 g,用无水乙醇10 mL溶解,作为样品3、4、5; 吸取上述样品,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯(9:1)为展开剂,饱和15 min后展开,取出,晾干,喷以5%香草醛硫酸溶液,在105℃加热至斑点清晰。通过观察色谱展开后斑点的有无、斑点的位置,即可对包合结果即包合物是否已经形成进行直观鉴别,见图1。
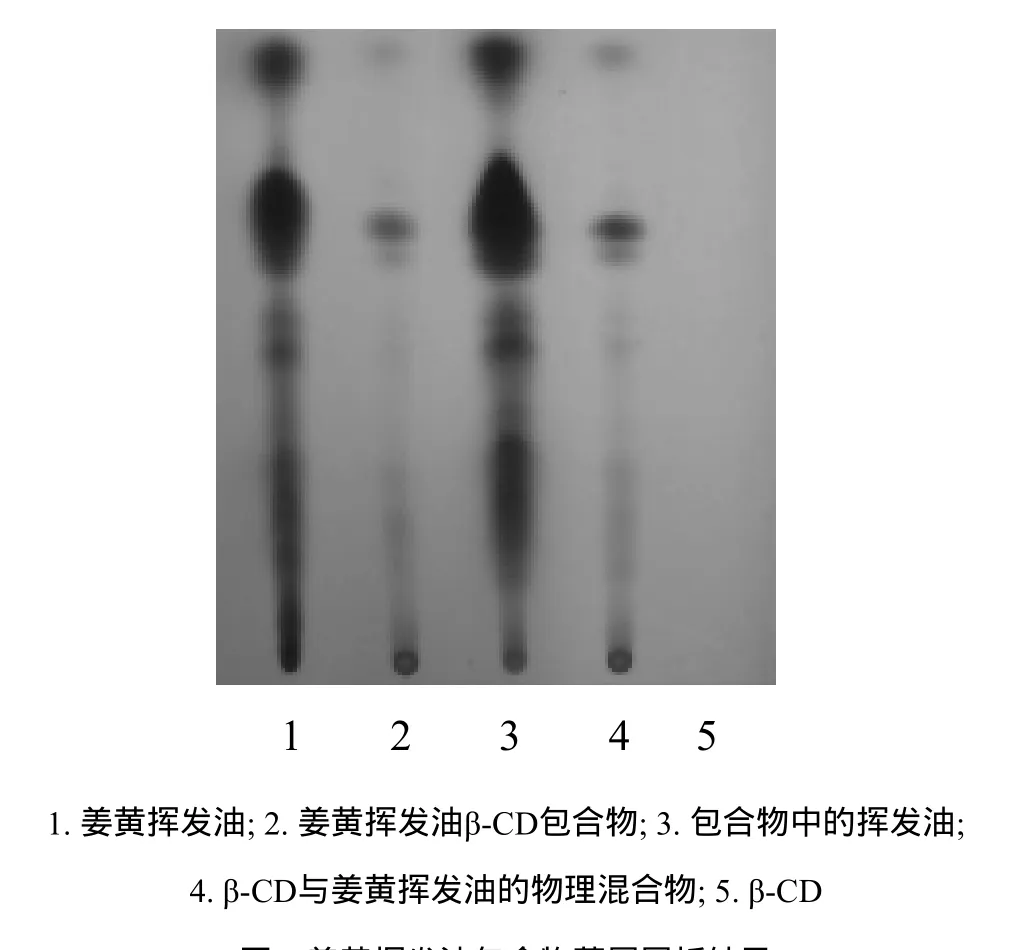
图1 姜黄挥发油包合物薄层层析结果
由图1可见,样品1、3、4在相同位置上显相同颜色斑点,样品2、5无相应斑点出现。样品1、3的薄层鉴别结果表明姜黄挥发油在用 β-CD包合前后化学成分无变化,样品1、2、5的薄层鉴别结果表明姜黄挥发油 β-CD包合物已经形成且 β-CD对包合物中挥发油的测定无干扰。
2.2.2 紫外分光光度法 精密量取姜黄挥发油、包合物中提取的挥发油、姜黄挥发油β-CD包合物、姜黄挥发油与 β-CD的物理混合物及 β-CD适量,分别加无水乙醇稀释溶解,稀释液滤过,取续滤液,以无水乙醇作空白,在200~800 nm 范围内进行紫外扫描,观察各自的紫外吸收变化。紫外扫描结果显示,姜黄挥发油、包合物中提取的挥发油均有吸收,所形成的紫外图谱基本一致,说明姜黄挥发油与 β-CD形成的包合物并未改变姜黄挥发油的理化性质。同时,姜黄挥发油与 β-CD的物理混合物也有吸收,但其波长出现轻微蓝移,可能是受 β-CD的影响,但二者光谱行为基本一致;而 β-CD则无吸收,说明 β-CD对测定结果无干扰; 姜黄挥发油β-CD包合物无吸收,证明包合物已经形成。
2.3 姜黄挥发油包合物的稳定性试验[12]
2.3.1 光稳定试验 精密称取姜黄挥发油β-环糊精包合物和按照物料比混匀所得的姜黄挥发油与β-环糊精的物理混合物适量各3份,平铺于称量瓶中,置(强度4500 lx)光照下放置6 d,于第 0,3,6 d取样,按“2.1.3”项下方法测定挥发油相对含量,见表4。结果表明,包合物在第3、6 d的挥发油相对含量有所下降,但下降速度相比物理混合物缓慢,较后者具有良好的光稳定性,在强光下不易分解。
2.3.2 高温试验 精密称取姜黄挥发油β-环糊精包合物和按照物料比混匀所得的姜黄挥发油与β-环糊精的物理混合物适量各3份,平铺于称量瓶中,置(60℃)恒温干燥箱内放置6 d,于第 0,3,6 d 取样,测定挥发油相对含量,见表4。结果表明,包合物在第3、6 d的挥发油相对含量呈逐渐下降的趋势,但较物理混合物,后者的相对含油量下降更为明显,可见姜黄挥发油β-CD包合物的热稳定性优于其物理混合物。
2.3.3 高湿试验 精密称取姜黄挥发油β-环糊精包合物和按照物料比混匀所得的姜黄挥发油与β-环糊精的物理混合物适量各3份,平铺于称量瓶中,置(RH 75 %,25 ℃)的密闭容器中放置6 d。于第 0,3,6 d 取样,测定挥发油相对含量,见表4。结果表明,包合物在第 3、6 d的挥发油相对含量均有所下降,但是降幅相比物理混合物小,在潮湿条件下,包合物的稳定性高于其物理混合物。

表4 姜黄挥发油包合物和物理混合物的影响因素稳定性试验(n =3)
3 结论与讨论
对于有效成分为挥发油的活性物质,由于挥发油极易氧化、挥发,直接将其混合于固体物料中容易造成有效成分的散失,影响制剂疗效。近年来,药物新技术β-环糊精(β-CD)包合技术在中药挥发油制剂中的应用,增强了药物的稳定性,提高了药物的生物利用度和疗效。本实验以挥发油包合率和包合物收得率加权综合评分值为指标,采用正交设计优化了姜黄挥发油包合物的制备工艺处方。包合物的薄层色谱法和紫外分光光度法鉴别结果表明包合前后姜黄挥发油的主要成分基本一致,包合物已经形成。姜黄挥发油β-CD包合物的稳定性试验结果证实包合物在强光、高温、高湿环境下的稳定性均得到了一定改善提高,且通过包合掩蔽了其不良气味,增加了患者的使用顺应性,达到了制备包合物的目的。
实验中发现,在挥发油 β-CD包合物的制备过程中,对包合物得率影响较大的因素有挥发油的投料量和包合温度。挥发油的投料量在一定范围内的增加有提高包合物得率的作用,但是当投料过多后则有时反而会降低包合效果。常温下(25℃) β-CD的水溶解度为1.88% , 50℃时其溶解度可增加至5.27%,所以当温度升高时使得更多的环糊精溶解,增加了与挥发油的更多接触,从而达到较好的包合效果,同时也可避免在温度过高搅拌时所造成挥发油的逸散[13]。由于挥发油有一定的黏性,不易分散,在包合时加入一定量的无水乙醇对挥发油进行稀释,不仅可以降低挥发油的黏性,还可以增加油在水中的分散性,进而增加了β-CD饱和水溶液中主客分子的碰撞机会,有利于包合。
[1] 韩婷,宓鹤鸣.姜黄的化学成分及药理活性研究进展[J].解放军药学学报,2001,17(2):95.
[2] 王琰,王慕邹.姜黄属常用中药的研究进展[J].中国药学杂志,2001,36(2):80.
[3] JAYAPRAKASHA GL.Chemistry and Biological Activities of Curcuma Longa[J].Trends in Food Science & Technology,2005,16(12):533.
[4] 肖小河,苏中武,乔传卓,等.姜黄属药用植物研究进展[J].中草药,1997,28(1):114.
[5] 叶祖光.姜黄的医理学[J].国外医药.中医中药分册,1992,14(2):22.
[6] 王锐,刘晓莉,葛斌,等.消乳增胶囊挥发油提取及其 β-环糊精包合工艺研究[J].中成药,2013,35(3):619.
[7] 李海亮,郝晶晶,龚慕辛,等.中药挥发油β-环糊精包合物的稳定性影响因素考察[J].中国实验方剂学杂志,2012,18(23):14.
[8] 李冬梅,张新春,尹晓飞.β-环糊精包合艾叶挥发油的研究[J].中国医院药学杂志, 2005, 25 (6): 519.
[9] 国家药典委员会.中华人民共和国药典.一部[S]. 北京: 中国医药科技出版社,2010:附录XD.
[10] 刘宇,殷中琼,魏琴,等.油樟叶挥发油 β-环糊精包合物的制备工艺研究及稳定性考察[J].中国中药杂志,2013,38(13):2105.
[11] 吴波,任静,杨妍,等.薄荷油-羟丙基-β-环糊精包合物的制备与验证[J].中国实验方剂学杂志,2013,19(11):25.
[12] 司奇,吴丹,曹青日,等.缬草挥发油β-环糊精包合物的制备与评价[J].中国中药杂志,2013,38(14):2309.
[13] 靳怡然,杜英峰,袁志芳,等.戒毒胶囊制备工艺中挥发油提取及其 β-环糊精包合工艺的研究[J].中成药,2008,30(11):1710.

