从何首乌制备高纯度二苯乙烯苷的分离纯化方法△
李瑶,管淑玉,李将,王群,邓婉婷
(广东药学院 中药学院,广东 广州 510006)
·中药工业·
从何首乌制备高纯度二苯乙烯苷的分离纯化方法△
李瑶,管淑玉*,李将,王群,邓婉婷
(广东药学院 中药学院,广东 广州 510006)
目的:找到一种新的高速逆流色谱溶剂配比体系,以期从何首乌中得到高纯度的二苯乙烯苷。方法:以弱碱性条件对何首乌粗提液初步纯化,优化弱碱性条件,得到的二苯乙烯苷粗品再用高速逆流色谱来进一步纯化。结果:用优化后的弱碱性条件处理得到的二苯乙烯苷粗品,纯度达到96%,用高速逆流色谱进一步纯化,得到的二苯乙烯苷的纯度可达99%。结论:这种分离纯化二苯乙烯苷的方法充分利用了其在弱碱性条件下较稳定的特性,优化弱碱性条件能制备出高纯度的二苯乙烯苷。这种方法不仅避免了大孔树脂等柱色谱分离时的吸附损失和大量溶剂的消耗,还能弥补二苯乙烯苷因难以通过结晶而达到更高纯度的缺憾。本研究提供了一种大量、可重复制备高纯度二苯乙烯苷的途径。
何首乌;二苯乙烯苷;高速逆流色谱;分离纯化;弱碱性
何首乌中的二苯乙烯苷(TSG,全称为2,3,5,4′-四羟基二苯乙烯2-O-β-D-吡喃葡萄糖苷)为白色无定形粉末,易溶于水、甲醇、乙醇等。现代药理研究表明,二苯乙烯苷具有清除自由基[1]、抗衰老[2]以及抑制酪氨酸酶活性等作用[3]。
二苯乙烯苷的分离和纯化多采用柱色谱的方法,吕丽爽[4]应用聚酰胺柱色谱系统初步纯化了何首乌的乙醇粗提液,而后通过溶剂结晶技术,首次分离得到了二苯乙烯苷白色针状晶体。然而,柱色谱的方法溶剂消耗量大,操作繁琐,结晶成功率低。高速逆流色谱(HSCCC)是一种连续高效的液液分配色谱,基于样品中各化合物在两相溶剂之间分配系统的不同来达到分离纯化的目的。HSCCC消除了固液色谱中由于固相载体带来的吸附损失,从而提高了样品的回收率[5]。HSCCC已被用来分离何首乌中的二苯乙烯苷。管淑玉等[6]采用HSCCC一步法从何首乌中分离得到了纯度达96%的二苯乙烯苷。二苯乙烯苷在强酸性条件下极不稳定,TSG的苷键迅速水解;在强碱性条件下TSG易被氧化为醌类化合物;在弱碱性条件下,TSG较稳定[7]。因此,本试验设计出利用弱碱性条件来初步纯化二苯乙烯苷,再用高速逆流色谱进一步纯化二苯乙烯苷的方法,避免了柱色谱分离时的吸附损失和大量溶剂的消耗,为制备高纯度的二苯乙烯苷提供了一种新的、简单、可行性高的途径。
1 仪器与试剂
1.1 仪器
TBE300A型高速逆流色谱仪(上海同田生化技术有限公司);8823A型紫外检测器(北京宾达英创科技有限公司);N2000在线色谱工作站、色谱柱(Dikma Technologies);LC-20A型高效液相色谱仪、UV-2550型紫外-可见分光光度计(日本岛津公司);RE-52CS 型旋转蒸发仪(巩义市予华仪器有限公司);超声机(深圳洁康PS-30)。
1.2 材料与试剂
何首乌药材购自于广州采芝林药店,由广东药学院刘基柱副教授鉴定为蓼科植物何首乌PolygonummultiflorumThumb.的干燥块根。2,3,5,4′-四羟基二苯乙烯2-O-β-D-吡喃葡萄糖苷对照品(中国食品药品检定研究院,批号:0844-201103);乙腈(美国Crude Company,色谱纯,批号:885900);蒸馏水(屈臣氏,批号:20140326);其余试剂均为国产分析纯。
2 方法
2.1 药材提取及前处理方法
2.1.1 药材提取方法 称取5.0 g何首乌药材打成粗粉,置于圆底烧瓶中,用75 mL的70%乙醇超声提取30 min,抽滤,滤渣再加75 mL的70%乙醇超声提取30 min,抽滤,合并2次滤液,浓缩至5 mL。
2.1.2 粗提液弱碱性处理方法 将上述浓缩液用等量乙酸乙酯多次萃取,照薄层色谱,直至365 nm下水层无二苯乙烯苷吸收(展开剂为乙酸乙酯∶甲醇∶水=20∶2∶1),合并乙酸乙酯层,蒸干。用10 mL蒸馏水溶解,将其分为5份,分别记为A、B、C、D、E,将A、B、C、D分别用1 mol·L-1的氢氧化钠溶液调节其pH至7.0、8.0、9.0、10.0;样品E的pH为3.5。将A、B、C、D分别用乙酸乙酯萃取至水层无二苯乙烯苷吸收,合并乙酸乙酯层,均浓缩至2 mL。将上述萃取浓缩后的样品按照《中华人民共和国药典》所述的方法进高效液相色谱仪,测定二苯乙烯苷的纯度和含量,取最优pH条件下的二苯乙烯苷粗品,用高速逆流色谱进一步纯化。
2.2 高速逆流色谱的分离方法
2.2.1 溶剂系统的调整 将4种溶剂按照比例(正己烷∶乙酸乙酯∶乙醇∶水=4.5∶50∶0.8∶50)置于分液漏斗中,充分混匀,静置分层。取等量的上下相置于试管中,加入一定量的何首乌粗提液,振荡,充分混匀,然后静置分层。取等量的上下层分别用紫外分光光度仪在320 nm处测吸光度,计算二苯乙烯苷在上下相中的分配系数K值。分配系数K=Cs /Cm,其中Cs指溶质在固定相中的浓度,Cm指溶质在流动相中的浓度,K值的最佳范围是0.5~2。
2.2.2 高速逆流色谱的参数设置 上层作为固定相,下层作为流动相。主机转速为800 r·min-1,顺时针旋转,紫外检测波长为280 nm,进样量为1 mL(样品浓度按生药计为1 g·mL-1),根据色谱图手动收集各色谱峰组分。固定相保留率是分离柱中保留的固定相体积与分离柱的柱体积之比,计算公式如下:
Sf=(Vs/Vc)×100%。
其中,Vs为分离柱中固定相的体积,Vc为分离柱柱体积。
2.3 纯度分析和含量测定
参考《中华人民共和国药典》2010版一部“何首乌”项下方法[8],对高速逆流色谱仪分离得到的二苯乙烯苷样品进行纯度分析和含量测定。所用色谱柱为Dikma Technologies C18柱(250 mm×4.6 mm,5 μm),柱温为25 ℃;检测波长为200~800 nm,全波长扫描;进样量为5 μL;流动相为乙腈-水(25∶75)。面积归一化法计算纯度。
3 结果与分析
3.1 弱碱性条件pH值的优化
粗提液在4个弱碱性条件下,初步纯化后测得各二苯乙烯苷的纯度和含量,见表1。
表1中的数据用,SPSS17.0方差分析,算得pH值在8~10之间时,TSG纯度的P>0.05,差异无统计学意义,pH 7时TSG纯度分别与PH 8.0、9.0、10.0时的TSG纯度比较,差异有统计学意义(P<0.05)。4个pH条件下TSG含量P=0.000<0.01,差异极显著。综合考虑TSG纯度和得率,选用pH 8.0的条件处理过的TSG粗品进高速逆流色谱。
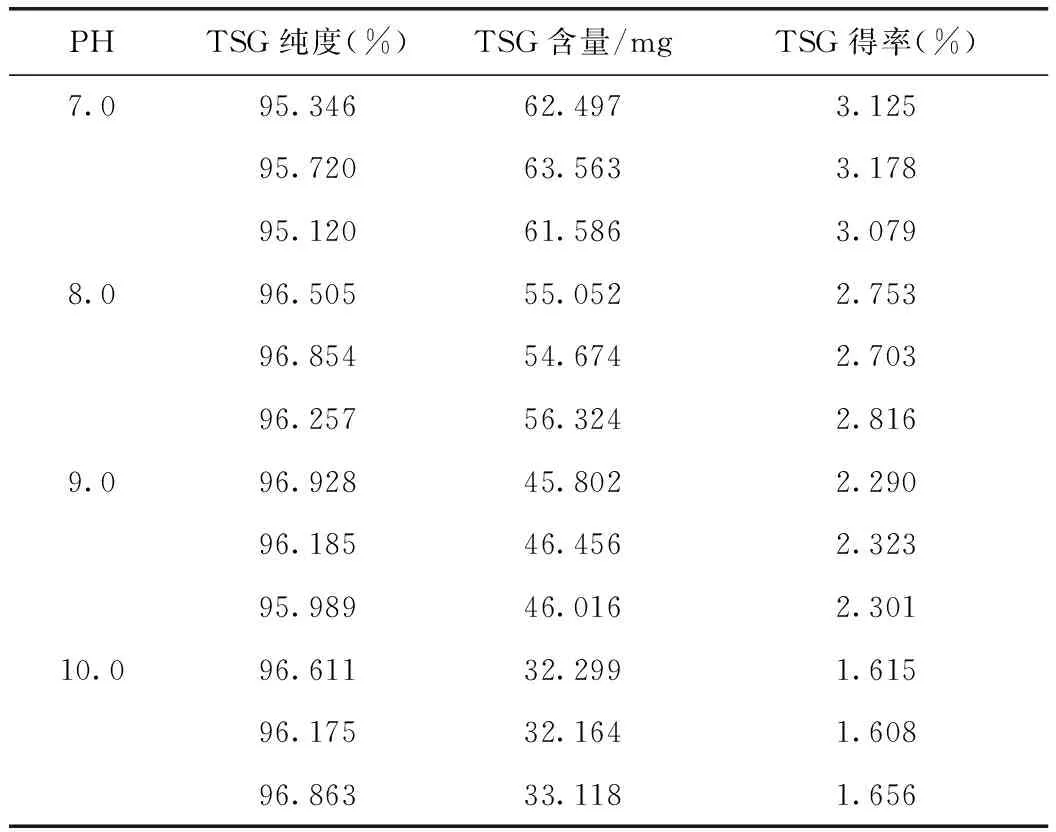
表1 各PH条件处理后TSG的纯度和含量
3.2 溶剂体系K值及固相保留率
逆流色谱仪中,固定相保留率按2.2.2中的公式计算,值为45.67%。TSG在溶剂体系中上下相的分配系数K值按照2.2.1中的公式计算,K值为1.196,在0.5 ~2范围之内。
3.3 高速逆流色谱分离纯化结果
选用pH 8.0条件下处理过的TSG粗品,用高速逆流色谱进一步纯化,其HSCCC谱图见图1。
取图1中2号峰所对应的馏分,按照2.3中的方法进行高效液相色谱鉴别,其液相结果见图2。高速逆流色谱分离得到的TSG纯品的纯度为99.15%,面积归一化法算得TSG的得率为2.704%。

图1 TSG粗品高速逆流色谱分离图

注:A.TSG样品色谱图;B.TSG对照品色谱图;C.阴性对照色谱图。图2 HSCCC中2号峰的液相结果图
4 讨论
4.1 二苯乙烯苷初步纯化
何首乌中主要含有多糖、蒽醌、黄酮、酚类、二苯乙烯苷类等活性成分[9]。本文依据蒽醌在弱碱性条件下不稳定,而TSG在弱碱性条件下稳定这一特性,采用弱碱性条件处理,以除去部分蒽醌类杂质。结果表明,弱碱性条件下处理何首乌粗提液,可得到纯度高达96%的TSG粗品,这种纯化方法操作简单,重复性好,具有进一步工艺放大的可能。
4.2 溶剂系统的调整
本文根据二苯乙烯苷在上下相中的分配系数K值对高速逆流色谱的溶剂体系进行调整。一般来说,K<0.5,出峰太快,峰之间的分离度较差;K>2出峰时间较长,峰形变宽,最佳K值应在1.0左右[10]。本研究适当增大了正己烷的比例,使得上相的疏水性更强,二苯乙烯苷在上相中的溶解度减小。最终测得的二苯乙烯苷在溶剂体系中的K值为1.196,出峰时间较合适,分离度较好。本研究中分离纯化二苯乙烯苷的方法避免了大孔吸附树脂等柱色谱分离时的吸附损失和大量的溶剂消耗,为制备高纯度的二苯乙烯苷提供了一种简单可行的途径。
[1] 周莹,刘广锋,冯娟,等.何首乌3种组分的提取及其清除DPPH自由基作用的研究[J].广东药学院学报,2014,30(3):301-304.
[2] 苗明三,方晓艳.制何首乌多糖对衰老模型小鼠抗氧化作用的研究[J].中药药理与临床,2002,18(5):23-24.
[3] Zequn Jiang,Jimin Xu,Minghai Long,et al.2,3,5,4′-tetrahydroxystilbene-2-O-β-d-glucoside(THSG)induces melanogenesis in B16 cells by MA Pkinase activation and tyrosinase upregulation[J].Life Sciences,2009,85(9):345-350.
[4] 吕丽爽.何首乌中二苯乙烯苷的制备及抗氧化机理研究[D].无锡:江南大学,2006.
[5] Oka F,Oka H,Ito Y.Systematic search for suitable two-phase solvent systems for high-speed counter-current chromatograph[J].J.Chromatogr.A,1991,538(1):99-108.
[6] 管淑玉,彭维,苏薇薇.高速逆流色谱法一步分离何首乌中的二苯乙烯苷[J].中药材,2008,31(7):1079-1080.
[7] 班翊,刘其礼,金悠,等.二苯乙烯苷的稳定性研究[J].中草药,2004(11):39-41.
[8] 国家药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2010:164-165.
[9] 张志国,吕泰省,姚庆强.何首乌的研究进展[J].解放军药学学报,2008,24(1):62-64.
[10] 曹学丽.高速逆流色谱分离技术及应用[M].北京:化学工业出版社,2005.
PurificationofHighPurityStilbeneGlycosidesfromPolygonummultiflorum
LIYao,GUANShuyu*,LIJiang,WANGQun,DENGWanting
(SchoolofTraditionalChineseMedicine,GuangdongPharmacuticalUniversity,Guangzhou510006,China)
Objective:To find a new system of HSCCC solvent rario for purification of high purity stilbene glycosides fromPolygonummultiflorum.Methods:The crude extract ofP.Multiflorumwas preliminary purified under the optimized weak alkaline.And the crude product of stilbene glycosides has been further purified by HSCCC.Result:The purity of stilbene glycosides crude product reached 96%.The stilbene glycosides further purified by HSCCC reach 99%.Conclusion:The high purity silbene glycoside could be isolated and purified by taking advantage of the stability of stilbene glycosides could under weak alkaline condition.The method could avoid adsorption loss and large solvent consumption in column chromatography like macroporous resin,and non-crystallizable stilbene glycosides,and the method provide a effective way to produce high purity stilbene glycosides in large scale.
Polygonum multiflorum;stilbene glycosides;HSCCC;purification;weakly alkaline
2014-07-12)
国家自然科学基金(81001702);省部产学研结合项目(2010B090400519);广东药学院人才启动基金(2007ZYX01);广东省大学生创新训练计划项目(1057312033)
*
管淑玉,副教授,研究方向:抗炎抑菌及色素调节活性物质研究;Tel:(020)39352177,Email:guanshy3@163.com
10.13313/j.issn.1673-4890.2015.4.020

