前列腺癌磁共振电阻抗成像新方法
刘 阳 郭建炎
1(厦门理工学院电气工程与自动化学院, 福建 厦门 361024)2(厦门理工学院光电与通信工程学院, 福建 厦门 361024)
前列腺癌磁共振电阻抗成像新方法
刘 阳1郭建炎2*
1(厦门理工学院电气工程与自动化学院, 福建 厦门 361024)2(厦门理工学院光电与通信工程学院, 福建 厦门 361024)
基于经肠道和尿道的体内电极方式,提出适用于人体深层、小体积前列腺癌诊断的磁共振电阻抗成像(MREEIT)新方法, 并通过仿真将该方法的成像结果与传统的体外电极MREIT方法进行对比。分别采用有限元方法及J-substitution算法,求解三维正问题和逆问题。仿真结果表明:在噪声存在的情况下,经肠道和尿道两种体内电极MREIT的成像效果均远优于体外电极方式;且在相同的噪声水平下,经尿道MREIT方式的成像效果更好。信噪比(SNR)为30且采用最佳电极配置方式时,经尿道和肠道体内电极MREIT得到的重构电导率与目标电导率之间的相对误差(RE)分别为10.32%和14.58%。研究提示,体内电极MREIT在前列腺癌诊断领域具有潜在应用价值。
前列腺癌;磁共振;电阻抗成像; J-substitution算法
引言
到目前为止,前列腺癌是美国男性中发病率最高、致死率第二的疾病种类[1]。前列腺特异性抗原(prostate-specific antigen, PSA)检测方法,由于特异度不高,只能被用作临床诊断中的替代性指标,而不能用于定性诊断[2-3]。超声指导的活检被认为是前列腺癌诊断的金标准,但由于其只能采样前列腺内离散点的信息,且作为有创检测技术无法在短时间内反复使用,因此研究一种无创的且具有较高敏感度和特异度的前列腺癌诊断技术是亟待解决的问题。
多项科学研究结果表明,正常及癌变前列腺组织的电导率差别很大[4-5],因此前列腺的电特性对于前列腺癌的诊断及后续治疗具有较高的医学应用价值。基于经肠道[6-7]和尿道[8-10]的体内电极电阻抗断层成像(electrical impedance tomography, EIT)技术曾被研究用于前列腺癌诊断,但该技术测量电压的个数远小于待重构未知数的个数,其逆问题表现出严重的病态性,最终导致重构图像分辨率较低,从图像上无法分辨出病变部位及病变程度。磁共振电阻抗成像(magnetic resonance electrical impedance tomography, MREIT)可以显著提高重构图像的分辨率和成像精度。韩国研究小组采用MREIT,对犬齿动物盆腔进行成像实验[11]。从重构图像中,可以辨别出前列腺及周边组织区域,具有较高的对比度,但目前该项技术并未用于前列腺癌的检测。
本研究将体内电极EIT的思想引入到磁共振电阻抗成像,提出了专门适合前列腺癌诊断的、经肠道和尿道的体内电极磁共振电阻抗成像方法。该方法与传统体外MREIT的对比结果表明,经肠道和尿道的体内电极MREIT方式具有更高的成像精度,这为未来前列腺癌的诊断提供了一种新途径。
1 方法
1.1 正问题描述
假设Ω为R3中的有界导电区域,Γ表示边界。σ为Ω区域的电导率,取正值。通过表面电极向物体注入微小电流,物体内电势分布φ满足如下Poisson方程和Neumann边界条件,有
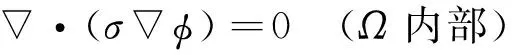
(1)
(2)
式中,n为物体表面单位外法线向量;Jinj为注入的表面电流密度,在电流注入电极位置非零。
物体内电场E及电流密度J分布为
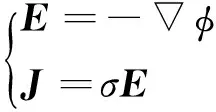
(3)
对于复杂人体组织模型,无法得到式(1)、(2)所描述的边值问题的解析解,可采用有限元(finite element method, FEM)方法得到其数值解。
1.2 逆问题描述
采用MREIT J-substitution算法[12]迭代更新物体内部电导率分布,有
(4)
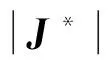
1.3 仿真设计
目前,用于电导率成像的人体盆腔仿真模型共有两种:二维圆形模型[8-9]及三维圆柱(模拟人体盆腔)与球或椭球(模拟其中的前列腺组织)组合模型[2-3]。本研究中采用直径为30 cm、高为20 cm的圆柱体模拟人体盆腔,采用横径4 cm、纵径3 cm、厚度为2 cm的倒置圆锥体模拟前列腺[8]。圆锥体的尖端距圆柱下表面6 cm,其中心偏离圆柱中心2.7 cm。模拟人体盆腔的外圆柱的电导率设为0.24 S/m[13],良性和癌变前列腺组织的电导率分别为0.15 S/m和0.1 S/m[3]。
基于目标电导率分布求解正问题,得到目标电流密度分布。通过在该电流密度上施加不同信噪比(signal-to-noise ratio, SNR)的高斯随机噪声,模拟实际测量得到的电流密度分布。用目标电导率与重构电导率之间的相关系数(correlation coefficient, CC) 和相对误差(relative error, RE),对重构结果进行定量评估[12]。
1.3.1 经肠道体内电极MREIT仿真设计
将带有4个表面电极的探测器经直肠伸入体内,注入电流并测量电压。探测器直径为2 cm、长度为11 cm[2],其上电极大小为0.5 cm×0.5 cm。为了考察电极位置对重构结果的影响,针对3种电极配置方案进行仿真:方案1,成对电极角度相对,高度相同;方案2,4个电极均配置在面向前列腺一侧;方案3,电极在高度方向和角度方向均匀分布。
经肠道MREIT仿真模型及电极配置模型如图1所示。本研究中的所有仿真均分别以电极1、3和电极2、4作为成对电极,注入两次双极性方波电流。为了清晰起见,体内电极方式的仿真模型中均不显示模拟人体盆腔的外圆柱。在MREIT中所使用的双极性方波电流的主要频率分量为10 Hz[14],且研究表明3 kHz以下的频率、2 A/m2的电流密度对人体来说是安全的[15]。为了满足这一安全标准,相对于3种电极配置方案,注入电流的强度分别为1.20,1.06及1.31 mA。
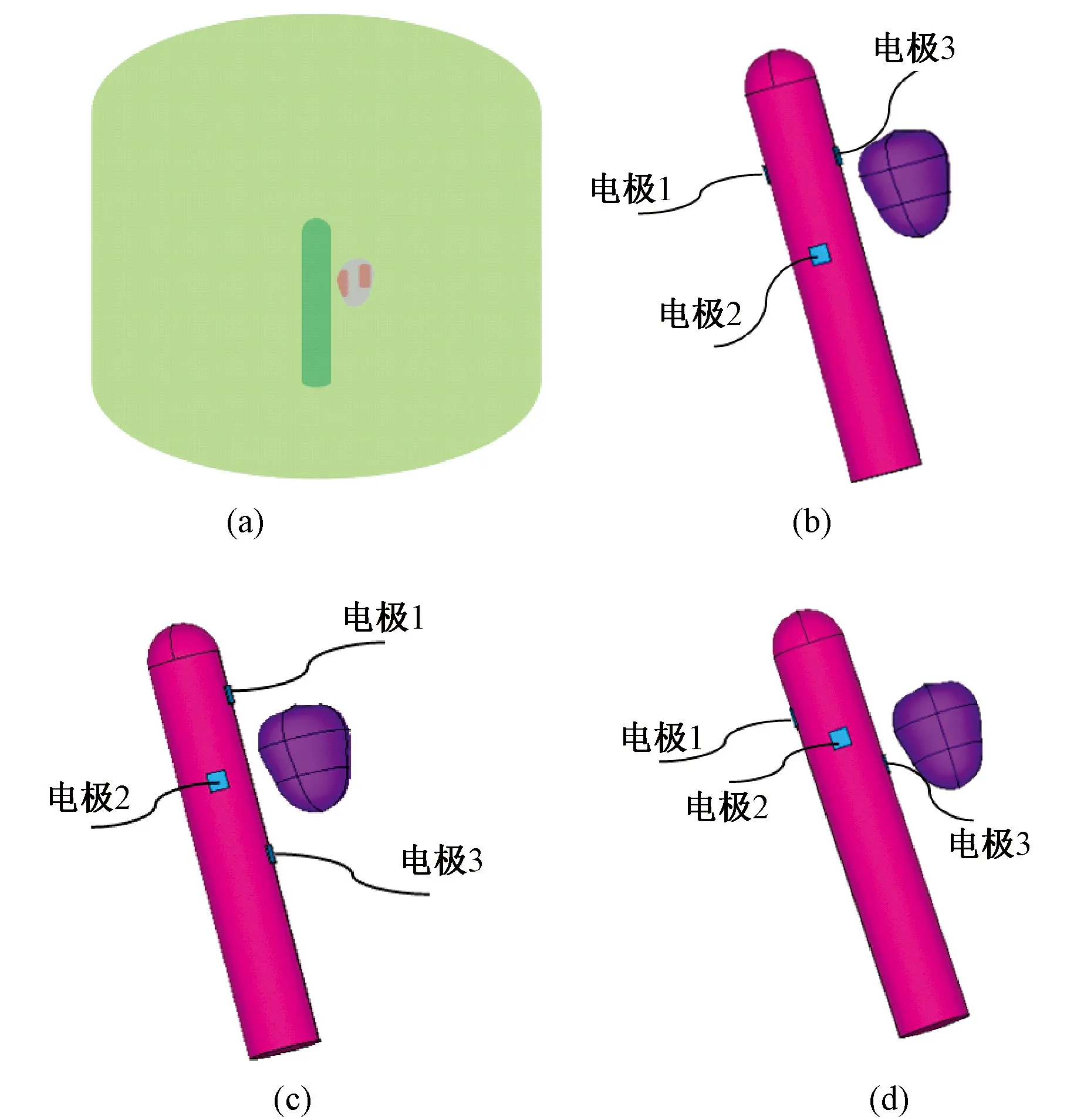
图1 经肠道MREIT仿真模型及电极配置。(a)经肠道MREIT仿真模型;(b)方案1;(c) 方案2; (d) 方案3Fig.1 Simulation model and electrode configurations of trans-rectal MREIT.(a)Simulation model of trans-rectal MREIT; (b)1st configuration; (c)2nd configuration; (d)3rd configuration.
1.3.2 经尿道体内电极MREIT仿真设计
将带有4个表面电极的探测器经尿道伸入体内。探测器直径0.8 cm[8],长9 cm,其上的电极大小为0.3 cm×0.3 cm。为了考察电极位置对重构结果的影响,针对类似于经肠道MREIT的3种电极配置方案进行仿真。
经尿道MREIT仿真模型及电极配置模型如图2所示。为了满足2 A/m2的安全电流标准,3种电极配置方案注入电流的强度分别为0.95,0.82及1.12 mA。
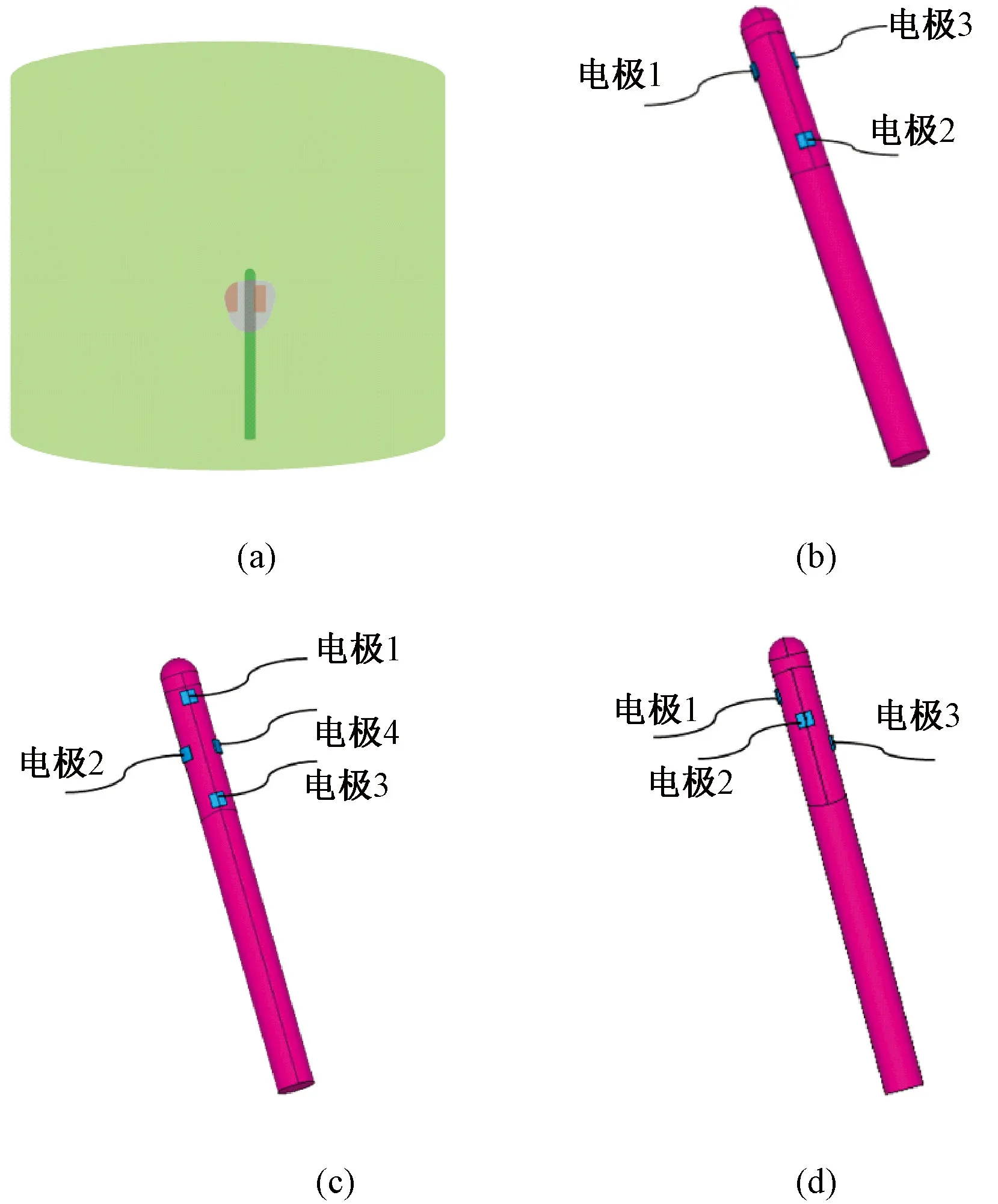
图2 经尿道MREIT仿真模型及电极配置。(a)经尿道MREIT仿真模型;(b)方案1(c)方案 2 (d) 方案3Fig.2 Simulation model and electrode configurations of trans-urethral MREIT. (a)Simulation model of trans-urethral MREIT; (b) 1st configuration; (c)2nd configuration; (d)3rd configuration
1.3.3 体外电极MREIT仿真设计
为了将所提出的体内电极MREIT方式与传统体外电极MREIT的成像效果进行对比,针对体外电极MREIT方式进行仿真。将4个面积为5 cm×5 cm的表面电极均匀地放置在圆柱的外表面,电极中心距圆柱下表面8 cm,即前列腺位于电极覆盖高度范围内。体外电极MREIT仿真模型如图3所示。为了满足相同的安全电流标准,注入的双极性方波电流的强度为3.22 mA。
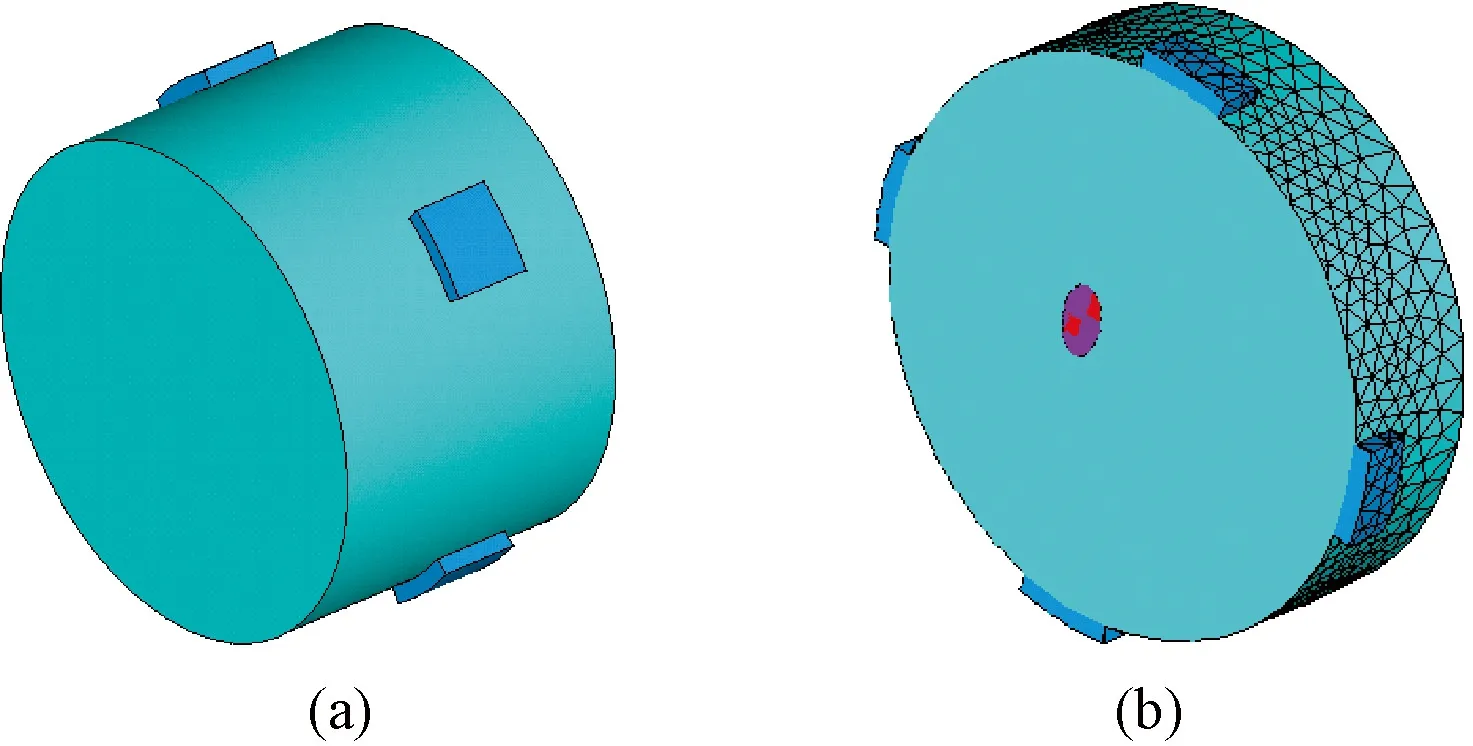
图3 体外电极MREIT仿真模型及有限元模型界面图。 (a)仿真模型;(b)有限元模型切面图Fig.3 Simulation model and cross-section image of FEM for external MREIT. (a)Simulation model; (b) FEM cross-sectional
2 结果
2.1 经肠道体内电极MREIT仿真结果
图4给出了目标电导率及不同噪声水平下经肠道MREIT不同电极配置方案的重构电导率分布,较深色为模拟的癌症组织,较淡色为良性组织,所有重构结果展示在图中均采用该表示方法。可以看出,电极配置方案3的重构结果最好,即使在SNR=30时,仍能从重构图像中分辨出癌变组织的位置和大小。
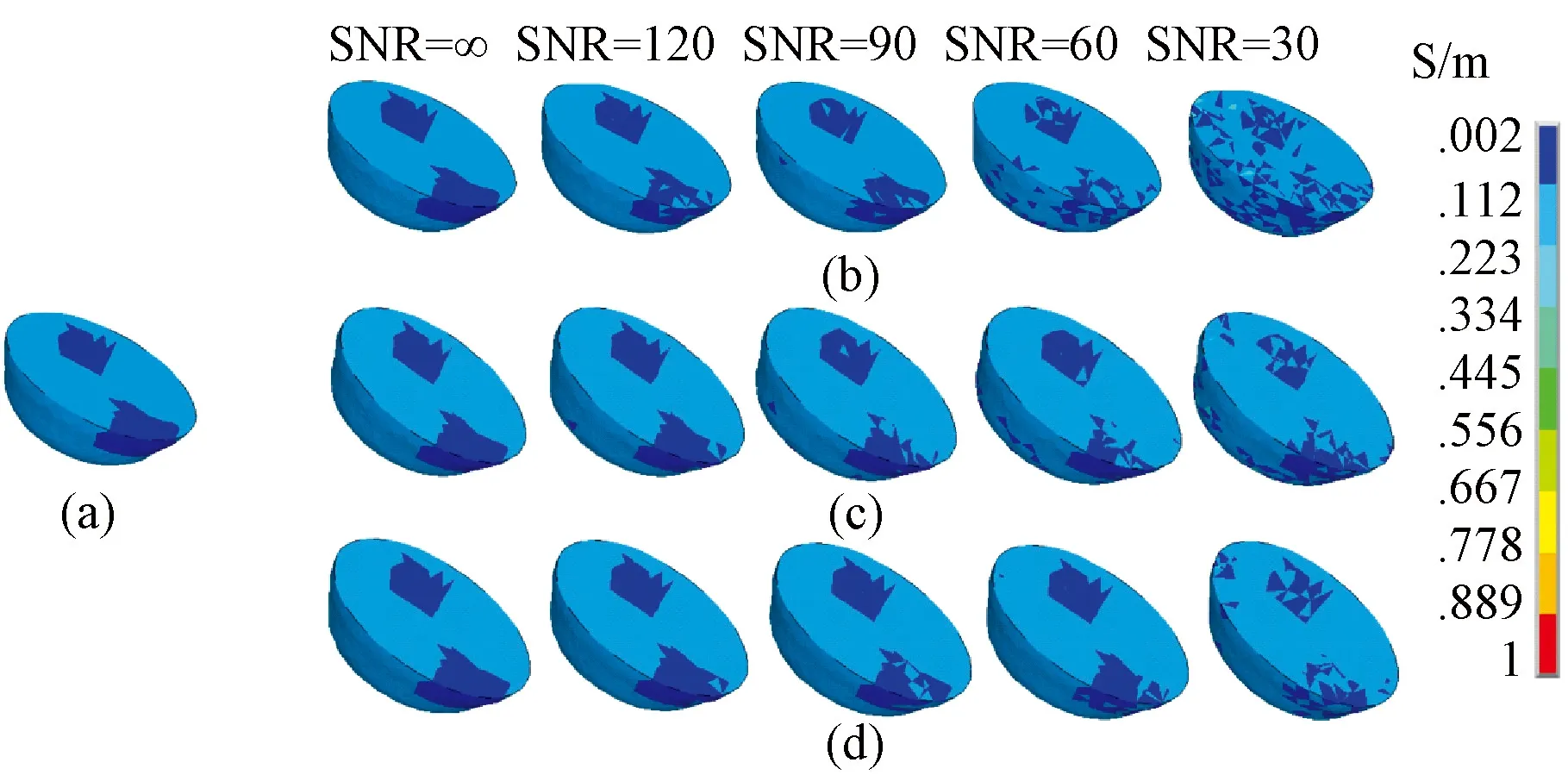
图4 不同SNR时各电极配置方案的经肠道MREIT重构电导率分布。(a)目标电导率分布;(b)方案1重构电导率分布;(c)方案2重构电导率分布;(d) 方案3重构电导率分布Fig.4 Reconstructed conductivity distributions achieved by trans-rectum MREIT with different SNRs and different electrode configuration manners.(a)Target conductivity distribution;(b) Reconstructed conductivity distributions achieved by the 1st manner; (c) Reconstructed conductivity distributions achieved by the 2nd manner; (d) Reconstructed conductivity distributions achieved by the 3rd manner.
2.2 经尿道体内电极MREIT仿真结果
图5给出了不同噪声水平下经尿道体内电极MREIT的成像结果。可以看出,电极配置方案2的重构效果最好,但在SNR=30时,任何一种电极配置方式,经尿道MREIT均能成像出其内部的癌变组织。
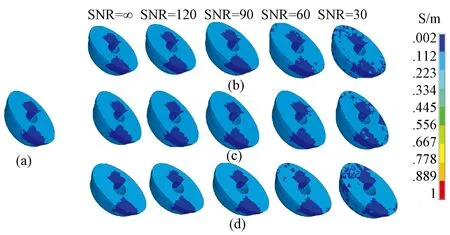
图5 不同SNR时各电极配置方案的经尿道MREIT重构电导率分布。(a)目标电导率分布;(b)方案1重构电导率分布;(c)方案2重构电导率分布;(d))方案3重构电导率分布Fig.5 Reconstructed conductivity distributions achieved by trans-urethral MREIT with different SNRs and different electrode configuration manners. (a)Target conductivity distribution; (b) Reconstructed conductivity distributions achieved by the 1st manner; (c) Reconstructed conductivity distributions achieved by the 2nd manner; (d) Reconstructed conductivity distributions achieved by the 3rd manner.
2.3 体外电极MREIT仿真结果
由图6体外电极MREIT重构结果可见,在SNR=∞时,重构电导率能精确反映目标电导率的分布情况。但当存在噪声时,即使在SNR=120的情况下,从重构图像中已很难分辨出良性及癌变组织。
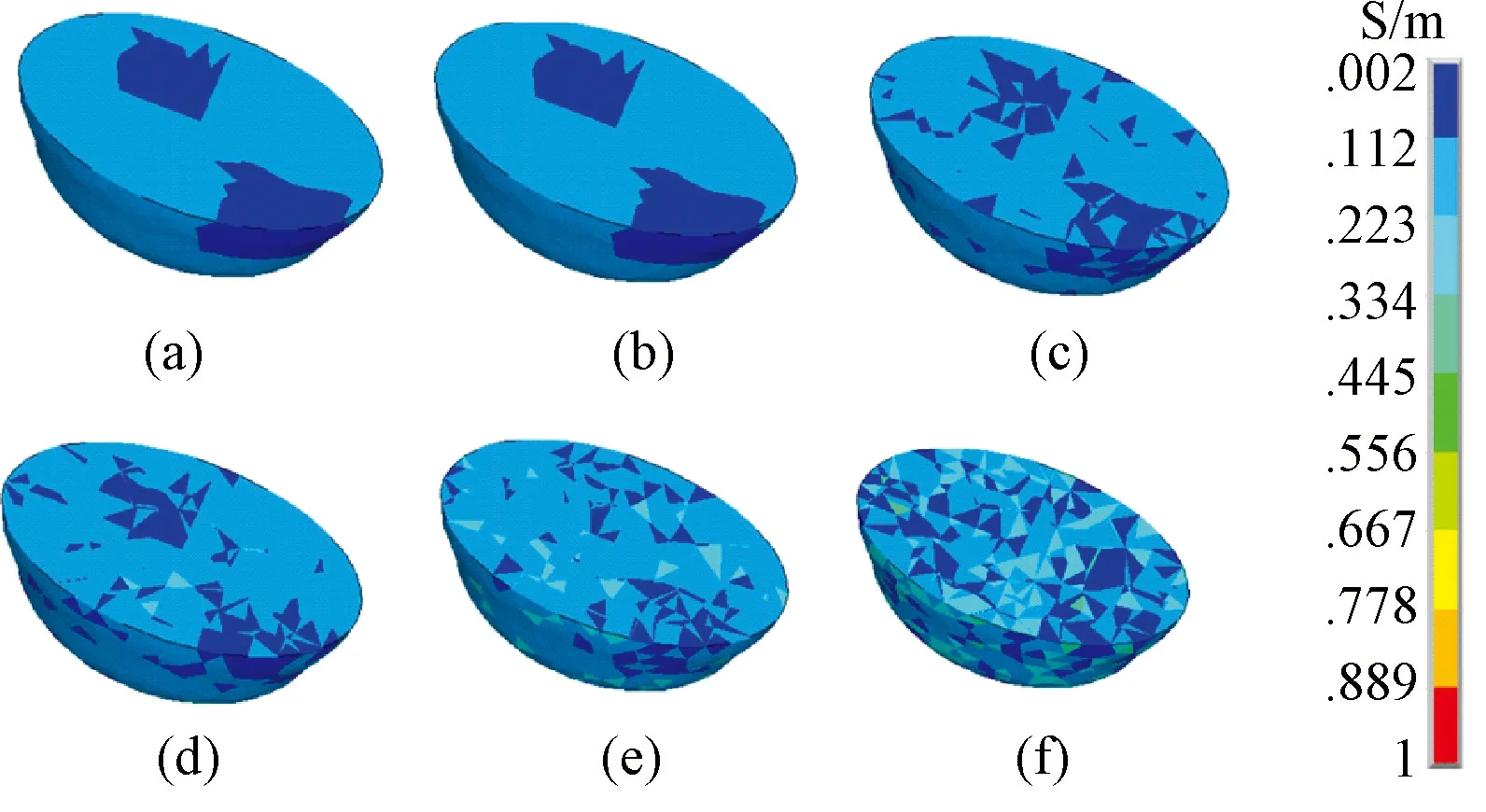
图6 目标电导率及不同噪声水平下体外电极MREIT重构电导率分布。(a)目标电导率;(b)~(f)分别为SNR=∞,120,90,60及30时的重构电导率分布Fig.6 Target and reconstructed conductivity distributions achieved by external MREIT with different noise levels.(a)Target conductivity distribution;(b)~(f)Reconstruction conductivity distributions with SNR=∞,120,90,60 and 30
2.4 3种MREIT成像结果对比
将图4~图6对比可以发现:在SNR=∞的理想情况下,两种体内电极MREIT方式的重构效果与体外方式相当,即重构电导率能精确地反映目标电导率分布;但当存在噪声时,两种体内电极方式的重构效果远远优于体外电极方式。图7展示了两种体内电极MREIT、不同电极配置方式时目标电导率与重构电导率之间的CC和RE曲线。由该图可以看出:经肠道体内电极配置方案1重构电导率与目标电导率之间的相关系数CC最小,相对误差RE最大,即其重构效果最差;经尿道体内配置方案2重构电导率与目标电导率之间的相关系数CC最大,相对误差RE最小,即其重构效果最好;除电极配置方案3在较低的噪声水平下(SNR=120)这种情况外,经尿道方式的重构效果均优于经肠道方式的重构效果。
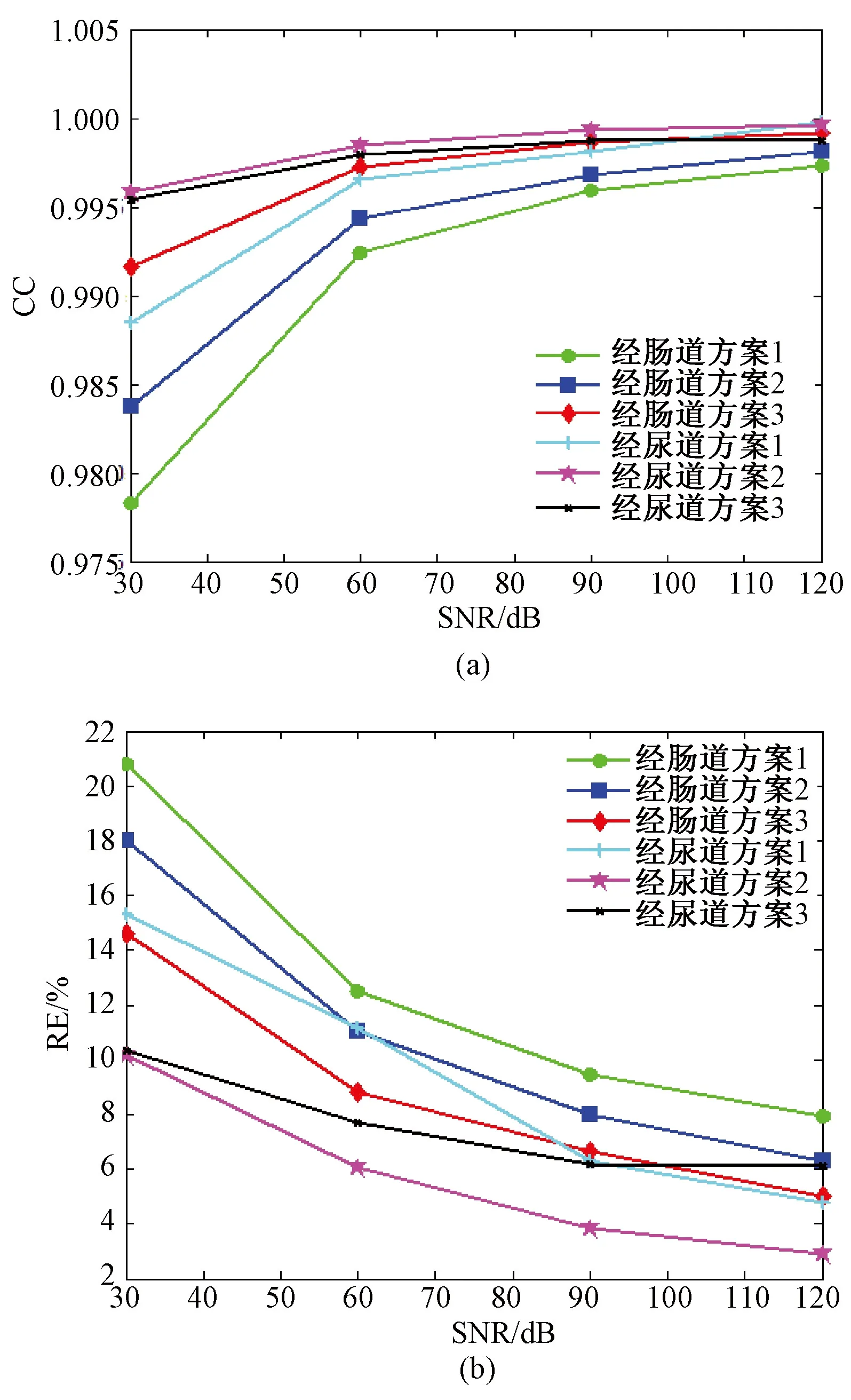
图7 不同噪声水平不同电极配置方式经肠道和尿道MREIT重构结果对比。(a)CC曲线;(b)RE曲线Fig.7 Comparison of reconstruction results between trans-rectal and trans-urethral MREITs with different electrode configurations at difference noise levels.(a)CC curve;(b)RE curve
3 讨论和结论
采用不同的电极对注入电流,会影响电流在周边组织的流通路径,导致周围组织内不同的电磁场分布,进而会影响不同组织区域内磁共振测量信号的信噪比及MREIT的重构效果[16]。从本仿真研究也可以发现,体内电极MREIT和不同的电极配置方式对重构结果影响较大。本研究中,对于经肠道和尿道体内电极MREIT均考虑了3种电极配置方案,并不排除在实际中存在比这3种方案更合理的电极配置方式的可能性。因此,在未来的研究中,基于优化理论,针对不同的周边组织形状和电磁材料属性,提出确定最优电极配置方案的方法,提高前列腺内测量信号的信噪比,进而取得最优的成像效果,确实具有重要的研究意义。笔者的目的在于研究新的尤其适合于前列腺癌检测的MREIT新方法,对比同样条件下体内电极MREIT与体外电极方式的成像效果。下一步将基于MRI图像构建包含皮肤、骨骼、肌肉以及盆腔器官的真实人体盆腔模型,在该模型上进行更加详细的研究。
本研究将体内电极EIT的思想引入到磁共振电阻抗成像,提出了专门适合于前列腺癌检测的经肠道和经尿道体内电极MREIT新方法。在将体内电极与传统体外MREIT的成像精度进行对比的同时,也对比了不同电极配置方案下两种体内电极方式的成像效果。仿真结果表明:在无噪声情况下,两种体内电极方式的成像效果与体外电极方式相当;但当噪声存在时,两种体内电极MREIT的成像效果远远优于体外方式,且经尿道MREIT的重构效果更优。仿真结果展现了体内电极磁共振电阻抗成像在前列腺癌诊断中的良好应用前景,有望为前列腺癌诊断提供一条新途径。
[1] Siegel R, Ward E, Brawey O,etal. Cancer statistics,2011: the impact of eliminating socioeconomic and racial disparities on premature cancer deaths [J]. Cancer J Clin, 2011, 61(4):212-236.
[2] Borsic A, Halter R, Wan Y,etal. Sensitivity study and optimization of a 3D electric impedance tomography prostate probe [J]. Physiol Meas,2009, 30(6): 1-22.
[3] Borsic A, Halter R, Wan Y,etal.Electrical impedance tomography reconstruction for three-dimensional imaging of the prostate [J]. Physiol Meas,2010,31(8): 1-18.
[4] Halter R J, Schned A, Heaney J,etal. Electrical impedance spectroscopy of benign and malignant prostatic tissues [J]. J Urol, 2008,179(4): 1580-1586.
[5] Halter R J, Schned A, Heaney J,etal. Electrical properties of prostatic tissues: I single frequency admittivity properties [J]. J Urol,2009,182(4): 1600-1607.
[6] Borsic A, Halter R, Wan Y,etal. Sensitivity study of a 3D electrical impedance tomography prostate probe [C]// Proceedings of World Congress on Medical Physics and Biomedical Engineering. Munich: Springer, 2009,25: 673-676.
[7] Wan Y, Halter R, Borsic A, et al. Sensitivity study of an ultrasound coupled transrectal electrical impedance tomography system for prostate imaging [J]. Physiol Meas,2010,31(8): 17-29.
[8] Jossinet J, Marry E, Montalibet A. Electrical impedance endo-tomography: imaging tissue from inside [J]. IEEE Trans Biomed Eng, 2002,21(6): 560-565.
[9] Jossinet J, Desseux A. Electrical impedance endotomography: sensitivity distribution against bipolar current patterns [J]. Physiol Meas,2004,25(1): 355-364.
[10] Jossinet J, Desseux A, Matias A. Assessment of electrical impedance endotomography for hardware specification [J]. Biomed Imaging Interv J, 2006,2(2): e24.
[11] Kim H J, Jeong W C, Kim YT,etal. In Vivo conductivity imaging of canine male pelvis using a 3T MREIT system [C]// J Phys Conf Ser, 2010,224:012020.
[12] Liu Yang, Zhu Sanan, He Bin. Induced current magnetic resonance electrical impedance tomography of brain tissues based on J-substitution algorithm: a simulation study [J]. Phys Med Biol,2009,54(14): 4561-4573.
[13] Rush S, Abildskov JA, Mcfee R. Resistivity of body tissues at low frequencies [J]. Circ Res, 1963,12(8): 40-50.
[14] Arpinar V E, Hamamura M J, Degirmenci E,etal. MREIT experiments with 200 μA injected currents: a feasibility study using two reconstruction algorithms, SMM and harmonic Bz [J]. Phys Med Biol, 2012, 57(13): 4245-4261.
[15] Giland O, Horesh L and Holder D S. Design of electrodes and current limits for low frequency electrical impedance tomography of the brain [ J]. Med Bio Eng Comput, 2007,45(7): 621-633.
[16] Lee BI, Oh SH, Kim T,etal. Basic setup for breast conductivity imaging using magnetic resonance electrical impedance tomography [J]. Phys Med Biol, 2006, 51(2): 443-455.
A Novel Method of Magnetic Resonance Electrical Impedance Tomography for Prostate Cancer Detection
Liu Yang1Guo Jianyan2*
1(SchoolofElectricalEngineeringandAutomation,XiamenUniversityofTechnology,Xiamen361024,Fujian,China)2(SchoolofOpto-ElectronicandcommunicationEngineering,XiamenUniversityofTechnology,Xiamen361024,Fujian,China)
prostate cancer; magnetic resonance; electrical impedance tomography; J-substitution algorithm
10.3969/j.issn.0258-8021. 2015. 04.016
2014-07-24, 录用日期:2014-12-31
福建省自然科学基金(2013J05102)
TM15;TP391.9
D
0258-8021(2015) 04-0496-05
*通信作者 (Corresponding author),E-mail: guonetmail@163.com

