镉在棕壤上的吸附过程及其对土壤酶活性的影响
江泳,王伟,王玉慧,赵培
(临沂市国土资源局,山东 临沂 276001)
镉在棕壤上的吸附过程及其对土壤酶活性的影响
江泳,王伟,王玉慧,赵培
(临沂市国土资源局,山东 临沂276001)
土壤对镉的吸附过程是影响镉在土壤溶液中的浓度、迁移性、潜在毒性的重要因素。土壤微生物活性作为土壤质量的重要指标之一,对土壤重金属的含量具有较好的指示作用。该文研究了重金属镉在棕壤中的吸附过程,及在此过程中土壤酶活性的变化。结果表明,随着溶液中Cd2+含量的增大,两种土壤对Cd2+吸附量逐渐增大,且吸附反应符合Freundlich模型。随着镉初始浓度的增加,土壤中脲酶和过氧化氢酶的活性均出现抑制现象,其中脲酶对镉的反应更加敏感。
镉;棕壤;吸附过程;土壤酶活性
引文格式:江泳,王伟,王玉慧,等.镉在棕壤上的吸附过程及其对土壤酶活性的影响[J].山东国土资源,2015,31(2):32-34.JIANG Yong, WANG Wei, WANG Yuhui, etc. Adsorption Effect of Cd in Brown Soil and Its Influence to Soilenzyme Activity[J]. Shandong Land and Resources, 2015,31(2):32-34.
0 引言
土壤重金属污染问题在国际上引起了广泛的关注。随着工农业的发展,我国受Cd,As,Pb,Hg,Zn等重金属污染的耕地面积近2000万hm2,约占总耕地面积的五分之一[1]。
吸附-解吸是控制重金属植物有效性的主要过程之一,土壤中重金属的吸附-解吸直接影响重金属在土壤及其生态环境中的形态转化和迁移,最终影响农产品的质量及人类的生存环境[2]。因此对重金属在土壤上吸附过程的研究,有助于对进入环境中的重金属行为及形态变化深入理解。
重金属离子进入土壤后将对土壤酶活性产生抑制或激活作用,进而影响土壤养分释放及从土壤中获取养分的作物生长,因此土壤酶活性的测定将有助于判断土壤重金属污染程度及其对作物生长的影响[3]。国内外众多学者已开始研究利用土壤酶活性评价土壤重金属污染的可行性[4-5],并取得了显著进展。
该文以土壤中典型的重金属镉为实例,从镉在土壤中的吸附过程及其对土壤酶活性的影响两个方面展开研究,旨在了解镉在土壤中吸附过程的同时伴随土壤酶活性变化的状况。
1 材料与方法
1.1供试土壤
实验土样为棕壤,将采取的土壤放于通风处,晾干,磨碎,过20目筛,土壤基本理化性质见表1。

表1 供试土壤基本理化性质
1.2等温吸附试验
称取5.0g过20目筛的土壤放入1组离心管中,以0.01mol L-1的KNO3溶液为介质,分别加入不同体积0.01mol L-1的CdCl2溶液,使上清液中Cd的浓度保持在0,2,6,10,15,20,30,50mg L-1;每个浓度重复4次,恒温25℃下震荡24h,离心,上清液用原子吸收测定Cd的含量,土样用于土壤酶活性的测定。土壤对Cd的吸附量:
(1)
式中:Qt为土壤对Cd的吸附量(mg kg-1),V0为吸附实验开始溶液体积(L),M为烘干土重量(kg),C0为吸附实验初始液浓度(mg L-1),Ct为t时刻平衡溶液浓度(mg L-1)。
1.3土壤酶活性测定
1.3.1过氧化氢酶活性的测定
取1g风干土,置于100mL三角瓶中,并注入40mL蒸馏水和5mL 0.3%过氧化氢溶液。将三角瓶放在往复式震荡机上,震荡20min。而后加入5mL 3mol/L硫酸,以稳定未分解的过氧化氢。再将瓶中悬浮液用慢速型滤纸过滤。然后吸取25mL滤液,用0.1mol L-1高锰酸钾滴定至淡粉红色终点。
1.3.2脲酶活性的测定
取1g风干土,置于50mL三角瓶中,加1mL甲苯。15min后加10mL l0%尿素液。摇匀后在37℃恒温箱中培养24h。过滤后取3mL滤液注入50mL容量瓶中,然后加蒸馏水至20mL。再加4mL苯酚钠溶液和3mL次氯酸钠溶液,随加随摇匀。20min后显色,定容。1h内在分光光度计上于波长578mn处比色。计算尿酶活性以24h后1g土壤中NH4-N的毫克数表示。
1.4数据分析
土壤对镉的吸附实验数据用Freundlich模型进行了模拟:
(2)
式中:Kf为土壤的吸附能力(dm3kg-1),n为吸附强度。
2 结果与分析
2.1镉在棕壤上的吸附过程
不同浓度镉在两种土壤上的吸附过程如图1所示,结果显示,镉浓度较低时,土壤对镉的吸附量随浓度的增加而快速增加,随着初始镉浓度的增加,土壤镉吸附率随着溶液中镉平衡浓度的增加而减小,这与前人的报道相一致[6-7]。相比两种土壤,不同镉处理浓度下,土样1对镉的吸附量均大于土样2,这主要与两方面的原因有关,首先,从土壤的机械组成来看,土样1的粘粒含量高于土样2,而研究发现粘粒高的土壤对镉的吸附量较大[8];其次,土壤的酸碱性对镉的吸附量有很大的影响,研究表明随着土壤pH的升高,土壤对镉的吸附量增加[9],而土样1的土壤比土样2稍高,这也可能是导致其吸附量相对稍高的原因。
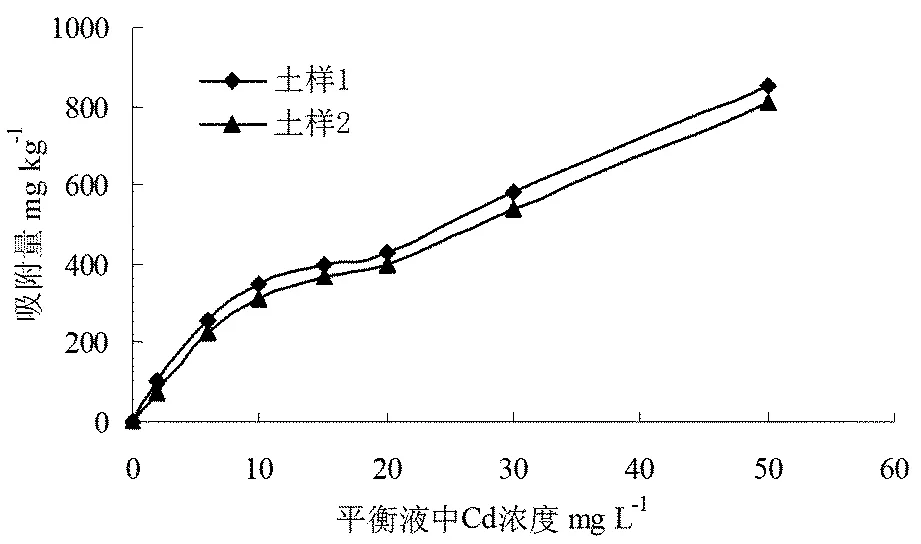
图1 不同浓度镉在土壤上的吸附量
2.2土壤对镉的吸附过程方程拟合
两种土样对镉的吸附过程通过Freundlich方程进行了拟合,拟合参数如表2所示。从表中可以看出,镉在两种土样上的吸附过程均可以通过Freundlich方程进行模拟,相关系数分别为0.9752和0.9326,达到极显著水平。两种土样中,土样1对镉的吸附能力(Kf=193.25)大于土样2(Kf=186.19)。

表2 土壤对镉的等温吸附方程拟合参数
注:**表示在0.01显著水平上相关
2.3镉的吸附对土壤酶活性的影响

图2 镉在土壤上的吸附对脲酶活性的影响

图3 镉在土壤上的吸附对过氧化氢酶活性的影响
镉在两种土样上的吸附均对土壤酶活性产生了很大的影响,图2为镉在两种土样上的吸附对土壤脲酶活性的影响。从图中可以看出,镉的吸附显著地抑制了土壤脲酶的活性,添加不同浓度的Cd后,立即表现出强烈的抑制作用,浓度越大,抑制率越大。实验结束时两种土样中脲酶的活性分别降低了79.16%和74.97%。图3为镉在两种土样上的吸附对土壤过氧化氢酶活性的影响,从图中可以看出,随着浓度的增加土壤过氧化氢酶活性明显降低,这与杨志新等的研究一致[10]。而两种酶中脲酶对镉的反应更加敏感,因此,可以通过土壤脲酶活性的变化来反应该土壤中镉的变化情况。
3 结论
通过镉在棕壤上的吸附过程以及此过程中土壤酶活性的变化研究。结果发现,随着溶液中Cd2+含量的增大,两种土壤对Cd2+吸附量逐渐增大,且吸附反应符合Freundlich模型;同时镉在棕壤上的吸附抑制了土壤脲酶和过氧化氢酶的活性。
[1]黄益宗,郝晓伟,雷鸣,等.重金属污染现土壤修复技术及其修复实践[J].农业环境科学学报,2013,32(3):409-417.
[2]陈苏,孙丽娜,晁雷,周启星,孙铁珩.不同浓度组合的镉、铅在不同污染负荷土壤中的吸附-解吸动力学行为[J].应用基础与工程科学学报,2007,15(1):32-43.
[3]卢显芝,金建华,郝建朝,等.不同土层土壤酶活性对重金属汞和镉胁迫的响应[J].农业环境科学学报,2009,28(9):1844-1848.
[4]傅丽君,刘智任,杨磊.镉、铜、铅复合污染对枇杷园土壤微生物的生态毒理效应[J].生态毒理学报,2009,(6):881-888.
[5]李博文,刘树庆.潮褐土镉、锌、铅复合污染与土壤酶活性的关系[J].吉林农业科学,2000,25(1):38-41.
[6]Yu S,He Z L,Huang C Y,等. Adsorption-desorption behavior of copper at contaminated levels in red soils from China.Journal of Environmental Quality, 2002,31(4):1129-1136.
[7]Markiewicz-Patkowska J,Hursthouse A,Przybyla-Kij H. The interaction of heavy metals with urban soils:sorption behaviour of Cd,Cu,Cr,Pb and Zn with a typical mixed brownfield deposit. Environment International, 2005, 31(4):513-521.
[8]李朝丽,周立祥.我国集中典型土壤不同粒级组分对镉吸附行为影响的研究[J].农业环境科学学报,2007,26(2):516-520.
[9]郭晋君,张沛,杏艳,等.pH对土壤吸附重金属镉的影响[J].广东化工,2013,8(40):116-117.
[10]杨志新,刘树庆.Cd,Pb,Zn单因素及复合污染对土壤酶活性的影响[J].土壤与环境,2000,9(1):15-18.
Adsorption Effect of Cd in Brown Soil and Its Influence to Soilenzyme Activity
JIANG Yong, WANG Wei, WANG Yuhui, ZHAO Pei
(Linyi Bureau of Land and Resources, Shandong Linyi 276001, China)
Adsorption process of Cd in soil is the important factor which influence concentration, migratory aptitude and potential toxicity of Cd in soil solution. As an important indicators of soil quality, soil microorganism activity has good instruction function as soil heavy metal content. In this paper, the adsorption process of Cd in brown soil and changes of soil microorganism activity have been studied. It is showed that with the increase of Cd in the solution, soil adsorption of Cd increases gradually, and the adsorption reaction conforms to Freundlich equation. Accompanying with the increase of initial concentration of cadmium, soil urease and catalase activity have been inhibited, and thereinto urease is more sensitive to Cd.
Cd; brown soil; adsorption process; soil microorganism activity
2014-04-12;
2014-07-03;编辑:王敏
江泳(1974—),男,浙江龙游人,主要从事地质环境治理工作;E-mail:jysky5@sina.com
X52
B

