磁性CuO-Bi2O3/Fe3O4-SiO2-MgO催化剂的制备及甲醛乙炔化性能
王俊俊,李海涛,马志强,王志鹏,郭江渊,赵永祥
(山西大学化学化工学院,精细化学品教育部工程研究中心,山西 太原 030006)
引 言
1,4-丁炔二醇(BD)是一种重要的基本有机化工原料,经加氢后可得到1,4-丁二醇,进一步向下游延伸可制备一系列高附加值的重要化学品,如四氢呋喃(THF)、γ-丁内酯(GBL)、聚四亚甲基乙二醇醚(PTMEG)、聚氨酯树脂(PU resin)、聚对苯二甲酸丁二醇酯(PBT)、聚丁二酸丁二醇酯(PBS)等[1-6]。工业上,1,4-丁炔二醇生产采用Reppe 法,即甲醛与乙炔在铜铋催化剂作用下发生缩合反应合成。按反应器的不同,Reppe 法分为固定床、淤浆床、悬浮床3 种工艺[7-9]。其中,淤浆床工艺具有反应条件温和、操作过程安全、选择性和经济指标高等优点,在工业生产中被广泛应用[10-11]。为了使气、液、固三相充分接触,提高催化反应的效率,淤浆床反应器中使用的催化剂一般为50~180 μm 的粉末,且反应通常在强搅拌下进行[12-13]。在反应结束后,催化剂颗粒高的磨损率致使其难以被分离回收,在一定程度上增加了操作费用,降低了生产效率。制备高活性、易于分离的CuO-Bi2O3纳米粉体或负载型CuO-Bi2O3催化剂一直被催化剂研究者与使用者所关注[14-19]。
近年来,磁性催化剂被大量研究和报道,这种催化剂不仅具有优异的催化性能,而且在反应完成后可以利用外加磁场对其进行分离回收,磁性催化现已被成功应用于磁稳定床、固体酸碱催化剂、光催化、生物催化等领域,成为了催化剂领域的研究热点[20-23]。宗保宁[24]将磁稳定床与磁性催化剂结合用于己内酰胺加氢精制,与釜式加氢工艺相比,催化剂耗量降低70%,反应器体积减少85%。将该技术用于精制氢气中CO 的甲烷化、蒸汽裂解乙烯选择性加氢和催化裂化轻汽油叠合醚化等反应,也显示出良好的工业应用前景。Guo 等[25]制备了固体碱催化剂Na2SiO3/Fe3O4用于催化合成生物柴油,该催化剂表现出较Na2SiO3优异的催化性能,可在外加磁场下回收再利用。Wang 等[26]采用水热法制备了磁性Bi2WO6/CoFe2O4光催化剂,该催化剂可用于快速高效地降解污染物双酚A。Asha 等[27]以Fe3O4为载体,采用包埋的方法固定Arthrobactersp.脂肪酶,酶蛋白负载量可达到24~45 mg·g-1,得到的固定化酶在pH 5~9 和高达70℃的条件下仍然保持较高的催化性能。然而,到目前为止,关于磁性CuO-Bi2O3催化剂的制备及炔化性能的相关研究未见文献报道。
本文在前期课题组制备高性能 CuO-Bi2O3/ SiO2-MgO 催化剂工作的基础上,进一步引入磁性能优异的Fe3O4为磁核,分别采用浸渍法和共沉淀法制备了不同Cu 含量的磁性CuO-Bi2O3/Fe3O4- SiO2-MgO 催化剂,研究了制备方法及Cu 含量对催化剂结构、织构及催化性能的影响,为开发高活性、易分离的甲醛乙炔化催化剂提供理论依据。
1 实验部分
1.1 Fe3O4 的制备
按照文献[28]方法,称取13.9 g FeSO4·7H2O和20 g Fe2(SO4)3,在恒温水浴60℃和机械搅拌条件下溶解于500 ml 蒸馏水中,向混合溶液中缓慢滴加25% NH3·H2O 溶液,调节pH 约为10.0,在60℃恒温条件下持续搅拌1 h,将生成的沉淀物进行磁分离,用蒸馏水洗涤至中性,真空60℃干燥2 h 后即得Fe3O4颗粒。
1.2 磁性CuO-Bi2O3/Fe3O4-MgO-SiO2催化剂的制备
1.2.1 浸渍法 称取一定量上述Fe3O4,超声分散于100 ml TEOS 的乙醇溶液形成悬浊液,在恒温水浴40℃和机械搅拌条件下,向悬浊液中缓慢滴加Mg(NO3)2·6H2O 水溶液100 ml,滴加完后继续搅拌30 min,向其中缓慢滴加NaOH(1 mol·L-1)溶液,控制pH 约为10.0,停止搅拌,保持恒温状态持续老化3 h,再将沉淀物用蒸馏水离心洗涤至中性。在120℃干燥4 h,马弗炉中400℃焙烧3 h,即得Fe3O4-SiO2-MgO 复合物载体,研磨成粒径为125~149 μm 的粉状备用。
称取一定量上述Fe3O4-SiO2-MgO 复合物载体,按催化剂中Cu 质量分数为20%、25%、30%,Bi质量分数为 2%分别配制 Cu(NO3)2·3H2O 和Bi(NO3)3·5H2O 混合溶液(配制过程中加入适量浓HNO3防止Bi3+的水解),等体积浸渍载体,在 120℃干燥后于400℃焙烧,即得磁性CuO-Bi2O3/ Fe3O4-SiO2-MgO 催化剂,分别标记为1-IM、2-IM、3-IM。
1.2.2 共沉淀法 按照制备Fe3O4-SiO2-MgO 复合物载体的方法与条件,按催化剂中Cu 质量分数为20%、25%、30%,Bi 质量分数为 2%,将Mg(NO3)2·6H2O 水溶液更换为所需浓度的Cu(NO3)2·3H2O、Bi(NO3)3·5H2O、Mg(NO3)2·6H2O的混合水溶液(配制过程中加入适量浓HNO3防止Bi3+的水解),制备磁性CuO-Bi2O3/Fe3O4-SiO2-MgO催化剂,分别标记为1-CP、2-CP、3-CP。
按照制备CuO-Bi2O3/ Fe3O4-SiO2-MgO 催化剂的方法与条件,在不加Fe3O4的条件下,按催化剂中Cu 质量分数为30%,Bi 质量分数为2%制备CuO-Bi2O3/ SiO2-MgO 催化剂,标记为3-CC。
上述各催化剂中,Cu、Bi、Fe、Si、Mg 的实际含量见表1。
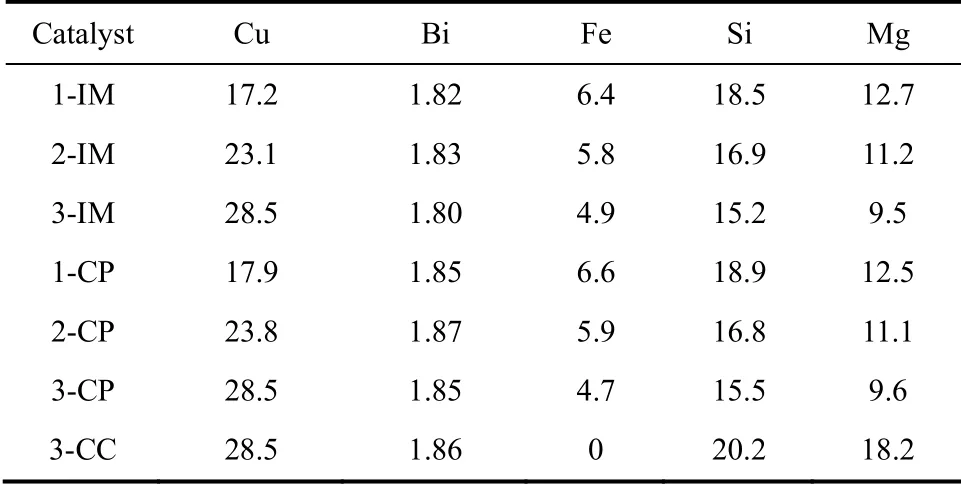
表1 不同方法制备的CuO-Bi2O3/Fe3O4-SiO2-MgO 催化剂的ICP 测定结果Table 1 ICP results of CuO-Bi2O3/Fe3O4-SiO2-MgO catalysts prepared by different methods/% (mass)
1.3 催化剂的表征
低温N2物理吸附-脱附测定在Micromeritics ASAP 2020 型自动物理吸附仪上进行,样品先于150℃下抽真空处理5 h,在-196℃下进行N2吸附。采用BET 法计算样品的比表面积。
XRD 表征在Bruker D8 Advance 型X 射线衍射仪上进行,使用Cu 靶,Kα辐射,管电压40 kV,管电流40 mA,扫描范围10°~80°,扫描速率0.1(°)·s-1。
H2-TPR 分析在天津先权TP-5067 动态吸附仪上进行,将30 mg(粒径0.28~0.45 mm)催化剂置于反应管中,通入5%H2-95%N2混合气(流量20 ml·min-1),基线平稳后,以10℃·min-1速率升温至800℃,采用TCD 检测器检测耗氢量。
样品的磁性在室温下利用Lake Shore 7410 VSM 振动样品磁强计测定。
催化剂中各元素的测定是在美国生产的Varian ICP-AES 光谱仪上进行测定。
1.4 催化剂的评价
甲醛乙炔化反应在500 ml 的四口玻璃烧瓶中进行。将研磨后的催化剂和甲醛溶液置于烧瓶中,将烧瓶置于油浴中,搅拌,通入氮气排尽系统内的空气,然后升温至90℃,恒温0.5 h 后,将氮气切换为乙炔气体进行乙炔化反应。1,4-丁炔二醇的定量分析采用Agilent 7890A 型气相色谱仪,1,4-丁二醇为内标,DB-5 毛细管柱(0.32 mm×50 m),FID检测器,反应液中未转化的甲醛采用碘量法滴定。
2 结果与讨论
2.1 N2 吸脱附表征
表2给出了不同方法制备的CuO-Bi2O3/Fe3O4- SiO2-MgO 催化剂的织构参数。从表中可以看出,当催化剂中Cu、Bi 含量相同时,共沉淀法制备的催化剂比浸渍法制备的催化剂具有更大的比表面积、更小的孔容及平均孔径。对于同一种方法制备的催化剂,其比表面积、孔容均随Cu 含量的增加呈现减小的趋势,平均孔径则变化不大。

表2 不同方法制备的CuO-Bi2O3/Fe3O4-SiO2-MgO 催化剂的织构参数Table 2 Textural parameters of CuO-Bi2O3/Fe3O4-SiO2-MgO catalysts prepared by different methods
图1及图2分别为不同方法制备的CuO-Bi2O3/ Fe3O4-SiO2-MgO 催化剂的N2吸附-脱附等温线及孔径分布。所有催化剂均表现出Ⅳ型吸附等温线,且具有迟滞环,表明两种方法制备的催化剂均为介孔结构。不同方法制备的催化剂的迟滞环形状不同,浸渍法制备的催化剂表现出H3 型迟滞环,集中在p/p0>0.7 区域,说明催化剂中的孔道主要由堆积孔构成,且孔径较大,分布范围较宽;共沉淀制备的催化剂表现出H2 型迟滞环,在p/p0=0.4~0.8 区域,说明催化剂中的孔道主要由硅凝胶形成,且孔径较小,分布范围相对较窄。
2.2 XRD 表征

图1 不同方法制备的CuO-Bi2O3/Fe3O4-SiO2-MgO 催化剂的N2 吸附-脱附等温线Fig.1 N2 adsorption-desorption isotherms of CuO-Bi2O3/Fe3O4-SiO2-MgO catalysts prepared by different methods
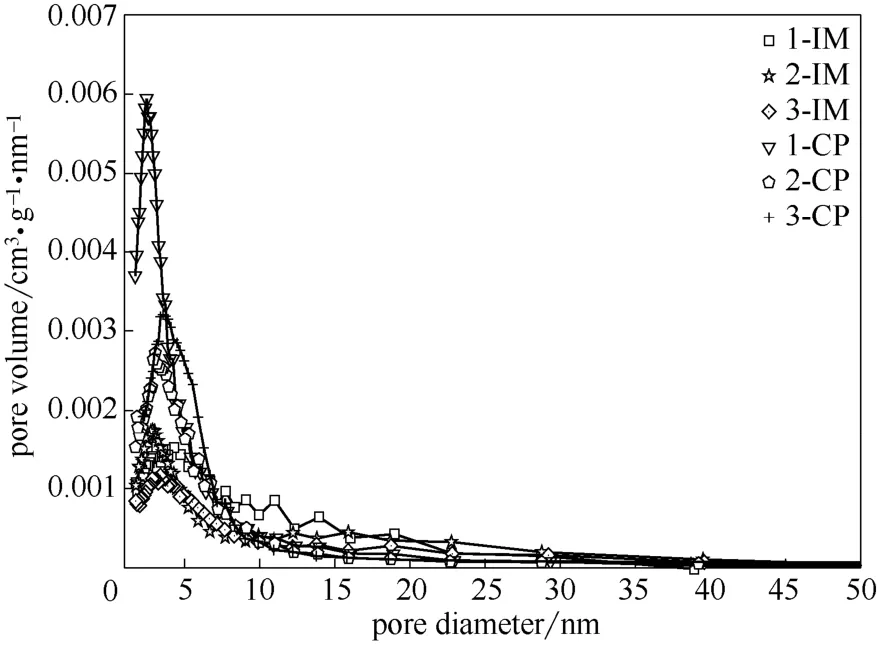
图2 不同方法制备的CuO-Bi2O3/Fe3O4-SiO2-MgO 催化剂的孔径分布Fig.2 Pore-size distribution of CuO-Bi2O3/Fe3O4-SiO2-MgO catalysts prepared by different methods
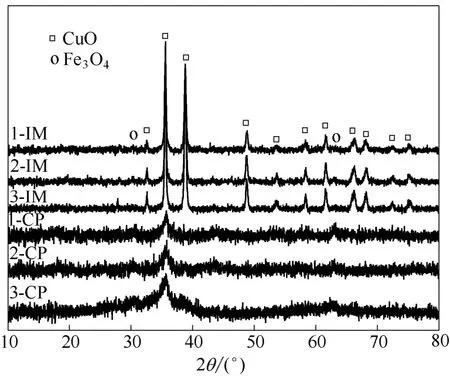
图3 不同方法制备的CuO-Bi2O3/Fe3O4-SiO2-MgO 催化剂的XRD 谱图Fig.3 XRD patterns of CuO-Bi2O3/Fe3O4-SiO2-MgO catalysts prepared by different methods
图3为CuO-Bi2O3/Fe3O4-SiO2-MgO 催化剂的 XRD 谱图。从图中可以看出,采用浸渍法制备的催化剂在2θ为35.5°、38.7°、48.7°、53.5°、58.3°、61.5°、66.2°、68.1°处均出现CuO 的特征衍射峰,峰形尖锐,且随铜含量的增加峰强度增强,表明浸渍法制备的催化剂中CuO 以较完整晶型存在,晶粒尺寸较大。而采用共沉淀法制备的催化剂仅在2θ为35.5°、38.7°处出现了较为弥散的、峰强度较小的CuO 特征衍射峰,表明共沉淀法制备的催化剂中CuO 结晶度较低,具有高的分散度。两种方法制备的样品均在2θ为30.2°、35.5°、62.7°处观察到微弱的Fe3O4的特征衍射峰,表明Fe3O4成功引入催化剂中。
2.3 H2-TPR 表征
选择Cu 质量分数为20%的催化剂1-IM 与1-CP,对其进行H2-TPR 表征,结果如图4所示。催化剂1-IM 与1-CP 均出现了3 个还原峰,其中350℃前的还原峰归属为CuO 的还原,350℃后的两个还原峰归属为Fe3O4的还原。1-IM 催化剂中CuO 的还原峰峰顶温度为343℃,而1-CP 催化剂中CuO 的还原峰峰顶温度较1-IM 中的低,为287℃。这表明,采用共沉淀法制备的催化剂中CuO 晶粒较小,高度分散于载体表面,易与氢气相互接触,从而在较低温度时被还原;而采用浸渍法制备的催化剂晶粒较大,晶型完整,难被H2还原[29],这与XRD 结果一致。
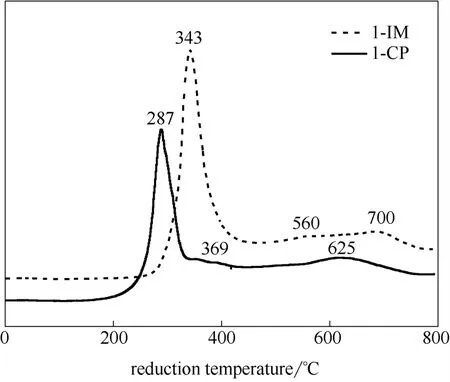
图4 不同方法制备的CuO-Bi2O3/Fe3O4-SiO2-MgO 催化剂的H2-TPR 谱图Fig.4 H2-TPR profiles of CuO-Bi2O3/Fe3O4-SiO2-MgO catalysts prepared by different methods
2.4 催化剂活性评价
将所制备的催化剂用于甲醛乙炔化反应,评价结果见表3。可以看出,催化剂的制备方法、Cu 含量对其甲醛乙炔化性能均有影响。对于同一种方法制备的催化剂,其催化性能随Cu 含量增加而增加,归因于催化剂中活性位点的增加。相比于催化剂中Cu 含量对催化活性的影响,制备方法的影响则更为明显,在制备的所有样品中,采用共沉淀法制备的催化剂的甲醛转化率、丁炔二醇选择性与收率均明显高于浸渍法。在甲醛乙炔化反应过程中,活性组分CuO 首先被甲醛还原为Cu+,生成的Cu+与乙炔进一步发生反应生成炔化亚铜的配合物,该物质为反应的活性中心;在CuO 与甲醛的还原过程中,CuO 的分散度是影响活性中心数目的重要因素[17],共沉淀法制备的样品中CuO 分散度较高,能形成更多的活性位,从而使催化剂表现出良好的催化活性与选择性。在所有样品中,3-CP 的催化活性最高,且高于非磁性催化剂3-CC,这可能与CuO 和Fe3O4产生了协同作用有关。

表3 不同方法制备的CuO-Bi2O3/Fe3O4-SiO2-MgO 催化剂的评价结果Table 3 Evaluation results of CuO-Bi2O3/Fe3O4-SiO2-MgO catalysts prepared by different methods
2.5 催化剂的磁性能及稳定性考察
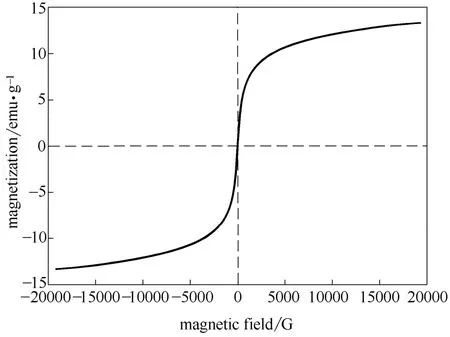
图5 CuO-Bi2O3/Fe3O4-SiO2-MgO 催化剂的磁滞回线Fig.5 Magnetic hysteresis loops of CuO-Bi2O3/Fe3O4-SiO2-MgO catalyst

图6 CuO-Bi2O3/Fe3O4-SiO2-MgO 催化剂的磁分离效果Fig.6 CuO-Bi2O3/Fe3O4-SiO2-MgO catalyst recovery with magnetic separation

图7 催化剂的稳定性评价结果Fig.7 Reusability of catalyst
选取活性最好的3-CP 催化剂,对其进行磁分离性能的考察。图5为室温下测定的催化剂的磁滞 回线,从图中可以看出,该催化剂具有较强的磁性,且其矫顽力为0,表明具有超顺磁性。图6为3-CP催化剂的磁分离效果。可以看出,在外加磁场的作用下,催化剂可以很快被分离出来,操作方法快速简单,有利于催化剂的回收再利用。
反应结束后,磁性催化剂通过外加磁场回收,非磁性催化剂采用离心方式回收,分离出的催化剂用蒸馏水洗涤数次,在真空干燥箱中干燥后,在相同条件下再对其进行评价。图7为磁性催化剂3-CP与非磁性催化剂3-CC 循环实验的评价结果。从图中可以看出,催化剂3-CP 经过6 次循环实验后,1,4-丁炔二醇收率由48.9%下降至36%,而催化剂3-CC 经4 次循环使用,1,4-丁炔二醇的收率从45.7%下降至不到20%,这表明制备的磁性催化剂的使用稳定性较非磁性催化剂更优。这可能是由两种催化剂的分离方式不同造成的。磁性催化剂通过外加磁场分离,回收率较高。而非磁性催化剂采用离心方式分离,操作过程中催化剂损失较多,从而表现出循环过程中催化性能的急剧下降。
3 结 论
制备方法与Cu 含量均对催化剂的甲醛乙炔化性能有重要影响,其中,制备方法的影响更为显著。与浸渍法制备的催化剂相比,采用共沉淀法制备的催化剂具有高的比表面,且活性组分CuO 具有良好的分散度及适宜的还原能力,经活化后可生成数量较多的炔铜配合物活性中心,使催化剂表现出高的催化活性及选择性。经对比,采用共沉淀法制备的Cu 质量分数为30%的催化剂表现出最高的催化性能。由于催化剂中成功引入了磁性粒子Fe3O4,使催化剂具有优异的超顺磁性,可以在反应完成后通过外加磁场快速从反应液中分离回收,简化了分离过程。此外,催化剂具有良好的使用稳定性,将回收后的催化剂重复评价6 次后,仍然具有较高的催化性能。
[1]Ge Y Y,Jia Z Q,Li H T,Gao P F,Zhang Y,Zhao L L,Zhao Y X.Amorphous aluminosilicates used as acid catalysts for tetrahydrofuran polymerization [J].Reac.Kinet.Mech.Cat.,2014,112 (2):467-475.
[2]Zhang Q,Zhang Y,Li H T,Gao C G,Zhao Y X.Heterogeneous CaO-ZrO2acid-base bifunctional catalysts for vapor-phase selective dehydration of 1,4-butanediol to 3-buten-1-ol [J].Appl.Catal.A:General,2013,466:233-239.
[3]Li H T,Zhao Y X,Gao C G,Wang Y Z,Sun Z J,Liang X Y.Study on deactivation of Ni/Al2O3catalyst for liquid phase hydrogenation of crude 1,4-butanediol aqueous solution [J].Chem.Eng.J.,2012,181/182:501-507.
[4]Hari Prasad Reddy K,Anand N,Sai Prasad P S,Rama Rao K S,David Raju B.Influence of method of preparation of Co-Cu/MgO catalyst on dehydrogenation/dehydration reaction path way of 1,4-butanediol [J].Catal.Commun.,2011,12 (10):866-869.
[5]Luo Ping (罗平),Wu Wenbao (武文豹),Li Yaohui (李耀会),Zhang Xiongbin (张雄斌),Lü Xiaowan (吕小婉),Li Xiaoding (李小定).Support containing catalyst for production of 1,4-butynediol by Reppe method,preparation method and application thereof [P]:CN,102125856 A.2011-07-20.
[6]Pinkos R,Lorenz R E,Beste Y A.Process for preparing 1,4-butanediol [P]:US,7759531 B2.2010-07-20.
[7]Reiss W,Schnur R,Winderl S,Hoffmann H,Zehner P.Process for the manufacture of butynediol [P]:US,3957888.1976-05-18.
[8]Fremont J M,Mills G.Preparation of butynediol [P]:US,4584418.1986-04-22.
[9]Hort E V.Low pressure catalytic ethynylation process [P]:US,4119790.1978-10-10
[10]Prater J L,Hedworth R L.Continuous,low pressure ethynylation process for the production of butynediol [P]:US,4117248.1978-09-26.
[11]Lu Yuehua (陆月华),Zhuo Zhen (卓震).Design points of butynediol slurry bed reactor [J].Chemical Plant Design(化工厂设计),1989,9 (4):15-21.
[12]Lin Xiping (林西平),Jia Hongdao (栗洪道).Synthesis and application of the acetylene glycol abroad [J].Petrochemical Technology(石油化工),1986,15 (2):111-117.
[13]Huangpu Yuanzhou (皇甫圆周).Development technology of preparation 1,4 - butyl acetylene glycol [J].Shaanxi Chemical Ⅰndustry(陕西化工),1995,15 (2):31-33.
[14]Wang Juanyun (王娟芸),Jiang Yi (蒋毅),Xie Jianchuan (谢建川),Chen Junhe (陈君和),Zhang Xiaoxia (张小霞),Jiang Wei (蒋伟).The research on preparation of butynediol using self-made malachite [J].Chinese Journal of Synthetic Chemistry(合成化学),2010,18 (B09):26-29.
[15]Gao Yuming (高玉明),Tian Hengshui (田恒水),Zhu Yunfeng (朱云峰).Catalytic synthesis on 1,4-butynediol by CuO/Bi2O3particles [J].Guangdong Chemical Ⅰndustry(广东化工),2008,35 (9):53-55.
[16]Yang G H,Xu Y B,Su X T,Xie Y H,Yang C,Dong Z J,Wang J D.MCM-41 supported CuO/Bi2O3nanoparticles as potential catalyst for1,4- butynediol synthesis [J].Ceram.Ⅰnt.,2014,40 (3):3969-3973.
[17]Zheng Yan (郑艳),Sun Zijin (孙自瑾),Wang Yongzhao (王永钊),Li Haitao (李海涛),Wang Shao’an (王韶安),Luo Min (罗敏),Zhao Jilong (赵吉龙),Zhao Yongxiang (赵永祥).Preparation of CuO-Bi2O3/SiO2-MgO catalyst and its ethynylation performance [J].Journal of Molecular Catalysis(China) (分子催化),2012:26 (3):233-238.
[18]Luo Ping (罗平),Zhao Xinming (赵新明),Li Haixia (李海侠),Zhang Hao (张浩),Li Yaohui (李耀会),Lü Xiaowan (吕小婉),Li Xiaoding (李小定).Research of EQ-201 acetylene catalyst in Reppe synthesizing 1,4-butynediol [J].Chemical Engineering Design Communications(化工设计通讯),2012,38 (5):87-90.
[19]Yang Mingxing (杨明星),Zhang Xiaofeng (张晓凤),Huang Qiufeng (黄秋锋),Lin Shen (林深).Study on preparation of CuO/Bi2O3/ ZSM-5 catalyst and catalytic properties for synthesis of butynediol [J].Journal of Molecular Catalysis(China) (分子催化),2007,21 (1):58-60.
[20]Gawande M B,Rathi A K,Nogueira I D,Varma R S,Branco P S.Magnetite-supported sulfonic acid:a retrievable nanocatalyst for the Ritter reaction and multicomponent reactions [J].Green Chem.,2013,15:1895-1899.
[21]Gawande M B,Branco P S,Varma R S.Nano-magnetite (Fe3O4) as a support for recyclable catalysts in the development of sustainable methodologies [J].Chem.Soc.Rev.,2013,42:3371-3393.
[22]Xiong Xiaolong (熊小龙),Liu Zili (刘自力),Xu Cuixia (徐翠霞),Qin Zuzeng (秦祖赠).Preparation and structure characterization of superparamagnetic supported catalyst H3PW12O40/ Fe3O4@SiO2and its application in olefinic alkylation desulfurization [J].CⅠESCJournal(化工学报),2014,65 (3):921-928.
[23]Zhang Yaping (张亚平),Jiao Qingze (矫庆泽),Wu Qin (吴芹),Li Hansheng (黎汉生).Preparation and catalytic performance of magnetic mesoporous silica supported basic ionic liquids [J].CⅠESCJournal(化工学报),2014,65 (12):4799-4804.
[24]Zong Baoning (宗保宁).Applications of the amorphous alloy catalyst and magnetically stabilized bed technology in petrochemical processes [J].Chinese Journal of Catalysis(催化学报),2008,29 (9):873-877.
[25]Guo P M,Huang F H,Zheng M M,Li W L,Huang Q D.Magnetic solid base catalysts for the production of biodiesel [J].J.Am.Oil Chem.Soc.,2012,89 (5):925-933.
[26]Wang C Y,Zhu L Y,Chang C,Fu Y,Chu X L.Preparation of magnetic composite photocatalyst Bi2WO6/CoFe2O4by two-step hydrothermal method and its photocatalytic degradation of bisphenol A [J].Chem.Commun.,2013,37:92-95.
[27]Asha C,Rajinder P,Subhash C T,Ghulam N Q.Arthrobacter sp.lipase immobilization on magnetic sol-gel composite supports for enantioselectivity improvement [J].Process Biochemistry,2009,44 (2):154-160.
[28]Polshettiwar V,Varma R S.Nanoparticle-supported and magnetically recoverable palladium (Pd) catalyst:a selective and sustainable oxidation protocol with high turnover number [J].Org.Biomol.Chem.,2009,7:37-40.
[29]Hurst N W,Gentry S J,Jones A,Brian D,McNicol.Temperature programmed reduction [J].Catal.Rev.Sci.Eng.,1982,24 (2):233-309.

